煤基碳量子点制备及对环境水中Cr(Ⅵ)的测定
闫立东, 胡朝帅,2, 程俊霞, 朱亚明*, 赵雪飞*
(1. 辽宁科技大学 化学工程学院, 辽宁 鞍山 114051; 2. 河北工业职业技术大学, 河北 石家庄 050091)
1 引 言
铬是现代工农业中应用最广泛的金属元素之一,在自然界中,通常以铬(Ⅲ)和铬(Ⅵ)的形式稳定存在。铬(Ⅲ)毒性较低,能调节人体糖和脂肪代谢功能,是人体正常生长发育的重要元素。Cr(Ⅵ)具有强烈的致癌性和致畸性,危害人类健康和生态系统[1-2]。因此,环境水中Cr(Ⅵ)的准确识别和测定对环境保护和人类安全至关重要。目前已开发出多种检测Cr(Ⅵ)的方法,如原子吸收光谱法[3]、电感耦合等离子发射光谱法[4]、分光光度法[5]等。但昂贵的仪器或繁琐的样品预处理过程限制了它们在各领域的实际应用。相比之下,碳量子点荧光性能猝灭技术因其响应快速、制备成本低、操作简单等特点,被广泛应用于化学传感技术中[5-8]。
碳量子点(Carbon quantum dots,CQDs)是2004 年Xu 等[9]在分离和纯化单壁碳纳米管时发现的近球形颗粒,其粒径小于10 nm,具有光致发光性能。2006 年,Sun 等[10]通过表面钝化合成了具有增强荧光发射效应的纳米颗粒,并命名为碳量子点。与传统含有过渡金属的半导体量子点相比,碳量子点不仅具有类似于传统量子点的发光性能与纳米尺寸特性,而且具有卓越的光学稳定性和水溶性、优异的化学惰性和低毒性、良好的生物相容性等,被广泛应用于光催化[11-12]、荧光探针[13-14]、吸附剂[15-16]、复合膜材料[17-18]和生物成像[19-21]领域。
荧光探针被认为是一种有效、快速、经济的离子检测方法[22]。鲁等[23]以间苯二胺和磷酸为原料,通过优化反应时间和温度合成了一种在365 nm 紫外光激发下发出亮绿色荧光的氮、磷掺杂碳量子点(N,P-CDs),将N,P-CDs 应用于金属离子检测中,发现其对Pd2+具有良好的选择性,检出限为0.995 μmol/L。Li 等[24]以山梨酸为碳源,以脯氨酸为氮掺杂剂,合成水溶性碳量子点(ACDs)并用于Cr(Ⅵ)的识别,检出限为34 nmol/L,该方法已成功用于校园实际水样中Cr(Ⅵ)离子检测。Fang[25]等以苯并噁嗪为原料,制备出发射绿色荧光的碳纳米颗粒(G-CNPs),G-CNPs 对Cr(Ⅵ)有良好的选择性和快速响应能力,检出限为0.58 μmol/L(S/N=3)。CHEN[26]以柠檬酸和1,6-二氨基己烷为前驱体,采用水热法制备了氮、硫共掺杂碳量子点(N, S/C-dots),该N, S/C-dots 对Cr(Ⅵ)表现出良好的选择性和敏感性,检出限为0.86 μmol/L。传统的碳量子点多采用昂贵的有机小分子为原料制得,近年来,以廉价、易得的木质素[27]、柿子叶[28]、无烟煤[29]、褐煤[30]和煤沥青[31-32]等为原料制备碳量子点的报道层出不穷。Liu 等[33]以O3氧化褐煤成功得到平均粒径约2.8 nm 且具有良好水溶性和光学性能的碳量子点(CQDs),该CQDs 对Fe3+具有高灵敏度和选择性猝灭效果,在10~150 μmol/L 范围内,碳量子点的荧光强度与Fe3+浓度具有良好的线性关系,检出限为0.26 μmol/L。然而,原煤及生物质中含有大量的金属离子,这或多或少会影响碳量子点在离子检测方面的应用。而煤经过热萃取后所得萃取物中Na、Mg、Al 含量较萃取前原煤降低80%,微量元素Be、Sr、Ba、Cd、V等较原煤减少99%[34]。鉴于此,本文以海拉尔褐煤热解萃取物(Hailaer brown coal pyrolytic extract,CPE)为碳源制备碳量子点,并将其作为荧光探针,可最大程度减少原料带来的金属离子干扰,对扩大碳量子点应用领域具有重要意义。
2 实 验
2.1 煤基碳量子点的合成方法
以海拉尔褐煤热解萃取物为碳源(采用鞍钢工业洗油400 ℃热解萃取海拉尔褐煤得到热溶物,表1 是褐煤热解萃取物的元素分析),HNO3为氮源,通过一步水热法合成氮掺杂煤基碳量子点。将萃取物充分研磨过200 目筛,称取1.0 g 左右萃取物加入到50 mL 硝酸溶液(5 mol/L)中,常温超声20 min;超声后将混合液转移到100 mL 聚四氟乙烯内胆高压反应釜内密封,将釜置于鼓风干燥箱中,以5 ℃/min 升温至180 ℃恒温7 h;然后取出自然降至室温,抽滤得到棕黄色液体,并以0.1 mol/L 的NaOH 溶液调至pH 为7;随后将溶液旋蒸(温度50 ℃,真空度0.1 MPa)剩余至40 mL 左右。将旋蒸后溶液离心(10 000 r/min) 20 min 以除去大颗粒和悬浮物,然后透析(MW:1 000 u)72 h,期间每6~8 h 换一次水;透析结束后收集透析袋内溶液并定容到100 mL,即得到淡黄色煤基氮掺杂碳量子点母液(绝对量子产率为1.36%)。NCQDs 的合成及应用流程图如图1 所示。取20 mL N-CQDs 溶液置于称量瓶中进行恒重实验,100 ℃干燥8 h,得到固体碳量子点。经计算,上述N-CQDs 溶液浓度为0.54 mg/mL,将N-CQDs 固体与溶液储存,备用。
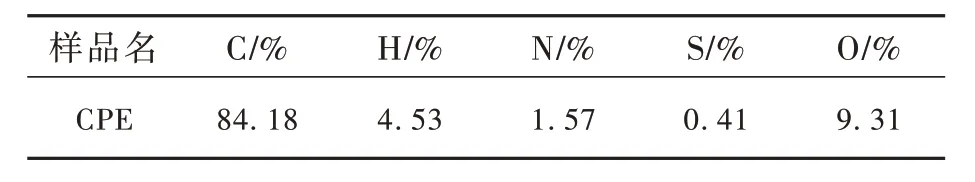
表1 CPE 的元素分析Tab.1 Ultimate analysis of CPE
2.2 碳量子点阴离子溶液的配制及荧光猝灭实验
准确移取3 mL 0.10 mg/mL 的N-CQDs 水溶液注入荧光比色皿中。分别各自加入3 μL 0.10 mol/L 人体或环境中常见的15 种阴离子溶液。室温(20 ℃)下搅拌均匀并静置60 s,在340 nm 激发波长下测量各混合液的荧光光谱。
3 结果与讨论
3.1 煤基碳量子点的表征
透射电子显微镜(TEM)具有表征和分析碳量子点形貌的功能,图2(a)、(b)分别为N-CQDs 溶液的透射电镜和粒径分布统计结果。TEM 结果显示,所合成的N-CQDs 呈类球形颗粒,溶液未发现明显团聚现象。高分辨率透射电子显微镜(HRTEM)显示N-CQDs 具有清晰、规则的晶格条纹,说明其具有结晶特性或有序结构。晶格间距0.35 nm,对应于石墨碳(002)晶面,表明N-CQDs存在类似石墨烯的晶态结构;粒径统计结果表明,N-CQDs 颗粒直径较小,大致分布在1.2~3.3 nm之间,平均粒径约为2.01 nm。
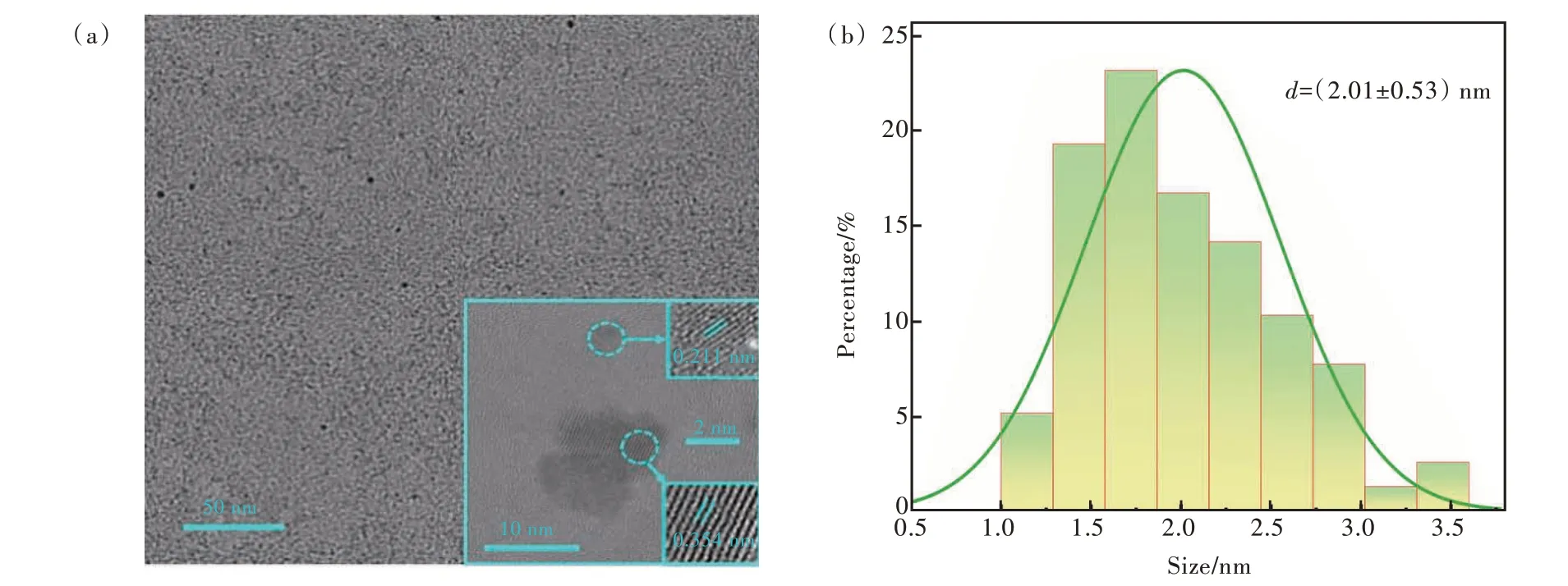
图2 N-CQDs 的TEM(a)及粒径统计(b)图Fig.2 TEM, HRTEM images(a) and particle size distribution(b) of N-CQDs.
拉曼光谱(Raman)和红外光谱(FT-IR)可用于表征N-CQDs 的碳质结构和官能团信息。从图3(a)N-CQDs 的FT-IR 谱可以得出,3 420 cm-1附近出现的强吸收归因于O—H 和N—H 的伸缩振动,2 800~3 000 cm-1之间微弱的振动是甲基的特征振动,1 718 cm-1处的特征峰归属于羰基的伸缩振动峰,1 596 cm-1和1 450 cm-1附近的振动归因于苯环中C=C 键的伸缩振动,而1 350 cm-1和1 250 cm-1附近的特征吸收分别对应于C—N 和C—O 键的伸缩振动[35-37]。图3(b)是N-CQDs 的拉曼光谱,可以看出,在1 343 cm-1和1 579 cm-1处有明显的拉曼特征峰存在(D 峰和G 峰),D 峰代表材料中碳原子晶的缺陷程度,G 峰由碳原子sp2杂化面内伸缩振动引起,代表材料中较为完整的石墨微晶片层结构,两峰的相对强度之比ID/IG为1.21,表明N-CQDs 是包含sp2碳团簇并具有部分缺陷的碳原子晶格结构[38]。
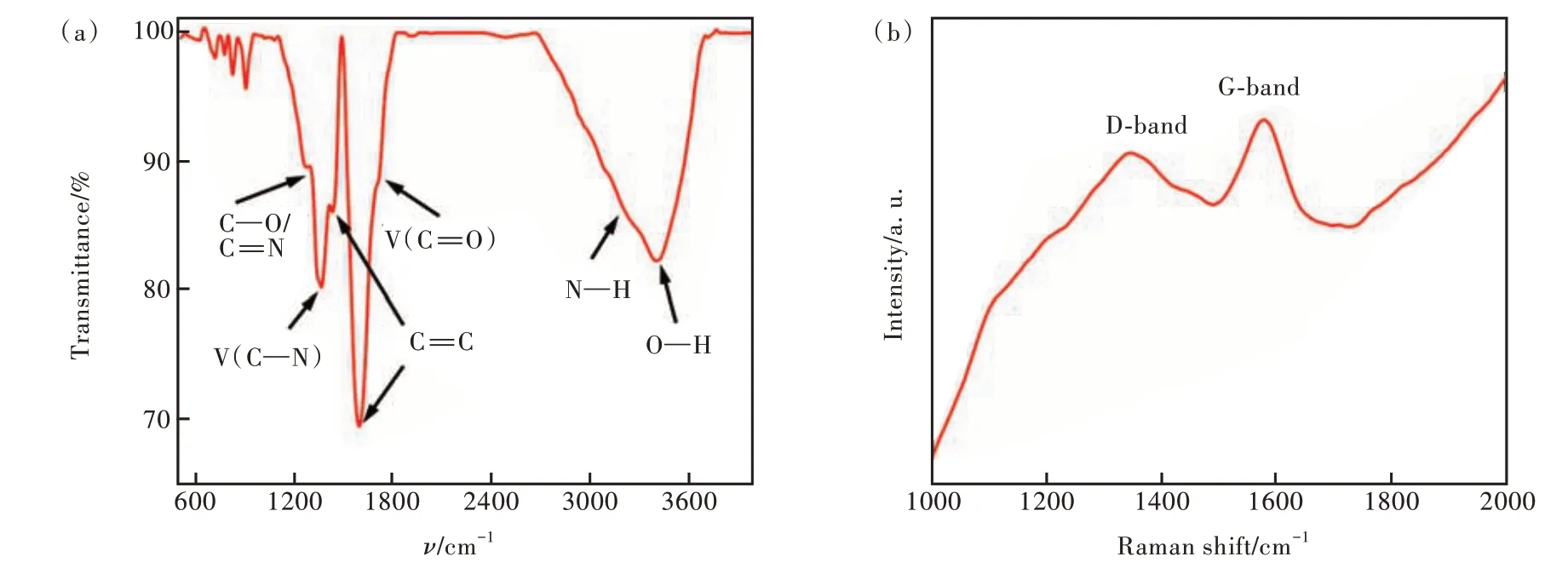
图3 N-CQDs 的FTIR 谱(a)和Raman 光谱(b)Fig.3 FT-IR(a) and Raman(b) spectra of N-CQDs
X 射线光电子能谱仪(XPS)通常用来表征NCQDs 表面的元素类型和含量及原子所处化学环境等信息。图4(a)中N-CQDs 的XPS 全谱图有三个强峰,位置分别在532.0,400.0,285.0 eV 附近,表明N-CQDs 中主要含有O、N 和C 元素,通过计算每种元素的积分面积,得到C(61.23%)、N(6.48%)和O(31.69%)三种元素含量。图4(b)为N-CQDs 的C1s 高分辨谱图,可以看出C 元素处在C=C/C—C(284.28 eV)、C—N/C—O(286.24 eV)和C=O(288.08 eV)四种不同化学态[39-40]。图4(c)是N-CQDs 的N1s 高分辨谱图,可以得出N元素分别以吡啶氮(399.28 eV)、吡咯氮(401.38 eV)和硝基芳烃氮(405.58 eV)三种化学态存在[41-42]。图4(d)为N-CQDs 的O1s 谱图,O 元素分别处在C=O(531.08 eV)、C—O/—OH(532.58 eV)和—NO2(534.98 eV)三种化学环境[43]。结合FT-IR 分析,XPS 结果表明,该N-CQDs 是以C 元素为基本骨架,并连有丰富的O、N 元素,主要以C=C、C=O、C—O 和—NO2等官能团形式存在,C—O、—NO2等含氧官能团存在于N-CQDs 表面,使其具有良好的亲水性,能够分散在水中长期不聚沉[44]。N-CQDs 中氮含量明显高于CPE,这说明CPE 经硝酸刻蚀后,N 元素被成功掺入N-CQDs中。N 元素的引入有效地调节了N-CQDs 电子结构,改善其物理化学性质,优化N-CQDs 多方面性能[45-47]。
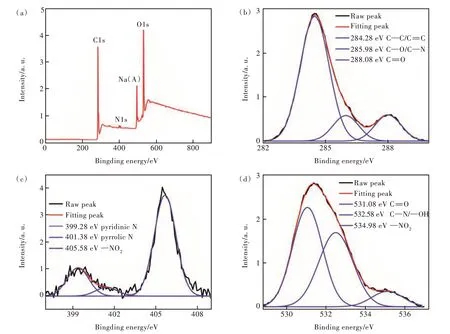
图4 N-CQDs 的XPS 全谱(a)、C1s 谱(b)、N1s 谱(c)、O1s 谱(d)。Fig.4 XPS wide energy spectrum(a), C1s(b), N1s(c), O1s(d) and their fitting curves of N-CQDs.
3.2 煤基碳量子点的光学性质
采用荧光光谱和紫外-可见吸收分光光度法分析了N-CQDs 的光学特性。图5(a)是N-CQDs水溶液的紫外-可见吸收光谱(UV-Vis)和荧光光谱,从UV-Vis 可以看出,N-CQDs 在紫外区出现很强的吸收峰,且在可见光区有长拖尾现象,287 nm处特征吸收峰归于芳香族C=C 键产生的π-π*跃迁以及C=O 键的n-π*跃迁[48-49]。N-CQDs 的荧光光谱在340 nm 处有强激发峰出现,以该波长进行激发,N-CQDs 在556 nm 处出现最大荧光发射峰。图5(a)中插图显示N-CQDs 溶液在340 nm 紫外光辐照下发出黄绿色荧光,在自然光下呈透明棕黄色。另外,N-CQDs 的吸收光谱和荧光发射光谱之间的重合非常小,二者有较大的斯托克斯位移(Stokes),材料的自吸收小,可有效消除因自吸收导致的荧光猝灭,从而提高检测精度[50]。
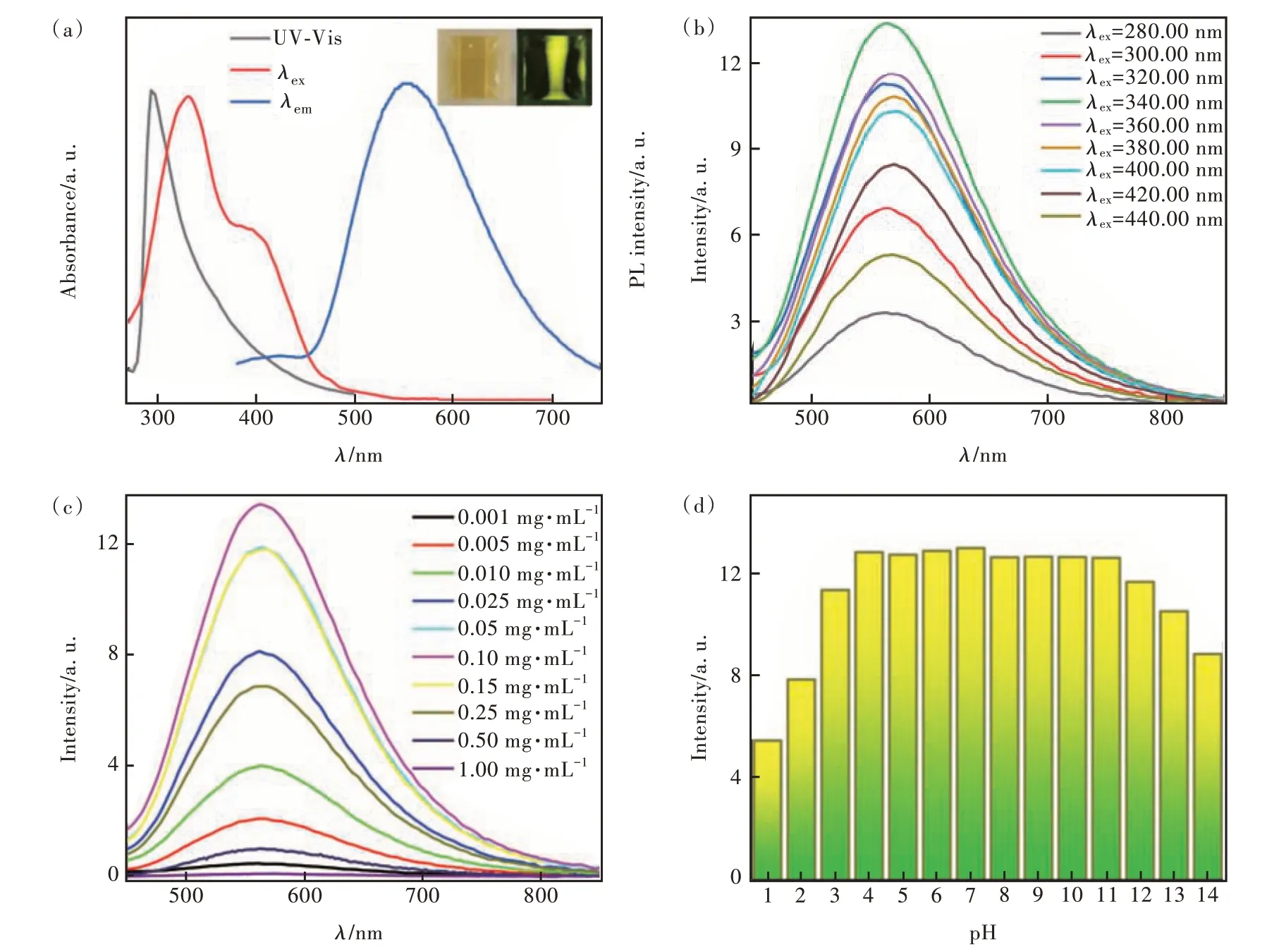
图5 N-CQDs 溶液的紫外-可见吸收光谱、荧光激发和发射光谱(a),不同激发波长下的荧光光谱(b),不同浓度的荧光光谱(c),340 nm 激发下不同pH 的荧光光谱(d)。 (a)中插图分别为自然光和340 nm 紫外光下的照片。Fig.5 (a)UV-Vis, fluorescence excitation, and emission spectra of the N-CQDs. (b)Fluorescence spectra with different excitation wavelengths.(c)Fluorescence spectra(λex=340 nm) at different concentrations. (d)Influence of pH on the fluorescence intensity(λex=340 nm). Insets in (a) are the photographs taken under daylight(left) and 340 nm UV light(right).
图5 (b)是N-CQDs 在280~440 nm 激发波长下的荧光光谱。可以看出,N-CQDs 的发射峰强度随激发波长增加出现先增大后减小趋势,340 nm 激发时荧光强度达到最大值。N-CQDs 的发射峰位置不随激发波长变化而改变,说明N-CQDs 发射峰不具有激发波长依赖性。分析认为,这是由于N-CQDs 具有较均匀的粒径和相同的表面结构所致,这与粒径具有较小的波动范围相吻合[51]。图5(c)是N-CQDs 溶液浓度为0.001~1.00 mg/mL 的荧光光谱,可以看出,随着N-CQDs 溶液浓度增加,荧光发射峰的位置不变,但荧光强度出现先增加后减小的趋势,N-CQDs 溶液浓度为0.10 mg/mL 时荧光强度最大(以下离子检测实验中,均以该浓度进行实验)。这种现象一方面归因于NCQDs 溶液荧光发射光谱的短波长端与其吸收光谱的长波长端有部分重叠,当N-CQDs 溶液浓度较大时,N-CQDs 分子的荧光发射光谱被另一些分子吸收,导致N-CQDs 溶液荧光强度降低,浓度越大荧光强度降低越显著。另一方面,N-CQDs 溶液浓度较低时,荧光物质分子间相互作用较弱,荧光强度较高,随着浓度的增加,分子间的相互作用增强,这使得荧光物质更容易发生非辐射跃迁,从而导致荧光强度降低[52-54]。图5(d)是不同pH 值对N-CQDs 溶液荧光强度的影响。可以看出,NCQDs 溶液荧光强度在4≤pH≤11 时基本保持不变。当1≤pH≤4 和11≤pH≤14 时,N-CQDs 溶液的荧光强度随着酸性和碱性的增强急剧下降,酸碱浓度相同的情况下,酸性条件影响强于碱性。推测认为,在pH≤4 时,N-CQDs 表面的—COOH、—OH 与H+形成氢键,N-CQDs 表面的羧基质子化会诱导碳量子点聚集,导致N-CQDs 的荧光强度下降。在较高的OH-存在下,N-CQDs 表面的COOH被OH-中和,破坏N-CQDs 表面官能团,导致荧光强度下降[55]。
图6(a)为N-CQDs 在不同浓度的NaCl 和KCl溶液中荧光强度(F/F0)变化情况。可以看出,Na-Cl 和KCl 浓度从0%增加到1%,N-CQDs 溶液的荧光强度仍保持相对稳定,说明N-CQDs 溶液具有较好的抗盐性;图6(b)为N-CQDs 溶液在常温下储存0 天、2 个月、5 个月和6 个月时的荧光光谱,结果显示,不同存放时间的N-CQDs 溶液荧光强度无明显改变,说明N-CQDs 具有很好的稳定性。综上所述,采用硝酸氧化刻蚀CPE 制备的N-CQDs具有较好的稳定性及抗盐性,这些特性表明其在离子识别、生物成像及传感器等领域具有很好的应用潜力。
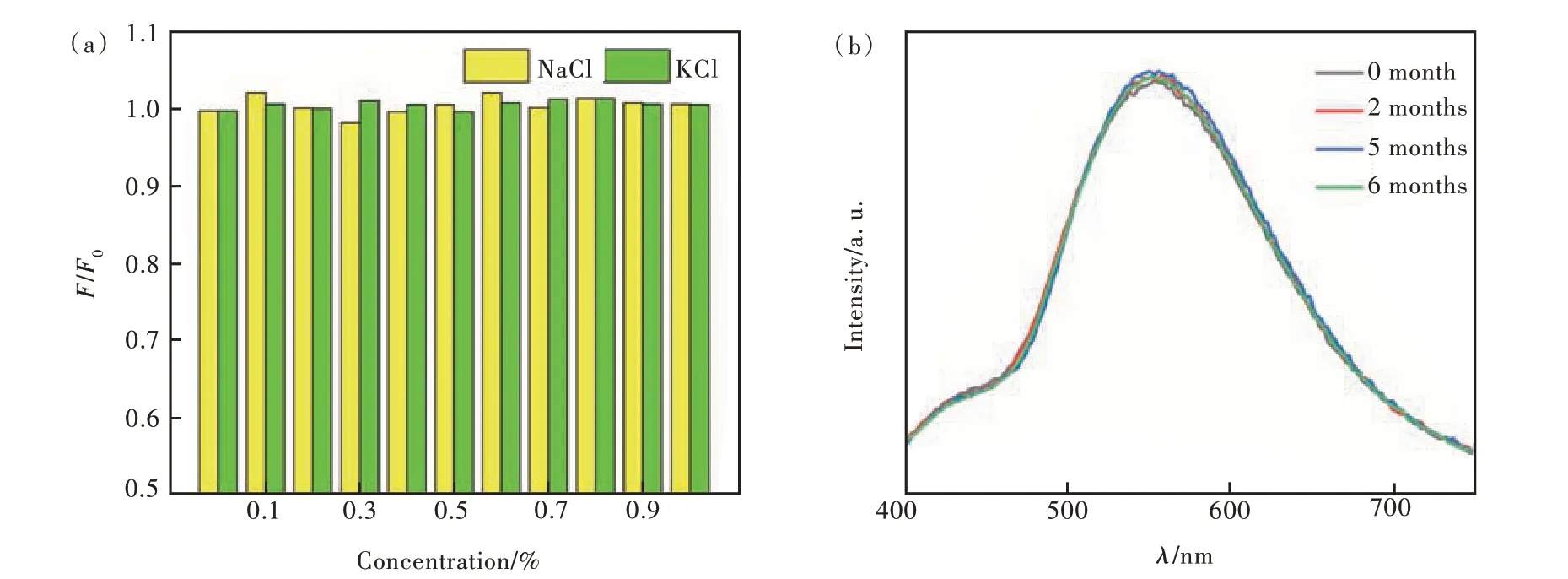
图6 (a)N-CQDs 溶液在不同浓度NaCl 和KCl 溶液中的荧光光谱;(b)存放不同时长N-CQDs 溶液的荧光光谱。Fig.6 (a)Fluorescence intensity of different concentrations of NaCl and KCl solution of N-CQDS. (b)Fluorescence intensity of N-CQDs for different time.
3.3 碳量子点在离子识别上的应用
离子识别是碳量子点常见的应用领域之一。因N-CQDs 溶液荧光强度在4≤pH≤11 变化很小,在进行离子识别过程中,调节天然水体至中性条件下进行。图7(a)为100 μmol/L 不同类型阴离子的N-CQDs 溶液荧光强度F/F0与空白样柱状图。可以看出,当Cr(Ⅵ)加入量为100 μmol/L 时,NCQDs 溶液的荧光强度降为原来的76.56%,而其他离子则不具备使N-CQDs 溶液荧光有效猝灭的性能,表明N-CQDs 对Cr(Ⅵ)具有选择识别性。在N-CQDs 实际应用中,通常要考虑常见阴离子与Cr(Ⅵ)共存下对N-CQDs 溶液荧光强度的影响。图7(b)是14 种不同阴离子与Cr(Ⅵ)共存下的荧光强度F/F0与空白样柱状图。可以看出,阴离子加入对N-CQDs 溶液荧光强度无明显干扰,与之前的报道相比(表2),该N-CQDs 溶液受其他阴离子干扰较小,且对Cr(Ⅵ)具有良好的选择识别能力,可以作为荧光传感器识别环境水中的Cr(Ⅵ)。
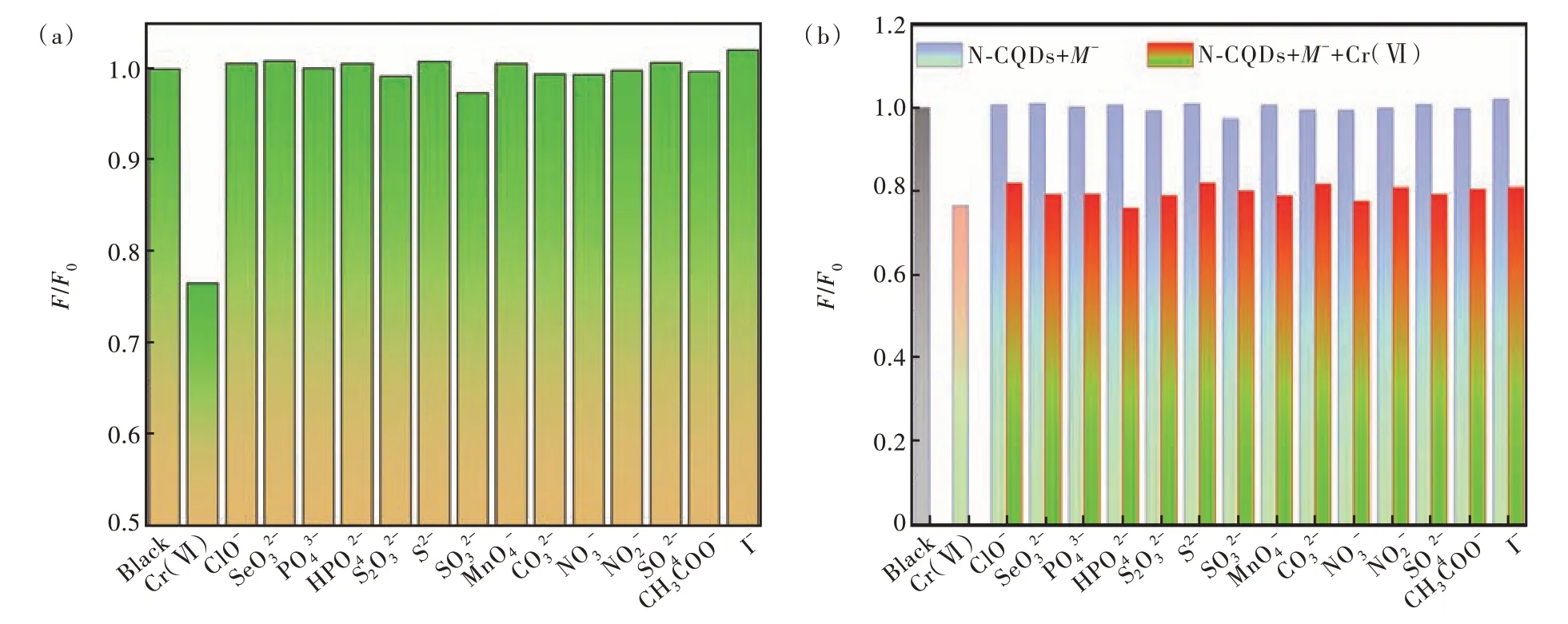
图7 (a)不同阴离子存在下N-CQDs 溶液的荧光强度;(b)不同阴离子与Cr(Ⅵ)共存下N-CQDs 溶液的荧光强度。Fig.7 (a)Relative fluorescence intensity of N-CQDs in the presence of different anions(100 μmol/L). (b)Relative fluorescence intensity of N-CQDs for Cr(Ⅵ) coexisting with 100 μmol/L of other anions.
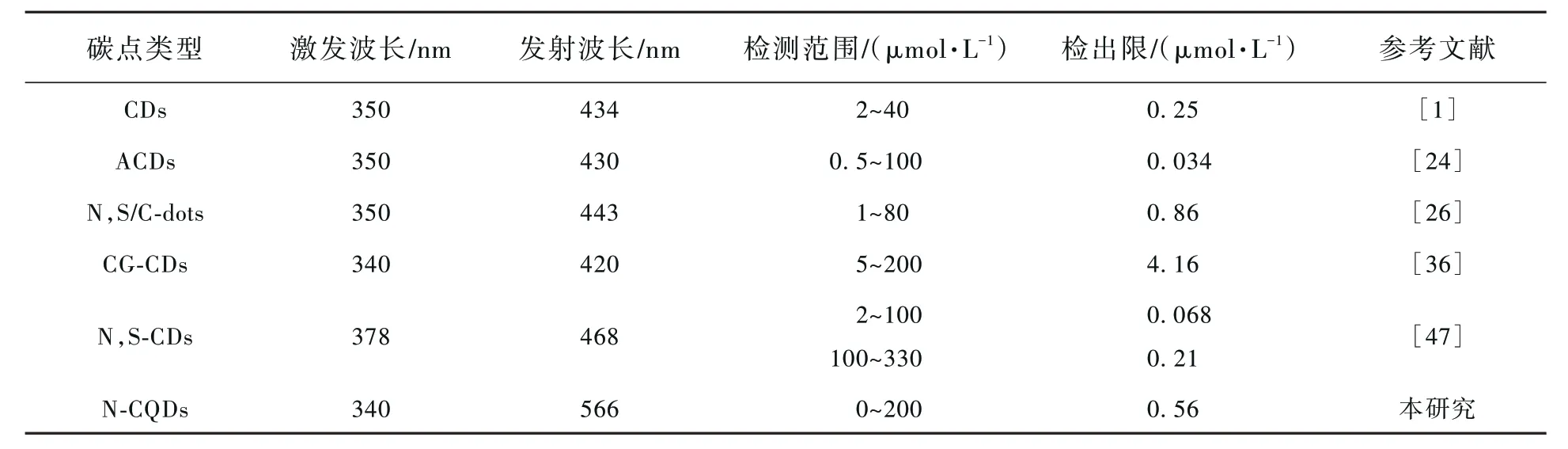
表2 不同方法检测Cr(Ⅵ)的比较Tab.2 Comparison of different methods for Cr(Ⅵ) detection
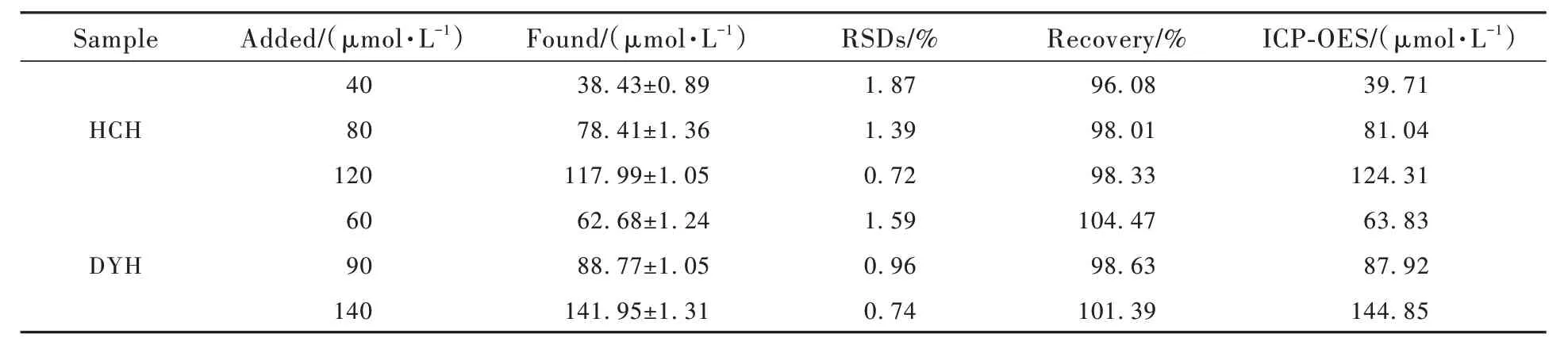
表3 N-CQDs 识别实际水样中Cr(Ⅵ)(n=5, 置信度95%)Tab.3 Determination of Cr(Ⅵ) in actual samples by N-CQDs(n=5, 95% confidence level)
为了进一步评估N-CQDs 溶液识别Cr(Ⅵ)的潜质,实验考察不同Cr(Ⅵ)浓度对N-CQDs 溶液荧光猝灭的影响。图8(a)是不同浓度的Cr(Ⅵ)溶液对N-CQDs 溶液荧光强度的影响结果。可以看出,随着N-CQDs 溶液中Cr(Ⅵ)浓度的增加,荧光强度逐渐降低,但N-CQDs 溶液发射光谱位置和形状没有变化,说明Cr(Ⅵ)对N-CQDs 溶液荧光有猝灭作用。图8(b)是N-CQDs 溶液加入Cr(Ⅵ)离子前后F0/F比值与Cr(Ⅵ)浓度关系曲线。添加Cr(Ⅵ)前后的相对荧光强度F0/F与Cr(Ⅵ)浓度关系以Stern-Volmer 方程表示:
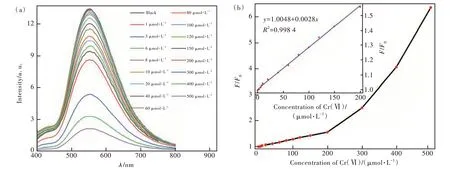
图8 (a)不同Cr(Ⅵ)浓度的N-CQDs 溶液荧光光谱;(b)F0/F 与Cr(Ⅵ)浓度关系曲线,插图为Cr(Ⅵ)浓度在0~200 μmol/L范围内的线性拟合图。Fig.8 (a)Fluorescence emission spectra of N-CQDs solution at different concentrations of Cr(Ⅵ) by 340 nm excitation wavelength. (b)Relationship between F0/F and the concentration of Cr(Ⅵ), insets show a linear relationship within the range of 0-200 μmol/L.
其中F0和F分别是N-CQDs 溶液加入Cr(Ⅵ)前后的荧光强度,KS是Stern-Volmer 方程猝灭常数,[Q]为猝灭剂Cr(Ⅵ)的浓度。
从图8(b)可以看出,N-CQDs 溶液的相对荧光强度比值随着Cr(Ⅵ)浓度增加而增大,且在0~200 μmol/L 范围内呈良好的线性关系,线性方程为y=1.0048+0.0028x,R2为0.998 4,其中x为Cr(Ⅵ)浓度。根据检出限(DOL)的计算式D=3δ/k(δ:N-CQDs 的空白标准偏差,k:拟合曲线的斜率)计算得到检出限为D=0.56 μmol/L,低于WHO 规定的限量值0.96 μmol/L,结果表明该碳量子点对Cr(Ⅵ)识别在较宽的浓度范围内都表现出较高的灵敏度。推测认为,当Cr(Ⅵ)浓度在 0~200 μmol/L 时,可与N-CQDs 表面的—COOH、—OH 或—NO2等官能团发生稳定的配位关系;当C(Ⅵ)浓度超过200 μmol/L 时,N-CQDs 表面官能团与Cr(Ⅵ)配位数发生改变,导致曲线无法呈现出良好的线性关系[56-57]。
3.4 实际水样中Cr(Ⅵ)的识别
鉴于N-CQDs 对Cr(Ⅵ)优异的识别性和抗干扰能力,本研究以N-CQDs 为荧光探针对春季海城河(HCH)水样与岫岩大洋河(DYH)水样中Cr(Ⅵ)含量进行定量研究。两种水样前处理方式相同,均采用高速离心(10 000 r/min,20 min)及滤膜(0.22 μm)过滤。分别用HCH 水与DYH 水配置0.10 mg/mL 的N-CQDs 溶液,荧光测试结果表明,两种水样中Cr(Ⅵ)的含量低于荧光探针的检出限,因此进行模拟添加检测实验。实验条件为:HCH 水样配置的N-CQDs 溶液Cr(Ⅵ)浓度分别为40,80,120 μmol/L,DYH 水样配置的N-CQDs 溶液Cr(Ⅵ)浓度分别为60,90,120 μmol/L。在340 nm激发波长下测定荧光光谱,每组样品做5 次平行分析,计算加标回收率。经计算,获得HCH 水样加标回收率为96.08%~98.33%,DYH 水样的加标回收率为98.63%~104.47%,二者的RSDs 均小于5%,检测结果与电感耦合等离子体发射(ICP-OES)测量结果相近,说明该检测方法具有良好精密度和准确度,能够用于实际水样中Cr(Ⅵ)检测(浓度0~200 μmol/L)。
3.5 碳量子点荧光猝灭机理探索
荧光猝灭是荧光分子表面基团与猝灭物质发生反应,导致荧光强度降低或猝灭,通常分为静态猝灭和动态猝灭。动态猝灭通常会降低碳量子点的荧光寿命,而静态猝灭则不会导致碳量子点的荧光寿命发生明显变化。图9 是N-CQDs 溶液中加入Cr(Ⅵ)前后的荧光衰减曲线。经拟合计算后得到,加入Cr(Ⅵ)前后的荧光寿命分别是1.09 ns 和1.10 ns,Cr(Ⅵ)的加入对N-CQDs 荧光寿命影响不大,从而推断该猝灭过程属于静态猝灭[26,58-61]。荧光猝灭的原因可能是N-CQDs 表面—OH 和—COOH 等官能团与Cr(Ⅵ)形成不发光基态复合物,电子复合体在没有光子的情况下回到基态所致[33]。
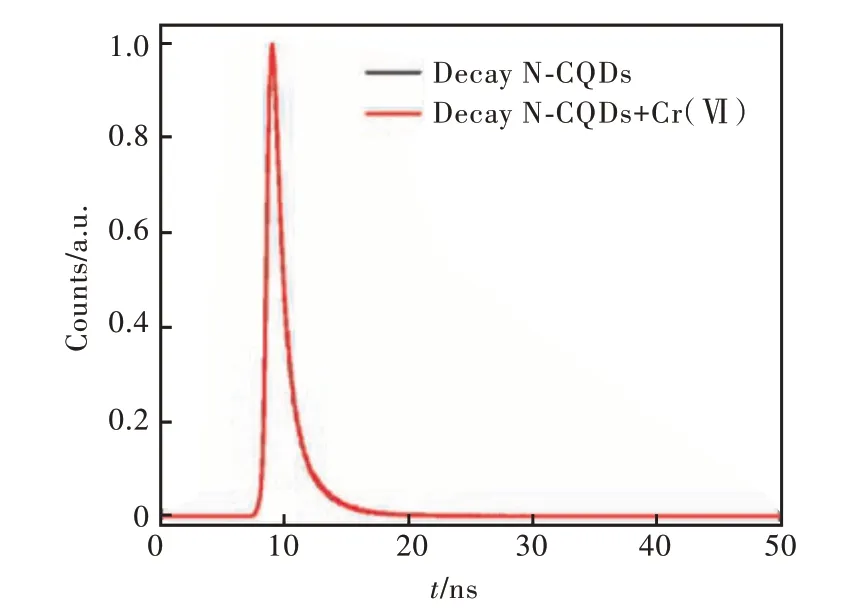
图9 N-CQDs 溶液添加Cr(Ⅵ)前后的荧光衰减曲线Fig.9 Fluorescence decay curves of N-CQDs before and after mixed with Cr(Ⅵ)
4 结 论
本文采用海拉尔褐煤热解萃取物为碳源,5 mol/L 的HNO3为氮源,采用一步水热法合成识别环境水中Cr(Ⅵ)的碳量子点材料。该N-CQDs 发出明亮的黄色荧光,并具有不依赖激发波长的发光特性。通过TEM、XPS 和FT-IR 表征,发现NCQDs 分散均匀,平均粒径为2.01 nm,表面含有碳、氮和氧三种元素,并表现出良好的水溶性、稳定性和高荧光强度。基于Cr(Ⅵ)能够有效猝灭N-CQDs 溶液荧光性能,在Cr(Ⅵ)浓度为0~200 μmol/L 时,可建立了一种高灵敏度和选择性的Cr(Ⅵ)识别方法,检出限为0.56 μmol/L。HCH 与DYH 河水加标回收实验表明,N-CQDs 能够用于实际水样中Cr(Ⅵ)的检测,加标回收率RSDs 为96.08%~104.47%,可以作为一种简单、快速、灵敏地识别Cr(Ⅵ)的新方法,同时为褐煤的高附加值利用提供了新的应用方向。
本文专家审稿意见及作者回复内容的下载地址:http://cjl. lightpublishing. cn/thesisDetails#10.37188/CJL.20230244.

