非离断Roux-en-Y 吻合术在远端胃癌根治术后的应用效果
王 杰,金 哲,李向楠
(1 镇平县人民医院,河南 镇平 474250;2 南阳市中心医院,河南南阳 473005;3 郑州大学第一附属医院,河南 郑州 450000)
远端胃癌(Distal gastric cancer,DGC)属临床常见病症,在我国发病率一直居高不下,据统计,2012 年该病症在全球发病约95.1 万例,而死亡率占全部癌症死亡病例的10%[1-3]。远端胃癌根治术(Total laparoscopic radical resection of distal gastric cancer,TLD)为临床针对DGC 患者重要手段之一,可有效切除病灶,但术后易致使患者出现营养不良[4]。因此,术后患者仍需开展消化道重建,以促进机体营养状态改善。Roux-en-Y 吻合术、非离断(Uncut)Roux-en-Y 吻合术属常见消化道重建方案,均对机体胃肠功能恢复具有积极作用。本研究收集我院DGC 患者130 例,旨在从营养指标、肠黏膜屏障功能、手术安全性等层面分析上述两种术式应用价值。现报道如下。
1 资料与方法
1.1 一般资料 选取我院2020 年1 月—2022 年3月收治的DGC 患者130 例,根据不同手术方式分为两组,每组65 例。观察组男40 例,女25 例;年龄49~67 岁,平均(56.62±3.96)岁;肿瘤长径3.2~6.9 cm,平均(5.38±0.75)cm;TNM 分期:Ⅲ期24 例,Ⅱ期21 例,Ⅰ期20 例。对照组男37 例,女28 例;年龄49~66 岁,平均(55.87±3.85)岁;肿瘤长径3.1~6.7 cm,平均(5.29±0.63)cm;TNM 分期:Ⅲ期26 例,Ⅱ期18 例,Ⅰ期21 例。两组基线资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经我院伦理委员会批准。
纳入标准:符合DGC 诊断标准[5];TMN 分期Ⅰ~Ⅲ期;临床资料完整;TLD 术后实施消化道重建;具备手术适应证;签署知情同意书。排除标准:胃部手术史;存在远处转移灶;其他恶性肿瘤;血液、免疫系统病症;术前新辅助化疗者。
1.2 方法 两组均行TLD 治疗,两组均取平卧位,全麻,作1 cm 长手术切口于脐下缘,建立气腹(维持12 mmHg),插入戳孔,探查腹腔,明确病灶位置,并观察淋巴结转移情况及周围组织侵犯情况,自左侧肋缘下腋前线作主操作孔(长12 mm),依次自右侧肋缘下腋前线2 cm 位置及平脐偏上2 cm位置左、右锁骨中线作辅助操作孔,并置入5 mm Trocar;清扫淋巴结,下拉结肠,以超声刀游离横结肠系膜前叶及大网膜,分离胃网膜左血管后离断,裸化胃大弯,清扫第4组淋巴结,游离结缔组织,再清扫第10 组淋巴结;剥离胰腺包膜,分离胃网膜右动静脉后离断,清除第6 组淋巴结,切除淋巴与结缔组织(十二指肠前壁附带处),分离胰腺上缘及肝总动脉旁淋巴结后切除,再分离出胃右动静脉,自根部离断,游离第一段十二指肠,显露脾动脉,清扫第8、9、11 组淋巴结;分离胃左血管并自根部离断,清扫第7 组淋巴结;待小网膜囊打开后,清扫第1.3.5.组淋巴结,游离胃远端,十二指肠自距幽门下缘3~5 cm 处离断,切割闭合2 次后离断胃远端。观察组实施Uncut Rouxen-Y 吻合术,距屈氏韧带约18 cm 位置及残胃大弯侧分别作0.5 cm 长手术切口,并实施残胃空肠吻合(切割闭合器进行)(见图1),闭合共同开口,具胃空肠吻合位置30 cm 及8 cm 处打开0.5 cm 切口,实施空肠-空肠侧侧吻合(见图2),闭合共同开口后,距胃空肠吻合口5 cm 位置闭合但不离断(见图3)。对照组实施传统Roux-en-Y 吻合术,距屈氏韧带远端20 cm 位置,闭合并离断闭合肠管(小肠),作1 cm 手术切口于胃残端,置入切割闭合器,实施残胃-远端空肠侧侧吻合,关闭共同开口,电刀烧灼黏膜,距胃空肠吻合口40 cm处及近端空肠位置实施侧侧吻合,闭合侧切口,电刀烧灼黏膜,4-0 微乔线加强吻合口(浆肌层)及闭合口;两组若未见活动性出血,则退出器械,常规引流,关闭切口。术后均予以两组抗感染、止痛等治疗。

图1 残胃空肠吻合

图2 空肠-空肠侧侧吻合

图3 胃空肠吻合口5cm 位置闭合但不离断
1.3 观察指标 (1)以主观综合营养评估法(SGA)[6]评估两组患者术前、术后1 个月、3 个月营养状况,分值>16 分为严重营养不良;8~15 为轻微营养不良,≤7 分为正常。(2)两组患者手术指标,包括重建时长、手术耗时、术中失血量、排气时间、恢复半流食时间。(3)取静脉血4 mL,室温凝固,3000 r/min 转速离心10 min(r=10 cm),取血清,酶联免疫法测定两组患者术前、术后1 个月、3 个月营养指标[铁蛋白(SF)、瘦素(LEP)]水平。(4)通过邻联茴香胺试剂法测定两组患者术前、术后1 d、3 d二胺氧化酶(DAO)含量,改良分光光度法测定D-乳酸含量。(5)两组术后吻合口狭窄、胃排空延迟、切口感染、输入袢梗阻并发症发生率。
1.4 统计学处理 数据采用SPSS22.0 统计学软件分析,计量资料采用±s表示,采用t检验,计数资料以n(%)表示,采用χ2检验,以P<0.05 表示差异有统计学意义。
2 结果
2.1 SGA 评分 术后1 个月、3 个月,两组患者SGA 评分均较术前降低,其中观察组降低幅度更明显(P<0.05)。见表1。
表1 两组治疗前后SGA 评分比较(±s,分)

表1 两组治疗前后SGA 评分比较(±s,分)
?
2.2 手术指标 与对照组相比,观察组患者术中失血量更少,重建时长、排气时间、手术耗时及恢复半流食时间更短(P<0.05)。见表2。
表2 两组手术指标比较(±s)
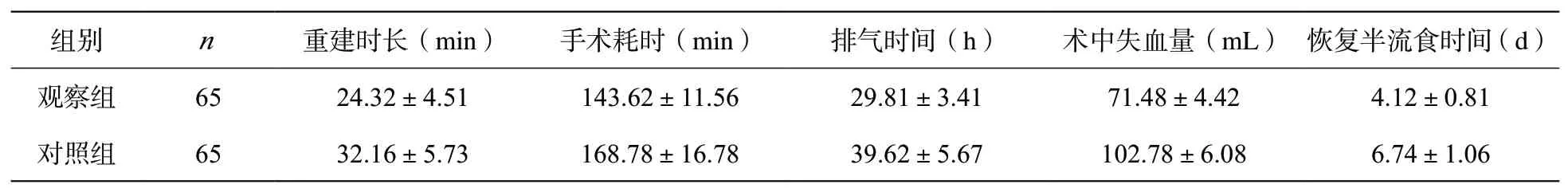
表2 两组手术指标比较(±s)
?
2.3 营养指标 术后1 个月、3 个月与术前相比,两组患者血清SF 水平均升高,LEP 水平均降低,其中观察组血清SF 水平升高幅度更显著,LEP 水平降低幅度更显著P<0.05)。见表3。
表3 两组治疗前后营养指标比较(±s,μg/L)

表3 两组治疗前后营养指标比较(±s,μg/L)
?
2.4 血清DAO、D-乳酸 术后1 d、3 d 与术前相比,两组患者血清DAO、D-乳酸水平均较升高,但观察组升高幅度更小(P<0.05)。见表4。
表4 两组治疗前后血清DAO、D-乳酸水平比较(±s)

表4 两组治疗前后血清DAO、D-乳酸水平比较(±s)
?
2.5 并发症 观察组65 例,吻合口狭窄1 例,切口感染1 例,并发症发生率为3.08%;对照组65 例,吻合口狭窄3 例,胃排空延迟4 例,切口感染1 例,输入袢梗阻1 例,并发症发生率为13.85%。两组并发症发生率比较,P<0.05。
3 讨论
TLD 是临床治疗DGC 常用术式,与传统开腹手术相比,其具有术后恢复快、创伤小、并发症少等优势[7]。但该术式亦存在一定难点,尤其是术后消化道重建,目前,临床多数学者认为,TLD术后对消化道实施重建,需同时考虑患者术后营养需求及手术安全性[8]。
现阶段,临床针对TLD 治疗DGC 患者术后多通过Roux-en-Y 吻合术重建消化道,可于一定程度恢复机体胃肠功能,促进机体营养状态改善,但该术式需离断空肠,无法保留空肠连续性及系膜血管弓完整性,从而易引发神经冲动传导障碍,造成空肠出现逆蠕动,增加术后并发症风险[9]。Uncut Roux-en-Y 吻合术是于空肠吻合口及胃空肠间封闭肠壁,结扎肠管,可降低对机体神经功能及血液循环影响,减少并发症发生[10]。同时该术式无需切断空肠系膜,不仅有助于保留机体空肠连续性及系膜血管弓完整性,且不会对小肠运动复合波传导产生影响,更有助于患者术后机体及营养状态恢复,简化手术操作步骤,减少术中出血,缩短手术耗时,降低并发症风险。本研究显示,与对照组患者相比,观察组术中失血量更少,重建时长、手术耗时、排气时间及恢复半流食时间更短,术后SGA 评分及血清LEP 水平更低,血清SF 水平更高,差异均有统计学意义(P<0.05),可见,Uncut Roux-en-Y 吻合术应用于TLD 术后患者治疗可进一步优化手术指标、促进机体营养状态改善、减少并发症。
有报道指出,DGC 患者受手术创伤影响,可致使肠黏膜受损,血清DAO、D-乳酸经受损肠黏膜大量入血,从而影响患者术后恢复[11]。D-乳酸为机体胃肠道细菌代谢产物,其表达与肠黏膜受损程度呈正相关;当机体肠黏膜细胞遭受损害时,DAO 表达可呈过度表达状态[12]。本研究显示,术后1 d、3 d,观察组患者血清DAO、D-乳酸水平低于对照组,差异具有统计学意义(P<0.05)。由此可见,TLD 术后患者开展Uncut Roux-en-Y 吻合术对机体肠黏膜屏障功能影响更小。这可能在于该术式无需离断空肠,继而有助于增加消化液分流,减少其对吻合口的刺激,故对机体肠黏膜屏障功能影响更小。
综上所述,UncutRoux-en-Y 吻合术应用于TLD 术后患者治疗,可进一步优化手术指标、促进机体营养状态改善、减少并发症发生,且对机体肠黏膜屏障功能影响更小。

