基于多准则决策的亚胺培南对头孢哌酮-舒巴坦治疗的重症感染患者风险-效益评价
蔡晓佳 王映芬 王文娟
(南方医科大学珠江医院药剂科, 广东 广州 510260)
重症感染一般是由致病微生物侵入人体内并繁殖而引起的,其中重症肺部感染较为常见临床症状主要有发烧、咳痰等[1-2]。在严重感染早期选择适当的抗生素可显著降低死亡率[3]。碳青霉烯类是β-内酰胺类抗菌剂,具有广谱活性;亚胺培南是首个用于临床的碳青霉烯类抗生素,可作用于人体全身且具有高抗菌活性,对链球菌、奈瑟菌、甲氧西林敏感葡萄球菌、嗜血杆菌、厌氧菌和常见的需氧革兰氏阴性医院病原体包括假单胞菌都有活性[4-5]。但亚胺培南容易被位于肾小管中的脱氢肽酶-1降解,故一般与脱氢肽酶-1抑制剂西司他丁共同给药[6]。头孢哌酮-舒巴坦是β-内酰胺与β-内酰胺酶抑制剂的抗生素组合,具有广谱性活性[7]。对于耐多药生物包括β-内酰胺酶-大肠杆菌、耐碳青霉烯类大肠杆菌以及耐碳青霉烯类鲍曼不动杆菌均表现出良好的体外活性,且这种效力不受产生病原菌的接种量大小的影响[8]。目前发现,重症感染一般被诊断为多种耐药菌的混合感染,且由于抗生素的使用,病原菌耐药性也不断增加,因此有很多关于亚胺培南联用头孢哌酮-舒巴坦疗效的报道,但二者联用的效益风险指标进行评价的研究鲜少。多准则决策模型是一种可以将较为复杂的问题进行碎片化处理的定量效益风险分析方法,具有进行多个准则权衡的优点,将该模型构建用于评定联合用药效益风险具有一定的灵活性,且容易理解。为此,本文基于多准则决策对亚胺培南联合头孢哌酮-舒巴坦治疗重症感染患者的效益-风险进行评价,以期为临床治疗提供更多方案及理论依据。
1 资料与方法
1.1 一般资料 收集并整理2020年3月—2022年5月收治于我院的98例重症肺部感染患者的临床资料,通过随机数字表法将98例患者随机分为单一治疗组和联合治疗组,每组49例。单一治疗组采用头孢哌酮-舒巴坦治疗,男性26例,女性23例,年龄22~80岁,平均(52.09±4.45)岁;联合治疗组采用头孢哌酮-舒巴坦联合亚胺培南的治疗,男性25例,女性24例,年龄23~78岁,平均(51.35±4.69)岁。本研究经南方医科大学珠江医院伦理委员会审核通过(3412KY215)。纳入标准:①患者年龄≥20岁。②临床资料完整无缺失。③完成血清学和影像学检查,诊断为重症肺部感染患者。④配合随访并签署知情同意书。排除标准:①既往使用抗生素、囊性纤维化或心内膜炎等疾病的患者。②需要透析的患者。③非细菌性肺炎、怀疑癌症引起的阻塞性肺炎以及慢性阻塞性肺疾病患者。④免疫缺陷、药物相互作用的患者。
1.2 观察指标
1.2.1 相关指标 控制感染时间、药物治疗时间、肺功能指标恢复时间、细菌学检查复常时间;治疗前和治疗10天后炎症因子指标血常规指标、肝肾指标和肺功能指标;治疗后总有效率以及不良反应发生率(皮疹、头晕、恶心、腹泻、局部疼痛、肾功能异常、肝功能异常)。
1.2.2 肺功能指标 通过肺功能仪(VPAPⅢST-A型,德国耶格公司)测定用力肺活量第1秒用力呼气容积(Forced expiratory volume in one second,FEV1)与用力肺活量(Forced vital capacity,FVC)并计算二者比值的平均值以及残气量(Residual volume,RV)与肺总量(Total lung capacity,TLC)的比值平均值。
1.2.3 肝肾功能指标 通过AU5421全自动生化分析仪(美国贝克曼库尔特公司)及配套试剂检测丙氨酸转氨酶(ALT)、谷草转氨酶(AST)、胱抑素C(Cys C)、β2微球蛋白(β2-MG)。
1.2.4 炎症因子指标 通过酶联免疫吸附法测定治疗前后IL- 6和TNF-α的水平和通过AU5421全自动生化分析仪测定CRP。
1.2.5 血常规指标 通过日本SYSMEX公司XE2100型血细胞分析仪进行检测白细胞计数(WBC)、血小板计数(PLT)、红细胞计数(RBC)。
1.4 随访以及诊断标准 通过电话等线上联系方式或门诊复诊等方式对患者病情进行术后1个月的随访,每周随访一次。治愈:感染症状消失,病原菌基本清除且肺功能以及炎症因子指标恢复正常水平;有效:症状基本消失且各项指标恢复良好;无效:症状无明显改善,存在不良反应。总有效率=(治愈例数+有效例数)/总数×100%。

2 结果
2.1 两组患者一般资料的比较 两组患者在年龄、性别以及基础疾病方面比较差异无统计学意义(P>0.05);联合治疗组的控制感染时间、药物治疗时间、肺功能指标恢复时间、细菌学检查复常时间与单一治疗组相比显著缩短,不良反应总发生率显著降低(P<0.05);联合治疗组的总有效率、病原菌清除率显著高于单一治疗组(P<0.05);两组患者治疗前的肺功能指标、血常规指标以及炎症因子指标比较差异无统计学意义(P>0.05),治疗后两组以上指标均有明显改善且联合治疗组CRP、PLT改善程度显著高于单一治疗组(P<0.05);两组肝肾指标治疗前、后比较差异均无统计学意义(P>0.05)。见表1。
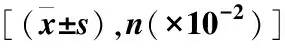
表1 两组患者一般资料的比较
2.2 效益-风险评价指标决策树的建立 建立亚胺培南联合头孢哌酮-舒巴坦治疗重症肺部感染患者的效益-风险评价指标决策树,见图1。效益和风险指标各占50%的权重,见表2。其中效益指标中对患者病情影响最大的是控制感染时间和肺功能指标恢复时间,风险指标影响较大是肾功能异常和肝功能异常两种不良反应。

图1 效益-风险评价指标决策树

表2 效益-风险指标及权重、最优值和最差值规定
2.3 效益、风险指标合并结果的比较 将单一治疗组和联合治疗组各48例患者的效益和风险指标进行合并结果显示,与单一治疗组相比,联合治疗组的总有效率、控制感染时间、药物治疗时间、肺功能指标恢复时间、病原菌清除率、细菌学检查复常时间、CRP、PLT以及不良反应发生率均得到明显改善(P<0.05),见表3。
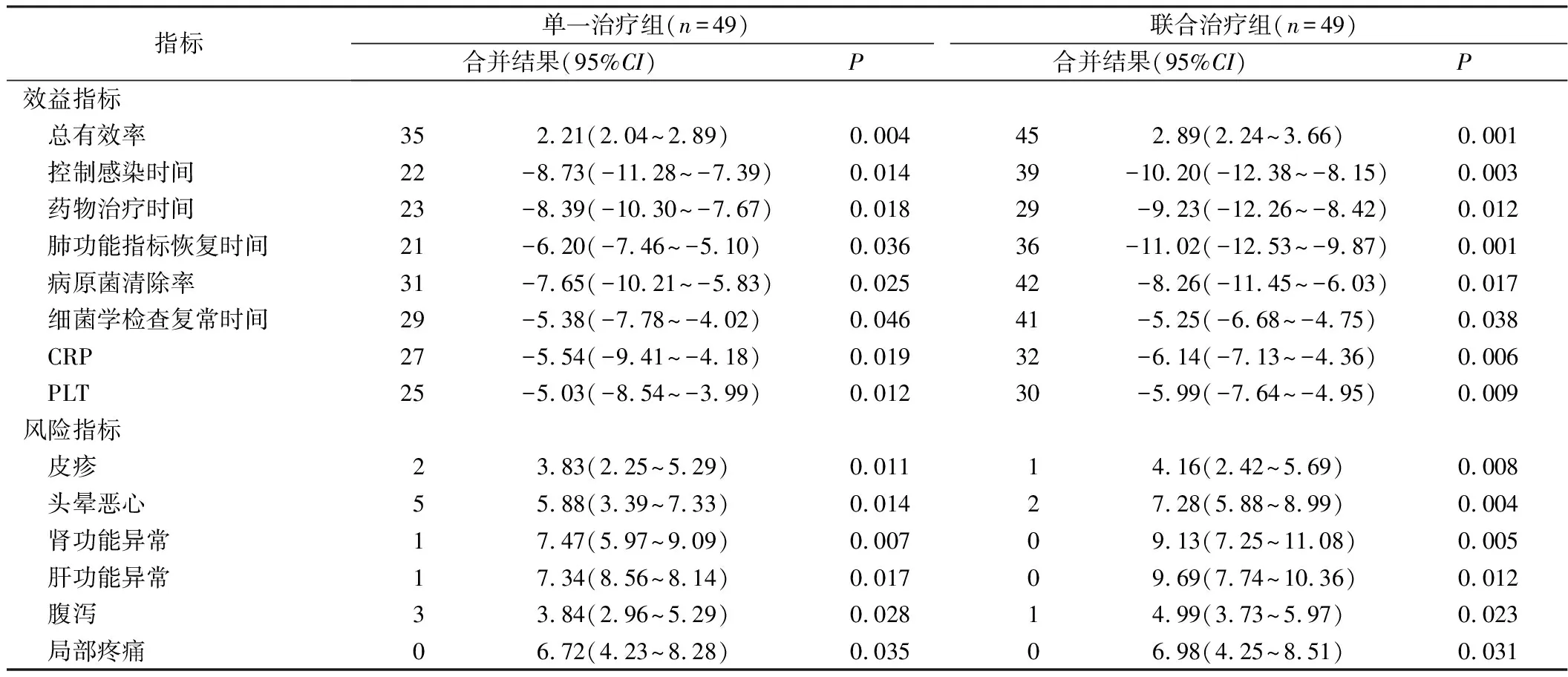
表3 效益、风险指标合并结果的比较
2.4 两种治疗方式的效益值和风险值比较 单一治疗组和联合治疗组治疗重症肺部感染患者效益值分别为60和78,根据蒙特卡洛模拟两组的效益值相差18,联合治疗组与对照相比显著提升,产生差异的概率达100%,见表4。二者风险值分别为56(单一治疗组)和72(联合治疗组),蒙特卡洛模拟后结果显示两组的风险值相差16,产生差异的概率达100%,见表5。
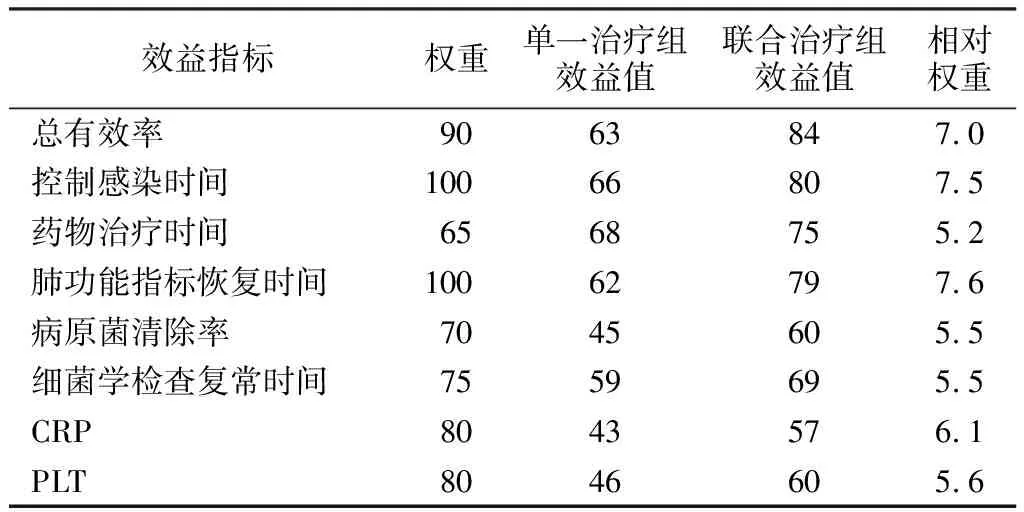
表4 治疗重症肺部感染患者的效益值比较
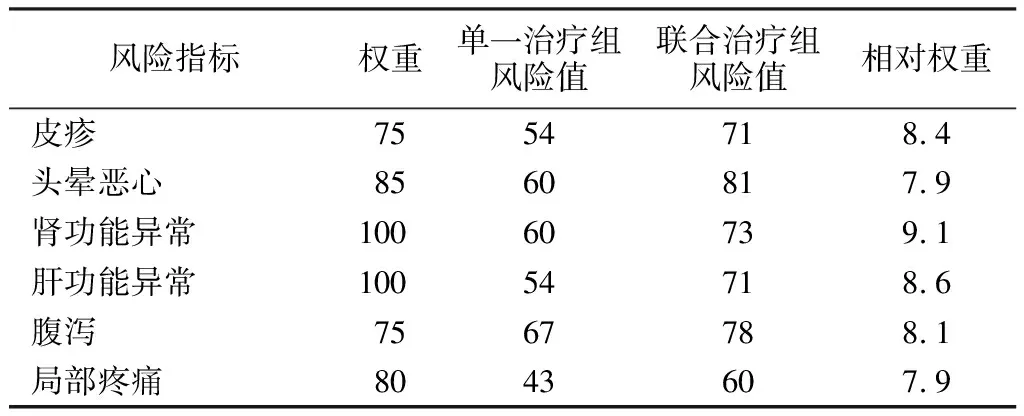
表5 治疗重症肺部感染患者的风险值比较
2.5 综合效益值、风险值的比较 综合效益和风险值发现联合治疗组的效益-风险值为75,比单一治疗组(58)高出17,95%CI(13.59~27.19),联合治疗组总效益-风险值高于单一治疗组的概率达100%,见图2、3。

图2 治疗重症肺部感染患者的效益-风险值
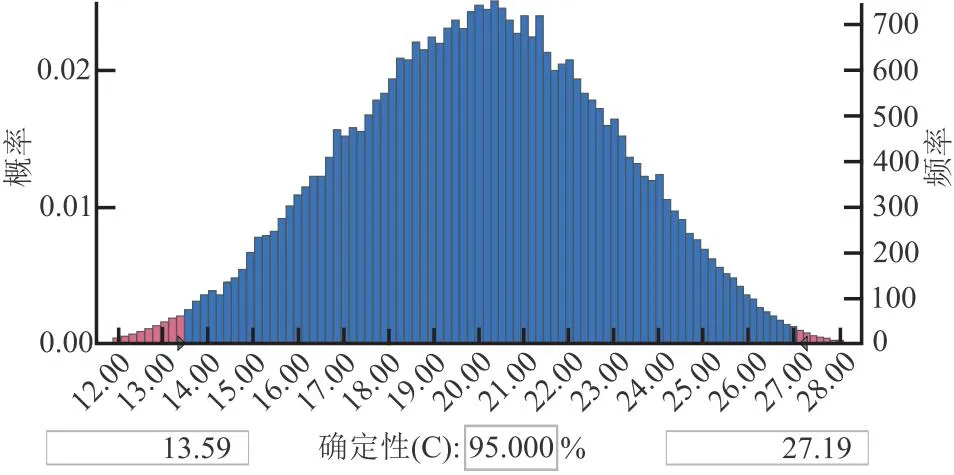
图3 治疗重症肺部感染患者的效益-风险差异模拟
2.6 效益-风险评价敏感性分析 亚胺培南联用头孢哌酮-舒巴坦治疗重症肺部感染患者的效益和风险同等重要,在0~100%风险相对权重范围内,联合治疗组的效益-风险总值总是高于单一治疗组,风险相对权重无论如何改变,评价结果都将保持不变,见图4,表明多准则决策评价模型的稳定性较好。
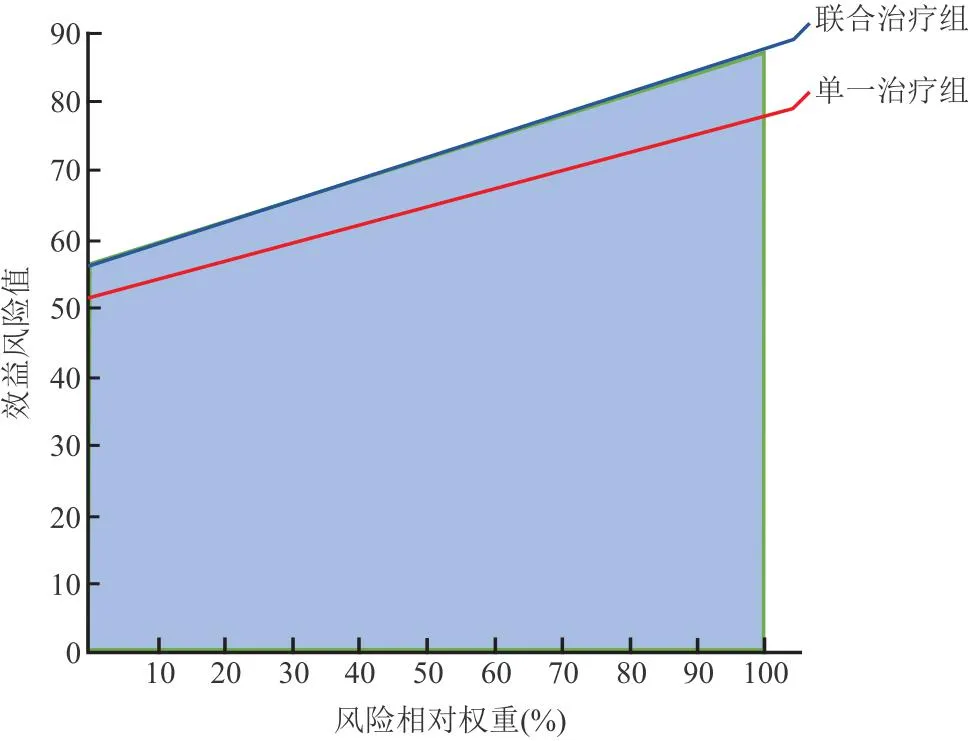
图4 治疗重症肺部感染患者的效益-风险评价敏感性分析
3 讨论
重症感染被认为是重症监护病房患者的重要预后决定因素,免疫能力较低患者的重症肺部感染可由多种细菌微生物引起,最常见的微生物是需氧革兰氏阴性杆菌,包括铜绿假单胞菌、肠杆菌科和不动杆菌[9-11]。虽然这些病原体都可能导致肺炎,但多种微生物感染的比率正在增加。在嗜中性粒细胞减少的癌症患者中,耐多药病原体感染可导致严重的发病率和死亡率,无其他体征和症状的发热通常是这些患者感染的最常见表现[12]。因此,早期和有效的抗生素治疗被认为是最大化生存的关键。碳青霉烯类抗生素(亚胺培南、美罗培南)是重症感染中最有效的抗生素之一,因为其满足了医学上对具有广谱活性、快速杀菌作用、有限促药特性和良好耐受性的化合物的需求[13]。
亚胺培南是第一个被发现的碳青霉烯类药物,具有强大高效的安全性以及广谱抗菌作用[14]。但在抗生素耐药性的时代为重症感染患者选择合适的初始治疗方案至关重要。由于重症感染患者出现耐多药病原体的风险更大,因此应开始接受广谱覆盖的治疗[15]。亚胺培南因其对医院获得性肺炎、腹腔内感染、败血症和发热性中性粒细胞减少症等适应证的疗效和安全性而成为降阶梯治疗的核心药物,多年来,亚胺培南对重要的细菌病原体保持了持续的临床疗效、耐受性和体外活性[16]。由于亚胺培南容易被位于肾小管中的脱氢肽酶-1降解,故一般与脱氢肽酶-1抑制剂西司他丁共同给药。西司他丁是一种肾肽酶抑制剂,可保护亚胺培南在肾中不被破坏,不仅可以在体内保持亚胺培南的活性,而且可以降低亚胺培南的肾毒性,充分发挥亚胺培南的抗菌作用[17]。这可能也是本研究中联合用药组风险指标肾功能异常显著低于单一用药组的原因。
头孢哌酮-舒巴坦是常用的β-内酰胺/β-内酰胺酶抑制剂组合,对碳青霉烯类耐药细菌感染的耐药率相对较低。头孢哌酮具有广谱活性,其杀菌作用一般是通过抑制细菌细胞壁合成而达到的。舒巴坦已被证明可增加细菌分离株对β-内酰胺类抗生素的敏感性。此外其不但能抑制β-内酰胺酶的活性,还具有增强头孢哌酮抗菌活性的作用。因此,头孢哌酮-舒巴坦联合碳青霉烯类药物(亚胺培南)是治疗碳青霉烯耐药鲍曼不动杆菌的有效方法[18]。本研究结果显示,在总体疗效方面,使用联合用药组总有效率为91.49%,而单一治疗组为72.34%;且基于多准则决策分析,联合治疗组的效益-风险总值总是高于单一治疗组,这与聂雪平[19]的研究结果是一致的。在不良反应方面,报道的最常见的全身和局部不良事件包括恶心、呕吐和注射部位反应,接受头孢哌酮-舒巴坦治疗的患者更常发生腹泻,与本文研究结果一致。皮疹、瘙痒炎、发热和低血压的不良反应报道较少,亚胺培南已被报道与癫痫活动有关,除了剂量超过制造商推荐的剂量外,与亚胺培南诱发癫痫相关的其他危险因素包括肾损害、并发中枢神经系统疾病等[20]。而在本文中两组不良反应发生率均较少,说明在临床上两种抗生素都比较安全。
尽管亚胺培南和头孢哌酮-舒巴坦都具有同样广泛的抗菌活性,但与头孢哌酮-舒巴坦相比,亚胺培南的胃肠道穿透性要低得多[21]。因此,治疗潜在的真菌定植和感染可能更多会与头孢哌酮-舒巴坦联用。本文基于多准则决策的研究结果也显示,亚胺培南联用头孢哌酮-舒巴坦治疗重症肺部感染患者的效益价值更高。
4 结论
亚胺培南联用头孢哌酮-舒巴坦治疗重症肺部感染的效果显著,可明显改善治疗过程中的相关指标以及不良反应发生率,具有临床推广价值。

