妊娠期高血压患者血清APOC4、APOA1 和FABP4 变化及意义
宋丽妞
(河南科技大学第一附属医院门诊部,河南 洛阳 471000)
妊娠高血压(Hypertensive disorder complicating pregnancy,HDCP) 是妊娠期特有的并发症,常导致早产、低体重初生儿和围产儿死亡,多于妊娠20 周后发病,临床常分类为妊娠期高血压(Gestational hypertension,GH)、 子痫前期(Preeclampsia,PC)和慢性高血压合并妊娠(Chronic hypertension complicated pregnancy,CHCP)[1-2]。 患者临床表现为高血压、蛋白尿和全身功能紊乱,具有较高的发病率和死亡率。 妊娠常影响人体糖脂代谢水平,至妊娠后期患者常表现为高脂血症状态, 加重妊娠期高血压病情进展, 导致孕妇子宫和胎盘处小动脉急性动脉粥样硬化,胎儿生长受限和宫内窘迫[3-4]。载脂蛋白(Apolipoprotein ,APO)可有效调节脂蛋白转化酶活性,是脂类运输的重要携带物质,常与受体结合后利于脂质为细胞摄取并利用, 相关研究报道, 血浆中不同APO 浓度与妊娠期高血压疾病密切相关[5]。 脂肪酸结合蛋白4(Fatty acid binding protein 4,FABP4)是临床常见的小分子载体蛋白,其对脂肪酸具有较高的亲和力, 参与糖脂代谢和妊娠高血压病情进展[6]。 本次研究旨在探讨妊娠期高血压患者血APOC4、APOA1 和FABP4 变化及意义,现整理如下。
1 资料与方法
1.1 一般资料 选取2018 年1 月至2021 年1 月我院收治的HDCP 患者90 例,根据中华医学会妊娠期高血压疾病诊治指南(2015)标准[7]将本研究中入组病例分组为GH 组(n=63)和PC 组(n=27)。 纳入标准:满足妊娠期高血压疾病诊治指南(2015)对HDCP 诊断标准;均为单胎妊娠;妊娠次数<3 次。排除标准:既往有高血压病史;肝肾功能不全;合并血液系统疾病;合并恶性肿瘤;认知功能障碍;临床资料不完整。 妊娠期高血压:年龄32~38 岁,平均年龄(35.36±1.27)岁;孕前期BMI 26~31 kg/m2,平均孕前期BMI(28.47±1.23) kg/m2;妊娠次数1~3 次,平均妊娠次数(2.05±0.24)次。子痫前期:年龄32~38 岁,平均年龄(35.23±1.38)岁;孕前期BMI 25~26 kg/m2, 平均孕前期BMI (28.31±1.33)kg/m2;妊娠次数1~3 次,平均妊娠次数(2.16±0.18)次。比较两组年龄、孕前期BMI 和平均妊娠次数无显著差异(P>0.05)。
1.2 方法
1.2.1 一般资料 根据本研究目的自行设计调查表,通过电子病历系统采集患者年龄、妊娠次数、孕前期BMI、学历水平、家族史等一般资料。
1.2.2 检测APOC4、APOA1 和FABP4 水平 入院后采集患者空腹静脉血5 mL 保存于不抗凝试管,离心(德国Hettich MIKRO220/220R 离心机)并分离血清(3 000 r,10 min),取上层清液置于-20 ℃冰箱保存,从采集到检验≤2 h。采用化学发光法检测患者血清APOA1 水平,仪器选择罗氏Cobas 6000全自动电化学发光分析仪, 试剂盒和试剂均由上海雅吉生物技术有限公司提供。 采用酶联免疫吸附 试 验 法 (Enzyme linked immunosorbent assay,ELISA)检测患者FABP4 和APOC4 水平,仪器采用SpectraMax iD5 多功能微孔板酶标仪,试剂和试剂盒由武汉菲恩生物科技有限公司提供, 操作过程严格根据仪器和试剂说明书进行。
1.2.3 24 h 尿蛋白定量 入院后准确留取24 h 尿液并添加甲苯防腐剂,采用干化学法测定患者24 h尿蛋白定量,仪器选择日立7600-020 全自动生化分析仪, 试剂和试剂盒由上海一研生物科技有限公司提供。
1.3 统计学方法 采用SPSS 22.0 统计学软件进行HDCP 患者一般资料分析,满足正态分布且方差齐的计量资料采用(±s)表示,采用两样本独立t检验比较两组组间差异,计数资料用率表示,采用χ2检验。 采用Pearson相关性分析APOC4、APOA1 和FABP4 水平与HDCP 患者病情严重程度关系,P<0.05 为差异有统计学意义。
2 结果
2.1 GH 组和PC 组一般资料比较 GH 组与PC 组年龄、妊娠次数、孕前期BMI、学历水平、家族史、睡眠时间、 不良生活方式和家庭月收入等一般资料比较无显著差异(P>0.05),见表1。
表1 GH 组和PC 组一般资料比较(±s)[n(%)]

表1 GH 组和PC 组一般资料比较(±s)[n(%)]
一般资料 GH 组(n=63) 子痫前期(n=27) χ2/t 值 P年龄(岁)<35 岁≥35 岁妊娠次数1 次2 次孕前期BMI(kg/m2)学历水平大专及大专以下大专以上家族史1.929 0.165 38(86.36)25(56.82)12(27.27)15(34.09)1.323 0.25 34(77.27)29(65.91)28.47±1.23 11(25.00)16(36.36)28.31±1.33 0.552 1.929 0.582 0.165 38(86.36)25(56.82)12(27.27)15(34.09)0.106 0.745有无睡眠时间(h)不良的生活方式35(79.55)28(63.64)7.12±0.78 16(36.36)11(25.00)7.03±0.890.408 0.239 0.632 0.626有无家庭月收入41(93.18)22(50.00)4652.23±213.36 19(43.18)8(18.18)4685.74±243.87 0.658 0.514
2.2 GH 组 和PC 组APOC4、APOA1 和FABP4 水平比较 GH 组APOC4 和FABP4 显著低于PC 组,APOA1 显著高于PC 组(P<0.05),见表2。
表2 两组APOC4、APOA1 和FABP4 水平比较(±s)
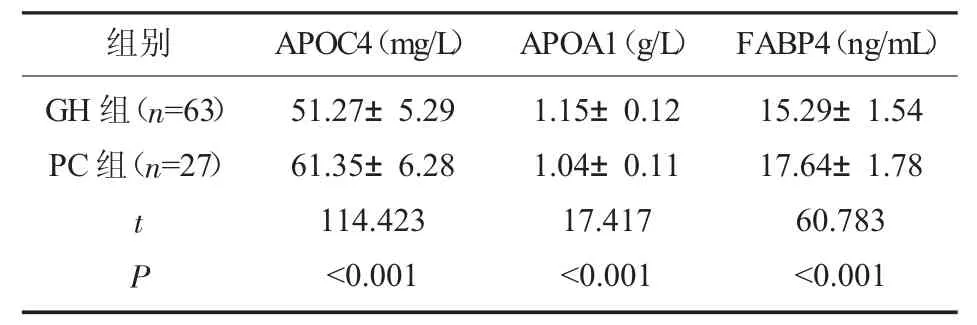
表2 两组APOC4、APOA1 和FABP4 水平比较(±s)
组别 APOC4(mg/L)GH 组(n=63)PC 组(n=27)t P 51.27±5.29 61.35±6.28 114.423<0.001 APOA1(g/L)1.15±0.12 1.04±0.11 17.417<0.001 FABP4(ng/mL)15.29±1.54 17.64±1.78 60.783<0.001
2.3 GH 组和PC 组血压和尿蛋白水平比较 GH组收缩压、舒张压和24 h 尿蛋白定量显著低于PC组(P<0.05),见表3。
表3 两组血压和尿蛋白水平比较(±s)
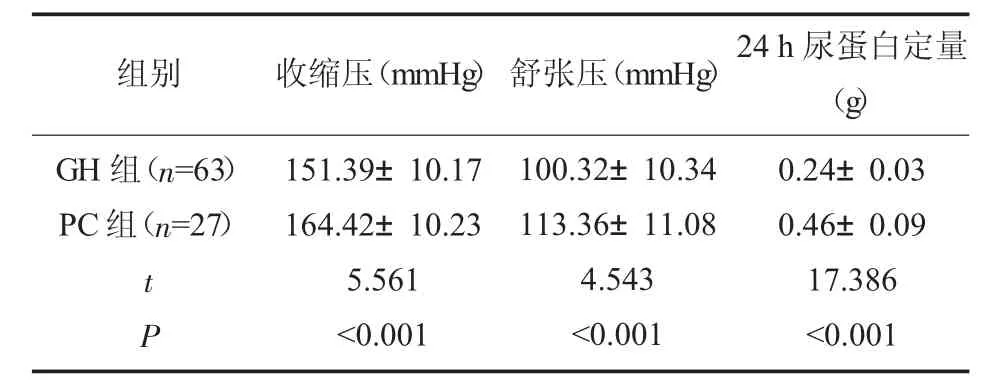
表3 两组血压和尿蛋白水平比较(±s)
组别 收缩压(mmHg)舒张压(mmHg)GH 组(n=63)PC 组(n=27)t P 151.39±10.17 164.42±10.23 5.561<0.001 100.32±10.34 113.36±11.08 4.543<0.001 24 h 尿蛋白定量(g)0.24±0.03 0.46±0.09 17.386<0.001
2.4 相关性分析APOC4、APOA1 和FABP4 水平与HDCP 严重程度关系 APOC4 与HDCP 严重程度呈正相关 (r=0.221,P<0.05),FABP4 水平与HDCP严重程度呈正相关 (r=0.215,P<0.05),APOA1 与HDCP 严重程度呈负相关(r=-0.252,P<0.05),见表4。

表4 APOC4、APOA1 和FABP4 水平与HDCP 严重程度的相关性分析
3 结论
妊娠期妇女由于内分泌水平变化常呈现不同水平血脂变化差异, 其血脂过度改变与妊娠期疾病关系密切。 自妊娠早期至妊娠末期孕妇血脂水平不断升高,显著增加HDCP 发病风险,随血脂水平升高患者血液粘稠度不断增加, 导致血液中血脂大量沉积于胎盘血管壁并损伤血管内皮细胞,不利于胎盘和胎儿发育[8-10]。 APOC4、APOA1 和FABP4 均是机体参与脂代谢的重要蛋白, 本研究比较了GH 组与PC 组年龄、 妊娠次数、 孕前期BMI、学历水平、家族史、睡眠时间、不良生活方式和家庭月收入等一般资料,发现均无显著差异,提示本研究中所取样本具有较高的可比性。 结果显示,GH 组APOC4 和FABP4 显 著 低 于PC 组,APOA1 显著高于PC 组。APOE 是临床常见富含甘油三酯和胆固醇和脂蛋白成分, 其功能是通过肝细胞摄取乳糜微粒、VLDL 和HDL,进而介导脂蛋白清除[11]。 其中APOC4 是在肠道和肝脏合成的脂质结合蛋白, 通过影响脂蛋白代谢的酶和受体达到控制胆固醇代谢的目的,APOC4 参与血液和淋巴组织运输脂质, 而脂质水平与饮食中脂肪的含量有密切的关系,既往研究报道[12],子痫前期患者血清APOE 和APOC3 水平均显著升高, 与本研究中部分结果相类似, 分析原因可能与子痫前期患者体内氧化应激水平与炎症因子水平有关,APOE 中含有某种特殊生理机制可能激活脂蛋白脂肪酶并促进甘油三酯的清除过程, 进而增加子痫的进展风险,但该研究中并未对APOC4 水平变化及与妊娠高血压疾病关系行进一步探讨。 本研究中子痫前期患者APOC4 水平显著高于妊娠期高血压,APOC4 基因位于19 号染色体APO E/C1/C4/C2 基因簇,其外显子Leu36Pro 和Leu96Arg 多态性与血脂水平关系密切[13]。Low-Kam C 等[14]的研究报道了血浆中80% APOC4 存在于低密度脂蛋白中,余下20%存在于高密度脂蛋白中。 故推测APOC4 水平变化与糖脂代谢有内在关系, 其可能通过脂质代谢作用于血管内皮细胞参与HDCP 疾病进展。 血管内皮细胞是覆盖于血管内壁的上皮细胞, 其作用是分开血管腔并利于血液流动, 具有调节血管收缩功能、 防血小板黏附和防炎症细胞浸润的作用[15],子痫前期患者APOC4 水平较低,患者内皮细胞功能相对较差,故引发血小板黏附、血栓形成和全身小动脉痉挛的风险显著增加。
FABP4 是细胞质基质蛋白家族中一员, 多存在于成熟脂肪细胞, 可逆性结合于各种疏水性配体,具有调节糖脂代谢、巨噬细胞胆固醇积聚和介导炎症反应的作用。 本研究结果显示,随HDCP 疾病进展, 患者由妊娠期高血压进展入子痫前期后FABP4 表达显著增加。 有学者在对大鼠妊娠高血压脂代谢水平与FABP4 的相关性研究中发现[16],糖脂代谢水平和炎症水平与FABP4 表达呈正相关,FABP4 通过影响脂代谢水平和介导炎症反应进而参与HDCP 发病与进展, 与本研究中部分观点相类似, 故认为HDCP 患者由于巨噬细胞积累所致脂肪组织的炎症反应,FABP4 表达水平低将导致巨噬细胞炎症水平降低, 可有效控制HDCP病情发展。 本研究中子痫前期患者APOA1 水平低于妊娠期高血压患者, 提示随HDCP 疾病严重程度增加,APOA1 水平不断下降。 APOA1 是肝脏和小肠合成的高密度脂蛋白的结构蛋白, 是243 个氨基酸残基组成的单一多肽链, 其分子中含有8个由22 个氨基酸残基组成的两亲性α 螺旋结构域,既可结合脂质,又可与水环境相互作用,具有体积最小、密度最大的特点,通过识别细胞壁上脂多糖和磷壁酸活化卵磷脂-胆固醇酰基转移酶,降低TLR4 的信号表达和传导, 抑制炎症因子的生成, 达到清除组织中的脂质而起到抗动脉粥样硬化的作用,具有高密度脂蛋白受体识别功能,故在正常妊娠期具有较高表达水平。 而高密度脂蛋白具有从血管中清除脂质的作用, 是血管的重要保护因子[17], 故认为子痫前期APOA1 下降可能与患者血管保护因素减弱有关。 行相关性分析发现,APOC4 水平、FABP4 水平与HDCP 严重程度呈正相关,APOA1 与HDCP 严重程度呈负相关,因此临床中可通过检测APOC4、FABP4 和APOA1 判断HDCP 疾病进展水平, 临床医师可以以此为参考,对HDCP 患者的治疗和预后有良好的指导意义。
综上所述,APOC4 和FABP4 与HDCP 严重程度呈正相关,APOA1 与HDCP 严重程度呈负相关,临床可通过检测APOC4、FABP4 和APOA1 水平判断HDCP 严重程度和预后恢复水平。

