血小板内皮聚集受体-1基因多态性与间歇性血液透析患者血管通路感染的相关性
闫晓辉,赵娟茹,梁 衍
(1.陕西省人民医院肾内科,陕西 西安 710065;2.陕西省人民医院老年病科,陕西 西安 710065)
间歇性血液透析(intermittent hemodialysis,IHD)是终末期肾病患者有效生存手段,且血管通路是血液透析顺利进行的基本保证[1-2],而血管通路感染可引起败血症、菌血症等并发症,严重时可导致患者死亡[3]。因此,寻找影响血管通路感染的因素对提高IHD患者临床治疗效果有重要意义。血小板内皮聚集受体-1(platelet endo thelial aggregation receptor 1,PEAR1)是血小板内皮聚集受体,不仅在血小板活化聚集过程中起着重要作用,也是评估血管内皮损伤的蛋白质,参与机体血管内皮相关的生理病理改变过程[4-5]。有研究表明,PEAR1的多个基因位点与激动剂诱导的血小板聚集活性显著相关[6-8]。但关于PEAR1基因多态性是否影响血液透析患者血管通路感染的发生发展尚未明确。基于此,本研究探讨IHD患者中PEAR1基因多态性与血管通路感染的相关性,以期为临床优化治疗措施提供借鉴。
1 资料与方法
1.1 一般资料
选择2019年1月至2022年1月于陕西省人民医院收治的105例接受IHD治疗的患者为观察组,另选择同期入院体检的50例健康者为对照组。纳入标准:(1)接受IHD治疗的患者透析时间1 a以上,且有完整透析记录,血管通路均为长期管路;(2)健康受试者均无肝肾功能不全;(3)无精神功能障碍,可正常交流,且病历资料齐全者;(4)受试者均为本人自愿、直系亲属支持参与,并签署知情同意书者。排除标准:(1)合并有获得性免疫缺陷综合征、淋病等特殊疾病者;(2)合并有影响PEAR1基因多态性检测结果的血液系统疾病者;(3)合并有严重心脑血管等实质性病变者;(4)存在脑外伤或出血性疾病者;(5)合并大面积外伤伴随全身感染者;(6)同时参与其他课题研究者。观察组:男76例,女29例;年龄55~75(65.35±3.33)岁;体质量指数(body mass index,BMI)20.18~26.72(23.35±2.18)kg·m-2。 对照组:男35例,女15例;年龄 56~75(65.74±3.41)岁;BMI 20.24~26.68(23.71±2.23)kg·m-2。观察组和对照组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究经陕西省人民医院伦理委员会审核批准。
1.2 荧光定量聚合酶链式反应(polymerase chain reaction,PCR)检测受试者PEAR1基因多态性
2组受试者入组后抽取10 mL空腹静脉血置于乙二胺四乙酸抗凝管中,然后进行全血DNA提取,提取步骤根据DNA提取试剂盒说明书进行操作,获得的DNA样本置于-20 ℃冷藏柜中保存。采用平台的扩增阻碍突变系统引物与多重Taqman MGB探针组合技术检测PEAR1基因的rs122937342c2位点多态性,PEAR1上游引物序列:5′-AAATGGAGGTGTCTTCCAAACC-3′,下游引物序列:5′-CCCAGTGAATCGGTCACAGA-3′。使用荧光定量PCR扩增,根据试剂盒及检测仪器要求进行操作。PCR反应体系:10×扩增缓冲液2.0 μL,dNTPs 2.0 μL,正反向引物各0.5 μL,r-Taq DNA聚合酶0.2 μL,DNA 200 μg,高压双蒸水补足反应总体积至20 μL。PCR扩增条件:94 ℃预变性180 s,94 ℃变性 30 s,55 ℃退火50 s,72 ℃延伸60 s,重复30个循环;再次72 ℃延伸5 min,获取PCR产物在 4 ℃ 环境下保存。限制性片段长度多态性实验:在恒定电压下,将DNA样品置于 0.4 g 琼脂糖熔化制成的琼脂糖凝胶中进行电泳,基因型条带使用凝胶成像系统记录,观察2组受试者PEAR1基因型和等位基因型分布,并行遗传平衡定律(哈迪-温伯格)检验。
1.3 IHD患者分组及临床资料收集
观察组患者入组24 h内进行影像学、血清学、病原学等检查,患者出现多形性红斑、紫瘢等症状,血清炎症因子异常升高,经CT检查显示血管通路长期出现不同程度的狭窄甚至闭塞,经病原学检查存在感染菌株可判断为血管通路感染。根据是否发生血管通路感染将IHD患者分为感染组(n=68)和未感染组(n=37),收集2组患者临床资料,包括性别、年龄、体温、BMI、收缩压(systolic blood pressure,SBP)、舒张压(diastolic blood pressure,DBP)、透析时间、透析频率、三酰甘油(triacylglycerol,TG)、总胆固醇(total cholesterol,TC)、低密度脂蛋白(low-density lipoprotein,LDL)、高密度脂蛋白(high-density lipoprotein,HDL)、肌钙蛋白T(troponin T,TnT)、白细胞(white blood cell,WBC)计数、血小板计数(platelet,PLT)、血细胞比容(hematocrit,Hct)、降钙素原(procalcitonin,PCT)、中性粒细胞/淋巴细胞比值(neutrophil/lymphocyteratio,NLR)、血小板/淋巴细胞比值(platelet/lymphocyteratio,PLR)、高血压史、糖尿病史、高血脂史、抽烟史、饮酒史等。
1.4 统计学处理

2 结果
2.1 观察组和对照组受试者PEAR1基因型与等位基因型分布及哈迪-温伯格平衡检验
2组受试者PEAR1基因位点有G和A 2个等位基因;检出3种基因型,包括野生型(GG)、突变杂合型(GA)、突变纯合型(AA)。观察组患者的GG基因型频率、G等位基因型频率均高于对照组,差异有统计学意义(P<0.05);2组基因位点等位基因频率符合均哈迪-温伯格平衡(P>0.05)。结果见表1。
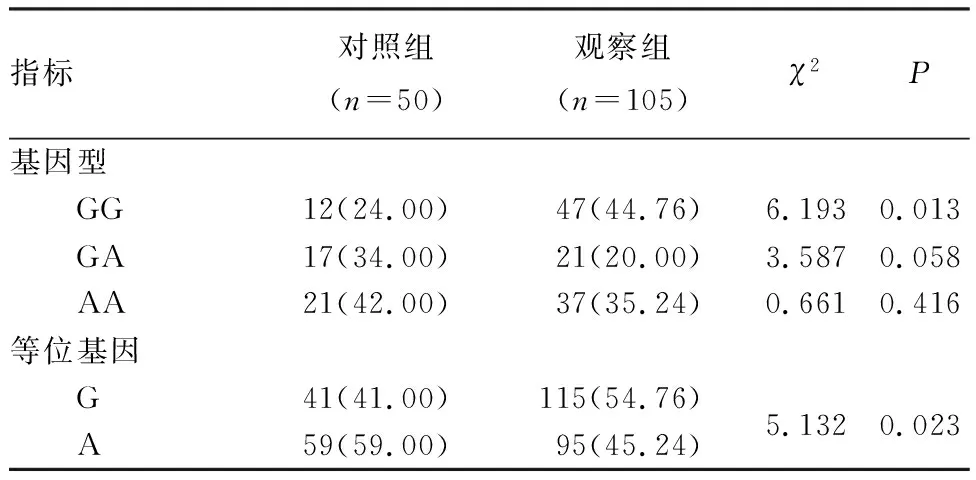
表1 观察组和对照组受试者PEAR1基因型及等位基因型分布比较Tab.1 Comparison of PEAR1 genotype and allele type distribution between the observation group and control group 例(%)
2.2 影响IHD患者发生血管通路感染的单因素分析
感染组与未感染组患者性别比例、体温、BMI、SBP、DBP、TC、TG、LDL和HDL水平及GA和AA基因型频率、高血脂史占比、抽烟史占比、饮酒史占比差异无统计学意义(P>0.05);未感染组患者年龄、透析时间≥3 a占比、透析频率1周≥3次占比、PEAR1 GG基因型频率、PEAR1 G等位基因频率及TnT、WBC、PLT、Hct、PCT、NLR和PLR水平和高血压史占比、糖尿病史占比均低于感染组,PEAR1 A等位基因频率高于感染组,差异有统计学意义(P<0.05)。结果见表2。
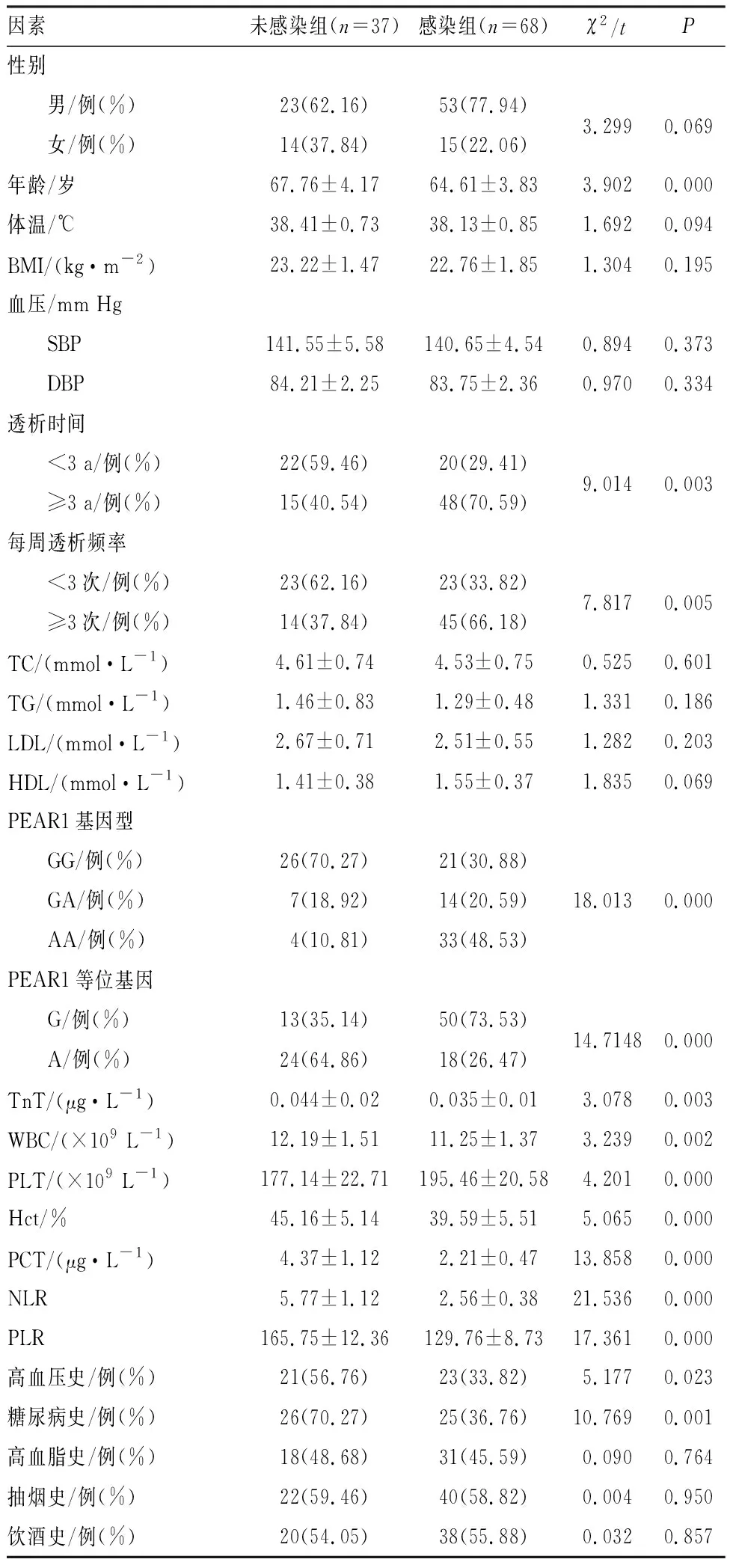
表2 影响IHD患者发生血管通路感染的单因素分析Tab.2 Univariate analysis of factors associated with the development of vascular access infection in patients with IHD
2.3 影响IHD患者发生血管通路感染的危险因素多因素分析
Logistic回归分析结果显示,透析时间长、年龄大及高透析频率、高NLR、高PLR和PEAR1携带G等位基因是IHD患者发生血管通路感染的危险因素(P<0.05)。结果见表3。
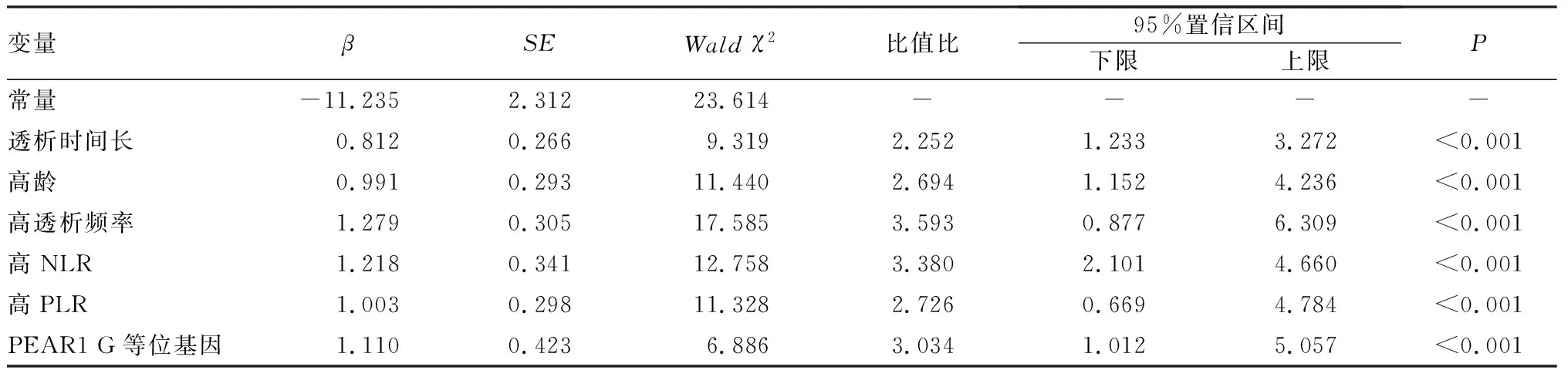
表3 IHD患者发生血管通路感染的危险因素多因素logistic分析Tab.3 Logistic regression analysis of risk factors affecting the development of vascular access infections in patients with IHD
3 讨论
相关研究显示,终末期肾病患者的肾脏无法维持机体内的新陈代谢,因此造成体内杂质无法排出;而利用IHD可快速有效地清除血液中各种有害、多余的代谢产物,但是在2次透析之间,体内会累及大量毒素和水分,导致患者因透析前、后体内水分及血压变化过大引起血流动力学不稳定,损伤心肺血管系统,进而增加患者血管通路感染风险,影响治疗效果[9-11]。有报道指出,IHD患者血管通路感染的发生发展受操作规范情况、卫生环境、血管相关疾病、基因易感性等多种因素的影响,其中基因的多态性可导致患者个体间的差异,并且相关基因突变会增加患者血管内皮细胞的易感性,给临床治疗带来较大挑战[12-13]。因此,及早了解影响患者血管通路感染的基因易感性,对临床针对性干预具有积极作用[14]。
PEAR1在血小板和内皮细胞中过表达,有研究发现,PEAR1基因的rs12041331携带A等位基因的血小板聚集活性增强,是炎症反应等多种激动剂促血小板聚集反应的关键部分[15-17]。有研究对PEAR1 rs12041331的AA纯合子及其与经皮冠状动脉患者病情进展情况进行相关性分析发现,与AA纯合子相比,GG+GA基因型频率偏高的患者血管内皮损伤相关疾病的发生风险增加3倍[18-19]。以上结果虽已表明,PEAR1基因多态性表达与血管内皮及炎症反应有一定相关性,但并未明确PEAR1基因多态性是否影响血液透析患者血管通路感染情况。本研究结果显示,2组受试者PEAR1基因位点有2个等位基因G和A,检出3种基因型,包括GG、GA、AA,哈迪-温伯格平衡值为0.229,提示所选样本具有群体代表性。本研究结果显示,感染组患者的PEAR1 GG基因型频率和G等位基因型频率均高于未感染组,提示PEAR1 rs12041331的基因型可能参与IHD患者血管通路感染的发生发展,临床可进一步探索PEAR1基因多态性对血液透析患者血管通路感染的影响。
本研究单因素分析显示,年龄、透析时间、透析频率、PEAR1 GG基因型频率及G等位基因频率、TnT、WBC、PLT、Hct、PCT、NLR和PLR水平、高血压史和糖尿病史是影响IHD患者血管通路感染的相关因素;多因素logistic分析结果显示,透析时间长、年龄大及高透析频率、高NLR和高PLR水平及PEAR1携带G等位基因是影响IHD患者发生血管通路感染的危险因素;说明PEAR1携带G等位基因与IHD患者血管通路感染的发生发展有显著相关性,G等位基因是IHD患者发生血管通路感染的易感基因,这提示早期检测血液透析患者的PEAR1基因型及等位基因频率对血液透析患者具有临床价值和意义。本研究评估PEAR1 rs122937342c2基因多态性与IHD患者血管通路感染情况的关系,研究结果将为临床抗炎和修复血管内皮损伤治疗的遗传易感性提供参考,同时为有效保护患者血管通路正常,保证长期血液透析顺利进行提供数据支持。
4 结论
PEAR1基因多态性表达与IHD患者血管通路感染存在相关性,G等位基因可作为IHD患者发生血管通路感染的易感基因,早期进行PEAR1基因多态性筛查对辅助临床判断血管通路情况提供参考,应用价值颇高。但本研究样本量较少,未进行前瞻性随机研究,具有一定的局限性;未来可进一步扩大样本量、延长血液透析时间并进行前瞻性研究验证PEAR1基因多态性表达与IHD患者血管通路感染的相关性。

