含铜430不锈钢在模拟生理盐水环境下的耐蚀性能研究
闫星宇,邹德宁,李苗苗,张英波,李雨浓
(西安建筑科技大学冶金工程学院,陕西 西安 710055)
0 前 言
430铁素体不锈钢是世界上用途最广泛的一种中等Cr含量的铁素体不锈钢[1],由于具有良好的机加工性能、强的耐腐蚀能力和较低的成本,被广泛应用于餐饮设施、家用电器以及医疗器械中[2-5]。铜是众多生物不可或缺的微量元素,也是重要的杀菌元素,含铜不锈钢已被证明拥有广谱抗菌性和优异的力学性能[6]。因此,在430铁素体抗菌不锈钢中添加铜有望提高材料的抗菌性能,可进一步拓宽其应用领域。不锈钢在服役过程中常常与含有氯离子的溶液接触,氯离子会影响不锈钢表面钝化膜的稳定性,是诱发不锈钢点蚀的重要原因之一[7,8],故对于不锈钢在氯离子溶液中的耐蚀行为研究至关重要。
铜作为一种合金元素,对不锈钢的耐蚀性能有很大的影响。Zhao等[9]制备了Mn-N双相不锈钢并研究了添加不同含量铜元素对其耐蚀性能的影响,发现0.5%Cu的加入可以显著提高不锈钢的抗点蚀能力;Xi等[10]研究了不同Cu含量分别对固溶处理和时效处理316L奥氏体不锈钢耐蚀性能的影响,认为在固溶处理后随着Cu含量的增加,不锈钢的点蚀电位以及保护电位增加,但在时效处理后随着Cu含量的增加点蚀电位以及保护电位逐渐降低;Jeon等[11]在WBASE双相不锈钢中加入Cu元素后,由于Cu元素的添加提高了Cr的活性,导致Cr、Mn、Fe等氧化物以及硫化物的数量和面积增多,进而降低了不锈钢的抗点蚀能力。但铜元素对430不锈钢耐蚀性能的研究鲜有文献报道,研究在工业化生产的430铁素体不锈钢中加入铜元素对其耐蚀性能的影响是非常有必要的。本工作所选用2种不同430铁素体不锈钢均为工业化生产,借助电化学测试、扫描电子显微镜(SEM)、能谱仪(EDS)和X射线光电子能谱仪(XPS)等表征手段,研究了铜元素对430铁素体不锈钢的耐蚀性、钝化膜特性和腐蚀后形貌的影响,以期为含铜430铁素体不锈钢在医疗器械中的应用提供参考。
1 试 验
所选材料为某钢铁集团生产的2种430铁素体不锈钢,由真空感应炉冶炼,经过热轧、冷轧、退火等工艺,最终轧制成厚度为0.6 mm的薄板,其化学成分如表1所示。试样经机械切割成10 mm×10 mm的金属薄片后,通过水磨砂纸进行打磨,用金刚石抛光剂对试样进行机械抛光,将试样放入乙醇溶液中超声波清洗15 min备用。
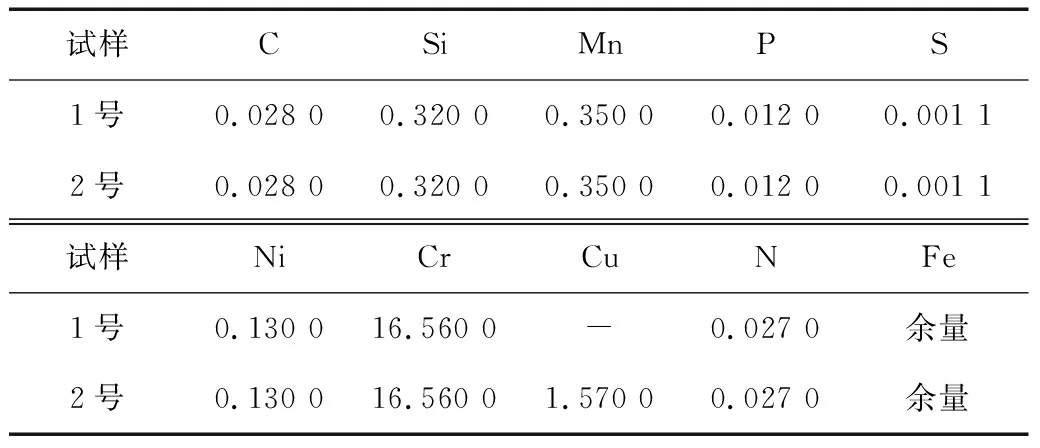
表1 试验钢的化学成分(质量分数) %Table 1 Chemical composition of test steel (mass fraction) %
电化学试验在GAMRY Reference 600+工作站常温下模拟生理盐水(质量分数0.9%NaCl)环境完成,分别使用动电位极化、交流阻抗谱以及Mott-Schottky测试研究了试验钢的腐蚀行为和钝化膜特性。动电位极化曲线扫描采用三电极体系,饱和甘汞电极(SCE)、铂电极分别作为参比电极和对电极,试验钢作为工作电极进行电化学测试,测试面积为1 cm2。每个试样进行3次重复试验。
开路电流电位测试时间为3 600 s,开路电位达到稳定,在0.1 V(vs SCE)条件下极化600 s去除试样表面氧化膜。动电位极化测试的扫描速率为5 mV/s,选用-0.5~0.5 V(vs SCE)为测试电位区间。交流阻抗测试频率范围为1.0×(106~10-2) Hz,正弦扰动电压为10 mV。
采用Mott-Schottky曲线研究Cu元素对430铁素体不锈钢钝化膜半导体特性的影响,首先对工作电极在电位为0.1 V(vs SCE)极化600 s以去除空气中形成的氧化膜,之后在0.3 V(vs SCE)条件下恒电位极化3 600 s使不锈钢表面形成钝化膜,测试频率为1 000 Hz,测试电位区间为-0.25~0.50 V(vs SCE),正弦扰动电压为10 mV。采用Thermo Escalab250 XI型X射线光电子能谱仪(XPS)对试样表面钝化膜进行成分分析,X射线源为Al Kα,加速电压为12 kV,发射电流为6 mA。
采用Gemini SEM 300场发射扫描电子显微镜(SEM)对2种试验钢显微组织进行分析,并对试验钢极化测试后表面点蚀形貌进行观察,结合附带能谱分析(EDS)对腐蚀后形貌进行面扫描以确定腐蚀后试样表面元素分布情况。
2 结果与讨论
2.1 电化学行为
图1为2种试验钢在模拟生理盐水(0.9%NaCl溶液)中的动电位极化曲线。可以从看出2种430铁素体不锈钢在阳极极化区均出现腐蚀电流密度增加缓慢、电位迅速升高的钝化行为,此钝化区间的出现与2种不锈钢在Cl-环境中都可形成稳定的钝化膜有关,这种膜进一步阻碍了腐蚀的进行[12]。同时,2号不锈钢极化曲线明显下移,表明维钝电流密度增加,试样表面钝化膜的溶解速率增大。2种不锈钢在过钝化电位之前都有一定程度的波动,且在经过过钝化电位前都产生一个转折点,该点为腐蚀过程中的点蚀电位。通过塔菲尔外推法对极化曲线进行了拟合,拟合出的电化学参数见表2,其中Ecorr为自腐蚀电位,Jcorr为自腐蚀电流密度,Eb为点蚀电位。加入Cu后430铁素体不锈钢的自腐蚀电流密度增大,自腐蚀电位减小,较大的腐蚀电流密度和较小的自腐蚀电位在一定程度上可以说明其腐蚀性倾向性越大,因此,在430不锈钢加入Cu元素后的腐蚀倾向性更大。1号试验钢点蚀电位大于2号试验钢的点蚀电位,说明2号试验钢比1号试验钢先进入过钝化区间,点蚀倾向更高,耐蚀性较差。上述现象说明,加入Cu元素后的430铁素体不锈钢的钝化膜对基体的保护作用减弱。

图1 2种试验钢在0.9%NaCl溶液中的动电位极化曲线Fig. 1 Potentiodynamic polarization curves of two experimental steels in 0.9%NaCl solution

表2 2种试验钢极化曲线Tafel拟合结果Table 2 Tafel fitting results of polarization curves for two types of experimental steels
为了进一步评估2种不锈钢的耐蚀性,测量其在0.9%NaCl溶液中的交流阻抗谱如图2所示。2种试验钢的阻抗谱均为容抗弧特征,说明2种430铁素体不锈钢有相似的阻抗特性。Nyquist阻抗谱只存在于在第一象限,频率由高到低时会依次出现高频容抗弧、中频容抗弧以及低频容抗弧,主要影响因素依次为电极表面的物质吸附、电极表面腐蚀产物膜、电极表面电荷转移的过程。根据得到的Nyquist阻抗谱可以看到,2种试验钢的容抗弧先后经过高频、中频以及低频,表明2种试验钢在电化学测试中表现出来的行为与试验钢表面化学吸附、钝化膜以及电荷转移有关[13]。1号相较2号容抗弧半径更大,表现出的阻抗值越大,耐蚀性越强。图2b Bode-相位角曲线中,1号试验钢在表征钝化膜的中频段相位角明显较高,在接近90°的相位角平台也更宽。因此,1号试验钢阻抗值较大,耐蚀性更好,表明430铁素体不锈钢中加入Cu元素后其钝化膜表现出的电容特性不稳定,电容响应特性变差。图2c Bode-阻抗谱中低频阻抗模值|Z|同样是不锈钢耐蚀性能中的重要参数,低频时模值|Z|越高,钝化膜的反应阻力越大,不锈钢耐蚀性越好。当频率为100 Hz时,1号试验钢阻抗模值|Z|为109.91 Ω·cm2,2号试验钢阻抗模值|Z|为32.60 Ω·cm2,表明2号试验钢钝化膜的电极反应阻力较小,相比于1号试验钢更容易进行电化学腐蚀。综上,在430铁素体不锈钢中加入Cu元素,减小了钝化膜反应阻力,增大了腐蚀速率。

图2 2种试验钢在0.9%NaCl溶液中交流阻抗谱Fig. 2 Two types of test steels in 0.9% NaCl solution
图3为所采用的等效电路图,拟合出的阻抗谱数据见表3。其中Rs为溶液电阻,Rct为电荷转移电阻,Rf为钝化膜电阻,CPE为双电层电容,Q为钝化膜电容,由Y0与n值来确定实际电容与理想电容的偏离程度,n值越大且接近于1时越接近理想电容。由数据可以看出,Rct值与Rf值在加入Cu元素后明显减小,n值相近,说明1号试验钢的电荷转移时的阻力以及钝化膜电阻较大,即发生反应时的电阻较大,相较于2号试验钢更加耐腐蚀。在等效元件中,拟合出的钝化膜电容Q值越大,钢表面形成的腐蚀产物膜越容易遭到破坏[14]。

图3 等效电路Fig. 3 Equivalent circuit diagram

表3 交流阻抗谱拟合参数结果Table 3 Results of AC impedance spectrum fitting parameters
因此Cu元素的加入降低了430铁素体不锈表面钝化膜的保护作用。
2.2 钝化膜分析
Mott-Schottky分析可以确定不锈钢钝化膜的类型、缺陷密度以及缺陷扩散率,研究钝化膜在不同电位下半导体特性和载流子密度。本工作利用钝化膜的微分电容C与外加电位E之间的Mott-Schottky关系,根据如下方程进行[15]:
(1)
式中,C为真空电荷层电容,F/m2;ε为钝化膜介电常数,F/m;ε0为真空介质介电常数,通常为8.85×10-12F/m;e为电子电荷,通常为1.6×10-19C;ND为施主密度,m-3;E为外加电位,mV;Efb为平带电位,mV;k为玻尔兹曼常数,为1.38×10-23J/K;T为绝对温度,K。通过Mott-Schottky曲线上线性斜率以及截距可以得到ND和Efb。
图4为2种不锈钢在0.9%NaCl溶液中的Mott-Schottky曲线。2种试验钢钝化膜的Mott-Schottky曲线形状非常相似,证实2种钢的钝化膜特性相似,Cu的加入并没有改变430铁素体不锈钢中钝化膜的半导体结构。在-0.25~0.50 V(vs SCE)施加电位下,在平带电位以上有1个线性区域且曲线斜率为正,表明2种试验钢的钝化膜都具有N型半导体行为,与2种钢的(Fe,Cr)氧化物有关[16]。表4列出了根据方程(1)计算的平带电势Efb和施主密度ND的值。平带电势(Efb)代表了一个主要电子缺陷在P型和N型半导体之间建立过渡的区域,它决定了导电离子在电解液中氧化还原电位的能带位置,电荷转移又控制这些位置跨越钝化膜半导体/电解质界面、半导体与电解质的接触电位、界面以及钝化膜半导体的稳定性[16]。施主密度ND随Cu元素的加入而降低,这意味着Cu的加入提高了钝化膜的阳离子空位浓度[11]。430铁素体不锈钢加入Cu元素后钝化膜半导体转化电位减小是由于富Cu相作为第二相析出对钝化膜的致密性造成影响,Cu元素的加入使得钝化膜中的电子转移加快,电子转移量相应增大,直接削弱了钝化膜的自我修复能力[17]。

图4 2种试验钢在0.9%NaCl溶液平带电势中的Mott-Schottky曲线Fig. 4 Mott Schottky curve test of two experimental steels in a flat band potential of 0.9%NaCl solution
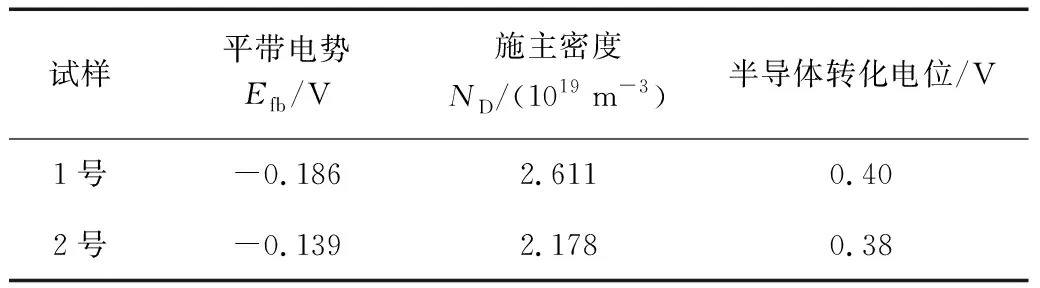
表4 2种试验钢的平带电势、掺杂密度以及钝化膜半导体转化电位Table 4 Flat band potential, doping density, and passivation film semiconductor conversion potential of two experimental steels
由电化学试验可知,在430铁素体不锈钢中加入Cu元素以后,改变了钝化膜中的化学成分。图5为1号和2号试验钢通过X射线光电子能谱仪(XPS)以及利用结合能评估钝化膜中的元素状态,钝化膜主要由Cr、Fe以及O等元素组成, 并且在2号试验钢钝化膜成分中发现了Cu元素。图5a,5b为Cr2p3/2的光电子能谱,分别存在Cr、Cr(OH)3和Cr2O33个组成峰,并且Cr(OH)3和Cr2O3的峰强度显著高于Cr,说明Cr元素中Cr(OH)3和Cr2O3对钝化膜起主要作用。图5c,5d拟合出了Fe2p3/2的光电子能谱,为Fe、FeO、Fe2O3以及FeOOH 4种组成峰,添加Cu元素后形成的FeO、Fe2O3以及FeOOH等铁氧化物或铁氢氧化物中的占比减少,表明Cu元素对铁氧化物的形成有抑制作用。图5e,5f为O 1s的光电子能谱拟合结果,得到了OH-、O2-和H2O 3种组成峰。图5g为2号试验钢钝化膜中得到的关于Cu2p3/2的光电子能谱,拟合得到了Cu、Cu2O和CuO 3种组成峰,表明Cu元素影响了2号试验钢表面钝化膜组成成分。
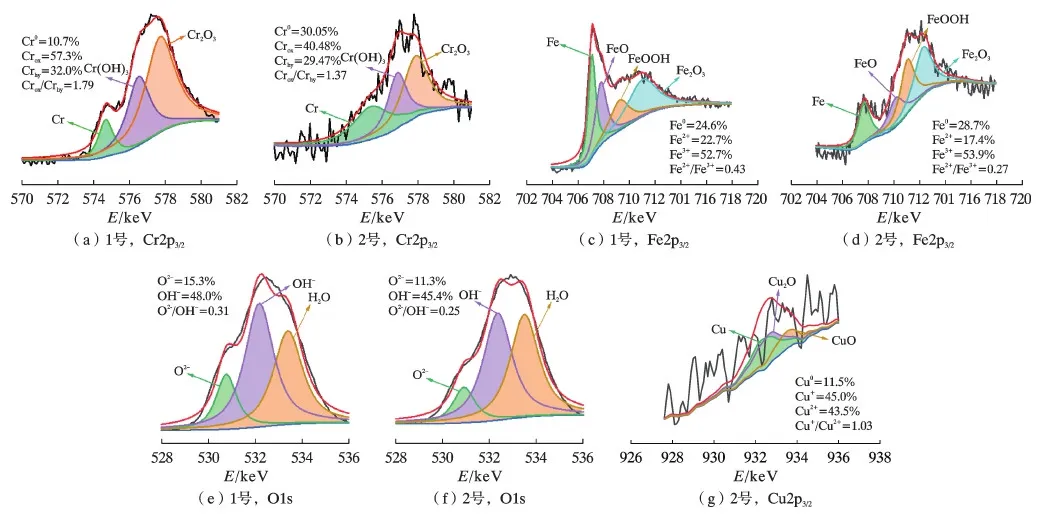
图5 2种试验钢在0.9%NaCl中钝化膜的XPS谱Fig. 5 XPS spectra of passivation films on two experimental steels in 0.9%NaCl
金属表面钝化膜的半导体特性与膜的化学成分有关[17],钝化膜中耐蚀性与Fe、Cr元素的富集有关。有文献表明[17],耐蚀性的提高主要是由于钝化膜中铬氧化物和铬氢氧化物的形成,Cr2O3和Cr(OH)3含量越高,钝化膜中的缺陷越少,由图5a,5b可以看到,加入Cu元素元素后2号试验钢表面钝化膜Cr2O3和Cr(OH)3含量降低,说明2号试验钢钝化膜中缺陷增多。由Fe2O3、FeOOH等缺陷铁氧化物组成的钝化膜通常表现为以电子导电为主的N型半导体性质,这是因为氧空位或阴离子空位占主导地位[18],而FeO、Cr2O3富集的钝化膜通常表现为以空穴导电为主的P型半导体性质,归因于阳离子空位[19,20],结合Mott-Schottky曲线以及XPS分析可以看出由于铁氧化物、铬氧化物等造成了不同性质离子空位,使得钝化膜表现出不同半导体特性;铜离子与铬离子争抢氧离子,抑制Cr2O3的生成,铜离子释放越多,形成的阳离子空位越多[21]。图5a,5b中的Cr2O3含量明显降低,从57.3%下降到40.48%,造成阳离子空位增多,根据电荷守恒原理,空位浓度的增加导致缺陷密度的增加,降低了钝化膜的稳定性。
2.3 金相组织及腐蚀形貌
图6为2种铁素体抗菌不锈钢显微组织及对应位置的EDS能谱分析,其中区域1、区域3能谱分析为不锈钢基体中元素含量,其余为析出第二相元素含量。可以看出2种不锈钢基体均为铁素体,元素浓度与试验钢元素浓度相近;点扫描结果表明区域2 Cr元素含量约是区域1 Cr元素的2倍,确定其为富Cr相;区域4的Cu元素含量是区域3基体Cu元素含量的23倍,与区域4类似的析出相为富Cu相,均匀弥散地分布在基体表面[22,23]。

图6 2种试验钢微观组织及能谱Fig. 6 Microstructure and energy spectroscopy of two experimental steels
图7为2种试验钢表面点蚀形貌。可以看到,2种钢腐蚀后形貌都可以看到点蚀坑,1号试验钢中的点蚀坑比2号试验钢点蚀坑尺寸小,深度较浅且数量少,2号试验钢表面形貌相较而言,破坏程度更大,间接表明添加Cu元素后的430不锈钢耐点蚀能力下降。

图7 2种430铁素体不锈钢腐蚀后形貌Fig. 7 Morphology of two types of 430 ferritic stainless steel after corrosion
图8为2种试验钢电化学腐蚀后的点蚀坑EDS分析。可看到2号试验钢腐蚀坑周围存在Cu元素,表明腐蚀坑周围有富Cu相存在,且点蚀坑氯离子浓度相较于1号试验钢点蚀坑较高,说明富Cu相在腐蚀过程中对钝化膜进行破坏,腐蚀液中的氯离子更容易击穿钝化膜,造成钝化膜的不连续性。

图8 2种试验钢腐蚀后EDS分析Fig. 8 EDS analysis of the morphology of two experimental steels after corrosion
Cu元素对430不锈钢耐蚀性能的影响,实质上是由于腐蚀行为对富Cu相较为敏感。富Cu相成分理论上接近于纯Cu,在发生腐蚀过程中,富Cu相与钝化膜相比有较低的腐蚀电位,进而形成了微电池结构[24],富Cu相优先基体产生点蚀,促进了试验钢溶解,最终导致钝化膜的不稳定。
3 结 论
(1)Cu元素的加入导致点蚀电位降低,使得材料容易进入过钝化区间,加剧了钝化膜的破坏,恶化了430铁素体不锈钢的耐蚀性。
(2)Cu元素的加入提高了钝化膜中的阳离子空位浓度,施主密度ND随合金元素的加入而降低,不利于钝化膜的修复,同时抑制了钝化膜中Cr2O3的生成,降低了钝化膜的稳定性。
(3)Cu元素的加入容易使得析出的富铜相与基体产生电势差,形成微电池结构,富铜相优先腐蚀,导致耐点蚀性能下降,恶化了430铁素体不锈钢的表面形貌。

