二地鳖甲颗粒的质量标准
周 华,孙志兴,刘 顺,王 婕,吴旭彤,袁加才
(1.江苏省中医院,江苏 南京 210029;2.南京中医药大学 翰林学院,江苏 泰州 225300)
勃起功能障碍(ED),是指阴茎持续不能达到或维持足够的勃起以完成满意的性交,且病程达3个月以上[1-2],为男科最常见的性功能障碍之一。中医学将之描述为痿而不举,举而不坚,坚而不久,简称为阳萎。ED的病因分为精神类因素、器质性因素以及其他类因素等。目前ED的病理机制尚不明确,刘继红等[3]和肖尧等[4]指出:与腺苷信号水平有关,其中,NO-cGMP通路调控作用的发现是最为经典,研究也最为深入的。器质性因素对于ED具有直接的影响作用,与神经、血管和内分泌等方面有着密切的联系[5]。尽管目前相关的研究并不多,但还是有通过中医药的方法调整神经、血管和内分泌等方面,以整体调节的方式治疗ED的报道[1]。
二地鳖甲方由生地黄、熟地黄、菟丝子、茯苓、枸杞子、金樱子、丹参、天花粉、续断、桑寄生、鳖甲、牡蛎、丹皮和五味子等14味中药组成,为江苏省中医院徐福松教授临床经验方,主要用于阴虚火旺为主要表现的阳痿等男科病症,且颇有良效[6-10]。其中,菟丝子、枸杞子、续断和五味子均归肾经,具有补肝益肾之功效,是古今治疗ED中运用较多的药方。
江苏省中医院对二地鳖甲方进行了继承与创新,在保证疗效的情况下,将其开发为单剂量包装的颗粒剂,提高了二地鳖甲煎剂的稳定性。为更有效控制该制剂质量,确保临床用药的安全性和有效性,笔者在参考大量文献的基础上,建立了二地鳖甲颗粒中菟丝子、枸杞子、续断和五味子的薄层色谱法(TLC),以及2种活性成分五味子醇甲和川续断皂苷Ⅵ同时测定的高效液相色谱法(HPLC);以期对二地鳖甲颗粒的质量进行更加快速全面的控制,为其品质与临床用药安全的提升提供参考。
1 仪器与方法
1.1 仪器设备
Acquity Arc型高效液相色谱仪,美国沃特世公司;CAPCELL PAK C18 MGⅡ型色谱柱(4.6 mm×150 mm,5 μm),日本曹达集团;AX224ZH/E型电子天平,常州市奥豪斯仪器有限公司;BP-211D型十万分之一电子天平,北京市赛多利斯天平公司;SK6200H型超声清洗器,上海市科导超声仪器有限公司;R19676D型100~1 000 μL可调移液器,德国eppendorf公司;2 mL一次性使用无菌注射器,江苏省苏云医疗器材有限公司;HH-2型数显恒温水浴锅,金坛杰瑞尔电器有限公司;VISUALIZER 2型TLC,瑞士CAMAG公司。
1.2 实验材料
硅胶G板(批号:2021010)、硅胶板GF254(批号:20191122、20170406),青岛市海洋化工有限公司;聚酰胺薄膜板(批号:20191009),台州市路桥四甲生化塑料厂。
五味子醇甲(批号:Y14F10H80840,纯度≥98%),川续断皂苷VI对照品(批号:Y14F10H80840、ZI8M10L83256,纯度≥98%),上海市源叶生物科技有限公司;菟丝子对照药材,枸杞子对照药材,续断对照药材和五味子对照药材(批号:121232-201403、121072-201611、121033-201812和120922-201610),中国食品药品检定研究院;二地鳖甲颗粒(批号:2012001、2012002和2012003),江苏省中医院制剂部自制。
1.3 实验方法
1.3.1 五味子薄层色谱的鉴别
取二地鳖甲颗粒适量,研细,称粉末约5 g,加20 mL热水溶解,冷却后,用经H2O饱和的三氯甲烷振摇提取2次,每次15 mL,弃去水液。合并三氯甲烷溶液,用三氯甲烷液蒸干,残渣加三氯甲烷1 mL使其溶解,即得。
取适量五味子对照药材和缺五味子的阴性制剂,分别制成五味子对照药材及缺五味子的阴性制剂供试品溶液。缺五味子的阴性制剂为原方中去除五味子药材,按制剂工艺进行制备所得制剂。
取适量五味子醇甲对照品,加三氯甲烷溶解制成五味子醇甲对照品溶液。
参照文献[11]的方法,依次吸取上述4种溶液适量,点样于同一硅胶GF254薄层板上,以石油醚-甲酸乙酯-甲酸(30~60 ℃,体积比15∶5∶1)的上层溶液展开,取出晾干后,置于紫外光灯254 nm下检视。
1.3.2 菟丝子薄层色谱的鉴别
取二地鳖甲颗粒适量,研细,称粉末约1 g,加甲醇20 mL,水浴加热回流30 min,过滤,滤液浓缩至2 mL,即得。
取适量菟丝子对照药材和缺菟丝子的阴性制剂,同法分别制成菟丝子对照药材与缺菟丝子的阴性制剂供试品溶液。缺菟丝子的阴性制剂为原方中去除菟丝子药材,按制剂工艺进行制备所得制剂。
另取适量金丝桃苷对照品,加甲醇溶解制成金丝桃苷对照品溶液。
分别取上述供试品溶液、对照药材溶液、阴性样品溶液和对照品溶液适量,点于同一块聚酰胺薄膜板,以冰醋酸-水(体积比1∶1)展开,取出,晾干后,喷体积分数为5% AlCl3溶液,于105 ℃加热5 min,待冷却后,置于紫外灯366 nm下检视。
1.3.3 枸杞子薄层色谱的鉴别
参照文献[12]的方法,取二地鳖甲颗粒适量,研细,称粉末约1 g,加H2O 10 mL,超声处理30 min,过滤,滤液用经H2O饱和的乙酸乙酯振摇提取3次,每次20 mL,弃去水液,合并乙酸乙酯液,经乙酸乙酯液蒸干后,残渣加乙酸乙酯1 mL使其溶解,即得。
取适量枸杞子对照药材和缺枸杞子的阴性制剂,同法分别制成枸杞子对照药材和缺枸杞子的阴性制剂供试品溶液。缺枸杞子的阴性制剂为原方中去除枸杞子药材,按制剂工艺进行制备所得制剂。
分别取上述供试品溶液、阴性样品溶液和对照药材溶液适量,点于同一硅胶G薄层板上,参照文献[13]的方法,以乙酸乙酯-三氯甲烷-甲酸(体积比为3∶2∶1)溶液展开,取出晾干后,置于紫外光灯366 nm下检视。
1.3.4 续断薄层色谱的鉴别
参照文献[14]的方法,取二地鳖甲颗粒适量,研细,称粉末约5 g,加甲醇20 mL,超声处理30 min,过滤,滤液蒸干后,残渣加水20 mL使其溶解,用经H2O饱和的正丁醇振摇提取2次,每次20 mL,弃去水液,合并正丁醇液,用20 mL氨试液洗涤,弃去NH3·H2O,经正丁醇液蒸干,残渣加甲醇1 mL使其溶解,即得。
取适量续断对照药材及缺续断的阴性制剂,同法分别制成续断对照药材和缺续断的阴性制剂供试品溶液。缺续断的阴性制剂为原方中去除续断药材,按制剂工艺进行制备所得制剂。
取适量川续断皂苷Ⅵ对照品,加甲醇制成续断皂苷Ⅵ对照品溶液。
分别取上述供试品溶液、阴性样品液、对照药材溶液和对照品溶液适量,点于同一硅胶G薄层板上,以三氯甲烷-甲醇-10%(体积分数)NaOH(体积比为17∶7∶2)的下层溶液展开,取出晾干,喷以体积分数10% H2SO4甲醇溶液,于105 ℃加热至斑点显色清晰,在紫外光灯366 nm下检视,再置于日光下检视。
1.3.5 色谱条件
CAPCELL PAK C18 MGⅡ型,4.6 mm×150 mm色谱柱;纯H2O(A)-乙腈(B)作为流动相,检测波长为212 nm,柱温为30 ℃,流速为1.00 mL/min,进样体积为10 μL,梯度洗脱程序见表1。
1.3.6 对照品溶液的制备
取适量川续断皂苷Ⅵ对照品,精密称量后,加甲醇溶解,制成质量浓度为128.9 μg/mL溶液,作为川续断皂苷Ⅵ对照品溶液;取适量五味子醇甲对照品,精密称定后,加甲醇制成质量浓度为51 μg/mL溶液,作为五味子醇甲对照品溶液。
分别取上述2种对照品溶液适量,置于10 mL容量瓶中,制成含51.56 μg/mL川续断皂苷Ⅵ与10.2 μg/mL五味子醇甲的混合对照品溶液。
1.3.7 供试品溶液的制备
精密称定二地鳖甲颗粒粉末样品约1 g,置于25 mL棕色容量瓶,加甲醇适量,超声处理30 min,放至室温后,以甲醇定容至刻度,用0.22 μm滤膜过滤,取续滤液,即得。
1.3.8 阴性样品溶液的制备
分别取缺续断、缺五味子的阴性制剂适量,按1.3.7节方法制成阴性样品溶液。缺续断、缺五味子的阴性制剂为原方中分别去除续断、五味子药材,分别按制剂工艺进行制备所得制剂。
1.3.9 方法学的考察
1.3.9.1 专属性实验
分别取上述混合对照品溶液、二地鳖甲颗粒供试品溶液2种阴性样品溶液,按照1.3.5节色谱条件,进样10 μL,进行专属性实验。
1.3.9.2 线性关系实验
取适量川续断皂苷Ⅵ对照品溶液和五味子醇甲对照品溶液,精密称取,配制成质量浓度分别为51.56、10.2 μg/mL的初始混合对照品溶液。将初始混合对照品溶液精密稀释0、2、4、8、10和20倍,分别进样10 μL。按照1.3.5节色谱条件进行进样测定并记录川续断皂苷Ⅵ和五味子醇甲的峰面积。以色谱峰面积为纵坐标(Y),混合对照品质量浓度为横坐标(X),绘制标准曲线并进行线性回归。
1.3.9.3 精密度实验
精密吸取1.3.6节的川续断皂苷Ⅵ和五味子醇甲的混合对照品溶液,按照1.3.5节的色谱条件重复进样6次,每次10 μL,记录川续断皂苷Ⅵ和五味子醇甲的峰面积,计算相对标准偏差(RSD)。
1.3.9.4 重复性实验
分别称取同批颗粒6份,按照1.3.7节方法制成供试品,按照1.3.5节的色谱条件分别进样10 μL,测定并记录川续断皂苷Ⅵ和五味子醇甲的峰面积,计算RSD。
1.3.9.5 稳定性实验
取1.3.9.4节供试品溶液适量,分别于供试品溶液制备后0、2、4、8、12和24 h进样10 μL,测定并记录川续断皂苷Ⅵ和五味子醇甲的峰面积,计算RSD。
1.3.9.6 加样回收实验
精密称定二地鳖甲颗粒约0.5 g,共6份,分别加入川续断皂苷Ⅵ和五味子醇甲对照品适量,按1.3.7节的方法制备成供试品溶液,并按照1.3.5节的色谱条件进行测定。记录川续断皂苷Ⅵ、五味子醇甲的峰面积,计算加样回收率。
1.3.10 样品含量的测定
取3批二地鳖甲颗粒样品,按照1.3.7节的方法制备供试品溶液,按照1.3.5节的色谱条件分别进样10 μL,记录峰面积,并计算川续断皂苷Ⅵ含量与五味子醇甲含量。
2 结果与讨论
2.1 五味子薄层色谱的鉴别结果
五味子供试品薄层色谱的鉴别结果见图1。由图1可知:在与五味子对照药材、五味子醇甲对照品色谱相应的位置上,显出相同颜色的斑点,且阴性样品无干扰。

注:1为供试品溶液,2为五味子醇甲对照品溶液,3为缺五味子的阴性样品溶液,4为五味子对照药材溶液
2.2 菟丝子薄层色谱的鉴别结果
菟丝子供试品薄层色谱的鉴别结果见图2。由图2可知:在与菟丝子对照药材、金丝桃苷对照品色谱相应的位置上,显出相同颜色的斑点,且阴性样品无干扰。
2.3 枸杞子薄层色谱的鉴别结果
枸杞子供试品薄层色谱的鉴别结果见图3。由图3可知:在与枸杞子对照药材色谱相应的位置上,显出相同颜色的斑点,且阴性样品无干扰。
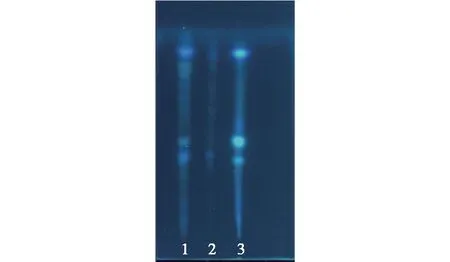
注:1为供试品溶液,2为缺枸杞子的阴性样品溶液,3为枸杞子对照药材溶液
2.4 续断薄层色谱的鉴别结果
续断供试品薄层色谱的鉴别结果见图4。由图4可知:在与续断对照药材、川续断皂苷Ⅵ对照品色谱相应的位置上,显出在相同颜色的斑点,且阴性样品无干扰。
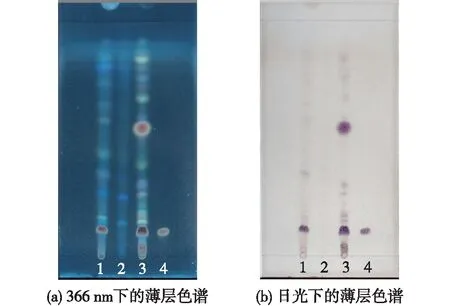
注:1为供试品溶液,2为缺续断的阴性样品溶液,3为续断对照药材溶液,4为川续断皂苷VI对照品
2.5 专属性的考察实验结果
专属性的考察实验结果见图5。由图5可知:阴性样品色谱在混合对照品色谱上无对应的色谱峰出现,说明阴性样品无干扰,此方法具有专属性。
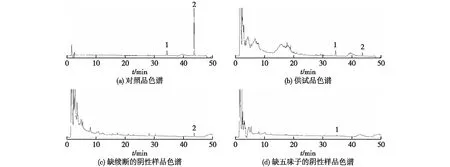
图5 专属性实验考察结果
2.6 线性关系的考察实验结果
线性关系考察得川续断皂苷Ⅵ的回归方程为Y=2.123 8X-8.860 1,r=0.999 9;五味子醇甲的回归方程为Y=59.988X+0.275 7,r=0.999 5。结果表明:川续断皂苷Ⅵ在2.578~51.560 μg/mL,五味子醇甲在0.510~10.200 μg/mL时,线性关系良好,可用于准确定量。
2.7 方法学的考察实验结果
五味子醇甲、川续断皂苷Ⅵ的HPLC精密度、重复性、稳定性和加样回收率结果见表2。由表2可知:本实验建立的方法具有良好的精密度、重复性、稳定性和加样回收率。
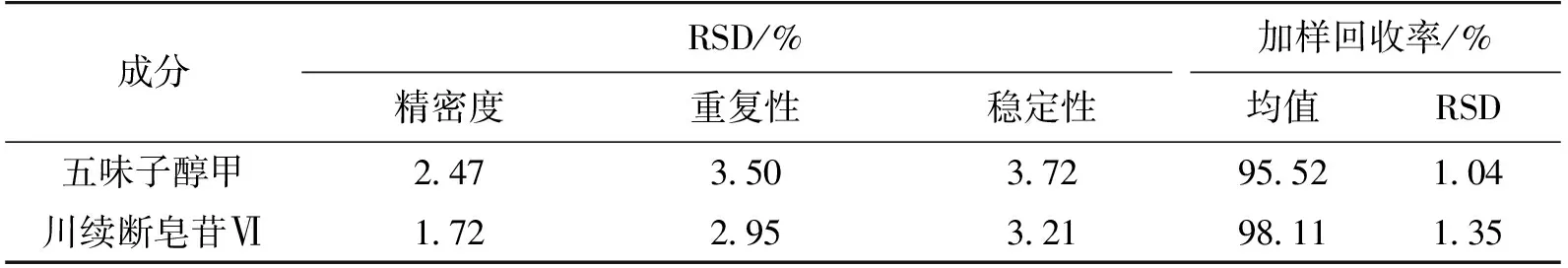
表2 五味子醇甲、川续断皂苷Ⅵ的HPLC精密度、重复性、稳定性和加样回收率实验结果(n=6)
2.8 样品含量的测定结果
样品含量的测定结果见表3。由表3可知:本研究所建立的定量检测方法准确、快速且灵敏,3批样品中的川续断皂苷Ⅵ和五味子醇甲批间差异较小,结果稳定可靠。
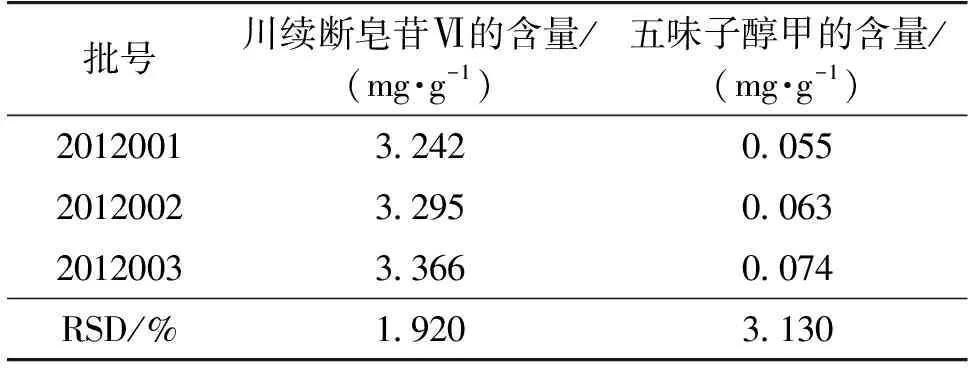
表3 含量测定结果(n=3)
3 结论
在查阅大量文献的基础上,通过采用不同供试品处理方法及展开剂进行试验,对二地鳖甲颗粒全方药都进行了TLC法定性鉴别研究,成功鉴别出菟丝子、枸杞子、续断及五味子4味药材。色谱斑点均清晰、分离效果较好,重现性好;其供试品溶液制备方法也比较为简单。因此,可作为制剂质量控制的定性指标。
采用HPLC法同时测定了颗粒中川续断皂苷Ⅵ、五味子醇甲2个活性成分的含量,所建立的方法灵敏准确、稳定可行;且其供试品溶液制备方法及色谱条件均较简单。因此,可为二地鳖甲颗粒的质量标准制定提供参考。
本研究在预实验阶段对二地鳖甲颗粒中的君药生地、熟地也进行了含量测定方面的研究,但由于其指标性成分如:梓醇、地黄苷D、毛蕊花糖苷,或受热后稳定性不足、易降解,或在制剂中含量较少,因此,考虑在后续的研究中引入HPLC-MS/MS等方法来满足更多指标性成分的含量测定。

