不同新冠病毒核酸检测系统结果一致性的验证及分析评价
李中秋,季全义
(北京市密云区鼓楼社区卫生服务中心检验科,北京 101500)
2020 年1 月20 日国家卫生健康委发布公告,将新型冠状病毒感染的肺炎纳入《中华人民共和国传染病防治法》规定的乙类传染病,并采取甲类传染病的预防、控制措施[1]。我区疾控在2022 年参加新冠病毒核酸检测工作期间,严格执行《新型冠状病毒核酸检测质控与实验室生物安全管理规范》,确保能及时发现和报告新型冠状病毒感染的肺炎病例,有效遏制疫情播散和蔓延。其间,世界卫生组织提出的“关切的变异株”有阿尔法、贝塔、伽玛、德尔塔和奥密克戎。当时奥密克戎株感染病例已取代德尔塔株成为主要流行株[2],在我国境内常规使用的 PCR 检测诊断准确性未受到影响,新冠病毒核酸检测阳性仍为确诊的首要标准。随着我区常态化新冠疫情防控措施的落实落细,检测标本量的不断增加,传统手工实时荧光定量PCR检测方法已经不能满足现有检测需要。高通量的病原体核酸提取检测系统开始在本实验室得到应用。本文对两种新冠病毒核酸检测系统的检测能力、结果一致性及生物安全风险进行了验证和分析。
1 资料与方法
1.1 一般资料
从菌毒种库(-70℃)[3]中随机选取2022 年10月—2022 年12 月已灭活确认阳性的新冠病毒感染(COVID-19)[4]者鼻咽拭子样本16 例,阴性样本4 例。
1.2 仪器与试剂
珀金埃尔默(PerkinElmer)explorer G3 高通量自动化病原体核酸提取检测系统(配置:Plate::handler Flex750 机 械 手 臂、3 台Chemagic 360 核 酸 提 取 仪、JANUS G3 自动化液体处理工作站、4titude 自动封膜机、LiCONiC LPX280 储 板 栈、BioTek MultiFlo 快 速分 液 器、2 台LightCycler 480 Ⅱ实 时 荧 光 定 量PCR仪)[5]、耐优(NAYO)ES96 全自动样品处理系统;ABI QuantStudio Dx 实 时 荧 光 定 量PCR 检 测 仪、Chemagic360 全自动核酸提取仪、北京大龙DM0636离心机、漩涡震荡仪、手动微量移液枪及吸头。
硕博源核酸提取纯化试剂(Nucleic Acid Extraction and Purification Kit)、明德生物新型冠状病毒 2019-nCoV 核酸检测试剂盒(荧光 PCR 法)。
1.3 检测方法
本实验室按要求参加室间质量评价。两种检测系统分别设置一个弱阳性对照质控样本和三个阴性对照质控样本,对照样本随机放在待测样本中间,同批参与核酸检测。所有试剂均在有效期内。使用明德生物新型冠状病毒 2019-nCoV 核酸检测试剂盒,靶基因为 ORFlab 和N 基因序列,以人类管家基因RNaseP作为内标,以保障检测结果的特异性与准确性。弱阳性和三个阴性对照样本的检测结果均满足质量控制要求时,方可进行检测结果的判定。
1.3.1 珀金埃尔默explorer G3 高通量自动化病原体核酸提取检测系统 通过耐优ES96 全自动样品处理系统、珀金埃尔默explorer G3 检测系统及相关试剂耗材,实现自动化核酸提取、PCR 体系构建、自动封膜、在线qPCR 扩增分析。
1.3.2 传统ABI QuantStudio Dx 实时荧光定量PCR 检测系统 在样本准备区生物安全柜内进行样本提取,使用Chemagic360 核酸提取仪进行提取纯化操作。在试剂准备区,取出 N 个(四个阴阳性质控品数+ 待检样本数)PCR 反应管,加好反应液。在样本准备区行加样封膜瞬时离心后,移至扩增和产物分析区。在ABI QuantStudio Dx 实时荧光定量PCR 检测仪上设置样品名称,选择荧光检测通道,设定循环参数后进行核酸检测。
1.4 检测结果判定标准
阴性质控要求: ROX 通道扩增曲线无指数增长或Ct ≥35, FAM 与VIC / HEX 通道扩增曲线无指数增长或 Ct ≥40。阳性质控要求: FAM 、 VIC / HEX 、 ROX三个通道扩增曲线均呈指数增长且 Ct <35。
1.4.1 阳性阴性判定值 利用 ROC 曲线法确定阳性阴性: FAM 通道扩增曲线呈指数增长且 Ct <38 为FAM 阳性;FAM 通道扩增曲线无指数增长或Ct ≥40为 FAM 阴性。 VIC / HEX 通道扩增曲线呈指数增长且 Ct <38 为 VIC / HEX 阳性;VIC / HEX 通道扩增曲线无指数增长或Ct ≥40 为 VIC / HEX 阴性。ROX 通道扩增曲线呈指数增长且 Ct <35 为 ROX 阳性; ROX 通道扩增曲线无指数增长或 Ct ≥35 为ROX 阴性。
1.4.2 样品检测结果判定 阳性样本判定标准: FAM 、VIC / HEX 和 ROX 三个通道均为阳性,可报告为阳性样本。阴性样本判定标准: ROX 通道为阳性, FAM 与VIC / HEX 通道为阴性,可报告为阴性样本。
1.5 统计学分析
通过医学统计学中配对定量资料的t检验比较两种系统检测新冠病毒样本的靶基因原始Ct 值有无差异。采用Kappa 一致性检验对两种检测系统阴阳性结果的四格表数据进行分析。
2 结果
两种系统检测20 份新冠病毒样本的靶基因(ORF1ab 和N 基因)原始Ct 值见表1、表2。计算t值为0.446,t0.05/2,19=2.093,|t|<t0.05/2,19,故P>0.05,两种系统检测新冠病毒样本的ORF1ab 基因Ct 值差异无统计学意义。计算t值为0.291,t0.05/2,19=2.093,|t| <t0.05/2,19,故P>0.05,两种系统检测新冠病毒样本的N 基因Ct 值差异无统计学意义。
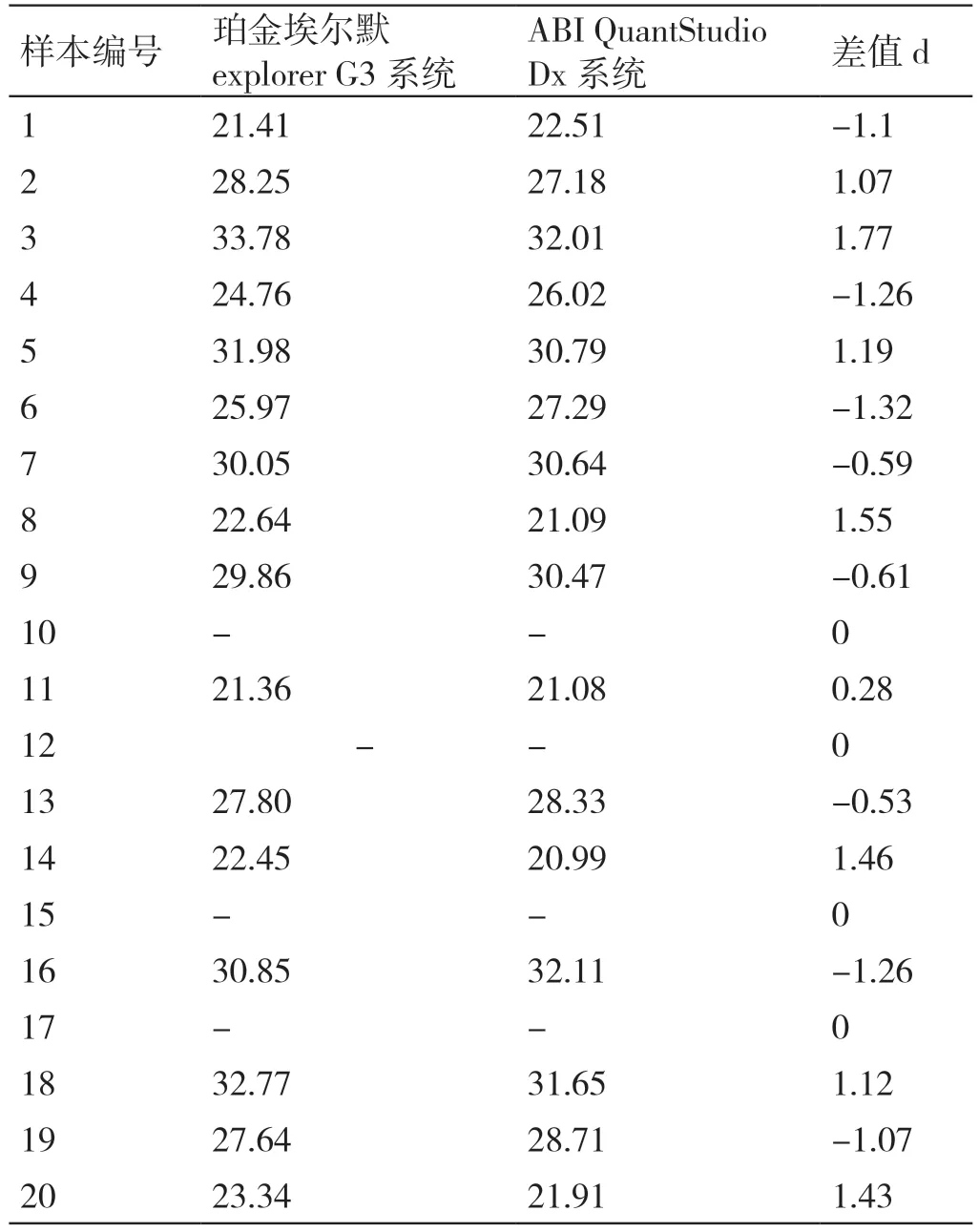
表1 两种系统检测ORF1ab 基因原始Ct 值
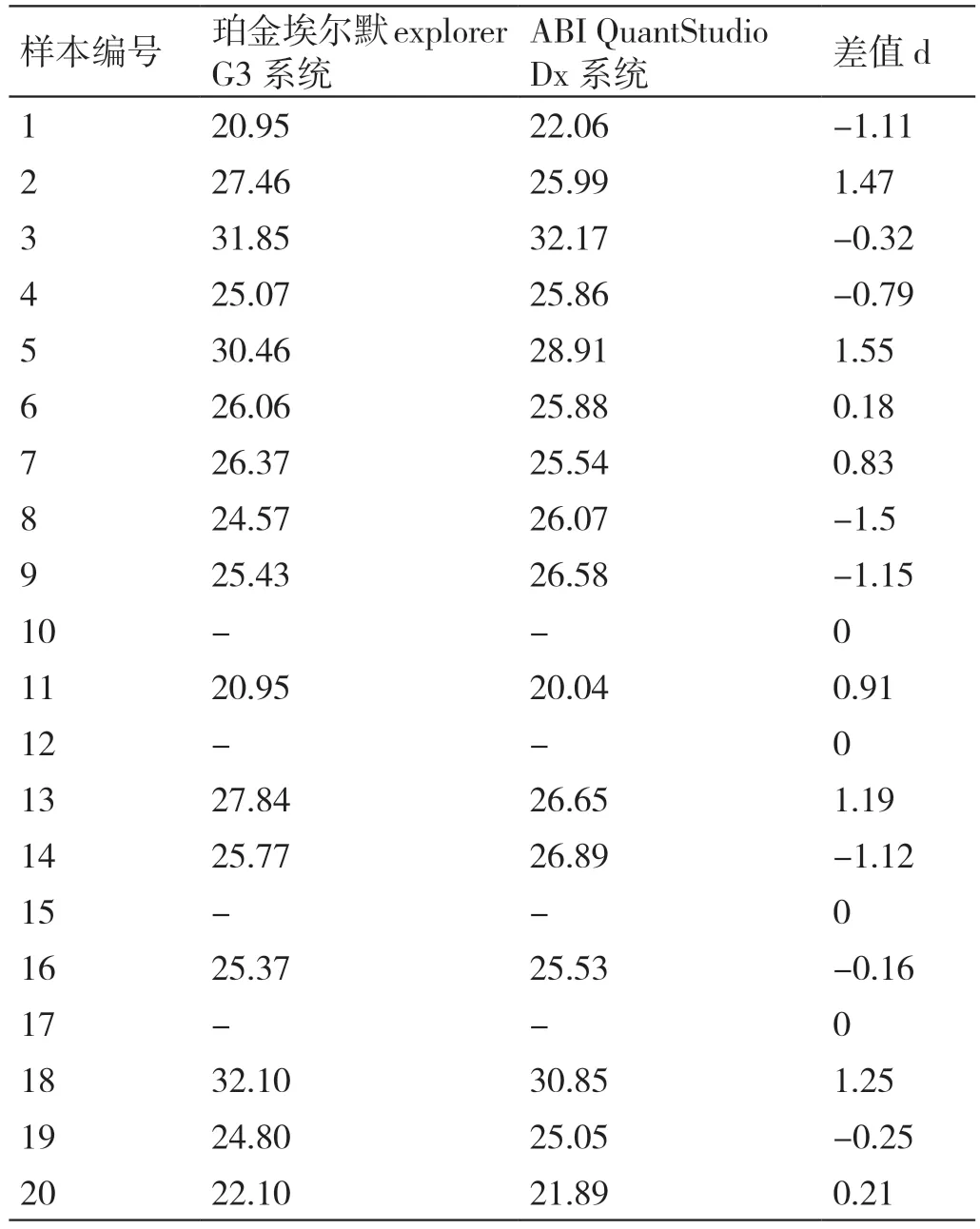
表2 两种系统检测N 基因原始Ct 值
两种系统检测20 份新冠病毒样本,ROX 通道(为内控RNaseP 指示通道)均为阳性,判定结果详见表3。两种系统检测新冠病毒样本的靶基因原始Ct 值经过“样品检测结果判定标准”中阴阳性结果判定后,整理成配对设计的四格表数据,采用Kappa 一致性检验进行分析,Kappa 系数=1,两种系统检测结果的一致性非常好。

表3 两种系统检测新冠病毒样本阴阳性结果
3 讨论
核酸检测的生物安全、效率、准确性是疫情防控工作中最重要的一环。实时荧光定量PCR 核酸检测是新冠检测公认的金标准,本文对两种实时荧光定量PCR 核酸检测系统进行对比分析的结果显示:两种系统检测新冠病毒样本的靶基因(ORF1ab 和N 基因)Ct 值差异无统计学意义,阴阳性判定检测结果的一致性非常好。ABI QuantStudio Dx 相关检测系统从核酸提取、试剂配制到PCR 检测的操作和衔接过程都需要进行大量精细操作,生物安全风险较大,操作空间至少需要三室,耗费大量人力、时间,因此无法满足日益增加的检测需求;反观珀金埃尔默explorer G3相关检测系统可实现自动化和标准化工作流程和操作步骤,全自动流程减少了检验人员与样本接触,有效降低了感染风险, 并大幅减少了人力需求;样本通量高,可全天候运行,迅速提升病毒检测能力;移液精度高,可减少人为失误;设备占用空间小,生物安全隐患小。
综上所述,传统手工核酸检测系统在样本量较少的情况下,可基本满足实验室需要,并可用于自动化核酸提取系统检测结果的复核检测。自动化核酸提取系统适合大批量检测,其同样具有良好的精确度和准确性,有利于进行质量控制和标准化。在新型冠状病毒大流行结束后,高通量自动化病原体核酸提取相关检测系统因其为模块化设计的自动化整合系统,能够根据疫情需要,迅速调整检测规模,同时也可用于其他实验室检测,可见此系统的广泛应用是实验室检测未来发展的趋势。

