肝爽颗粒治疗肝硬化(肝郁脾虚证)的临床综合评价
路振凯,张利丹,吕 健,谢雁鸣*
肝爽颗粒治疗肝硬化(肝郁脾虚证)的临床综合评价
路振凯1,张利丹1,吕 健2*,谢雁鸣1*
1. 中国中医科学院中医临床基础医学研究所,北京 100700 2. 中国中医科学院西苑医院,北京 100091
通过系统、多学科的方法对肝爽颗粒治疗肝硬化(肝郁脾虚证)进行多维度价值评估。按照《药品临床证据和价值评估管理指南》标准,基于循证医学证据,结合问卷调查、卫生技术评估、药物经济学评价等方法,利用多准则决策分析模型,从有效性、安全性、经济性、创新性、适宜性、可及性、中医药特色“6+1”维度对该药治疗肝硬化(肝郁脾虚证)的临床证据和临床价值进行综合评估,最终形成“临床证据和价值评估指数”。基于证据充分性结果和已知风险评价结果,肝爽颗粒安全性等级为B,认为风险可控、安全性较好;基于证据质量评价和证据价值评价结果,提示肝爽颗粒联合恩替卡韦在改善肝硬化患者丙氨酸氨基转移酶、天冬氨酸氨基转移酶、总胆红素、白蛋白、层黏连蛋白、Ⅲ型前胶原、透明质酸、Ⅳ型胶原蛋白方面优于单用恩替卡韦治疗(<0.05),有效性等级为A,认为该药有效性好、临床意义大;肝爽颗粒在临床、企业、产业3方面均具有一定创新性,创新性等级为B;根据肝爽颗粒治疗肝硬化的成本-效果结果显示,认为该药经济性较好,经济性等级B;综合医护人员和患者问卷得分情况,适宜性等级为B;与同类药相比,肝爽颗粒价格适中合理,可负担性好,覆盖全国26个省市自治区的2636家医院,可及性等级为B;基于中医药特色评定规则,中医药特色等级为B,认为该药中医药特色较为突出。综合“6+1”维度结果,运用CSC V2.0软件计算得出肝爽颗粒治疗肝硬化(肝郁脾虚证)的综合衡量价值为B类。基于肝爽颗粒各维度评价结果及综合评价分数,表明肝爽颗粒临床价值较好,建议进一步开展药效机制研究,提高循证证据质量,充分发挥肝爽颗粒的临床价值优势。
肝爽颗粒;肝硬化;肝损伤;肝郁脾虚证;临床综合评价
据统计每年有超100万人死于感染乙肝病毒相关疾病,其中肝硬化死亡率占52%[1],我国乙肝病毒感染者约7000万人,进展至肝硬化者占比高达60%,年发生率为0.4%~14.2%[2]。针对肝硬化的治疗西医强调抗病毒、免疫调节等措施,长期治疗不良反应明显且常有反跳现象及耐药性的发生[3]。马起山等[4]通过对全国范围内27家肝炎肝硬化住院患者的调查发现,肝炎肝硬化治疗费用明显高于间接费用(因住院而导致的经济负担,包括因治疗而导致的工作或学习时间的损失、家庭生活的变动等费用),医疗费用总体呈上升趋势,严重影响患者生活质量,造成大量的经济和社会负担。因此,寻求有效、安全可及性高的治疗方法具有重要意义。
肝硬化属中医“癥积”“臌胀”“肝着”等范畴,病机以本虚标实为主[5],患者感邪日久,脏腑虚损,气机阻滞,脾虚则完谷不化、痰湿内生,并见不思饮食之症,气滞则推动无力,血液运行受阻,病理产物堆积、热从内生,而至肝郁脾虚。肝爽颗粒化裁于《太平惠民和剂局方》经典名方逍遥散,包括柴胡、党参等13味中药,具有疏肝健脾、清热散瘀、保肝护肝、软坚散结的功效,适用于肝硬化(肝郁脾虚证),针对肝硬化伴胃底食管静脉曲张的患者,可明显降低出血风险,在改善肝区疼痛、乏力、腹胀等症状疗效显著[6]。
肝爽颗粒2019年载入中国中西医结合学会肝病专业委员会制定的《肝纤维化中西医结合诊疗指南》[7]。本研究基于有效性、安全性、经济性、创新性、适宜性、可及性、中医药特色“6+1”维度,评价该药物综合价值,为医院临床合理用药及国家基本药物目录准入等决策提供参考。
1 资料与方法
1.1 资料来源
本研究数据资料复杂,分别按不同维度对资料来源进行归总,见表1。

表1 “6+1”维度资料获取方式
1.2 文献检索
为全面获取肝爽颗粒治疗肝硬化的文献数据信息,使用“肝爽”“肝爽颗粒”“慢性肝炎”“乙型肝炎”“肝纤维化”“肝硬化”作为关键词在中国知网、万方、维普、中国生物医学文献数据库进行全文或主题词检索;以“Gan Shuang”“Gan Shuang Granule”“Chronic Hepatitis”“Hepatitis B”“Liver Fibrosis”“Liver Cirrhosis”作为关键词在PubMed、Web of Science、Embase、Cochrane数据库进行全文或主题词检索,时间限制为肝爽颗粒上市日期2006年1月1日至2021年5月10日,将检索出来的各类型的文献进行整理,分别建立安全性、有效性和经济性数据集。
1.3 问卷调查
根据调查对象的不同,设计医护版和患者版2个版本的调查问卷,在全国范围内以问卷星APP实施。
1.4 评价方法
肝爽颗粒临床证据和价值评估遵照2021年国家卫生健康委员会发布的《药品临床综合评价管理指南(2021年版试行)》和《中国药品综合评价指南参考大纲(第2版)》制定的相关规定和管理规范[8],应用循证医学、问卷调查、卫生技术评估、药品经济学评价等方法,从有效性、安全性、经济性、创新性、适宜性、可及性、中医药特色“6+1”维度对药品临床证据和临床价值进行综合评估,并形成“临床证据和价值评估指数”。此次研究基于多准则决策分析模型(multi-criteria decision analysis model,MCDA)[9],由135位专家会议投票对各维度进行赋权,采用中成药临床证据和价值评估软件(CSC V2.0)计算该药临床价值标准化分值,等频离散原则转化等级。评估流程见图1。

图1 临床证据和价值评估流程
1.5 质量控制
按国际公认的循证医学证据评价方法对本研究实施全过程进行质量控制,具体评价工具见表2。证据质量评价采用双人评价,各维度评价人撰写报告后由质量控制人员进行审核,由负责人汇总整合后,召开内部专家会议,对评价结果和报告内容进行全面审核及修订。
1.6 药理与药学特性
1.6.1 药理与药效学研究 肝爽颗粒中的柚皮苷通过抑制哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)通路,调节下游造血干细胞(hematopoietic stem cell,HSC)分子介导的调节性T细胞(regulatory T cell,Treg),抵抗肝细胞凋亡,维持其稳定性[10-11]。此外,肝爽颗粒可下调细胞色素P450 2E1/1A2(cytochrome P450 2E1/1A2,CYP2E1/1A2)活性,减少毒性产物-乙酰对位苯醌亚胺(-acetyl--benzoquinone imine,NAPQI)的生成,激活核因子红系2相关因子2(nuclear factor erythroid 2-related factor 2,Nrf2),增加抗氧化酶表达,加速药物成分的无害代谢,起到预防药物性肝损伤的作用[12-13]。研究发现,在肝爽颗粒干预3 d后的Wister大鼠ip-半乳糖胺构建急性肝损伤模型,干预组血清丙氨酸氨基转移酶(alanine aminotransferase,ALT)和天冬氨酸氨基转移酶(aspartate aminotransferase,AST)水平较对照组升高幅度明显减小,胆汁引流量升高,提示肝爽颗粒有较好的保肝利胆作用[14]。

表2 评价工具
1.6.2 急性毒性与长期毒性实验 急性毒性实验显示,小鼠每日ig肝爽颗粒浸膏生药量236 g/kg(相当于60 kg人临床日用剂量的157倍),连续观察7 d,小鼠一般状况良好,无1例死亡。长期毒性实验显示,大鼠ig肝爽颗粒生药量15、30、60 g/kg(分别为临床每日用量的15、30、60倍),在连续给药6个月后停药2周,大鼠一般状况良好、肝肾功能和生化指标均无明显影响,主要脏器的组织结构基本正常,未见毒性损害[15]。
1.6.3 药学质量评价 肝爽颗粒质量符合国家药品监督管理局相关规定,原辅料标准依照《中国药典》2020年版取得国家药品GMP认证证书,在河北省药品监督管理局备案。
2 结果
2.1 安全性
2.1.1 证据概述 根据SRS显示的数据,肝爽颗粒上市至2020年12月31日所有不良反应数据共184例,包括一般不良反应181例(占病例总数的98.37%)、严重不良反应3例(占病例总数的1.63%),平均年龄52.28岁,主要累积胃肠系统,表现为恶心、呕吐、皮疹、瘙痒等;根据安全性数据集显示在使用肝爽颗粒的1554例患者中共有23例发生不良反应,不良反应程度均为一般,无严重不良反应,主要表现为胃肠道症状,与SRS结果基本一致。
药品生产企业成立了药物警戒部和药品安全委员会,构建完善了质量管理体系及相关风险管理文件,建立不良反应报告和监测管理制度和药物警戒年度报告制度,定期进行安全性文献检索;按要求开展说明书更新工作;据企业记录近3年无因产品不合格而被召回的情况,未有被药品监管机构通报/ 约谈的相关情况。肝爽颗粒上市前开展的动物急性毒性实验与长期毒性实验结果显示,动物一般状况良好、肝肾功能和生化指标均无明显影响,主要脏器的组织结构基本正常,未见毒性损害。
2.1.2 证据评价 根据本品开展的安全性研究类型,表明证据比较充分,安全性结论较明确。因未开展主动监测无法准确获知肝爽颗粒严重不良反应发生率,故采用SRS数据与销售数据近似估计,
严重不良反应发生率近似估计值=SRS报告数×疗程用量×风险系数/销售量
其中风险系数反映了不良反应发生但未能上报SRS的情况。根据SCS V2.0软件计算结果,可知肝爽颗粒不良反应发生率为0.000 2%,国际医学科学组织理事会(Council for International Organizations of Medical Sciences,CIOMS)分级为非常罕见,已知风险较小。以证据充分性作为横坐标,已知风险作为纵坐标,构建安全性证据-风险矩象限(图2),通过计算安全性标准化效用分数为0.38,评价等级为B,即基于现有研究,认为风险较可控,安全性较好。

图2 安全性证据-风险矩阵
2.2 有效性
2.2.1 证据概述 肝爽颗粒是临床治疗肝炎肝硬化常用的颗粒剂,入选中国中西医结合学会肝病专业委员会制定的《肝纤维化中西医结合诊疗指南(2019年版)》[7],《中成药临床应用指南》推荐该药治疗自身免疫性肝病及肝硬化肝郁脾虚证,同时该药是中国协和医科大学出版社《临床路径释义》消化病分册中的推荐用药,并于2020年中华中医药学会肝胆病分会出台《肝爽颗粒治疗肝纤维化临床应用专家共识》(共识编号:GS/CACM274-2020)[16]。
有效性数据集纳入标准遵照PICOS原则,研究人群(P):以慢性肝硬化患者为本研究的目标人群,符合第9版《内科学》肝硬化的诊断标准;干预措施(I):口服肝爽颗粒+西医基础治疗(保肝、利尿等对症治疗措施);对照措施(C):单用西医基础治疗(保肝、利尿等对症治疗措施);结局指标(O):治疗后患者的血清ALT、AST、总胆红素(total bilirubin,TBIL)、白蛋白(albumin,ALB)、层黏连蛋白(laminin,LN)、III型前胶原(type III procollagen,PCIII)、透明质酸(hyaluronic acid,HA)、IV型胶原(type IV collagen,IV-C)水平及不良反应;研究类型(S):为随机对照试验,且不受语种及发表限制。排除标准:试验组联合中医外治等干预措施、联合其他中药制剂、非随机对照试验、无法获取全文。最终纳入30项研究[17-46],总样本量为2311例,其中试验组1157例,对照组1154例,纳入研究的基本特征见表3,基线均为均衡。30项研究均未报道研究方案、样本量估算、盲法实施、随机分配方案的隐藏情况。14项研究[17,19,21-23,27,29,37-39,41-44]报道了随机的具体实施方案,3项研究[17,21,23]采用抽签法,8项研究[19,22,27,29,37-39,41]采用随机编码表,2项研究[43-44]根据治疗方式随机,1项研究[42]根据入院方式随机,治疗方式和入院方式随机2种随机方式被评为具有高偏倚风险。5项研究报道通过伦理审查[20-22,28,44],19项研究报道患者均签署知情同意书[17-26,28-30,32,39,43-46]。1项研究[26]未完全报道预先指定的指标,存在选择性报告结果的情况;2项研究[45-46]未提前设定结局指标,偏倚风险未知。
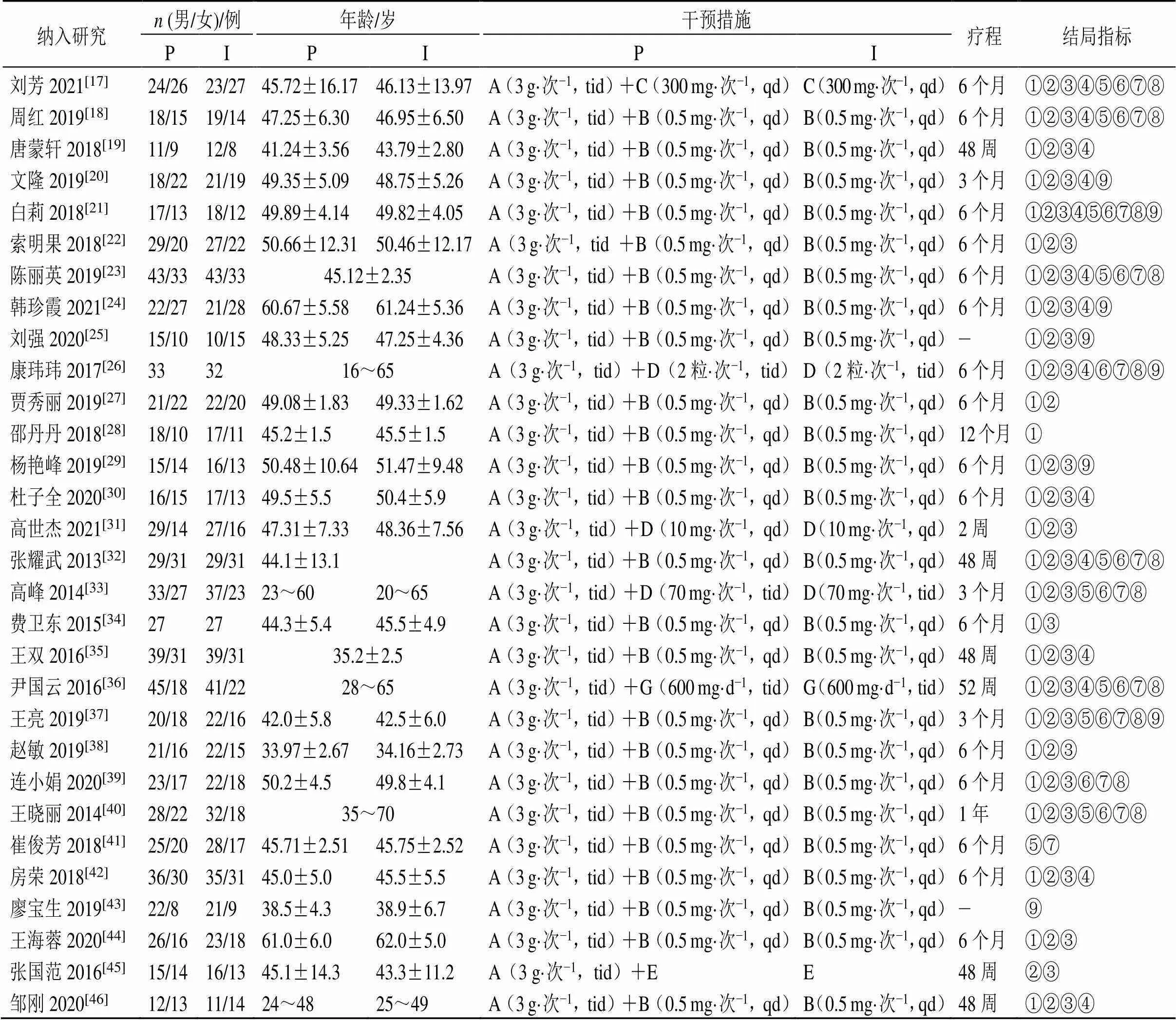
表3 纳入研究的基本信息
I-试验组 P-对照组 A-肝爽颗粒 B-恩替卡韦 C-富马酸替诺福韦二吡呋酯片 D-水飞蓟宾葡甲胺片 E-α-干扰素 ①ALT水平 ②AST ③TBIL水平 ④ALB水平 ⑤LN水平 ⑥PCⅢ水平 ⑦HA水平 ⑧Ⅳ-C水平 ⑨不良反应发生率 −未提及
I-experimental group P-control group A-Ganshuang Granules B-Entecavir C-Tenofovir Disoproxil Fumarate Tablets D-Silybin Meglumine Tablets E-alpha-interferon ①ALT level ②AST level ③TBIL level ④ALB level ⑤LN level ⑥PCIII level ⑦HA level ⑧IV-C level ⑨incidence of adverse reactions −not mentioned
Meta分析表明,肝爽颗粒联合恩替卡韦治疗在降低肝炎肝硬化患者ALT、AST、TBIL、ALB、LN、PCⅢ、HA、Ⅳ-C水平方面优于单用恩替卡韦治疗,差异具有统计学意义(<0.05),二者不良反应发生率比较,差异无统计学意义(=0.52>0.05),提示在恩替卡韦治疗的基础上联合肝爽颗粒不会增加用药风险。肝爽颗粒联合水飞蓟宾葡甲胺片治疗在降低肝炎肝硬化患者ALT、AST、TBIL水平方面与单用水飞蓟宾葡甲胺片治疗相比差异不具有统计学意义(>0.05)。Meta分析结果见表4。采用AMSTAR2标准评价Meta分析报告的质量,结果显示,本项Meta分析未报道相关利益冲突,总体质量较好。
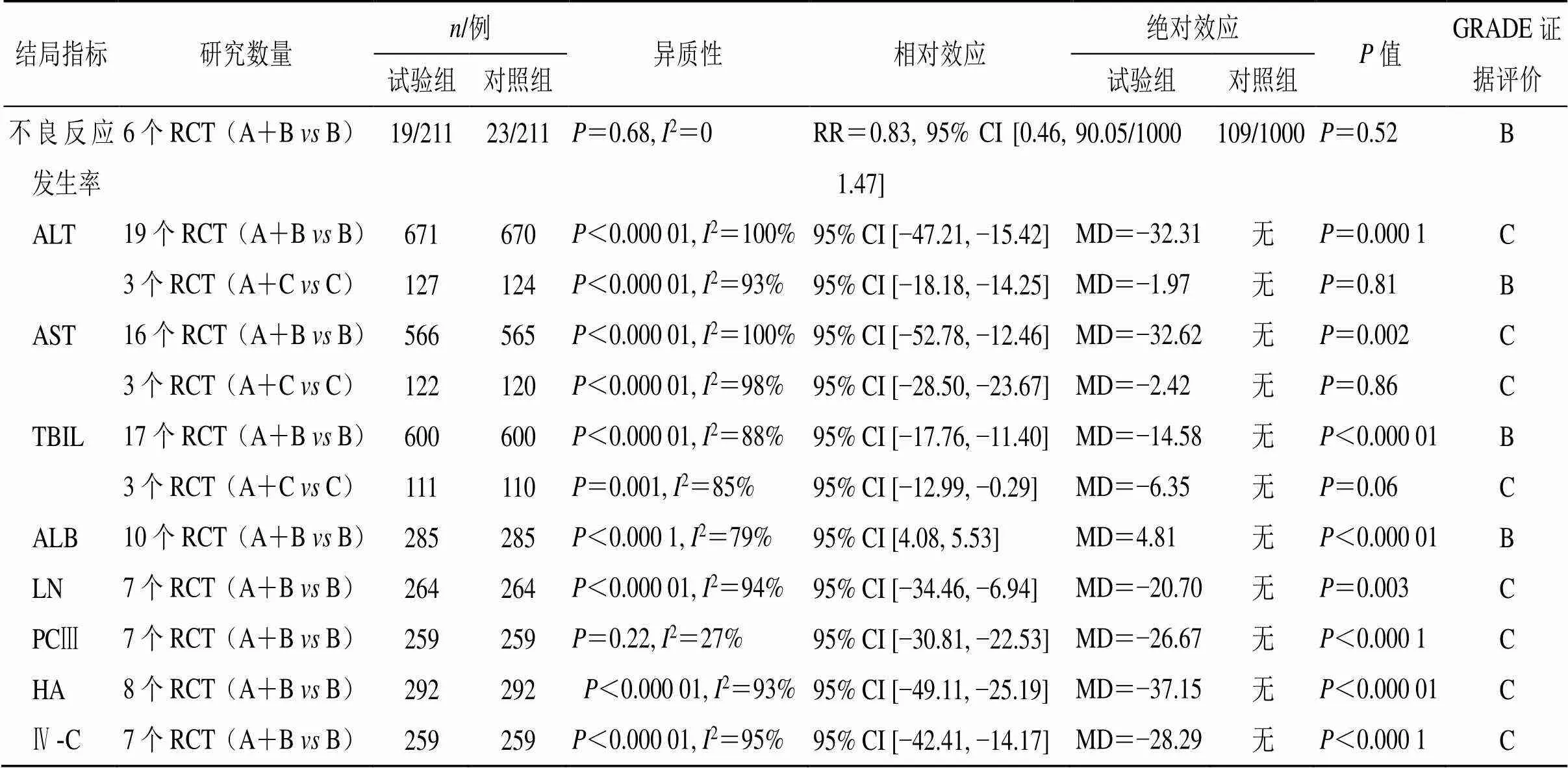
表4 纳入研究的基本信息证据概要
A-肝爽颗粒 B-恩替卡韦 C-水飞蓟宾葡甲胺片 ADR-药物不良反应
A-Ganshuang Granules B-Entecavir C-Silybin Meglumine Tablets ADR-adverse drug reactions
2.2.2 证据评价 从证据价值和证据质量2个方面对有效性进行评价,证据质量按照GRADE证据体系进行评价,GRADE评价结果见表4。
证据价值参照PICO原则,根据干预措施的情况、对照组是否为指南推荐用药以及结局指标的重要程度来衡量,采用加权乘积模型(weighted product model,WPM)[47],通过CSC V2.0软件计算可知,肝爽颗粒治疗肝硬化有效性证据价值为A;以证据价值为横坐标,证据质量为纵坐标,构建有效性证据价值-质量矩阵(图3),通过计算有效性标准化效用分数为0.74,评价等级为A,即有效性好,临床意义大。
2.3 经济性
2.3.1 证据概述 2021年6月北京中医药大学中药药物经济学评价研究所从医保角度出发,分别以肝爽颗粒为试验组,同类药复方鳖甲软肝片为对照组,开展北京某三甲医院信息系统的回顾性队列研究。采用成本-效果比(cost-effectiveness ratio,CER)和增量成本-效果比(incremental cost-effectiveness ratio,ICER)2种方法对试验组药物和对照组药物的经济性进行评价。结果显示代偿期试验组具有一定的成本效果比优势,敏感性分析结果具有稳定性。失代偿期试验组成本较高,ALT复常率较低,但差异无统计学意义。

图3 有效性证据价值-质量矩阵
本研究团队从全社会卫生体系角度出发,选择恩替卡韦作为对照组,肝爽颗粒+恩替卡韦作为试验组,采用Treeage Pro 2011软件构建治疗肝硬化的决策树模型。成本效果分析显示,试验组的成本高于对照组,同时所获得效果也高于对照组,以2020年人均可支配收入作为基础分析的参考阈值来看,患者的意愿支付价格高于两组ICER,提示肝爽颗粒加恩替卡韦更具有经济性。通过CASP经济学评价清单对肝爽颗粒的经济学研究进行再评价得知,经济学报告基于真实世界数据,提出了明确的问题,较为恰当地评价和比较了干预的效果和成本,但属于单中心研究,样本量较少,未考虑贴现率,未进行充分的敏感性分析,具有一定的局限性。
2.3.2 证据评价 从证据价值和证据质量2个方面对药物经济性进行评价,证据价值从增量效应水平和干预方案成本2个方面进行评价,采用成本-效果分析法,可知该药治疗肝硬化增量效应水平评价为C,增量效应较大,成本水平评价为B,成本水平一般。以增量效应水平为纵坐标,干预方案成本为横坐标,构建经济性价值评价矩阵(图4),通过计算经济性标准化效用分数为0.25,评价等级为B,即经济性价值较高。
2.4 创新性
2.4.1 证据概述 西医治疗肝硬化强调抗病毒、免疫调节、改善肝功能和抗纤维化等综合治疗方法。抗病毒药物包括干扰素和核苷类药物,其中干扰素治疗慢性乙肝的效果不甚满意,而一些新的核苷类药物远期疗效不好,常有反跳现象发生,如拉米夫定的核苷类药物,长期使用可能产生病毒变异、出现耐药性的问题。而中医药注重整体调理、防治并重,在肝硬化的长期治疗中具有明显优势。该药源于中医经典名方逍遥散,立足整体观念,适用于肝硬化(肝郁脾虚证),具有治肝兼顾脾胃,治肝不伤脾胃的特点,是治疗肝硬化辨证为肝郁脾虚证唯一的中成药,在保肝抗炎、逆转肝纤维化的同时,具有一定的抗抑郁作用,体现临床创新性[48]。企业在服务体系创新和产业创新方面开展了大量工作,秉承“专家、科技和学术带动企业发展”的理念,重科研、重质量,通过学术创新造福更多患者,制定完整的质量标准体系。

图4 经济性价值评价矩阵

2.5 适宜性
2.5.1 证据概述 2021年4月25日—6月30日在全国范围内以线上问卷APP的形式进行问卷调查,结果显示共调查使用肝爽颗粒的医护人员123人、服用肝爽颗粒的患者110名,受访者来自河北、天津、陕西等20个省市自治区,报告结果显示该药易为患者掌握和接受,无特殊技术和管理要求,对临床工作者以及使用本药品的患者具有较好的适宜性。
2.5.2 证据评价 本维度评价共设置2个一级指标,9个二级指标,结合问卷调查结果,最终得出适宜性评分为3.15,等级为B,见表5。
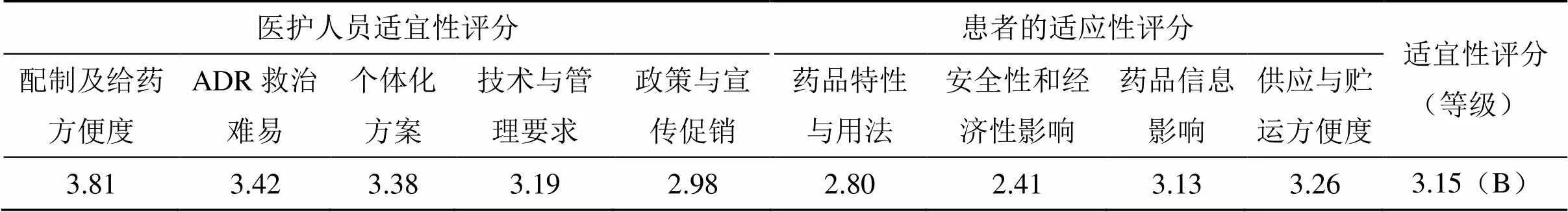
表5 肝爽颗粒适宜性调查结果汇总
根据医护版及患者版调查问卷结果所得
Based on the results of the medical and patient versions of the questionnaire
2.6 可及性
2.6.1 证据概述 肝爽颗粒中位价格为42.99元/盒,日治疗费用为14.33元,按照2个月的疗程计算,疗程总金额为859.8元,价格较合理。肝爽颗粒限定日费用占治疗城镇居民可支配收入中位数的2.59%,占农村居民可支配收入中位数的10.32%,以人均可支配收入为参照,提示该药可负担性较好;销售覆盖北京、天津等26个省市自治区,覆盖医院2636家,其中三级医院448家,配备比为16.9%,二级医院1467家,配备比为55.6%,一级医院721家,配备比为27.3%。根据销售量估算每年接受治疗的人数达40.01万,其产能为每天100万袋,每年产能为25 200万袋;本方中涉及的13味药材资源丰富、可持续供应没有产地限制供应等,不存在短缺情况;同时,肝爽颗粒在使用过程中不需要特殊条件储存或运输,不需要使用特殊溶媒和特别注射与使用器具,不需要对患者采取与常规操作不同的治疗药物监测或相关生理指标检测,无相关费用的增加。
2.6.2 证据评价 根据赋分标准[49],肝爽颗粒药品价格水平为B、可获得性水平B、可负担性水平A,综合3方面结果,通过CSC V2.0软件计算得到肝爽颗粒可及性标准化效用分数为0.875,根据可及性评价等级转化规则评为B级,认为该药可及性较好。
2.7 中医药特色
2.7.1 证据概述 肝爽颗粒源于宋代《太平惠民和剂局方》中医经典名方逍遥散,针对肝硬化的病因、病机的特点组方而成。作为主要病因,患乙型肝炎的患者多由湿热疫毒所致,肝藏血,喜条达而恶抑郁,气机不畅,则肝气郁阻,脾运化失司,阴血暗耗、痰湿内生,五脏六腑失于濡养,反致肝气郁阻、脾气虚衰,血液运行受阻,病理产物堆积,热象内生,症见胁痛,乏力,纳差等。肝爽颗粒有疏肝健脾、清热活血之功效,针对肝硬化的病机特点,症状表现效果显著,且与同类药物相比,药性温和、不良反应少,安全性高。
2.7.2 证据评价 从中医药理论(证候、配伍、民族药等)、人用经验(1911年以前的经典名方、2000例已发表的真实世界研究)2个方面对肝爽颗粒中医药特色进行评估,该方源于经典名方“逍遥散”,具有疏肝健脾、清热活血的功效,药性温和,认为肝爽颗粒中医药特色等级为B。
2.8 临床综合评价结果
综合肝爽颗粒“6+1”维度的评价结果,根据CSC V2.0软件计算得知肝爽颗粒综合衡量价值分数为0.72,等级为B,认为该药临床综合价值良好,建议按程序有条件转化为基本临床用药管理的相关政策结果。
3 结论与建议
本研究以国家卫生健康委发布的《药品临床综合评价管理指南(2021年版试行)》为基础,响应“以药品临床价值为导向,推动有关证据用于国家基本药品目录的遴选和动态调整,提高合理用药水平”的号召,通过综合评价的方法,基于MCDA[50]对肝爽颗粒的安全性、有效性、经济性、适宜性、创新性、可及性6个维度进行评价,总共邀请循证医学、政策及方法学、经济学、统计学等相关领域的16位专家进行MCDA赋权,多层次的临床价值评估和量化结果显示肝爽颗粒临床价值较好,为医院临床合理用药及国家基本药物目录准入等决策提供一定参考。
本研究仍存在一定的局限性,建议进一步开展安全性相关的主动监测等,获取确切的安全性证据,完善药品说明书中不良反应情况。建议开展高质量的随机对照试验,提高有效性证据质量;同时应不断优化产品的生产工艺,提高现有标准,针对已知的不良反应,深度剖析不良反应根源,通过改进工艺、做皮试或改进剂型等方式深入研究;建议进一步明确临床定位,开展以临床价值为导向的精准用药机制研究,充分发挥肝爽颗粒的临床价值优势,加强药品信息的宣传,制作专门针对患者的药品使用宣传材料,使药品使用者对药品信息、用量用法、安全性等有更详细地了解,促进临床合理用药。
本研究中所使用的灰色文献均由制药企业提供。
利益冲突 所有作者均声明不存在利益冲突
[1] 王贵强, 王福生, 庄辉, 等. 慢性乙型肝炎防治指南(2019年版) [J]. 中国病毒病杂志, 2020, 10(1): 1-25.
[2] Liu J E, Liang W N, Jing W Z,. Countdown to 2030: Eliminating hepatitis B disease, China [J]., 2019, 97(3): 230-238.
[3] 王绍钧, 张慜鋆. 肝病药物的应用分析 [J]. 临床医药实践, 2010, 19(8): 433-435.
[4] 马起山, 梁森, 肖和卫, 等. 中国12个地区乙型肝炎相关疾病住院患者经济负担调查 [J]. 中华流行病学杂志, 2017, 38(7): 868-876.
[5] 翟昌明, 鲁放, 高雅. 慢性乙型肝炎早期肝硬化的中医病机特点探讨 [J]. 中国医药导报, 2022, 19(22): 110-113.
[6] 刘立, 李俊义, 刘春云, 等. 肝爽颗粒联合恩替卡韦对乙型肝炎肝硬化患者门静脉血栓发生的影响 [J]. 临床肝胆病杂志, 2022, 38(9): 2020-2026.
[7] 徐列明, 刘平, 沈锡中, 等. 肝纤维化中西医结合诊疗指南(2019年版) [J]. 中国中西医结合杂志, 2019, 39(11): 1286-1295.
[8] 张强, 王志飞, 谢雁鸣, 等. 中成药临床综合评价技术规范 [J]. 世界中医药, 2021, 16(22): 3394-3397.
[9] 杨硕, 谢雁鸣, 王连心, 等. 夏荔芪胶囊治疗前列腺增生(本虚标实证)的临床综合评价 [J]. 中草药, 2023, 54(9):2879-2888..
[10] Shi H B, Shi H L, Ren F,. Naringin in Ganshuang Granule suppresses activation of hepatic stellate cells for anti-fibrosis effect by inhibition of mammalian target of rapamycin [J]., 2017, 21(3): 500-509.
[11] Zhang X H, Zhang Y Z, Gao W,. Naringin improves lipid metabolism in a tissue-engineered liver model of NAFLD and the underlying mechanisms [J]., 2021, 277: 119487.
[12] 刘晓昆, 王立新. 肝爽颗粒通过Nrf2/HO-1信号通路缓解慢性肝损伤作用及机制研究 [J]. 天津中医药大学学报, 2021, 40(1): 98-103.
[13] 吴桥, 余朋飞, 毕研贞, 等. 肝爽颗粒浸膏减轻对乙酰氨基酚所致肝细胞损伤的作用机制 [J]. 临床肝胆病杂志, 2021, 37(1): 120-125.
[14] 刘峰, 党海霞, 马久太. 肝爽颗粒对大鼠实验性肝纤维化的影响 [J]. 中西医结合肝病杂志, 2005, 15(5): 286-287.
[15] Zhao J, Miao J, Wei X,. Traditional Chinese medicine Ganshuang Granules attenuate CCl4-induced hepatic fibrosis by modulating gut microbiota [J]., 2021, 18(11): e2100520.
[16] 中华中医药学会肝胆病分会. 肝爽颗粒治疗肝纤维化临床应用专家共识 [J]. 中西医结合肝病杂志, 2020, 30(5): 481-482.
[17] 刘芳, 季良, 姜海燕, 等. 肝爽颗粒联合富马酸替诺福韦二吡呋酯片对乙型病毒性肝炎肝硬化患者APRI、FIB-4的影响 [J]. 医学信息, 2021, 34(5): 104-106.
[18] 周红. 肝爽颗粒联合恩替卡韦分散片治疗失代偿期乙型肝炎肝硬化的临床效果 [J]. 现代中医药, 2019, 39(4): 66-68.
[19] 唐蒙轩, 钟耀东, 李宏真. 恩替卡韦分散片联合肝爽颗粒治疗乙型肝炎肝硬化失代偿期的效果及可行性研究 [J]. 现代诊断与治疗, 2018, 29(10): 1566-1568.
[20] 文隆, 卫志干. 肝爽颗粒联合恩替卡韦治疗乙肝后肝硬化效果及安全性分析 [J]. 医学食疗与健康, 2019(15): 72.
[21] 白莉, 罗小怀. 恩替卡韦与肝爽颗粒联合治疗慢性乙肝肝硬化的效果 [J]. 临床医学研究与实践, 2018, 3(35): 78-80.
[22] 索明果. 肝爽颗粒联合恩替卡韦治疗乙肝肝硬化的疗效及对患者肝功能的影响 [J]. 海峡药学, 2018, 30(11): 191-192.
[23] 陈丽英. 肝爽颗粒联合恩替卡韦抗病毒治疗乙肝肝硬化的效果及对患者肝功能影响观察 [J]. 当代医学, 2019, 25(16): 28-30.
[24] 韩珍霞. 恩替卡韦联合肝爽颗粒治疗乙型肝炎肝硬化失代偿期的效果研讨 [J]. 当代医药论丛, 2021, 19(6): 25-27.
[25] 刘强. 分析恩替卡韦联合肝爽颗粒治疗乙型肝炎后肝硬化的价值[J]. 养生保健指南, 2020(27): 70-71.
[26] 康玮玮, 卢颖, 陈煜. 肝爽颗粒治疗乙型肝炎肝硬化有效性与安全性的系统评价 [J]. 中国医药, 2017, 12(9): 1375-1378.
[27] 贾秀丽, 张伟, 王秋, 等. 恩替卡韦分散片联合肝爽颗粒治疗失代偿期乙型肝炎肝硬化患者的疗效观察 [J]. 健康大视野, 2019(13): 35.
[28] 邵丹丹. 肝爽颗粒联用恩替卡韦治疗乙肝肝硬化疗效观察 [J]. 医学新知杂志, 2018, 28(S1): 22-23.
[29] 杨艳峰. 58例乙肝肝硬化患者抗病毒治疗预后分析 [J]. 名医, 2019(9): 98.
[30] 杜子全. 恩替卡韦分散片联合肝爽颗粒治疗失代偿期乙型肝炎肝硬化患者的疗效观察 [J]. 健康必读, 2020(35): 197.
[31] 高世杰. 肝爽颗粒治疗肝硬化伴焦虑抑郁状态的临床研究 [J]. 心理月刊, 2021, 16(2): 41-42.
[32] 张耀武. 恩替卡韦分散片联合肝爽颗粒治疗失代偿期乙型肝炎肝硬化患者临床观察 [J]. 实用肝脏病杂志, 2013, 16(6): 550-551.
[33] 高峰, 李建红, 荀健. 肝爽颗粒治疗慢性乙型肝炎及代偿期肝硬化患者60例疗效分析 [J]. 山西职工医学院学报, 2014, 24(6): 24-25.
[34] 费卫东. 恩替卡韦分散片联合肝爽颗粒治疗失代偿期乙型肝炎肝硬化患者的临床疗效分析 [J]. 吉林医学, 2015, 36(1): 79-80.
[35] 王双. 恩替卡韦分散片联合肝爽颗粒对失代偿期乙型肝炎肝硬化的治疗价值分析 [J]. 中国继续医学教育, 2016, 8(9): 179-180.
[36] 尹国云, 郭小平. 探讨替比夫定联合肝爽颗粒治疗乙肝后肝硬化的疗效 [J]. 中外医疗, 2016, 35(28): 144-146.
[37] 王亮. 恩替卡韦联合肝爽颗粒治疗乙型肝炎后肝硬化的临床体会[J]. 中国保健营养, 2019, 29: 280.
[38] 赵敏. 肝爽颗粒联合恩替卡韦治疗乙型肝炎肝硬化失代偿期的临床效果观察 [J]. 首都食品与医药, 2019, 26(10): 64.
[39] 连小娟. 恩替卡韦联合肝爽颗粒在失代偿期乙肝肝硬化病人长期治疗中的安全性分析 [J]. 家庭医药·就医选药, 2020(12): 364-365.
[40] 王晓丽. 肝爽颗粒联合恩替卡韦治疗乙肝肝硬化临床疗效观察 [J]. 亚太传统医药, 2014, 10(4): 120-121.
[41] 崔俊芳, 张爱国, 范学科. 恩替卡韦分散片联合肝爽颗粒治疗失代偿期乙型肝炎肝硬化的价值评估 [J]. 临床医药文献电子杂志, 2018, 5(30): 76.
[42] 房荣, 马小勇. 肝爽颗粒联合恩替卡韦抗病毒治疗乙肝肝硬化的临床效果 [J]. 临床医学研究与实践, 2018, 3(3): 117-118.
[43] 廖宝生, 肖芸, 金克宁, 等. 肝爽颗粒联合恩替卡韦对乙肝肝硬化的作用分析 [J]. 临床医药文献电子杂志, 2019, 6(34): 38.
[44] 王海蓉. 肝爽颗粒联合恩替卡韦治疗代偿期乙型肝炎肝硬化患者临床研究 [J]. 中国药物与临床, 2020, 20(5): 760-762.
[45] 张国范. 干扰素加利巴韦林和肝爽颗粒治疗丙肝肝硬化 [J]. 医药论坛杂志, 2016, 37(3): 144-145.
[46] 邹刚, 学智. 恩替卡韦分散片联合肝爽颗粒对失代偿期乙型肝炎肝硬化的治疗效果探究 [J]. 中国农村卫生, 2020, 12(8): 45.
[47] 雷超, 张强, 王志飞, 等. 复方夏天无片治疗类风湿性关节炎的临床综合评价 [J]. 中草药, 2022, 53(21): 6810-6819.
[48] 樊亚东, 于爽, 张晓雨, 等. 肝爽颗粒对肝硬化和抑郁症“异病同治”的网络药理学机制分析 [J]. 天津中医药, 2021, 38(2): 240-246.
[49] 刘毅, 耿洪娇, 崔鑫, 等. 注射用灯盏花素治疗急性脑梗死和冠心病心绞痛的临床综合评价 [J]. 中草药, 2023, 54(19): 6413-6423.
[50] 刘炳林, 薛斐然. 药物临床价值评估的主要考虑因素及问题 [J]. 中国新药杂志, 2017, 26(5): 504-508.
Clinical comprehensive evaluation of Ganshuang Granules in treatment of liver cirrhosis (liver depression and spleen deficiency syndrome)
LU Zhen-kai1, ZHANG Li-dan1, LYU Jian2, XIE Yan-ming1
1. Institute of Basic Research in Clinical Medicine, China Academy of Chinese Medical Sciences, Beijing 100700, China 2. Xiyuan Hospital, China Academy of Chinese Medical Sciences, Beijing 100091, China
To evaluate the multi-dimensional value of Ganshuang Granules (肝爽颗粒) by systematic and multidisciplinary methods.According to the “Guidelines for the Management of Clinical Evidence and Value Evaluation of Drugs” standard, based on the evidence of evidence-based medicine and combined with questionnaire survey, health technology assessment (HTA), pharmacoeconomic evaluation and other research methods, the multi-criteria decision analysis model(MCDA) was used to comprehensively evaluate the clinical evidence and clinical value of the drug from the “6 + 1” dimensions of effectiveness, safety, economy, innovation, suitability, accessibility and characteristics of traditional Chinese medicine, and finally the “clinical evidence and value evaluation index” were formed.Based on the results of evidence adequacy and known risk assessment, the safety level of Ganshuang Granules is B, which is considered to be controllable and safe. Based on the results of evidence quality evaluation and evidence value evaluation, it is suggested that the efficacy of Ganshuang Granules combined with was superior to entecavir alone in improving alanine aminotransferase, aspartate aminotransferase, total bilirubin, albumin, laminin, type III procollagen, hyaluronic acid and type IV collagen in patients with cirrhosis (< 0.05), and the effectiveness level is A, which is considered to be effective and of great clinical significance. Ganshuang granules have certain innovation in clinical, enterprise and industry, and the innovation level is B; According to the cost-effectiveness results of Ganshuang Granules in the treatment of liver cirrhosis, it is considered that the drug is economical and economy grade is B; Based on the medical staff and patient questionnaire scores, suitability level is B; Compared with similar drugs, the price of Ganshuang granules is moderate and reasonable, and the affordability is good. It covers 2636 hospitals in 26 provinces, municipalities and autonomous regions across the country, and the accessibility level is B; Based on the evaluation rules of traditional Chinese medicine characteristics, the characteristic grade of traditional Chinese medicine is B, which is considered to be more prominent. Based on the results of “6 + 1” dimension, CSC V2.0 software was used to calculate the comprehensive measurement value of Ganshuang granules in the treatment of liver cirrhosis (liver stagnation and spleen deficiency syndrome) as category B.Based on the evaluation results and comprehensive evaluation scores of each dimension of Ganshuang Granules, it is shown that the clinical value of Ganshuang Granules is good. It is suggested to further carry out research on the pharmacodynamic mechanism, improve the quality of evidence-based evidence, and give full play to the clinical value advantages of Ganshuang Granules.
Ganshuang Granules; liver cirrhosis; liver injury; liver depression and spleen deficiency syndrome; comprehensive clinical evaluation
R285.64
A
0253 - 2670(2023)22 - 7526 - 10
10.7501/j.issn.0253-2670.2023.22.029
2023-03-13
国家重点研发计划项目(2018YFC1707400)
路振凯,在读博士,从事中药上市后评价研究。Tel: 13287760721 E-mail: 651411803@qq.com
通信作者:谢雁鸣 E-mail: ktzu2018@163.com
吕 健 E-mail: dr.jianlyu-tcm@outlook.com
[责任编辑 潘明佳]