中药毒性相关数据库的研究现状及对比研究
聂嘉璇,钱文秀,王曼姝,王佳艺,张 悦,刘慧敏,马 宁,宋丽丽,李遇伯
中药毒性相关数据库的研究现状及对比研究
聂嘉璇,钱文秀,王曼姝,王佳艺,张 悦,刘慧敏,马 宁,宋丽丽*,李遇伯*
天津中医药大学中药学院,天津 301617
中药毒性研究是中药安全性研究的重要议题,将具有毒性的中药成分及其作用机制进行整理是进行中药毒性研究的基础。因此,通过当前国内外中药毒性研究相关的数据库进行综述,总结中药毒性研究相关数据库的研究现状,突出中药毒性研究相关数据库在科学研究中的重要性,为中药毒性研究工作提供参考,促进中药毒性研究的进一步发展。
中药;毒性;数据库;对比研究;毒性成分
中药作为我国的宝贵财富,已有数千年历史[1-2],广泛用于预防和治疗疾病[3],在新型冠状病毒肺炎期间发挥了重要作用[4–6],是中华民族的智慧结晶。随着中药的现代化和国际化,对其质量控制的要求也越来越高[7]。同时,由于用药不合理、质量不稳定等原因,导致中药引发不良反应的情况时有发生。当前社会各界对中药安全重视程度越来越高,但其在发挥强大的治疗作用的同时,安全性问题也不容忽视[8]。同时,中药中化合物的数量庞大,其功效、理化性质和药动学的评价多样[9],使得研究者较难筛选适用的药物及成分[10],降低了中药研究者的工作效率,如何通过快速、高效手段推动中药安全性研究进程是一项亟待解决且重要的工作。
进入21世纪,数据库技术迎来了快速发展的时期,数据库具有对数据信息进行挖掘、存储、计算、分析等功能,能够帮助提高科研工作的效率,有助于提高中药研究的效率和准确性[10-11],因而将其应用于中医药领域是研究者关注的热点。目前,用于辅助科研工作的数据库一般不会只用于数据存储,而是会在数据库中设置多种功能以提高数据库的使用价值,已在多个领域[12-18]被广泛使用。通过资料考察发现,当前数据库技术在中医药领域的研究中已逐渐占据重要地位,目前已上线使用的数据库种类多样[19],能够基本满足不同科研方向的研究需求。中药毒性研究相关数据库的构建有助于开展中药毒性研究[20],本文通过对现有用于中药毒性研究相关的数据库进行分类并简要介绍,阐述数据库在中药毒性研究中的重要作用,为从事中药毒性研究的研究者提供参考。
1 中药毒性研究相关数据库现状
数据库是在各种信息研究过程中对大量的原始资料进行分析、整理、补充和完善而建立起来的。随着计算机技术的不断发展,数据库在中药毒性领域研究发挥着重要作用。本文通过PubMed、Web of Science和中国知网等在线数据库使用“traditional Chinese medicine”“toxicity”“database”等检索词检索并筛选在中药毒性研究中使用的到数据库进行整理。将目前常用于中药毒性研究的数据库主要分为以下几种。(1)疾病相关数据库:这类数据库收录了导致疾病损伤的中药及成分,阐明了疾病与环境暴露等之间的关系,可以更好地说明化学成分和疾病间的关系,如LiverTox数据库[21]、药物性肝损伤专业数据库(Hepatox)[22]、TCM-Mesh数据库[23];(2)成分相关数据库:这类数据库收集了与中药成分相关信息,可以将药材与成分进行关联,该类数据库用于中药毒性研究时常用于收集毒性成分的相关信息,如TCM Database@Taiwan数据库[24]、中医药综合数据库(traditional chinese medicine integrated database,TCMID)[25]、本草组鉴数据库(HERB)[26],中药系统药理学数据库和分析平台(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP)[27];(3)机制靶点相关数据库:这类数据库包含了中药的药物及靶点信息,将药物与靶点信息进行关联,有助于中药功能及机制研究,如比较毒物基因组学数据库(comparative toxicogenomics database,CTD)[28]、副作用资源数据库(side effect resource,SIDER)[29]、中医药百科全书数据库(encyclopedia of traditional Chinese medicine,ETCM)[30]、中药系统毒理学数据库(traditional Chinese medicine system toxicology database,TCMSTD)[31]、中药血液吸收成分及代谢物数据库(database of constituents absorbed into the blood and metabolites of TCM,DCABM-TCM)[32]、TCMBank数据库[33];(4)代谢相关数据库:可提供中药毒性成分代谢相关的信息,为中药毒性成分代谢研究提供基础,如草药成分体内代谢数据库(herbal ingredients in-vivo metabolism database,HIM)[34];(5)风险评估相关的数据库:这类数据库收录中药潜在有毒元素的信息,并利用模拟模型进行风险评估,可以提高风险评估效率,如中药中金属和类金属概率风险评估数据库(risk assessment of metals and metalloids in traditional Chinese medicine,MRTCM)[35]。
1.1 CTD数据库
CTD数据库是由毒理学数据网络提供的可以公开免费访问的毒理信息资源库,该数据库通过人工整理和相互关联已发表文献中的化学、基因、表型、解剖学、疾病、分类群和暴露内容,协调了化学暴露及其生物影响的跨物种异质数据,收集了17 117种化学成分、54 355个基因、6187种表型、7274种疾病和202 000次暴露事件等,包括化学-基因相互作用、化学-疾病、基因-疾病、化学-表型和化学-环境暴露数据,可供研究者查阅有毒化学品相关的信息,为研究者更好地理解疾病与患病的关系,有助于研究者探索受环境影响疾病的发病机制[28,36-41]。
1.2 TCM Database@Taiwan数据库
TCM Database@Taiwan数据库由台湾中国医药大学整理完成,适应目前中药研究中需要更多的中药三维小分子结构的要求,研究者通过收集文献信息等方式进行构建,包含从453种中药中分离出的20 000多种化合物及化合物的cdx(2D)和Tripos mol2(3D)2种格式的下载和虚拟筛选,研究者可通过简单和高级检索查找分子特性、子结构、中药成分和中药分类等信息,方便研究者进行中药成分的查找和满足其虚拟筛选的需要[24]。
1.3 TCMID数据库
TCMID数据库最初于2013年推出,旨在实现中医药现代化和标准化的综合数据库,通过文献信息收集和整合TCM Database@Taiwan、HIT等多个数据库信息,包括超过49 000个处方、8159种药材、43 413种成分、4633种疾病和8182种药物。此外,附加了中药材与中药成分相关的质谱图,以显示不同产地中药材品质的差异,为药材和成分鉴定提供依据,加强对中药不同药理作用的潜在生物过程的探索,促进了方剂和药材的机制研究[9,25]。
1.4 LiverTox数据库
LiverTox数据库由美国国家糖尿病、消化和肾病研究所的肝病研究院与美国国家医学图书馆合作创立,是1个多层次、信息和互动的数据库,公开提供有关化学药、中草药和食品补充剂引起的肝损伤的全面准确信息,提供已知或可能导致肝损伤的药物超过1400多种,包括其诊断、原因、频率、临床模式、病程和已知或可能的肝损伤机制,供医生、研究者和公众免费访问,该网站还提供每种药物肝损伤完整、准确的临床特征信息摘要及文献,有助于患者寻求药物引起的肝损伤信息,并对相关专家的研究有很大帮助。同时,该网站简要描述了每种药物的肝毒性风险,可用于支持肝损伤预防和控制的临床研究,为临床诊断和管理肝损伤提供指导[21,36,42-43]。
1.5 Hepatox数据库
Hepatox数据库依托上海交通大学医学院附属仁济医院承担的国家科技部十二五重大专项课题构建,是中国建立的第1个在线药物性肝损伤数据库,且为免费开放,其包括最新资讯、医学知识、药物信息、专业术语、行业资源、资料下载和在线应用7大版块。其中药物信息版块整理总结了400多种化学药和中草药导致药物肝损伤的症状、诊断和机制等信息,尤其总结了导致肝毒性的中药诊疗信息,有助于公众了解不同药物的肝毒性信息,还可以帮助医生或患者在处方或服药时监测可能发生的肝损伤风险。该数据库允许用户根据药物名称或药物类别搜索感兴趣的药物。有助于用户快速获取信息。同时,Hepatox是一个交互式网站,允许用户提交与药源性肝损伤相关的病例报告,极大帮助了药物性肝病的诊断、管理、预防和治疗[22,36,44]。
1.6 TCMSP数据库
TCMSP数据库是在中药系统药理学的框架下建立的,包括499种中草药的29 384种成分、3311种靶点和837种相关疾病,并提供了12个重要的吸收、分布、代谢和排泄(absorption, distribution, metabolism and excretion,ADME)相关特性,如人体口服生物利用度、半衰期、药物亲和性、Caco-2渗透性、血脑屏障和类药五项规则等,TCMSP数据库还提供每种活性成分的作用靶点和相关疾病,可以建立化合物靶点和疾病靶点网络,供用户查看和分析药物作用机制,有助于研究者对中草药作用机制的研究,可用于药物筛选和评价,加速了中药的药物发现[27]。
1.7 SIDER数据库
SIDER数据库将药物、靶点和不良反应的数据结合起来,记录1430种药物、5880种不良反应和140 064对药物不良反应的数据,收集了上市药品及其记录的药品不良反应的信息,包括药物不良反应频率、不良反应分类、药物-靶点关系等,更全面记录药物治疗作用机制和引起不良反应的方式,有助于阐明并减少药物不良反应。此外,SIDER数据库还包含1组药物适应证和不良反应发生频率,这些信息可用于降低药物不良反应发生,并降低假阳性率,提高药物使用安全[29]。
1.8 HERB数据库
HERB数据库是1个中药高通量实验和参考指导的数据库,分析了来自1037个高通量实验的6164个基因表达谱,并将全面的药物转录组学数据集与现代药物的最大数据集CMap进行映射,总结中药材/成分与现代药物机制之间的联系,包括7263种草药、12 933种靶标和49 258种成分,成为评估药物疗效和发现新药物靶点的有力方法,为中药现代化和新药发现提供依据[26]。
1.9 HIM数据库
HIM数据库收集了中草药活性成分的体内代谢信息,及其相应的生物活性、毒性、ADME和临床研究概况。目前,HIM包含了来自673种药材的361种成分和1104种相应的体内代谢物,可用于搜索中药活性成分的代谢物,还可用于获得与查询化合物潜在相似的生物活性的化合物,并且可以提供查询分子的其他化学和生物学信息。因此,HIM数据库可以为中药活性成分体内代谢信息提供系统准确的数据,为中药、药物设计、生药、药物代谢等领域研究者提供有价值的信息[34]。
1.10 TCM-Mesh数据库
TCM-Mesh数据库系统记录了从各种资源中收集的中药相关信息,用于搜索中药制剂、小分子及基因和疾病。该数据库包含6235个中药材、383 840个化合物、14 298个基因、6204个疾病、144 723个基因与疾病关联、3 440 231对基因相互作用、163 221个不良反应记录和71个毒性记录,基于Web的软件构建了中药与治疗疾病之间的网络,基于此数据库可以有效建立“化合物-蛋白质/基因-疾病”网络,并以高通量的方式揭示小分子的调控原理,有助于从分子水平上了解中药制剂的潜在机制[23]。
1.11 ETCM数据库
ETCM数据库包括中医常用药材和配方及其成分的全面和标准化的信息,纳入403种中药、3962个复方、7274个中药成分、2266个疾病靶标,包括草药基本性质和质量控制标准、配方组成、成分药物相似性、中药成分、草药和配方的预测靶基因和其他信息。不仅包括中药材和配方的详细药用特性,而且还提供了中药靶基因与现代疾病间的潜在联系。此数据库为用户提供了1个易于使用的平台,可以从各方面浏览、搜索和分析中医药相关信息,促进中药的功能和机制研究[30]。
1.12 TCMSTD数据库
TCMSTD数据库是由天津中医药大学2022年创建的国内外首个中药系统毒理学数据库,该数据库通过手动收集文献信息等方法,收录有毒中药252种、不良反应制剂22首、化学成分4361种、有毒成分226种、毒性靶点2425种,系统整合和分析有毒中药的研究成果,提供中药成分毒性作用和毒性靶点预测功能,有助于更好地进行中药毒性研究[31]。
1.13 MRTCM数据库
MRTCM是1个综合性数据库,包括消费数据库、污染物数据库和概率风险评估算法,涉及4000万条消费数据和14种中药潜在有毒元素浓度及利用蒙特卡罗模拟评估8个要素的风险,适用于中药的风险评估。总体而言,通过该数据库中医药风险管理可以显著提高风险评估效率,为决策者优化风险管理提供合理指导[35]。
1.14 DCABM-TCM数据库
DCABM-TCM数据库是第1个系统收集中药方剂和中草药血液成分的数据库,包括血液中实验检测到的原型和代谢物,及通过人工文献挖掘得到的相应的详细检测条件。DCABM-TCM数据库收集了192个处方和194种中草药的1816种血液成分及其化学结构,并整合了其相关注释,包括理化、ADME和毒性特性及相关靶点、途径和疾病。此外,DCABM-TCM数据库还支持2种基于血液成分的分析功能,用于中药分子机制阐释的网络药理学分析,及用于中药新药研发的基于靶点/途径/疾病的候选血液成分、中药或方剂筛选[32]。
1.15 TCMBank数据库
TCMBank数据库是目前世界最大的中医药数据库,该数据库提供了9192种草药、61 966种成分、15 179个靶标、32 529种疾病及其内在关联信息,该数据库还提供了草药中活性成分以mol2格式存储的3D结构。研究者可以在TCMBank的下载页面访问这些数据,并用于中药的虚拟筛选。此外,该数据库还针对中西药间可能发生的不良反应,设计了1个新颖算法的技术,利用人工智能辅助的预测模型获得了中西医可能的不良反应风险的预测结果,为用户提供了一个方便的网站,让用户可以自由探索草药、成分、基因靶标及相关通路或疾病间的关系[33]。
2 数据库在中药毒性研究中的应用情况
中药毒性研究是现代药学中的一个重要领域,其主要目的是研究中药的毒性和不良反应,为临床用药提供科学依据。目前,数据库主要用于毒性成分筛选、毒性信息整理、核心毒性靶标挖掘等多方面,是中药毒性研究中的重要基础,为中药毒性研究提供帮助。见图1。
2.1 毒性成分筛选
中药毒性成分的筛选是进行中药毒性研究的基础,可以通过相关数据库收集毒性成分作为后续研究的前提。阐明中药的活性成分对于理解中药的机制,促进中药的合理使用及中药衍生药物的开发尤为重要。通过数据库技术可以更加高效的筛选出中药毒性成分,将阐明中药的药理机制并促进其现代化。李雅秋等[45]使用SIDER等数据库收集与心脏毒性有关的化合物作为构建定量构效关系模型的训练集,模型灵敏度高达95%,特异度为60%,整体预测准确率达到83%,构建良好的预测心脏毒性的模型,可以筛选出具有潜在心脏毒性的中药化学成分,减少不良反应,为中药的安全性研究和药物开发提供有价值的信息。张丹等[46]使用TCMSP等数据库收集成分及靶标信息,通过蛋白相互作用分析及通路富集分析和分子对接等方法发现雷公藤碱乙、雷酚内酯和山海棠二萜内酯A可与细胞周期蛋白D1、丝裂原活化蛋白激酶8、血管内皮生长因子A、肿瘤抑制基因p53、白细胞介素-6(interleukin-6,IL-6)、肿瘤坏死因子毒性靶标有着较好的相互作用与结合活性,从而初步确定以上3种成分可能为昆明山海棠的毒性成分,为发现昆明山海棠的可能毒性机制提供依据。
2.2 毒性信息整理
毒性信息可以帮助研究者了解相关药物与临床数据,为中药安全性提供帮助。近年来,随着中医药的广泛接受和认可,其诱发的肝毒性也逐渐增多。我国约26.81%的肝毒性临床病例是由草药和膳食补充剂引起的。因此,应重视草药引起的肝毒性[47]。Li等[48]通过分析Hepatox数据库收集药物性肝损伤患者的临床数据。发现接受治疗护肝片组丙氨酸氨基转移酶和天冬氨酸氨基转移酶的正常化率显著高于对照组,为探索护肝片对不同致敏药物诱导的药物性肝损伤提供帮助。Teschke等[49]使用LiverTox数据库整理自2011年以来报道的肝毒性药物,为快速找到与某种药物相关的肝毒性信息。通过对上述信息的分析,可以更好地了解药物的作用机制和潜在风险,以提高中药质量和安全性。
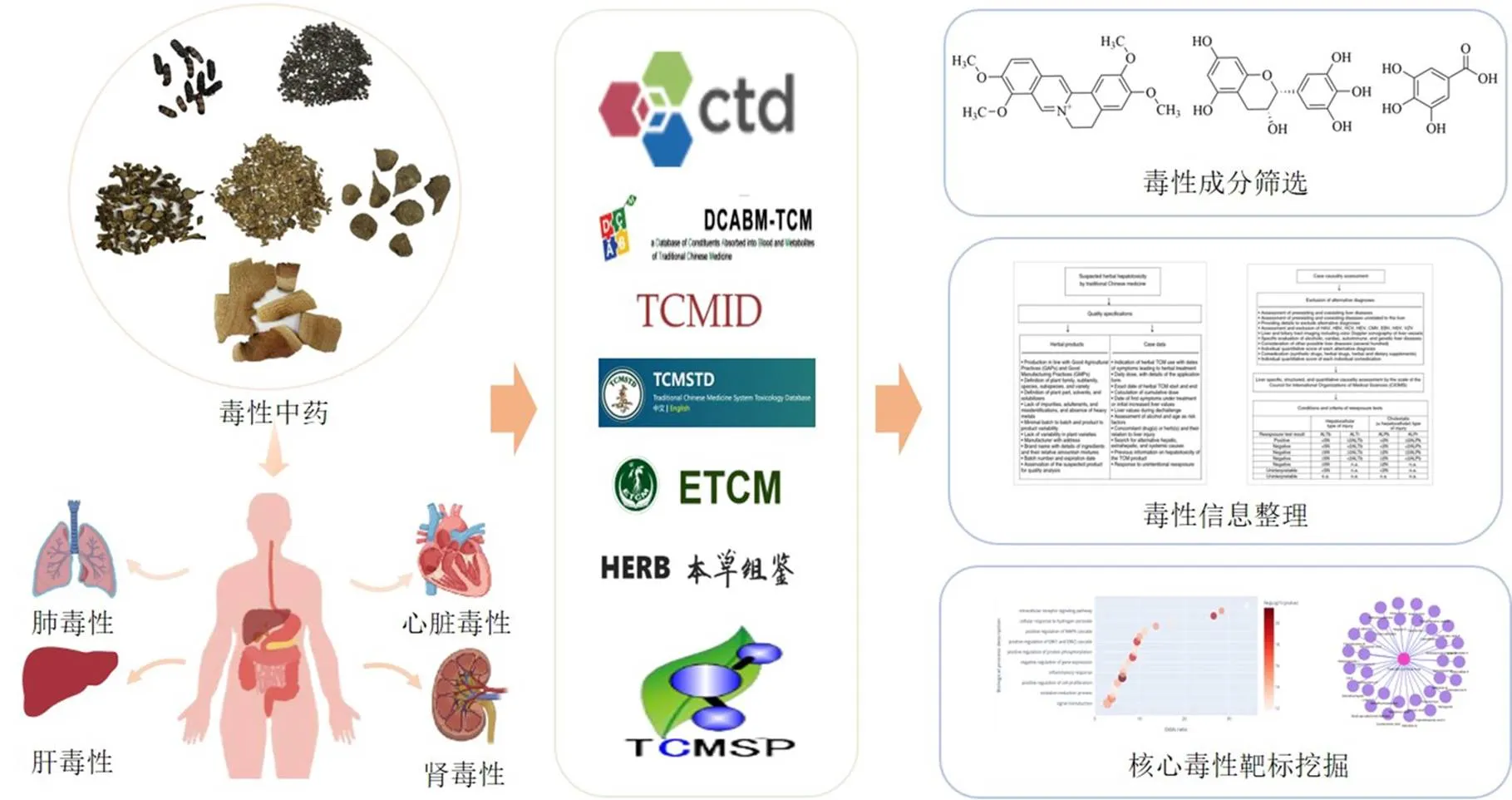
图1 中药相关毒性数据库应用情况概述
2.3 核心毒性靶标挖掘
由于中药的复杂性,对中药的疗效、不良反应和作用机制不明,阻碍了其发展。在研究毒理学信息中,可以通过相关数据库需要收集毒性靶点,发现与毒性成分密切相关的靶点,阐明其蛋白靶标及化合物与靶标间的关系。Dai等[50]利用TCMSP等数据库建立了马钱子靶点和中枢神经系统相关基因集,构建了“成分-目标”交互式活动网络,得到5个马钱子毒性相关成分和40个相关基因组。结果表明()-士的宁表现出更强的神经毒性作用,胆碱能受体毒蕈碱1是马钱子产生神经毒性的潜在靶点,本研究为马钱子毒性研究提供帮助。此外,补骨脂肝毒性研究已引起广泛关注[51]。曹站霞等[52]通过CTD等数据库筛选补骨脂潜在毒性成分,并收集肝损伤相关靶蛋白,然后与成分作用靶标匹配得到共有靶基因,构建补骨脂肝损伤潜在毒性成分-靶标-通路网络,筛选得到25个补骨脂潜在毒性成分,并发现蛋白激酶B1等可能是补骨脂致肝损伤的关键靶点,为进一步阐明其肝损伤物质基础和作用机制提供参考和依据。Liao等[39]使用TCMDatabase@Taiwan等数据库检索泽泻导致肝肾毒性的化合物与靶点,最终发现10个化合物,228个靶标与泽泻诱导的肝肾毒性有关,通过数据库与网络药理学等联合进一步阐明了泽泻诱导的肝肾毒性的机制。Xiao等[53]使用CTD数据库匹配的毒理学信息,建立其潜在毒性成分的数据集并获取相关靶点,得到藤茶的潜在肝毒性靶点,得到藤茶的34个潜在毒性成分和57个潜在的肝毒性靶点,为进一步研发相关功能产品提供了参考。Chen等[54]根据TCMSP、CTD等数据库筛选雷公藤多糖的主要生物活性成分和相关靶点,发现雷公藤多糖有145个肝毒性靶点,其可能诱发的肝脏毒性也与IL-17信号通路和辅助性T细胞17细胞分化的调节显著相关,揭示其可能诱发肝毒性的机制,为雷公藤多糖肝毒性研究提供依据。
3 中药相关毒性数据库对比研究
通过对不同数据库进行整合和梳理,进一步对不同数据库中的毒性信息进行对比研究,揭示中药相关毒性数据库中存在的共性和差异,有助于毒性研究分析,以期提高中药安全性评估的准确性和完整性,有助于进一步完善相关毒性数据库,还可以为中药的合理使用和监管提供参考。见表1。
目前在中药毒性研究中应用到的数据库较多,但是CTD数据库主要针对化学药研究;SIDER数据库主要针收录药物不良反应信息;LiverTox、Hepatox数据库主要提供针对肝损伤相关中药的信息;HIM数据库收录体内代谢相关毒性,纳入信息较为局限,对于中药毒性研究相对不够集中;TCMID、TCM Database@Taiwan、TCM-Mesh、TCMSP、HERB、ETCM等数据库主要进行中药系统药理学研究,多关注基于吸收的原型成分与治疗相关靶点相互作用的直接作用,不同量的多种成分在各种疾病的治疗中作用。然而,没有适当的数据库来确定中药毒性成分、靶标、途径和生物活性的多维关联,对于中药毒性研究不够系统[55]。TCMSTD数据库虽然较为系统整理了中药毒性数据,但是毒性成分少,建立数据库所用的算法较老,且是1种新开发的数据库,应用较少。因此,在中药毒性研究中应用的数据库主要是中药药理学和成分挖掘、筛选相关的数据库,仍需加强开发利用专注于中药毒性研究的数据库,对有毒中药的研究内容进行系统的整合,推动中药毒性研究工作。

表1 中药相关毒性数据库的主要特点
4 中药毒性数据库应用前景分析
计算机和人工智能的应用在中医药领域的药物虚拟筛选和设计中发挥着重要作用,应用前景巨大[55]。中药毒性研究是中药现代化研究的重要组成部分,但是毒性的机制仍不明晰[56],通过文献总结发现,数据库技术因其便捷、快速、高效等特点,已被成功运用于中药领域的研究中,将候选化合物的靶点与毒性靶点关联后,应用数据库技术和网络药理学结合研究潜在的肝毒性机制,模拟分子对接以揭示分子机制,无疑会促进中医药的传承、创新和发展[57]。但目前数据库技术用于中药药理学研究的居多,疾病类数据库研究以肝损伤为代表[58]。但中药成分众多,进行中药毒性研究需要把所有相关文献进行查阅并整理[59],导致目前中药毒性研究进展缓慢[52,60],而数据库技术又是基于现有的研究成果建立起来的,需要研究者不断维护,因此在中药毒性研究领域的应用较少。
数据库技术在中药毒性领域中的应用仍处于起步阶段,进行中药毒性研究不够便捷,像TCMSTD这样专注于中药毒理学研究的数据库使用仍不够广泛。因此,未来希望可以进一步完善TCMSTD数据库,在中药毒性研究中得到更加广泛的应用。同时,研究者可充分利用数据库技术,开发出更加适合中药毒性研究的数据库,推动数据库在中药毒性研究更加精准的应用。
5 结语与展望
传统有关中药毒性研究的信息大多从文献检索中获得的,既耗时又困难。而可公开访问的数据库提供有关中药毒性相关的目标的全面信息,可以提供一个方便和有用的平台,将成为帮助研究者进行中药安全性研究的有力工具[36]。本文介绍了在中药毒性研究中应用到的数据库并列举了其在中药毒性研究的成功案例,体现中药毒性相关数据库在毒性成分筛选、毒性信息整理、核心毒性靶标挖掘等多方面的应用,既说明了数据库技术在中药毒性研究中的重要价值,又为推动中药毒性研究进展提供了参考思路。总之,数据库为用户提供了一个方便的界面来浏览、搜索、可视化和下载关键信息[26],可以更好地管理中药毒性研究信息,有助于深入了解中药毒性的本质,为进行毒性关联性分析的基础,找出中药毒性与药物成分、剂型、用法用量等因素间的关联性,进一步优化中药的安全性评估方法,对现有的中药相关毒性数据库进行整合和完善,提高数据的准确性和完整性,为监管部门提供决策依据,发现中药在现代化过程中存在的问题和挑战,从而为中药的现代化发展提供指导。
数据库技术在中药毒性研究中具有重要的价值和应用前景,为中药的安全性和有效性评价提供科学依据。随着计算机技术的不断发展,相信数据库会更加贴合中药毒性研究、增加中药配伍毒性的评价,将中药方剂等毒性研究整合成丰富的知识网络。数据库技术定将成为未来中药快速发展进程中不可或缺的重要工具,为中医药大数据领域提供优质的资源[26],提高研究效率和准确性,为中药研究的安全性和有效性评价提供有力支持,将使中医药与现代医学和药理学标准更好的接轨。
利益冲突 所有作者均声明不存在利益冲突
[1] Coghlan M L, Haile J, Houston J,. Deep sequencing of plant and animal DNA contained within traditional Chinese medicines reveals legality issues and health safety concerns [J]., 2012, 8(4): e1002657.
[2] Shi J C, Gao X X, Zhang A R,. Characterization of multiple chemical components of GuiLingJi by UHPLC-MS and1H NMR analysis [J]., 2022, 12(3): 460-469.
[3] 罗超, 涂斯婧, 李宁宁, 等. 中药复方治疗抗精神病药物所致代谢综合征的用药规律和潜在作用机制研究[J]. 中草药, 2022, 53(5): 1494-1503.
[4] Luo L, Jiang J W, Wang C,. Analysis on herbal medicines utilized for treatment of COVID-19 [J]., 2020, 10(7): 1192-1204.
[5] 王耘, 潘博宇, 房森彪, 等. 利用网络药理学方法探讨针对新型冠状病毒肺炎以ACE2为治疗靶点的5味中药的作用机制和组分配伍[J]. 中草药, 2020, 51(18): 4691-4697.
[6] Wu D Y, Hou X T, Xia Z S,. Analysis on oral medication rules of traditional Chinese medicine prescriptions for prevention of COVID-19 [J]., 2021, 13(4): 502-517.
[7] Lu X Y, Jin Y Y, Wang Y Z,. Multimodal integrated strategy for the discovery and identification of quality markers in traditional Chinese medicine [J]., 2022, 12(5): 701-710.
[8] 张冰, 吕锦涛, 张晓朦, 等. 基于“药性” 的中药“毒-效” 认知与药物警戒思考 [J]. 中国药物警戒, 2021, 18(5): 411-415.
[9] Xue R C, Fang Z, Zhang M X,. TCMID: Traditional Chinese Medicine integrative database for herb molecular mechanism analysis [J]., 2013, 41(Database issue): D1089-D1095.
[10] Lin Y M, Zhang Y, Wang D Y,. Computer especially AI-assisted drug virtual screening and design in traditional Chinese medicine [J]., 2022, 107: 154481.
[11] 顾志荣, 毛小文, 祁梅, 等. 数据融合技术在中药研究领域的应用 [J]. 中草药, 2023, 54(18): 6159-6171.
[12] de Sousa Luis J A, Barros R P C, de Sousa N F,. Virtual screening of natural products database [J]., 2021, 21(18): 2657-2730.
[13] 刘明皓, Faez I K, 肖雨晴, 等. 基于分子对接与动力学模拟的用于治疗新型冠状病毒肺炎的中药活性成分虚拟筛选研究 [J]. 生物医学工程学杂志, 2022, 39(5): 1005-1014.
[14] 于洋, 左平春, 张楠, 等. 计算毒理学在农药风险评估中的应用 [J]. 农药科学与管理, 2017, 38(4): 24-30.
[15] 姜允申. 计算毒理学和量子毒理学在我国环境医学与药物学研究中的应用及前景 [A] // 2020中国环境科学学会科学技术年会论文集[C]. 南京: 中国环境科学学会, 2020: 85-89.
[16] Vuorinen A, Bellion P, Beilstein P. Applicability ofgenotoxicity models on food and feed ingredients [J]., 2017, 90: 277-288.
[17] Silva M H. Use of computational toxicology (CompTox) tools to predicttoxicity for risk assessment [J]., 2020, 116: 104724.
[18] Forest V. Experimental and computational nanotoxicology—Complementary approaches for nanomaterial hazard assessment [J]., 2022, 12(8): 1346.
[19] 王凤雪, 高宇, 刘海波. 中药网络药理学研究流程及代表性数据库工具 [J]. 中国现代中药, 2021, 23(6): 1111-1118.
[20] 张贵彪, 陈启龙, 苏式兵. 中药网络药理学研究进展 [J]. 中国中医药信息杂志, 2013, 20(8): 103-106.
[21] Hoofnagle J H, Serrano J, Knoben J E,. LiverTox: A website on drug-induced liver injury [J]., 2013, 57(3): 873-874.
[22] 中国药物性肝损伤首个网站“HepaTox” 正式发布 [J]. 上海交通大学学报: 医学版, 2014, 34(6): 938.
[23] Zhang R Z, Yu S J, Bai H,. TCM-Mesh: The database and analytical system for network pharmacology analysis for TCM preparations [J]., 2017, 7(1): 2821.
[24] Chen C Y C. TCM Database@Taiwan: The world’s largest traditional Chinese medicine database for drug screening in silico [J]., 2011, 6(1): e15939.
[25] Huang L, Xie D L, Yu Y R,. TCMID 2.0: A comprehensive resource for TCM [J]., 2018, 46(D1): D1117-D1120.
[26] Fang S S, Dong L, Liu L,. HERB: A high-throughput experiment- and reference-guided database of traditional Chinese medicine [J]., 2021, 49(D1): D1197-D1206.
[27] Ru J L, Li P, Wang J N,. TCMSP: A database of systems pharmacology for drug discovery from herbal medicines [J]., 2014, 6: 13.
[28] Davis A P, Wiegers T C, Johnson R J,. Comparative toxicogenomics database (CTD): Update 2023 [J]., 2023, 51(D1): D1257-D1262.
[29] Kuhn M, Letunic I, Jensen L J,. The SIDER database of drugs and side effects [J]., 2016, 44(D1): D1075-D1079.
[30] Xu H Y, Zhang Y Q, Liu Z M,. ETCM: An encyclopaedia of traditional Chinese medicine [J]., 2019, 47(D1): D976-D982.
[31] Song L L, Qian W X, Yin H Q,. TCMSTD 1.0: A systematic analysis of the traditional Chinese medicine system toxicology database [J]., 2023, 66(9): 2189-2192.
[32] Liu X Y, Liu J Y, Fu B Z,. DCABM-TCM: A database of constituents absorbed into the blood and metabolites of traditional Chinese medicine [J]., 2023, 63(15): 4948-4959.
[33] Lv Q J, Chen G X, He H H,. TCMBank-the largest TCM database provides deep learning-based Chinese- western medicine exclusion prediction [J]., 2023, 8(1): 127.
[34] Kang H, Tang K L, Liu Q,. HIM-herbal ingredientsmetabolism database [J]., 2013, 5: 28-28.
[35] Xu X H, Li L M, Zhou H,. MRTCM: A comprehensive dataset for probabilistic risk assessment of metals and metalloids in traditional Chinese medicine [J]., 2023, 249: 114395.
[36] Luo G W, Shen Y T, Yang L Z,. A review of drug-induced liver injury databases [J]., 2017, 91(9): 3039-3049.
[37] Davis A P, Grondin C J, Johnson R J,. Comparative toxicogenomics database (CTD): Update 2021 [J]., 2021, 49(D1): D1138-D1143.
[38] 刘福志, 朱丹丹, 陈扬佳, 等. 基于CTD数据库的双酚A及其衍生物双酚F和双酚S的生物信息学分析 [J]. 毒理学杂志, 2022, 36(5): 442-447.
[39] Liao Y L, Ding Y L, Yu L,. Exploring the mechanism offor the treatment of pregnancy induced hypertension and potential hepato-nephrotoxicity by using network pharmacology, network toxicology, molecular docking and molecular dynamics simulation [J]., 2022, 13: 1027112.
[40] 闫小妮, 田国祥, 贺海蓉, 等. CTD数据库架构及数据获取查询与提取方法 [J]. 中国循证心血管医学杂志, 2019, 11(8): 905-909.
[41] 陆韻, 侯凌燕, 胡洪营, 等. 毒理基因组学研究进展 [J]. 生态环境学报, 2010, 19(9): 2232-2239.
[42] 姚克宇, 张舒琪, 金锐, 等. 药物致肝损伤数据集的比较研究 [J]. 中国药物警戒, 2023, 20(5): 568-573.
[43] 本刊编辑部. 美国国立卫生研究院推出肝损伤相关药物免费数据库LiverTox [J]. 中华医学图书情报杂志, 2012, 21(11): 15.
[44] 茅益民. HepaTox: 促进中国药物性肝损伤临床和转化研究的专业网络平台 [J]. 肝脏, 2014, 19(8): 575-576.
[45] 李雅秋, 王旗. 构建用于预测中药化学成分心脏毒性的定量构效关系模型 [J]. 北京大学学报: 医学版, 2017, 49(3): 551-556.
[46] 张丹, 董一珠, 吕锦涛, 等. 基于网络药理学与分子对接方法探讨昆明山海棠的毒性机制 [J]. 北京中医药大学学报, 2019, 42(12): 1006-1015.
[47] Zulkifli M H, Abdullah Z L, Mohamed Yusof N I S,.toxicity studies of traditional Chinese herbal medicine: A mini review [J]., 2023, 80: 102588.
[48] Li J, Zhang J Z, Xu X R,. Hugan Tablets for the treatment of RUCAM based drug-induced liver injury: A propensity score matching analysis using a nationwide database [J]., 2021, 14(12): 1543-1550.
[49] Teschke R, Wolff A, Frenzel C,. Review article: Herbal hepatotoxicity: An update on traditional Chinese medicine preparations [J]., 2014, 40(1): 32-50.
[50] Dai J L, Liu J J, Zhang M X,. Network toxicology and molecular docking analyses on strychnine indicate CHRM1 is a potential neurotoxic target [J]., 2022, 22(1): 273.
[51] 王曼姝, 孙思彤, 袁宇, 等. 功能代谢组学在中药毒性评价中的研究策略及其应用 [J]. 中草药, 2023, 54(2): 349-358.
[52] 曹站霞, 陈毓龙, 李伟霞, 等. 基于网络药理学和细胞试验探讨补骨脂致肝损伤的毒理机制 [J]. 中国现代应用药学, 2022, 39(16): 2052-2062.
[53] Xiao F Y, Qiu J H, Zhao Y. Exploring the potential toxicological mechanisms of vine tea on the liver based on network toxicology and transcriptomics [J]., 2022, 13: 855926.
[54] Chen Y, Wang Y F, Song S S,. Potential shared therapeutic and hepatotoxic mechanisms ofpolyglycosides treating three kinds of autoimmune skin diseases by regulating IL-17 signaling pathway and Th17 cell differentiation [J]., 2022, 296: 115496.
[55] Xu H Y, Zhang Y Q, Wang P,. A comprehensive review of integrative pharmacology-based investigation: A paradigm shift in traditional Chinese medicine [J]., 2021, 11(6): 1379-1399.
[56] Gao P, Chang K, Yuan S,. Exploring the mechanism of hepatotoxicity induced bybased on network pharmacology, molecular docking and experimental pharmacology [J]., 2023, 28(13): 5045.
[57] Wang Z Y, Li S. Network pharmacology in quality control of traditional Chinese medicines [J]., 2022, 14(4): 477-478.
[58] Wang J B, Song H B, Ge F L,. Landscape of DILI-related adverse drug reaction in China Mainland [J]., 2022, 12(12): 4424-4431.
[59] Gao Y B, Fan H, Nie A Z,. Aconitine: A review of its pharmacokinetics, pharmacology, toxicology and detoxification [J]., 2022, 293: 115270.
[60] 杨彬, 高文远, 张艳军. 基于转录组学-蛋白质组学-多肽组学整合关联分析策略的动物药蛋白多肽类成分研究思路及方法 [J]. 中草药, 2019, 50(5): 1033-1038.
Research status and comparative study on toxicity related databases of traditional Chinese medicine
NIE Jia-xuan, QIAN Wen-xiu, WANG Man-shu, WANG Jia-yi, ZHANG Yue, LIU Hiu-min, MA Ning, SONG Li-li, LI Yu-bo
School of Traditional Chinese Medicine, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China
The study of toxicity of traditional Chinese medicine (TCM) is an important topic in safety research of TCM. Toxic TCMs’ components, and their mechanisms of action is the foundation for conducting toxicity research of TCM. Therefore, a review is conducted on the current databases related to the toxicity research of TCM both domestically and internationally, summarizing the current research status of databases related to TCM toxicity research, highlighting the importance of databases related to TCM toxicity research in scientific research, providing reference for the study of toxicity of TCM and promoting the further development of toxicity of TCM.
traditional Chinese medicine; toxicity; database; comparative study; toxic component
R285
A
0253 - 2670(2023)22 - 7588 - 09
10.7501/j.issn.0253-2670.2023.22.035
2023-04-15
国家中医药管理局青年岐黄学者支持项目
聂嘉璇(1998—),女,硕士研究生,研究方向为中药学。E-mail: niejiaxuan2021@163.com
通信作者:宋丽丽,女,副教授,硕士生导师,从事代谢组学和中药分析研究。E-mail: sll0204@163.com
李遇伯,女,教授,博士生导师,从事代谢组学、毒性评价研究。E-mail: yuboli1@163.com
[责任编辑 赵慧亮]