冠心病合并冠状动脉钙化的影响因素及列线图预测模型建立
石丽媛,孙静,荆飞闯
作者单位:河北中石油中心医院心内一科,河北 廊坊065000
冠心病以动脉粥样硬化斑块的存在导致冠状动脉血流受限为特征[1]。据报道,中国仅有约0.2%的成年人心血管处于健康状态,冠心病病人达到1 100万例,并是导致过早死亡的第二大原因[2]。冠状动脉钙化(CAC)是冠状动脉粥样硬化的标志物,其可以通过胸部计算机断层扫描(CT)并采用Agatston评分进行量化[3]。CAC不仅与冠心病的发展和程度有关,还与冠心病的病死率有关[3]。因此,实现个体化预测冠心病病人合并CAC的发生风险至关重要。目前,探究冠心病病人发生CAC的危险因素,对于改善冠心病病人预后有重要意义,且是临床研究热点,而如何实现个体化精准预测冠心病病人合并CAC的发生风险,是亟待解决的问题。列线图模型可以通过将某事件发生的危险因素整合在一起,从而实现个体化预测该事件发生的风险[4]。因此,本研究旨在分析冠心病合并CAC发生的独立危险因素,构建预测CAC发生的列线图模型,以期为临床筛选高风险冠心病病人,尽早制定防治策略提供参考。
1 资料与方法
1.1 一般资料 以河北中石油中心医院2019年1月至2021年6月确诊的390例冠心病病人为研究对象,符合1979年WHO有关冠心病的诊断标准,并结合临床冠状动脉CT造影(CTA)确诊。根据CTA的Agatston法积分[5]将390例冠心病病人分为CAC组(305例,CAC评分>0),非CAC组(85例,CAC评分=0)。CAC组男167例,女138例,年龄范围40~75岁,年龄(62.85±7.68)岁,身体质量指数(BMI)(23.86±2.32)kg/m2;非CAC组男45例,女40例,年龄范围40~75岁,年龄(55.29±8.42)岁,BMI(22.97±2.16)kg/m2。
纳入标准:①首次确诊,无心肌梗死病史;②能耐受CTA检查者;③无感染性疾病、精神疾病或恶性肿瘤。排除标准:①钙、磷代谢异常;②肾上腺、甲状腺功能紊乱;③经皮冠状动脉介入治疗(PCI)史、冠状动脉搭桥术史;④近期有服用降血脂药物如阿托伐他等;⑤肝、肾功能障碍;⑥合并血液疾病、病毒性心肌炎、心律失常。病人或其近亲属知情同意,本研究经河北中石油中心医院伦理委员会批准(批号201811-002)。
1.2 冠状动脉CTA检查 入组冠心病病人心率控制在70次/分以下,保持屏息状态25~30 s,采用日本东芝双源320排螺旋CT完成扫描,造影剂为优维显370,自肘静脉注射,从气管隆突下方扫描至膈顶下方1 cm,0.6 mm厚度,最后将数据传至影像工作站,采用SmartScore软件Agatston积分系统计算钙化积分。积分基本单位为每1 mm2,CT值≥400 Hu为4,300~399 Hu为3,200~299 Hu为2,130~199 Hu为1,峰值积分×钙化面积=CAC评分。
1.3 研究方法
1.3.1 研究指标 由知悉研究内容的两位护士,且具有3年以上护理经验,收集入组研究对象以下临床资料。(1)一般资料:年龄、高脂血症、BMI、高血压、吸烟、糖尿病、性别、饮酒。(2)临床资料:入院时低密度脂蛋白胆固醇(LDL-C)、脂蛋白、超敏C反应蛋白(hs-CRP)、血肌酐、血清磷、总胆固醇、三酰甘油、血糖、尿酸、血清钙、高密度脂蛋白胆固醇(HDLC)、糖化血红蛋白(HbA1c)等。
1.3.2 列线图模型建立与验证 通过单因素分析筛选出冠心病病人合并CAC的相关因素,随后采用logistic回归分析筛选出冠心病病人合并CAC的独立危险因素;根据以上独立危险因素建立预测冠心病合并CAC风险的列线图模型,并对该模型进行验证。
1.4 统计学方法 采用SPSS 23.0软件处理数据,计量资料(年龄、BMI、三酰甘油、LDL-C等)均以描述,CAC组与非CAC组间比较行t检验;计数资料(性别、高脂血症等)以例(%)描述,两组间比较采用χ2检验。多因素logistic回归分析影响冠心病合并CAC的独立危险因素。将危险因素(LDL-C、高血压、高脂血症、年龄、糖尿病)引入R软件(3.6.3),应用rms程序包构建预测冠心病合并CAC的列线图预测模型。另作受试者操作特征(ROC)曲线计算曲线下面积评估列线图模型区分度。采用校准曲线及Hosmer-Lemeshow拟合优度检验评估该模型预测冠心病合并CAC的准确度。P<0.05为差异有统计学意义。
2 结果
2.1 冠心病合并CAC的单因素分析 本研究390例冠心病病人中有305例合并CAC,发生率为78.21%。两组间在性别、饮酒、吸烟、总胆固醇、HDL-C、三酰甘油、血肌酐、血清钙、脂蛋白、血清磷、镁、hs-CRP以及尿酸相比差异无统计学意义(P>0.05)。两组病人高血压比例、年龄、高脂血症比例、BMI、LDL-C、血糖、糖尿病比例以及HbA1c相比差异有统计学意义(P<0.05)。见表1。
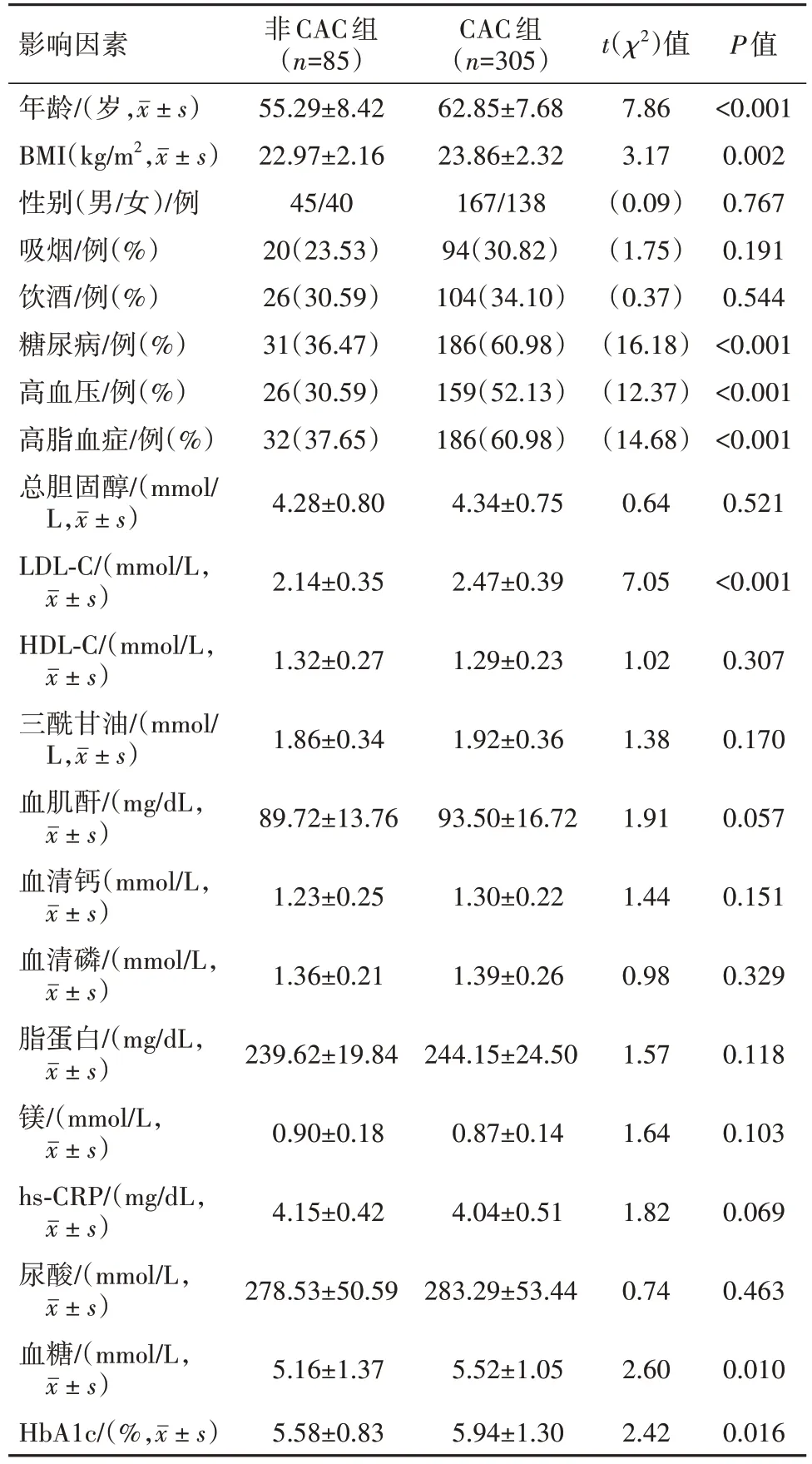
表1 冠心病390例合并冠状动脉钙化(CAC)的单因素分析
2.2 冠心病合并CAC的多因素logistic回归分析以是否发生CAC作为因变量(未发生=0,发生=1),对单因素分析中差异有统计学意义的糖尿病、年龄、高血压、BMI、高脂血症、LDL-C、血糖以及HbA1c这8个因素进行赋值(见表2),纳入多因素logistic回归分析。结果显示,年龄、高血压、高脂血症、LDL-C、糖尿病是影响冠心病合并CAC的独立危险因素(P<0.05)。最终得到公式:Z=0.119×年龄+0.861×高血压+0.856×高脂血症+2.032×LDL-C+1.033×糖尿病-13.968。见表3。

表2 冠心病合并冠状动脉钙化的影响因素的赋值方式
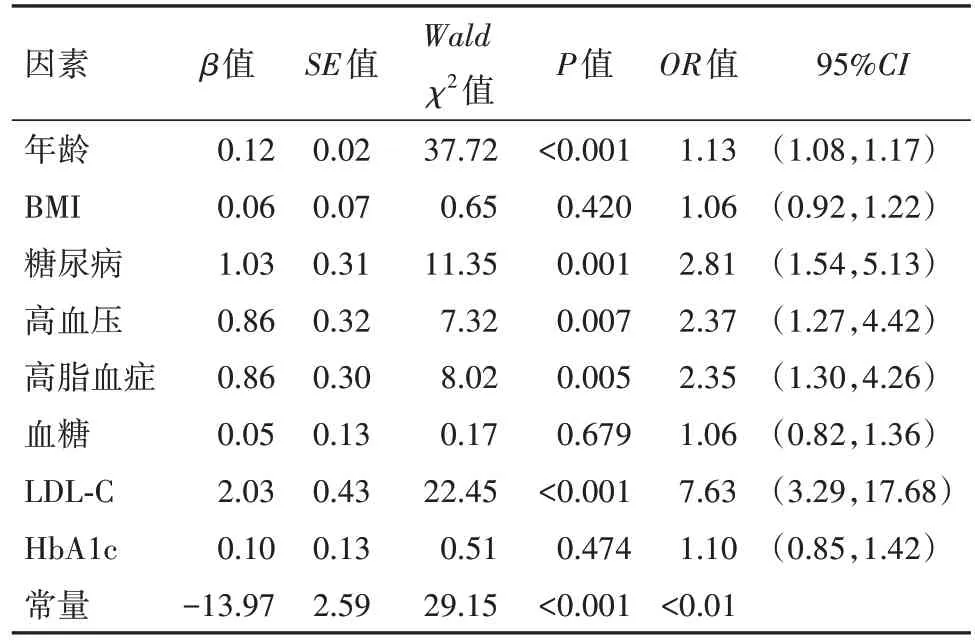
表3 冠心病390例合并冠状动脉钙化的多因素logistic回归分析
2.3 预测冠心病合并CAC的列线图模型建立 根据logistic回归分析结果,绘制列线图模型结果显示:LDL-C水平增加0.2 mmol/L,列线图模型评分上升9.5分;年龄增长5岁,列线图模型评分上升14.6分;高血压为22.3分,糖尿病为23.8分,高脂血症为21.7分。列线图预测值的实例:某病人LDL-C水平为2.80 mmol/L,年龄55岁,有高血压,无糖尿病,无高脂血症,则该病人的总评分为:62.5+43.0+22.3+0+0=127.8分,对应的合并CAC风险为0.84。详见图1。
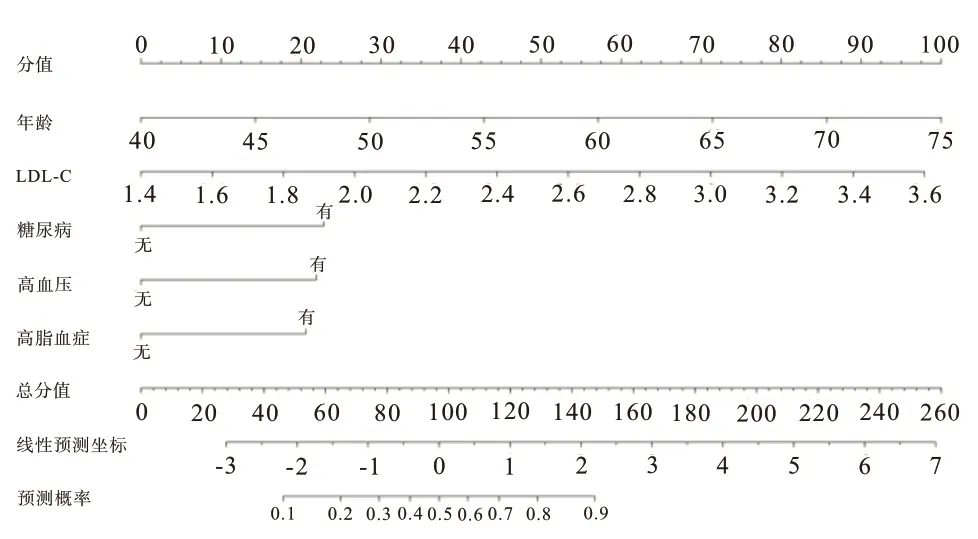
图1 预测冠心病合并冠状动脉钙化发生风险的列线图模型建立
2.4 预测冠心病合并CAC的列线图模型验证ROC结果显示,列线图模型预测冠心病合并CAC发生风险的曲线下面积为0.85,95%CI:(0.81,0.90),约登指数为0.59,临界值>0.78,灵敏度为79.00%,特异度为80.00%,表明该列线图模型区分度较好,见图2。绘制校准曲线以及采用Hosmer-Lemeshow拟合优度检验评估准确度,校准曲线斜率接近1(图3),表明该模型预测冠心病病人发生CAC风险与实际风险一致性良好,且Hosmer-Lemeshow拟合优度检验χ2=7.22,P=0.513,说明该列线图模型具有较好校准度。
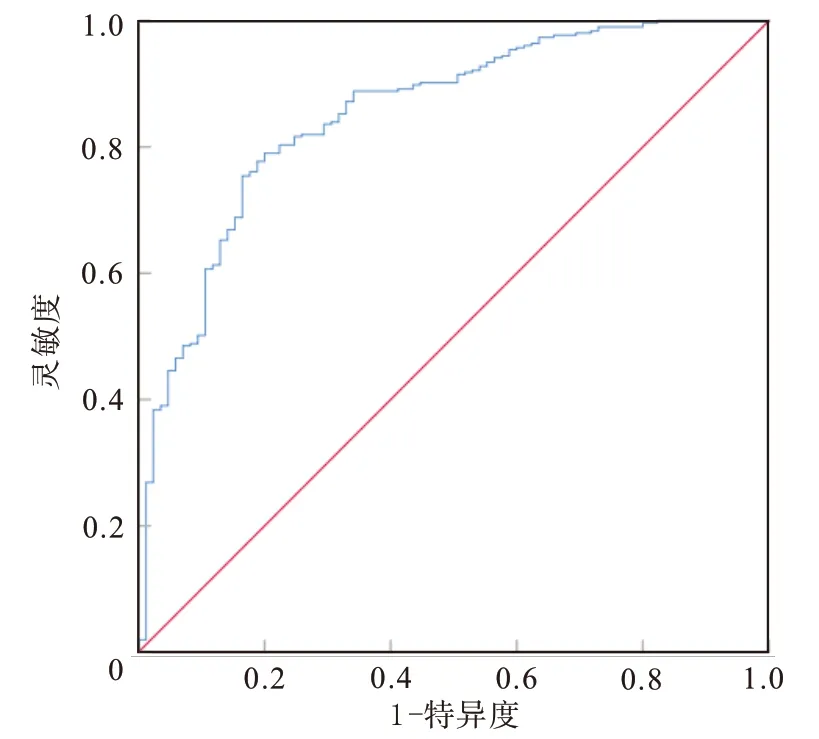
图2 列线图模型预测冠心病合并冠状动脉钙化发生风险的ROC曲线
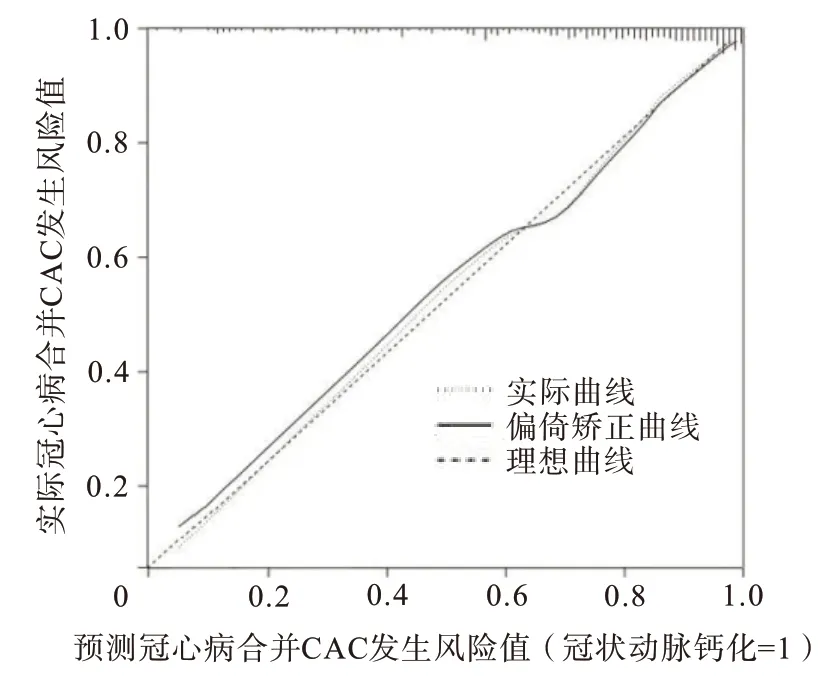
图3 列线图模型预测冠心病合并冠状动脉钙化发生风险的校准曲线
3 讨论
冠心病仍是全球病死率较高的一种疾病,其基本病理变化是冠状动脉粥样硬化。CAC是指钙盐在冠状动脉血管壁的沉积,并且为冠状动脉粥样硬化疾病的重要标志,对预测冠心病病人临床预后、总冠状动脉斑块负荷及心血管事件有重要价值[3,6]。CAC严重心肌梗死和冠状动脉猝死风险增加。此外,严重钙化病变病人在心血管介入治疗时也较为棘手,增加手术难度,术后临床结局也较差,包括增加手术失败风险、增加冠状动脉夹层比例,甚至增加长期病死率风险[7-8]。一项有关冠状动脉风险发展的研究发现,CAC评分为1~19分、20~99分以及≥100分的病人在随访12.5年中,冠心病的发病率和病死率分别增加2.6倍、5.8倍和9.8倍[9]。本研究390例冠心病病人中有305例合并CAC,发生率为78.21%。对冠心病合并CAC发生的危险因素进行探究,对于早期防治CAC发生有重要指导意义。
随着生活习惯转变及老龄化加剧,近年来冠心病发病率仍在增加,CAC发生率也逐渐增加,如何更好预测冠心病病人发生CAC风险成为关键问题[10]。本研究通过单因素和多因素logistic回归分析发现,高脂血症、年龄、糖尿病、LDL-C、高血压是影响冠心病合并CAC的独立危险因素,这与既往研究结果一致[11]。列线图模型相较于logistic回归分析具有更直观、更生动、更简单的优点,实现预测结果的个体化、可视化、量化,达到临床良好预测效果[4]。目前,已有学者将列线图模型应用于预测急性冠脉综合征病人PCI后血运重建,冠状动脉扩张症病人5年心血管不良事件、老年稳定性冠心病病人认知衰弱风险[4,12-13]。然而,还未有关应用列线图模型预测冠心病合并CAC的报道。本研究基于上述独立影响因素构建预测冠心病病人合并CAC发生风险的列线图模型,有助于临床工作者结合病人自身情况直观地分析以上因素不同水平状态对冠心病病人合并CAC的影响权重,以识别高风险病人并尽早预防。
研究显示,CAC随年龄增长而增加,在40~49岁人群中发生率为50%,60~69岁人群中发生率为80[14]。本研究结果发现,年龄增长5岁,对应列线图模型增加14.6分。随着年龄增加,冠心病血管衰老不断加重,而衰老会通过诱导血管平滑肌细胞(VSMC)的成骨转化、内皮细胞释放囊泡、重塑细胞外基质、磷代谢失衡、DNA损伤、炎症反应和减少抗衰老因子表达来促进血管钙化[15];年龄增长的同时,骨组织吸收钙离子能力减弱,血液循环中钙离子增多,这也导致钙盐在血管内壁沉积,从而引起CAC[16]。本研究中糖尿病增加列线图模型评分23.8分,可能是由于糖尿病病人体内的高血糖和胰岛素抵抗通过增加柠檬酸循环中的葡萄糖氧化来增加氧化应激,一方面氧化应激会上调Runt相关转录因子-2并促进VSMC钙化;另一方面在高氧化应激和高血糖状态下,内皮通透性增加,VSMC处于促钙化因子及高血糖环境中,而肿瘤坏死因子-α会诱导骨形态发生蛋白-2的产生,从而推动VSMC的成骨和钙化[14,17]。石丽媛等[6]研究发现高血压是冠心病合并CAC的独立危险因素。本研究中高血压增加列线图模型评分22.3分。原因可能是:冠心病合并原发性高血压的血压增高会引起血管内皮损伤、血管功能障碍,内膜对脂质通透性增加,促进动脉粥样硬化斑块中骨细胞样细胞形成,Runt相关转录因子2(Runx2)、性别决定区Y框蛋白等骨相关蛋白表达,诱导血管矿化过程,从而导致血管钙化发生[16,18]。高脂血症增加列线图模型评分21.7分,分析其原因:高脂血症能够诱导白细胞介素增强子结合因子3(ILF3)上调表达,ILF3通过正向调控骨形态发生蛋白2水平并激活Smads信号通路来诱导Runx2的转录,同时ILF3抑制转录激活1表达,从而促进Runx2核转位并调节成骨分化,从而促进动脉粥样硬化钙化[7]。本研究结果表明LDL-C是冠心病病人合并CAC的独立危险因素,LDL-C每增加0.2 mmol/L水平,列线图模型评分增加9.5分,相应合并CAC发生风险增加,可能是LDL-C能够驱动VSMC分化为成骨细胞,进而刺激血管钙化[19]。针对列线图模型所示冠心病病人合并CAC的危险因素,除不可控因素年龄外,临床医护人员应加强对基础疾病如高血压、糖尿病及高脂血症的筛选和管理,对患有高血压、糖尿病及高脂血症病人在诊治过程中给予特别关注,严格把控药物使用;对未合并高血压、糖尿病及高脂血症病人需要积极做好预防工作。对于LDL-C异常增高的病人临床医护人员需要高度重视,结合临床检查尽早诊断,以降低CAC发生风险。
此外,本研究进一步对列线图进行验证,结果显示校准曲线斜率接近1,且Hosmer-Lemeshow拟合优度检验χ2=7.22,P=0.513,表明此模型的准确度较好;ROC曲线显示其预测冠心病合并CAC的曲线下面积为0.85,说明该模型区分度较好。本研究根据列线图模型评分能计算出病人各自并发CAC的风险,假如某冠心病病人列线图得分为129分,对应CAC预测概率为0.79,高于预测模型的高危临界值0.78,则该病人属于CAC发生的高危人群,应对该病人给予重点关注,从而有效减少CAC发生。
综上所述,本研究结果表明高血压、年龄、高脂血症、LDL-C以及糖尿病是冠心病病人合并CAC发生的独立危险因素。本研究建立的冠心病合并CAC的列线图预测模型具有较好区分度及准确度均较好,预测高危临界值为0.78,将为临床医护人员评估冠心病病人合并CAC风险及制定治疗方案提供参考,具有临床推广应用价值。然而,本研究纳入冠心病病人样本量有限,所研究的影响因素有限,不排除结果存在偏倚;所构建模型仅进行内部验证,未纳入新的数据集进行外部验证,难以排除过拟合情况;下一步采用多中心研究方法,结合临床实践完善预测冠心病合并CAC发生风险的列线图模型,以期能早日用于临床。

