卵巢微囊性间质瘤病理特点与MRI 特征
陈平莲,王靖红
(1 定州市人民医院病理科 河北 定州 073000)
(2 定州市人民医院CT 核磁科 河北 定州 073000)
卵巢微囊性间质瘤(microcystic stromal tumour,MST)最初是2009年由Irving和Young[1]报道并描述了形态特征,瘤组织由微囊区、实性富于细胞区及纤维性间质组成,缺乏其他任何类型的性索-间质肿瘤形态、缺乏上皮成分,不含有畸胎瘤或其他生殖肿瘤成分。2014 年第四版女性生殖器官肿瘤世界卫生组织分类,在性索-间质肿瘤中新增加了微囊性间质瘤,并归为纯粹间质性肿瘤。本文报道1 例该肿瘤的MRI影像学特征及病理特点并复习相关文献,旨在提高对此肿瘤影像学及病理学特性的认识。
1 病例资料
1.1 一般资料
患者女性,38 岁,平素月经规律,主因月经间期少量出血3 个月,偶有下腹痛来院。患者精神状态可,大便正常,小便正常,体重无明显变化。查体患者皮肤无黄染、出血及皮疹,全身浅表淋巴结未触及肿大,头颅脊柱四肢无畸形,双眼外观无异常,双侧瞳孔对光反射灵敏。静脉血检查激素六项,其中孕酮0.05 nmol/L,低于正常范围0.20~1.40 nmol/ L,其余均在正常范围;妇科彩超提示:子宫内膜增厚,右卵巢内囊实性团块,盆腔内可见积液。宫腔镜观察:宫颈管形态正常,宫腔形态呈筒状,左侧输卵管开口可见,右侧输卵管开口处为盲端,前壁内膜弥漫性增厚,后壁可见多发息肉样占位,术中右卵巢见直径5 cm 囊实性肿物,子宫正常大小,左附件及右侧输卵管未见异常,故腹腔镜行肿物剥除术。
1.2 检查方法
MRI 检查方法:检查前嘱患者空腹4~6 h,膀胱呈半充盈状态,采用PHILIPS 公司1.5T 超导型磁共振系统,病例平扫加增强,选用正交体部线圈,患者取仰卧位,常规扫描范围从耻骨联合扫至髂前上棘。常规扫描:矢状位T2WI;轴位T1WI、T2WI、T2WI-SPAIR、DWI(b值为800 s/mm2);冠状位T2WI-SPAIR。增强扫描(注射钆喷替酸葡甲胺后):轴位T1WI 压脂后动态增强扫描;矢状位与冠状位T1WI 压脂延迟扫描。FOV 根据患者实际体型调整。轴位层厚4 mm,层间距1 mm,矢状位及冠状位层厚5 mm,层间距1 mm。病例MRI 资料由2 名经验丰富的主治医师对检查图像进行分析,分析内容包括:肿瘤位置、形态、大小、边缘情况、病灶内部出血、坏死及囊变情况,与正常子宫肌层做参考的信号变化特点,表观弥散系数值变化,肿瘤强化特点及周围淋巴结情况。
病理检查方法:标本经10%中性福尔马林固定,石蜡包埋、切片,常规HE 染色,光镜观察。免疫组化采用DAKO 全自动免疫组化仪进行染色,S-P 法,DAB显色,PBS 代替一抗做阴性对照。Vimentin、WT1、CD10、CyclinD1、Ki-67、Calretinin、α-inhibin、EMA、CK7、CK、Syn、SMA、CD99、CD56 抗体工作液均购自北京中杉金桥生物技术有限公司。Vimentin、Syn、α-inhibin、CK7、CK、SMA 细胞质棕黄色判读为阳性,EMA、CD10 细胞膜细胞质棕黄色判读为阳性,WT1、CyclinD1、Ki-67 细胞核棕黄色判读为阳性,CD99、CD56 细胞膜棕黄色判读为阳性,病例病理资料由2 名经验丰富的主治医师对检查图像进行分析及判读。
1.3 影像学结果
MRI1.5T:右侧附件区可见不规则等T1长T2异常信号,信号不均匀,最大截面约5.3 cm×4.5 cm,上下约5.5 cm,信号不均匀,内可见裂隙状及条片状短T2异常信号,与周围组织分界欠清;增强MRI 扫描示:右侧附件区异常信号呈明显不均匀持续强化。子宫后壁异常信号各期强化信号同子宫肌层。影像学影像:右侧附件区肿瘤,不除外恶性病变,请结合临床(附图见图1)。
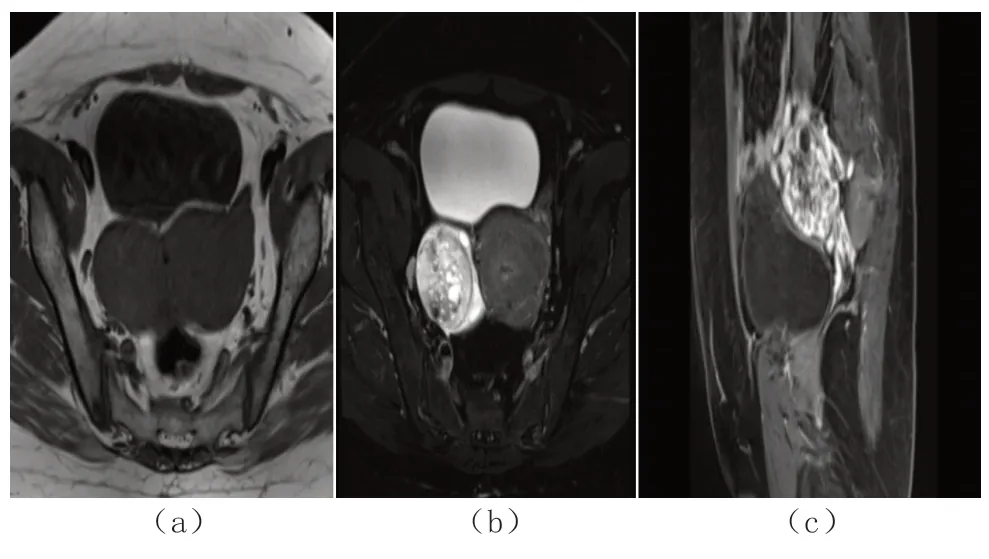
图1 MRI 影像
1.4 病理检查
大体检查:不整形组织一堆,总大小4.5 cm×4.5 cm×1.5 cm,切面囊实性,灰白灰褐质中。
镜下检查:细胞丰富区呈小叶状分布,小叶内见大小不一、多少不等的微囊,部分区域微囊融合成大的不规则囊腔,囊腔空亮,偶可有淡蓝色液体,周围肿瘤细胞温和,呈圆形或椭圆形,大小相对一致,细胞质细颗粒状,弱嗜酸,细胞核类圆形或短梭形,核仁小,未见明显核分裂,小叶间是胶原化或黏液变性的间质,肿瘤中未见其他任何类型的性索-间质肿瘤的成分及上皮肿瘤组织(图2)。
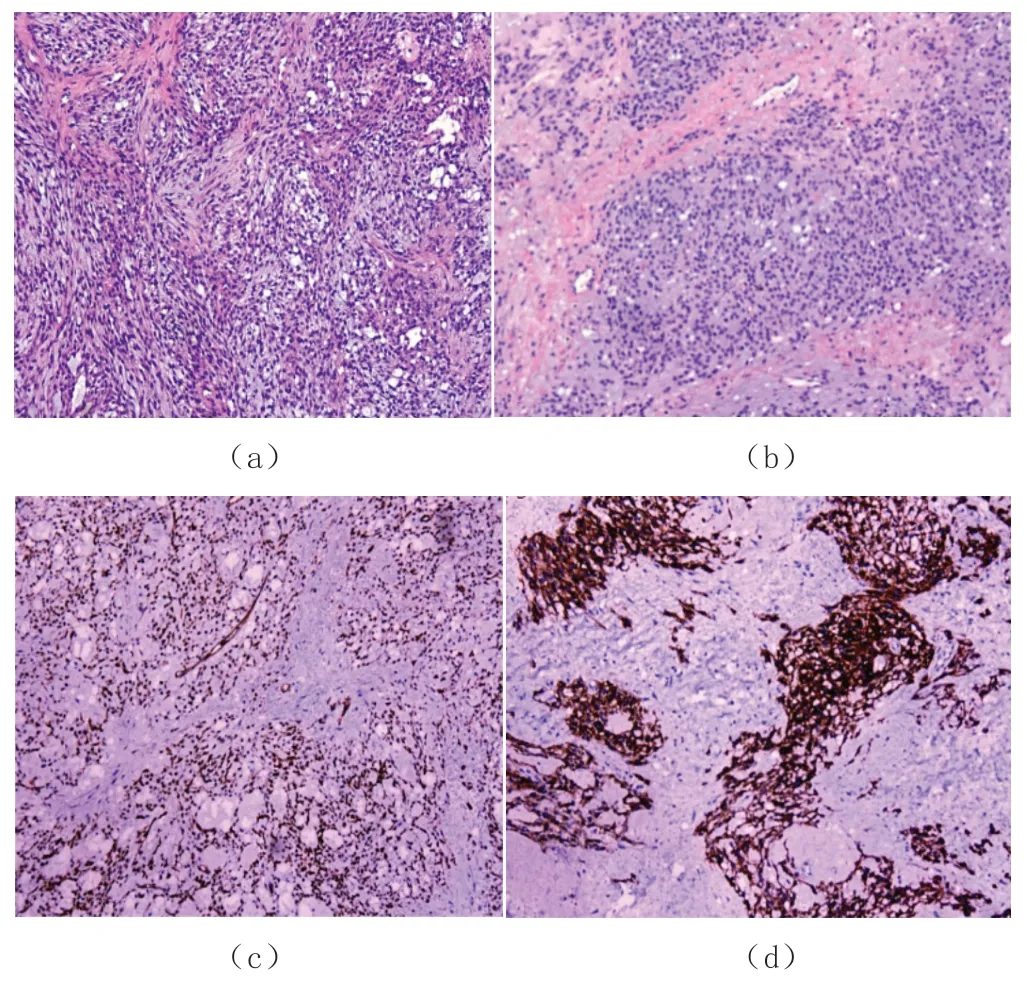
图2 病理检查结果
免疫组化:Calretinin(-)、Vimentin(+++)、EMA(-)、CK7(-)、α-inhibin(-)、CK(-)、Ki-67(约5%+)、Syn(小灶+)、WT1(+++)、SMA(-)、CD99(-)、CD56(-)、CD10(+++)、CyclinD1(++)(图C、D)。
特殊染色:网状纤维(-)。
2 讨论
2014 年第四版女性生殖器官肿瘤世界卫生组织分类,在性索-间质肿瘤中新增加了微囊性间质瘤,并归为纯粹间质性肿瘤。WHO 女性生殖系统2020 年版世界卫生组织女性生殖道肿瘤分类著作中纳入了该瘤种。MST 是一种罕见且独特的肿瘤,具有明确的微囊性模式和B-catenin(+)、FOXL2(+)、WT1(+)、CyclinD1(++)、CD10(+)、Vimentin(+)、α-inhibin(-)、Calretinin(-)的免疫表型。患者发病年龄广泛,20~69 岁不等,MST部分患者在健康体检时偶然发现,部分可能因腹腔疼痛不适检查时发现。临床检查表现为盆腔包块,绝大部分为女性卵巢发病,偶见男性睾丸MST 的报道[2]。肿瘤多单侧发生,平均直径9 cm,瘤体多呈囊实性或单纯实性、囊性,实性区灰白质硬。瘤组织中微囊的形成与实性富细胞区和纤维性间质共存,微囊卵圆形或不规则,囊液略嗜碱或透亮,多数病例瘤细胞多圆形或椭圆形,大小相对一致,细胞质细颗粒状,弱嗜酸,细胞核小,类圆形,但是也有瘤细胞核明显异型的报道[3]。已有报道中,大部分表现为良性肿瘤的生物学行为,术后无复发[4]。本文报道病例随访未见复发。文献亦有卵巢MST 伴有CTNNB1基因3 号外显子突变同时检出伴大网膜转移的病例[4]及卵巢MST 伴有APC 突变,术后9 年出现双侧腹壁下、直肠子宫凹陷及大网膜多处播散的病例[5]。
文献中关于卵巢MST 的影像学特征描述得非常少,Jeong 等[6]描述其在影像学上表现为复杂的混合囊性和实性肿块,具有明显的囊性结构。Murakami 等[7]报告了1 例MST 的MRI 结果,显示主要是囊性病变,T2加权成像上具有高信号强度,T1加权成像上具有等信号强度。这与本例MST 的MRI 结果具有一致性,MST 影像学结果可靠地反映了潜在的组织病理学特征。本文介绍了该肿瘤的MRI 特征且描述了其组织病理学形态,有助于更好地认识其影像学表现与特定组织病理学形态之间相关性,有助于临床医生及早识别这种肿瘤。
卵巢MST多数病例与Wnt/β-catenin信号通路失调有关,具有CTNNB1 基因3 号外显子发生了杂合性错义点突变[8]。少数病例的APC 基因发生失活突变,或影响APC 基因的5q 缺失,所产生的蛋白失去降解β-catenin 的能力。以上两种情况都导致β-catenin 在细胞核蓄积。CTNNB1 或APC 基因在卵巢MST 中存在相互排斥的突变,前者更为常见。两种机制发生的肿瘤未见病理形态学差异。因此少数情况下,卵巢MST 是家族性腺瘤性息肉病的结肠外表现,并且是可能触发该综合征识别的哨兵事件[9]。Wnt/β-catenin 信号通路失调亦与细胞周期蛋白D1 的上调密切相关。
卵巢MST 病理的小叶状及微囊性结构不是其独有的形态模式,在充分取材的基础上,需要与以下肿瘤鉴别:①卵泡膜细胞瘤。瘤细胞呈胖梭形或卵圆形,细胞质淡染色、空泡状,但瘤细胞弥漫分布,缺乏小叶结构及微囊结构;②幼年型粒层细胞瘤。瘤细胞弥漫性或结节性分布,伴有不规则滤泡结构,滤泡腔内含有嗜酸性或嗜碱性液体,间质为纤维卵泡膜样细胞,可伴有黄素化和水肿,免疫组化Calretinin 及α-inhibin 阳性表达且网状纤维染色瘤细胞呈巢分布;③硬化性间质瘤。瘤组织由富细胞的假小叶和少细胞的硬化胶原纤维带或水肿带相间构成,假小叶内含有丰富的薄壁血管和瘤细胞,免疫组化Calretinin、α-inhibin 及CD34 阳性表达;④卵黄囊瘤。瘤组织由微囊、疏松的黏液样基质和大小不等、相互吻合的迷路样裂隙构成,内衬扁平、立方上皮细胞,并有不同程度非典型性,具有大的泡状核,核仁明显,尚可见S-D 小体和透明小体;⑤类癌,瘤细胞岛状、腺泡状或筛网状排列,大小比较一致,免疫组化CK、CD56 及Syn不同程度阳性表达;⑥类固醇细胞瘤。瘤细胞弥漫片状排列,或呈囊状、束状,瘤细胞圆形,胞质丰富,嗜酸性或透明状,细胞核圆形,位于中央,核仁明显。突出的核仁不同于微囊性间质瘤,且后者Calretinin 及α-inhibin 阴性;⑦ 午菲管肿瘤。瘤组织内见大小不等的囊状结构,部分融合呈筛状,部分紧密排列,形成网状小管状,肿瘤细胞呈立方状或柱状,被覆囊壁的瘤细胞扁平状或鞋钉样,免疫组化CK、Vimentin、Calretinin 及α-inhibin 阳性表达。
卵巢MST 是临床工作中极为少见的肿瘤,国内外报道不足40 例。肿瘤无典型临床特征,患者一般无激素相关症状[9],少数有雌激素升高的表现,术前诊断困难,故手术切除肿瘤时若没有确切恶性的证据,建议保留女性生育能力,避免过度治疗。Parra 等建议若术后病理组织学形态符合MST,加做β-catenin、CD10、CyclinD1、WT1、inhibin、SF1 免疫组化项目,必要时进行CTNNB1 和APC突变的分子检测辅助诊断。鉴于MST 有转移的报道极可能是APC 综合征的哨兵事件,患者需要长期随访监测。

