兽用疫苗生产中常用细胞系的致瘤性研究
刘昕泽,宗树成,王楠,张贺楠,谢云浩,郭富城,巴利民
(1.中牧实业股份有限公司 北京 100070;2.农业农村部兽用生物制品与化学药品重点实验室 北京 100095)
细胞培养技术为几个世纪以来疫苗生产的最关键的一个里程碑,最初的疫苗来源于被感染机体的体液、组织或者器官,最常用的是使用感染的鼠(小鼠、大鼠、豚鼠、地鼠等)、兔子、羊等动物的组织器官经研磨后获得。1930 年后,研究人员开始使用鸡胚进行病毒培养,并用于人和动物疫苗生产,目前该方法仍然被大量使用,但SPF 鸡胚的来源受限,供应不足,疫苗生产周期长、产量低等特性,科研人员开始寻求更为方便的易于大规模培养的病毒培养方法,因此细胞培养技术被应用到疫苗生产[1,2]。最初使用的细胞基质是从动物体内分离出来的原代细胞,不进行冻存储备或者在一定程度上作为基础细胞库进行少量冻存。原代细胞增殖能力有限,传代的代次往往不高于5 代,因此每批疫苗都必须重新制备新的原代细胞。此外原代细胞分离培养时受动物个体差异,存在污染风险、批间差较大等问题。随着对疫苗产量需求和疫苗安全性要求越来越高,迫切需要开发出安全、稳定、经济、高效的疫苗生产用细胞基质。有研究人员在1954 年使用猴肾细胞生产脊髓灰质炎病毒,成为疫苗领域的一个标志性事件[3,4]。此后,MDBK、HEK293、MDCK、EB66、BHK-21、PK、ST、marc145 等细胞陆续被开发,应用于人或动物疫苗生产。这些细胞均表现出无限增殖的能力,疫苗生产时建立基础种子库和生产用细胞种子库,可随时从细胞库中复苏细胞进行疫苗生产[5]。但是这些细胞系进行持续传代时存在染色体遗传变异的可能性,具有潜在的遗传不稳定性和致瘤性。因此在疫苗生产中必须限定细胞代次进行使用,只有传代代次较低的非致瘤性的细胞方可用于疫苗生产。在产品申报和疫苗生产时对生产用细胞基质进行致瘤性检验尤为重要[6]。为确保生物制品的安全性,本文根据WHO 和2020 年版《中华人民共和国兽药典》推荐的方法,对目前实验室保存的几种用于研发生产的传代细胞系致瘤性进行了系统研究,为在兽用生物制品研发、生产中如何正确规范使用细胞基质提供数据支撑[7]。
本实验室保存的HEK-293 细胞系、LLC-PK1 细胞系、Marc145细胞系、PK15 细胞系、Vero 细胞系、ST 细胞系、BHK-21 细胞系均为兽用疫苗生物制品研发、生产中常见的传代细胞系。其中HEK-293 用于腺病毒及其腺病毒载体等疫苗生产,HEK-293T 主要用于腺病毒的包装和亚单位疫苗生产,Marc145 细胞应用在猪蓝耳病等疫苗生产,PK15 细胞应用于猪圆环病等疫苗生产,Vero 细胞应用于犬瘟热-狂犬病联苗、猪乙型脑炎活疫苗等疫苗生产,ST主要应用于猪瘟、猪伪狂犬疫苗生产,BHK-21 细胞作为已知具有致瘤性的细胞,应用于口蹄疫、伪狂犬病、狂犬病、SVV 等灭活疫苗生产。本试验对这7 种细胞进行致瘤性试验,为生产兽用疫苗安全性评价提供试验依据。
1 材料与方法
1.1 材料及试剂
1)细胞。HEK-293 细胞第30 代、HEK-293T 细胞第30 代、LLC-PK1 细胞第30 代、Marc145 细胞第30 代、PK15 细胞第35 代、Vero 细胞第140 代、ST 细胞第35 代、胎猪原代肾上皮细胞第8 代、BHK-21 细胞第50 代,上述使用细胞中,胎猪原代肾上皮细胞为实验室使用SPF 胎猪肾组织自行分离的原代细胞,其余均为实验室基础种子库细胞。其中Vero 为ATCC 引进细胞株,代次以ATCC 原始细胞代次进行记录,其余细胞原始代次不清晰,以在本试验开始传代记录为第一代。
2)试验动物。Nu/Nu 裸鼠6 周龄雌鼠,共计90 只,购自北京维通利华实验动物技术有限公司,饲养于北京市海淀区兴隆实验动物养殖厂。
1.2 方法
1)试验分组。将90 只裸鼠随机平均分成9 组,每组10 只,分HEK-293 细胞组、HEK-293T 细胞组、LLC-PK1 细胞组、Marc145细胞组、PK15 细胞组、Vero 细胞组、ST 细胞组,每种细胞接种10 只裸鼠,胎猪原代肾上皮细胞阴性对照组和BHK-21 细胞阳性对照组各接种10 只裸鼠。
2)细胞收集与接种。将生长状态良好的细胞消化、重悬、计数,试验组每种细胞取2×108个细胞,阳性对照组取1×108个细胞,阴性对照组取2×108个细胞。
3)细胞接种。将收集的细胞1 000 r/min,离心5 min,分别用1 mL 无菌PBS 重悬。每只裸鼠右腋下皮肤消毒后,皮下缓慢注射0.1 mL 细胞悬液(表1)。
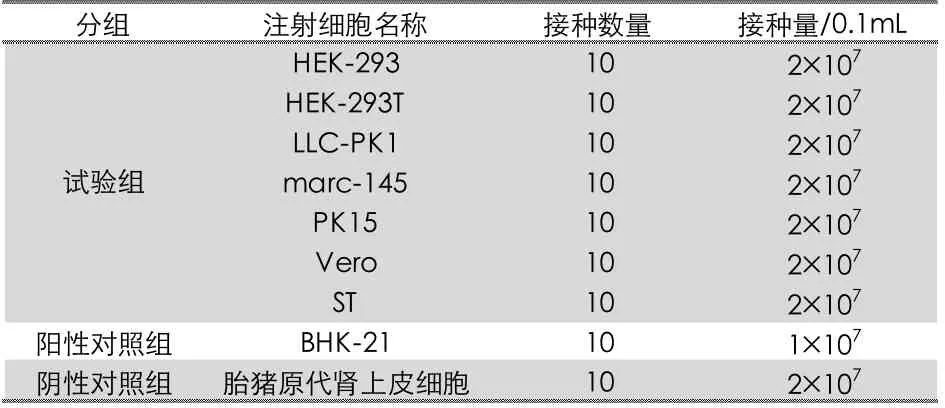
表1 试验动物分组
4)观察与剖检。接种后的裸鼠每周观察两次,每次间隔3~4 d,观察接种部位有无结节或肿块。持续观察至5 周,对各试验组中出现肿块的裸鼠进行剖检,做病理切片分析;对各试验组中未出现肿块的裸鼠分别取半数做剖检,做病理切片分析。阴性对照组和阳性对照组在5 周取半数剖检,做病理切片分析。对剩余裸鼠持续观察至12 周后,全部剖检,做病理切片分析。
5)病理组织切片。裸鼠颈部脱臼处死后,剪开接种部位,取接种部位附近皮肤、颌下淋巴结、肺脏、皮下组织、肝脏、脾脏,如有结节或肿块,取出皮下结节或肿块,将组织放入4%多聚甲醛溶液中固定,将固定后的样品制备石蜡包埋切片,经H-E 染色后镜检。
2 结果与分析
2.1 阳性、阴性对照组结果
试验观察至5 周(第35 天),接种BHK-21 细胞系的阳性对照组内裸鼠肋下均出现明显肿块(图1 A),肿块直径7.9~16.3 mm,精神萎靡,采食量下降,剖检后发现,裸鼠的淋巴结、肺脏、肝脏均无明显结节。对裸鼠的肿块、淋巴结、肺脏、肾脏、肝脏进行病理切片检测,结果显示,肿块组织细胞异型性大,核分裂明显,核仁大而清晰,成团块或岛屿型(图2 A)。部分裸鼠病理切片显示肺脏有转移现象(图2 B)。接种胎猪原代肾上皮细胞系的阴性对照组内裸鼠,精神、饮食未出现异常表现,接种部位无明显结节和肿块产生(图1 B),剖检后颌下淋巴结、肺脏、肾脏、肝脏未出现异常。病理切片检测结果,未发现肿瘤细胞。

图1 裸鼠病理解剖学检查
2.2 试验组结果
试验观察至5 周(第35 日),接种HEK-293、LLC-PK1、Marc145、PK15、Vero、ST 细胞系的各试验组裸鼠,精神、饮食未出现异常表现,未见结节或可疑肿块组织(图1 C、E、F、G、H、I)。从各组中分别取5 只裸鼠进行剖检,对接种部位皮肤、淋巴结、肺脏、肾脏、肝脏进行病理切片检测,未发现肿瘤细胞。继续饲养观察至12周后,将各组剩余裸鼠全部剖检并对接种部位皮肤、淋巴结、肺脏、肾脏、肝脏组织进行病理切片检测,均未发现肿瘤细胞。
试验观察至5 周(第35 日),接种HEK-293T 细胞系的裸鼠均出现精神萎靡、采食量下降的异常表现,接种部位均有可疑肿块产生,肿块直径5.8~10.6 mm(图1 D),对肿块进行病理切片检测为鳞状细胞癌细胞(图3 D)。对其他组织进行病理切片检测,未发现有肿瘤细胞。
3 结果与讨论
生产用细胞系一般由人或动物原代细胞或细胞系中获得的具有特殊遗传、生化特性或特异性标记的细胞群。2020 版兽药典生产用细胞标准致瘤性检验要求,对至少10 无胸腺小鼠,各皮下或肌肉注射107个被检细胞,持续观察12 周,对接种部位进行剖检及病理学检查,各淋巴结和各器官中应均无结节及肿瘤,以确保在生物制品生产时不会产生致瘤性。
本文对动物生物制品研发、生产中7 种常见细胞系的致瘤性进行了系统研究,可见HEK293-T 细胞对裸鼠具有致瘤性,未发生转移。阳性对照BHK-21 细胞系接种后肿瘤细胞由接种部位转移,在肺部组织中可观察到肺部鳞状细胞瘤细胞,因此HEK293-T 细胞、BHK-21 细胞不能用于活疫苗的生产,当用于灭活苗生产时需系统评估制品经灭活剂灭活后细胞基因组核酸对动物机体存在的潜在致瘤性风险。本实验室保存的HEK-293、LLC-PK1、Marc145、PK15、Vero、ST 细胞系无致瘤性,但有些研究表明Vero、Marc145、HEK-293 细胞存在致瘤性[8],这种结果差异可能是因为细胞代次不同或者细胞高变异株亚型引起的,因此用于生物制品生产的细胞基质必须在限定代次内使用,不可高于规定的最高代次,以免出现致瘤性风险[9]。■

