流苏子根中化学成分的分离鉴定和抗菌活性研究
白路遥,杨雪飞,鲁春华*,沈月毛
(1.山东大学药学院天然产物生物学教育部重点实验室,山东 济南 250012;2.中国科学院昆明植物研究所植物资源与生物技术研究室,云南 昆明 650201)
流苏子[Coptosapelta diffusa (Champ.ex Benth.)Steenis]是茜草科流苏子属植物,主要分布于中国长江流域及其以南各地和日本的温带地区[1]。《中华本草》记载其根为药用部位。将其根部加水煮沸后清洗,或直接将根研末调涂患处可治疗皮炎、湿疹瘙痒、荨麻疹、风湿痹痛、疮疥等皮肤病。作为一种传统中草药,其化学成分和药理活性研究较少。目前,从该植物中已报道的化学成分共约50 个[2-4],包括蒽醌、萘醌、香豆素和萜类等。本课题组前期已从其地上部分分离得到结构新颖的环烯醚萜苷和愈创木烯型倍半萜等化合物[3]。
为进一步挖掘流苏子中的化学成分,本实验对其根部的化学成分进行系统分离,共鉴定了12 个化合物(图1),包括6 个萘醌lapachol(1)、hydroxyhydrolapachol(2)、dehydro-α-lapachone(3)、α-lapachone(4)、rhinacantin A(5)和β-lapachone(6),2 个蒽醌2-carbomethoxyanthraquinone (7) 和7-hydroxy-2-methylanthraquinone(8),1 个香豆素isoscopoletin(9),1 个环烯醚萜alyxialactone(10),1 个芳香化合物(3S)-3-(hydroxymethyl)-3H-isobenzofuran-1-one(11)和1 个木脂素(7’S,8S,8’R)-4,4’-dihydroxy-3,3’,5,5’-tetramethoxy-7,9-epoxylignan-9’-ol-7-one(12)。通过纸片扩散法筛选了化合物1~12 的抗菌活性,并利用微量稀释法进行了最小抑制浓度测定。此外,采用高效液相色谱法(high performance liquid chromatography,HPLC)对主要成分拉帕醇(lapachol,1)进行了含量测定。
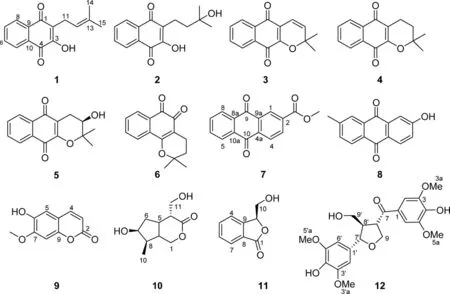
图1 化合物1~12 的化学结构
1 仪器与材料
Bruker Avance 400 MHz 型核磁共振仪(德国Bruker 公司);分析型高效液相色谱仪Thermo Scientific UltiMate 3000 (Hypersil GOLDTM,5 μm,250 mm ×4.6 mm);旋转蒸发仪R-100 (BUCHI Labortechnik AG);柱色谱硅胶(200~300 目,青岛海洋化工厂);硅胶薄层层析板(烟台江友硅胶开发有限公司);葡聚糖凝胶(25~100 μm,GE Healthcare Bio-Sciences AB);氘代试剂(上海新铂化学有限公司);石油醚、二氯甲烷、乙酸乙酯、甲醇(分析纯,天津恒兴化学制造有限公司)。酵母提取物(OXOID),胰蛋白胨(OXOID),氯化钠(国药基团化学试剂有限公司)。
流苏子根于2020 年10 月采集于广西防城港市上思县南屏乡汪乐村向十万大山森林公园方向平龙山木材检查站(北纬21°51′47.37″,东经107°53′0.85″,509 米处)。由中国科学院昆明植物研究所杨雪飞、杨锦超鉴定为流苏子 [Coptosapelta diffusa(Champ.ex Benth.)Steenis],标本号为yangxf0209,收藏于中国科学院昆明植物研究所标本馆。抗菌实验所用病原指示菌:金黄色葡萄球菌(Staphylococcus aureus ATCC25923)、耻垢分枝杆菌(Mycobacterium smegmatis MC2155)、变形杆菌(Proteusbacillus vulgaris CPCC160013)和白色念珠菌(Candida albicans 5314)菌株均保存于山东大学天然产物化学生物学教育部重点实验室。
2 提取与分离
新鲜流苏子根剪成小段,自然风干称重(600.0 g)。用95 %乙醇浸泡1 周,超声辅助提取30 min,共提取3 次,合并乙醇提取液,40℃减压浓缩得提取物浸膏(40.0 g)。该提取物首先经正相硅胶柱层析(250.0 g),石油醚-乙酸乙酯(100 ∶1~10 ∶1,v/v)梯度洗脱,根据TLC 检测(紫外和磷钼酸显色) 结果分为25 个组分(Fr.A~Y)。
Fr.J(2.5 g)经正相硅胶柱层析(80.0 g),石油醚-乙酸乙酯(200 ∶1~100 ∶1) 梯度洗脱,得到化合物1(2.2 g)。Fr.K(104.9 mg)经正相硅胶柱层析(10.0 g),石油醚-乙酸乙酯(200 ∶1~100 ∶1)梯度洗脱,得到组分Fr.K1~K3。Fr.K1(36.8 mg)经Sephadex LH-20 凝胶柱层析,二氯甲烷-甲醇(1 ∶3)洗脱,得到化合物3(10.2 mg)。Fr.K2(60.1 mg)经Sephadex LH-20 凝胶柱层析,二氯甲烷-甲醇(1 ∶3)洗脱,得化合物7(4.9 mg)。Fr.L(88.1 mg)经葡聚糖凝胶柱层析,二氯甲烷-甲醇(1 ∶3)洗脱,得化合物4(5.1 mg)。Fr.Q(25.8 mg)经葡聚糖凝胶柱层析,MeOH 洗脱,得化合物8(1.7 mg)。Fr.R 经Sephadex LH-20 柱层析,甲醇洗脱,得到7 个组分(Fr.R1~R7)。Fr.R2(11.7 mg)经正相硅胶柱层析(2.5 g),石油醚-乙酸乙酯(30 ∶1)等度洗脱,得到化合物6(2.2 mg)。Fr.U(900.0 mg)经Sephadex LH-20 柱层析,MeOH 洗脱,得到19 个组分(Fr.U1~U19)。Fr.U8(270.0 mg)经Sephadex LH-20 柱层析,甲醇洗脱合并后又经正相硅胶柱层析(2.0 g),二氯甲烷-甲醇(500 ∶1) 等度洗脱,得到化合物2(12.6 mg)、5(2.5 mg)和11(3.4 mg)。Fr.U13(31.5 mg)经正相硅胶柱层析(2.0 g),二氯甲烷-甲醇(200 ∶1)等度洗脱,得到化合物9(9.9 mg)。Fr.W(0.6 g)经正相硅胶柱层析(12.0 g),石油醚-乙酸乙酯(15 ∶1~1 ∶2)梯度洗脱,得到Fr.W1~W6。Fr.W2(106.5 mg)经Sephadex LH-20 柱层析,甲醇洗脱,得到化合物12(2.2 mg)。Fr.W4(120.0 mg)经Sephadex LH-20 柱层析,甲醇洗脱后又经正相硅胶柱层析(1.5 g),二氯甲烷-甲醇(100 ∶1~50 ∶1)梯度洗脱,得到化合物10(7.8 mg)。
3 结构鉴定
化合物1:黄色片状结晶,C15H14O3。1H NMR(400 MHz,CDCl3)δ:8.11(1H,dd,J=7.7,1.4 Hz,H-8),8.09(1H,dd,J=7.7,1.4 Hz,H-5),7.74 (1H,td,J=7.7,1.4 Hz,H-7),7.67(1H,td,J=7.7,1.4 Hz,H-6),7.30(1H,s,OH),5.21(1H,m,H-12),3.31(2H,d,J=7.3 Hz,H-11),1.79 (3H,s,CH3-14),1.68 (3H,s,CH3-15);13C NMR(100 MHz,CDCl3)δ:184.5(C-1),181.7(C-4),152.7(C-3),134.8(C-7),133.8(C-13),133.0(C-9),132.8(C-6),129.5(C-10),126.8(C-8),126.1(C-5),123.5(C-2),119.7(C-12),25.7(C-15),22.6(C-11),17.9(C-14)。以上数据与文献[5]对比,鉴定化合物为拉帕醇lapachol。
化合物2:黄色粉末,C15H16O4。1H NMR(400 MHz,CDCl3)δ:8.12(1H,dd,J=7.6,1.5 Hz,H-5),8.08(1H,dd,J=7.6,1.4 Hz,H-8),7.76 (1H,td,J=7.6,1.4 Hz,H-6),7.69(1H,td,J=7.6,1.5 Hz,H-7),2.71(2H,t,J=6.6 Hz,H-11),1.70(2H,t,J=6.6 Hz,H-12),1.31(6H,s,CH3-14,CH3-15);13C NMR(100 MHz,CDCl3)δ:184.8(C-4),181.3(C-1),153.0(C-2),134.9(C-6),133.0(C-7),129.5(C-9),132.9(C-10),126.8(C-5),126.2(C-8),124.7(C-3),71.0(C-13),41.6(C-12),29.1(C-14,15),18.3(C-11)。以上数据与文献[6]对比,鉴定化合物为hydroxyhydrolapachol。
化合物3:黄色粉末,C15H12O3。1H NMR(400 MHz,CDCl3)δ:8.10 (2H,dd,J=7.0,1.7 Hz,H-5,8),7.71 (1H,td,J =7.0,1.7 Hz,H-6),7.68 (1H,td,J =7.0,1.7 Hz,H-7),6.66(1H,d,J=10.0 Hz,H-11),5.73(1H,d,J=10.0 Hz,H-12),1.56 (6H,s,CH3-14,15);13C NMR(100 MHz,CDCl3)δ:181.9(C-1),179.9(C-4),152.5(C-3),134.0(C-6),133.2(C-7),131.6(C-10),131.5(C-9),130.9(C-12),126.3(C-5),126.3(C-8),117.9(C-2),115.5(C-11),80.5(C-13),28.4(C-14,15)。以上数据与文献[7]对比,鉴定化合物为dehydro-α-lapachone。
化合物4:黄色粉末,C15H14O3。1H NMR(400 MHz,CDCl3)δ:8.09(1H,dd,J=6.6,1.8 Hz,H-8),8.07(1H,dd,J=7.4,1.7 Hz,H-5),7.68(1H,m,H-7),7.66(1H,m,H-6),2.63(2H,t,J=6.6 Hz,C-11),1.82(2H,t,J=6.6 Hz,C-12),1.44(6H,s,CH3-14,15);13C NMR(100 MHz,CDCl3)δ:184.4(C-1),180.1(C-4),154.7(C-3),133.8(C-7),132.8(C-6),132.0(C-9),131.2(C-10),126.4(C-5),126.0(C-8),120.2(C-2),78.2(C-13),31.4(C-12),26.5(C-14,15),16.8(C-11)。以上数据与文献[8]对比,鉴定化合物为α-lapachone。
化合物5:黄色粉末,C15H14O4。1H NMR(400 MHz,CDCl3)δ:8.04(1H,m,H-5),8.02(1H,m,H-8),7.63(1H,m,H-6),7.60(1H,m,H-7),3.82(1H,m,H-12),2.83(1H,m,H-12a),2.65(1H,m,H-12b),1.41(3H,s,CH3-14),1.35(3H,s,CH3-15);13C NMR(100 MHz,CDCl3)δ:184.8(C-1),179.5(C-4),153.8(C-3),134.0(C-7),133.2(C-6),132.1(C-9),131.2(C-10),126.4(C-5),126.0(C-8),118.2(C-2),80.2(C-13),68.4(C-12),25.4(C-11),24.7(C-15),21.7(C-14)。以上数据与文献[9]对比,鉴定化合物为rhinacantin A。
化合物6:黄色粉末,C15H14O3。1H NMR(400 MHz,CDCl3)δ:7.91(1H,dd,J=7.7,1.4 Hz,H-8),7.76(1H,dd,J=7.7,1.3 Hz,H-5),7.63 (1H,td,J=7.7,1.4 Hz,H-6),7.48(1H,td,J=7.6,1.3Hz,H-7),2.44(2H,t,J=6.7 Hz,C-11),1.81(2H,t,J=6.6 Hz,C-12),1.40(6H,s,CH3-14,15);13C NMR (100 MHz,CDCl3)δ:179.9(C-1),178.6(C-2),162.1(C-4),134.8(C-6),132.7(C-10),130.7(C-7),130.2(C-9),128.6(C-8),124.1(C-5),112.8(C-3),79.3(C-13),31.6(C-12),26.8(C-14,15),16.2(C-11)。以上数据与文献[10]对比,鉴定化合物为β-lapachone。
化合物7:黄色粉末,C16H10O4。1H NMR(400 MHz,CDCl3)δ:8.95(1H,d,J=1.7 Hz,H-1),8.41(1H,dd,J=8.1,1.7 Hz,H-3),8.39(1H,d,J=8.1 Hz,H-4),8.36(1H,m,H-8),8.35(1H,m,H-5),7.84(1H,m,H-6),7.83 (1H,m,H-7),4.02 (3H,s,OCH3);13C NMR(100 MHz,CDCl3)δ:182.6(C-9),182.3(C-10),165.6(COO),136.1 (C-4a),135.2 (C-9a),134.6 (C-3),134.5 (C-6),134.4 (C-7),133.6 (C-2),133.5 (C-10a),133.4(C-8a),128.7(C-1),127.6(C-4),127.5(C-8),127.4(C-5),52.8(OCH3)。以上数据与文献[11]对比,鉴定化合物为2-carbomethoxyanthraquinone。
化合物8:黄色粉末,C15H10O3。1H NMR(400 MHz,DMSO-d6)δ:11.05(1H,s,OH),8.09(1H,m,H-5),8.07(1H,m,H-4),7.97(1H,s,H-1),7.71(1H,d,J =8.0 Hz,H-3),7.50 (1H,d,J =2.6 Hz,H-8),7.24(1H,dd,J =8.6,2.6 Hz,H-6),2.50(3H,s,CH3);13C NMR(100 MHz,DMSO-d6)δ:183.3(C-9),181.5(C-10),163.5(C-7),145.2(C-2),135.7(C-3),135.7(C-9a),133.5(C-8a),131.4(C-4a),130.2(C-4),127.3(C-1),127.3 (C-5),125.7 (C-10a),122.0 (C-6),112.7(C-8),21.8(CH3)。以上数据与文献[12]对比,鉴定化合物为7-hydroxy-2-methylanthraquinone。
化合物9:黄色粉末,C10H8O4。1H NMR(400 MHz,DMSO-d6)δ:7.92(1H,d,J=9.4 Hz,H-4),7.22(1H,s,H-5),6.79(1H,s,H-8),6.22(1H,d,J=9.4 Hz,H-3),3.82(3H,s,OCH3);13C NMR(100 MHz,DMSO-d6)δ:161.2(C-2),151.7(C-6),150.0(C-9),145.7(C-7),144.9(C-4),112.1(C-5),110.9(C-10),110.0(C-3),103.2(C-8),56.4(OCH3)。以上数据与文献[13]对比,鉴定化合物为isoscopoletin。
化合物10:白色粉末,C10H16O4。1H NMR(400 MHz,CD3OD)δ:4.39(1H,m,H-1a),4.11(1H,m,H-7),4.08 (1H,m,H-1b),3.80 (1H,m,H-11a),3.70(1H,m,H-11b),2.56(1H,m,H-4),2.55(1H,m,H-5),2.22(1H,m,H-9),2.16(1H,m,H-6a),1.77(1H,m,H-8),1.62(1H,m,H-6b),1.05(3H,d,J =6.8 Hz,CH3-10);13C NMR (100 MHz,CD3OD)δ:176.0 (C-3),76.0(C-7),69.5(C-1),59.3(C-11),46.3(C-4),42.6(C-9),42.2(C-8),40.7(C-6),35.4(C-5),12.2(C-10)。以上数据与文献[14]对比,鉴定化合物为alyxialactone。
化合物11:黄色粉末,C9H8O3。1H NMR(400 MHz,CDCl3)δ:7.86(1H,d,J=7.6 Hz,H-4),7.63(1H,m,H-5),7.50(1H,t,J=7.6 Hz,H-6),7.45(1H,d,J=7.6 Hz,H-7),5.50 (1H,m,H-3),4.07 (1H,dd,J =8.4,3.4 Hz,H-10a),3.86(1H,dd,J=12.5,5.6 Hz,H-10b);13C NMR (100 MHz,CDCl3)δ:170.4 (C-1),146.6(C-9),134.3(C-5),129.6(C-6),126.5(C-8),125.9(C-4),122.1(C-7),81.7(C-3),64.0(C-10)。以上数据与文献[15]对比,鉴定化合物为(3S)-3-(hydroxymethyl)-3H-isobenzofuran-1-one。
化合物12:白色粉末,C22H26O9。1H NMR(400 MHz,CD3OD)δ:7.40 (2H,s,H-2,H-6),6.72(2H,s,H-2’,H-6’),4.64 (1H,m,H-7’),4.27 (1H,m,H-8),4.22(1H,m,H-9a),4.19(1H,m,H-9b),3.92(6H,s,H-3’a,H-5’a),3.86 (6H,s,H-3a,H-5a),3.67(2H,m,H-9),2.64 (1H,m,H-8’);13C NMR(100 MHz,CD3OD)δ:198.9(C-7),147.8(C-3),147.8(C-3’),147.7(C-5),147.7(C-5’),141.3(C-4),141.3(C-4’),131.5 (C-1’),127.3 (C-1),106.3 (C-2),106.3(C-6),103.8(C-2’),103.8(C-6’),84.0(C-7’),70.2(C-9),59.9(C-9’),55.5(3’a,5’a-OCH3),55.3(3a,5a-OCH3),53.4(C-8’)。以上数据与文献[16]对比,鉴定化合物为(7’S,8S,8’R)-4,4’-dihydroxy-3,3’,5,5’-tetramethoxy-7’,9-epoxylignan-9’-ol-7-one。
4 抗菌活性筛选
4.1 纸片扩散法测抗菌活性 利用纸片扩散法[17]测定化合物1~12 的抗菌活性。从-80 ℃冰箱中取出保存于20%甘油管中的各指示菌,解冻后在LB 平板上划线,37 ℃培养10~12 h。挑取单克隆菌株分别接种于1 mL 的LB 液体培养基中,置于220 rpm,37 ℃摇床中培养过夜。取LB 液体培养基将菌液稀释100倍,混匀后倒入灭菌的LB 平板中,凝固后待用。用镊子将直径6 mm 的圆形滤纸片夹起,加入2 μL 的化合物溶液(各化合物分别用甲醇溶解,浓度为20 μg/μL),挥干溶剂后放置于含指示菌的LB 平板上,倒置于37 ℃的培养箱中培养,24 h 后观察并记录抑菌圈的有无及大小,结果见表1。
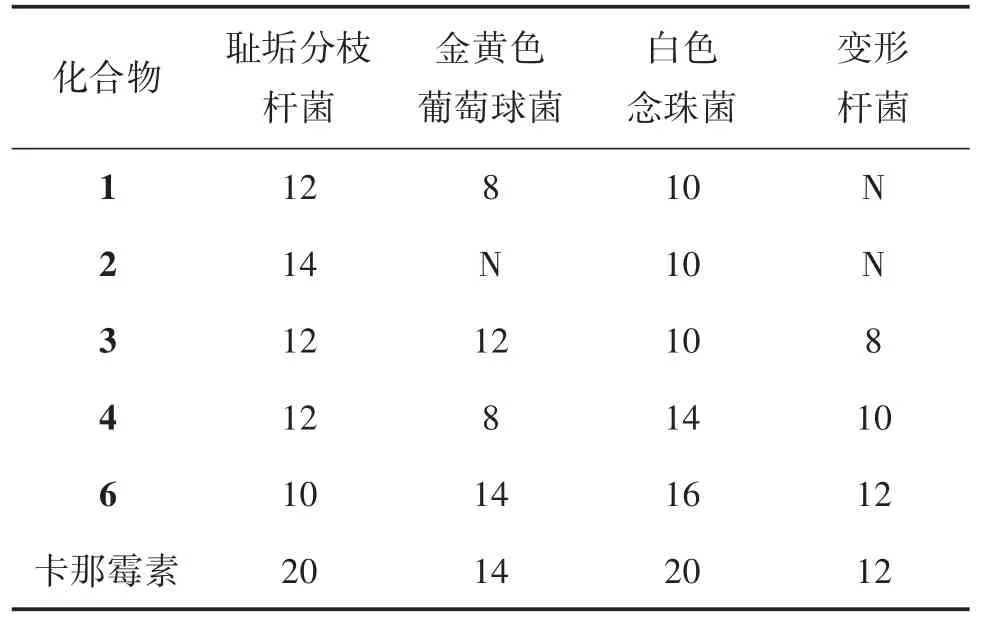
表1 抗菌结果(抑菌圈直径大小单位:mm;N:无抑菌圈)
4.2 最小抑菌浓度(MIC)测定 采用微量肉汤稀释法[18]测定上述有抑菌活性化合物的MIC。将菌液用无菌的液体LB 培养基稀释104倍。首先,在96 孔板中加入100 μL 的LB 液体培养基,采用对倍稀释法加入药物,每个孔加入菌液100 μL,重复3 次。药物终浓度分别为128、64、32、16、8、4、2 和1 μg/mL。阴性对照:仅加LB 液体培养基和菌液;阳性对照:加入卡那霉素,药物浓度分别为128、64、32、16、8、4、2 和1 μg/mL。37 ℃培养16~24 h,没有可见菌生长的最低浓度即为MIC 值。结果见表2。
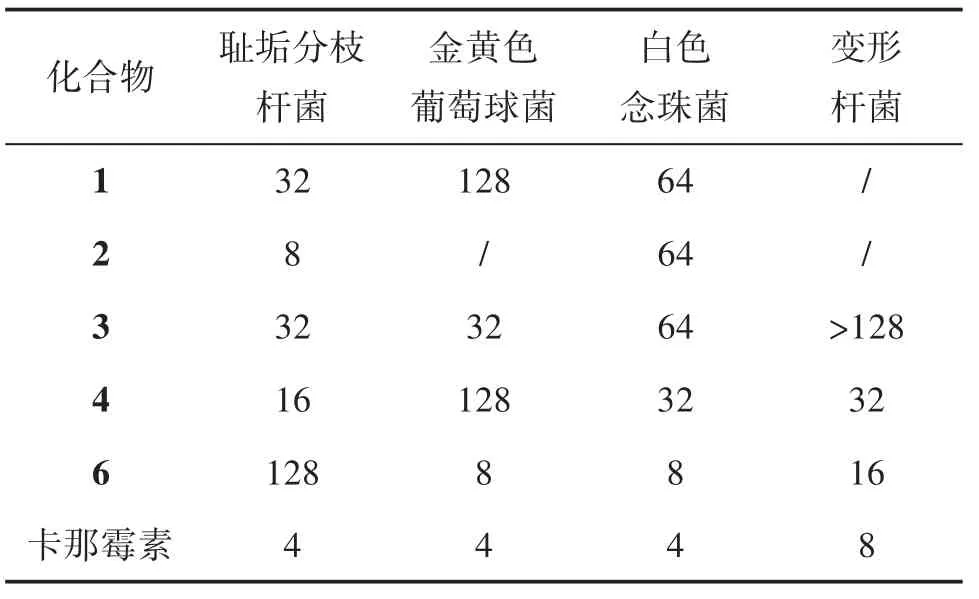
表2 化合物对4 种病原菌的MIC(μg/mL)
5 拉帕醇(lapachol,1)的含量测定
5.1 色谱条件 流动相由0.5‰甲酸水溶液(A)和乙腈(B)组成,流速为1 mL/min,50% B(0~30 min)等度洗脱。柱温30 ℃,进样量20 μL,检测波长254 nm。
5.2 溶液的制备 对照品溶液:精密称取lapachol 3.500 mg,置入具塞的5 mL 容量瓶中,甲醇溶解并稀释至刻度定容,摇晃均匀,制成浓度为0.7 mg/mL 的溶液。
供试品溶液:精密称取3.306 0 g 流苏子干燥根,用95%乙醇浸泡1 周,超声辅助提取30 min,共提取3 次。合并提取液,40℃减压浓缩得到184 mg 乙醇提取物,甲醇溶解,置入具塞的10 mL 容量瓶中,定容至刻度,摇晃均匀,通过0.22 μm 微孔滤膜过滤后,取滤液100 μL 稀释至1 mL 为供试品溶液。
5.3 线性关系的考察 将对照品溶液用甲醇稀释成一系列不同浓度的对照品溶液(700、350、175、87.5、43.75 和21.875 mg/L)进行测定。以浓度为横坐标,峰面积为纵坐标,进行线性回归。测定一系列不同浓度的对照品溶液的峰面积,以浓度为横坐标,峰面积为纵坐标,计算得到lapachol 的线性回归方程:y=1.7239x+8.9959,其中x 为浓度,y 为峰面积,回归系数r=0.9999 (图2)。表明lapachol 在21.875~700 mg/L 范围内与峰面积呈现较好的线性关系。
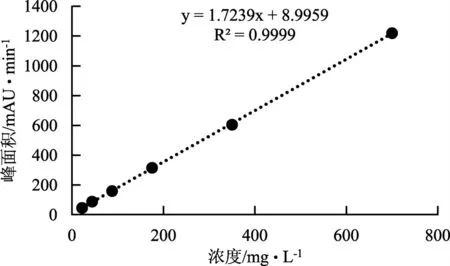
图2 lapachol 的标准曲线
5.4 样品的含量测定 按外标法,测得lapachol 的峰面积为211.9190,计算出流苏子根中lapachol 的含量为3.56 g/kg(干重)。
6 结果与讨论
本研究对流苏子根的化学成分进行了系统分离,共鉴定了12 个化合物的结构,其中4~6 和10~12 为首次从该植物中分离得到。采用纸片扩散法和微量稀释法进行了抗菌活性筛选,结果表明:1~4 对耻垢分枝杆菌表现出较好的抗菌活性,其MIC 值为8~32 μg/mL;化合物6 对金黄色葡萄球菌、白色念珠菌和变形杆菌表现出较好的抗菌活性,其MIC 分别为8、8和16 μg/mL。通过HPLC 定量分析测定主要成分lapachol 在根(干重)中的含量为3.56 g/kg,表明流苏子可以作为拉帕醇的资源植物。Lapachol 是一种天然存在的1,4-萘醌类成分,具有抗肿瘤[19]、抗寄生虫[20]、抗疟疾[21]、抗菌[22]等多种药理活性。该研究结果为流苏子根抗菌消炎的民间药用价值提供了科学依据,并为其深入研究与开发利用提供了科学依据。

