驱动压指导的肺保护性通气策略对COVID-19感染康复期患者术后发生肺部并发症的影响
江连祥,陈文胜,余 伟,胡美珠,曹 亚,姚卫东,陈永权
皖南医学院弋矶山医院麻醉科,安徽 芜湖241000
术后肺部并发症(PPCs)是全麻机械通气后患者最常发生的呼吸系统问题[1,2]。据报道,全世界范围内,每年手术量超过3亿台,其中约10%患者伴发术后肺部并发症,延长了住院时间,增加了病死率,严重影响了患者的预后[3,4]。
随着我国新型冠状病毒(COVID-19)防疫政策的改变,多数人已受到病毒感染。肺是COVID-19最易攻击的靶器官,机体感染病毒后呼吸肌力减弱,肺通气受限,储备功能明显下降[5,6]。该类人群在接受手术治疗后,30 d死亡率及术后肺部并发症发生率显著上升[7]。研究证实小潮气量复合呼气末正压(PEEP)的肺保护性通气策略(LPVS)可改善急性呼吸窘迫综合征(ARDS)患者的氧合,降低死亡风险[8];对于择期全麻手术的一般患者视情况亦可实施肺保护性通气策略[9,10]。然而,针对COVID-19感染康复患者肺保护性通气策略能否降低PPCs的发生风险尚无定论。本研究旨在将驱动压力指导的个体化PEEP 复合小潮气量通气策略用于COVID-19感染康复患者的全麻手术中的呼吸管理,通过观察术后肺部超声评分和PPCs发生率,探究肺保护性通气策略的临床价值,为新冠患者术中呼吸管理提供参考。
1 资料和方法
1.1 研究对象
本研究为随机对照试验,经医院伦理委员会批准(2022 伦审研第83 号),所有患者均知情同意。纳入2022年12月~2023年2月在全身麻醉下接受择期非心脏手术,ASA I~III级,年龄≥18岁,新冠感染1个月内轻型患者[11,12]。排除标准:体质量指数(BMI)<18 kg/m2或>30 kg/m2;患有慢性阻塞性肺疾病、胸壁畸形或既往有胸外科手术史患者;合并有严重的心脏、肾脏或肝脏等疾病患者;新冠感染中、重度或目前仍存在明显症状患者。
1.2 样本量计算
新冠感染康复期患者围手术期PPCs发病率约为51.2%[7],本试验期望驱动压指导的个体化PEEP肺保护性通气策略可使PPCs发病率降低50%,设检验效能为80%,α为0.05,每组需53例患者。考虑到10%的误差,本研究共纳入患者118例,采用计算机随机分为两组,每组59例:肺保护性通气策略组(LPVS组)和常规机械通气组(对照组)。
1.3 麻醉过程
患者入室后常规予以血压、心率、脉搏血氧饱和度、体温及呼气末二氧化碳(PetCO2)等体征监护。予以静脉注射咪达唑仑0.025~0.075 mg/kg、舒芬太尼0.1~0.5 µg/kg、依托咪酯0.1~0.3 mg/kg,顺式阿曲库铵0.1~0.2 mg/kg麻醉诱导行气管插管。麻醉维持予以丙泊酚1~4 mg/(kg·h)和瑞芬太尼0.02~0.15 μg/(kg·h)静脉泵注。常规机械通气组患者呼吸参数设置为潮气量6~10 mL/kg,吸气与呼气比(I:E)为1:2,PEEP≤5 cmH2O,呼吸频率为12 次/min,随后以PetCO2数值在35~45 mm Hg为目标对潮气量和呼吸频率调整。肺保护性通气策略组设VT为6 mL/kg,I:E为1:2,PEEP值采用驱动压指导个体化滴定:PEEP从2 cmH2O开始,逐渐增加1 cmH2O,每个呼气末正压维持10个呼吸周期,记录每个呼气末正压时最后一个周期的驱动压(ΔP)(ΔP=平台气道压力―呼气末正压),以最低驱动压对应的PEEP值作为该机械通气的最佳PEEP。同时,每隔30 min进行1次手法肺复张,呼吸频率可根据PetCO2水平调整。术毕患者常规带气管插管送至麻醉恢复室,Steward苏醒评分≥4分送返病房。
1.4 观察指标
主要观察指标包括:术后5 d内PPCs发生状况,包括呼吸道感染、呼吸衰竭、胸腔积液、肺不张、气胸及支气管痉挛等,并联合墨尔本评分量表(第2版)(MGS-2)进行界定[2,13]。次要观察指标包括:术后1 d肺超声评分:将肺进行12分区,使用改良肺超声评分方法,对肺通气状态进行评价,0分:清晰A线和肺滑动征或0-2条B线;1分:≥3条B线或出现被平滑胸膜线分隔的胸膜下小实变;2分:多条合并B线或者出现被增厚、不规则胸膜线分隔的胸膜下小实变;3分:>1 cm×2 cm的胸膜下实变[14];PACU 低氧血症发生风险(SpO2<90%);术中PetCO2水平和气道峰压等。
1.5 统计学分析
采用SPSS 26.0统计软件进行统计学分析。计量资料采用均数±标准差表示,组间差异采用独立样本t检验;计数资料使用例或百分比(%)表示,组间差异采用χ2检验或Fisher's精确概率;特定人群亚组交互作用采用二项分布式Logit关联函数的广义线性模型进行分析;P<0.05认为差异有统计学意义。
2 结果
2.1 一般资料的比较
两组患者在性别、年龄、身高、体质量、BMI、ASA分级、手术后肺部并发症风险评分(ARISCAT评分)、新冠感染康复时间及手术时长等方面,差异无统计学意义(P>0.05,表1)。
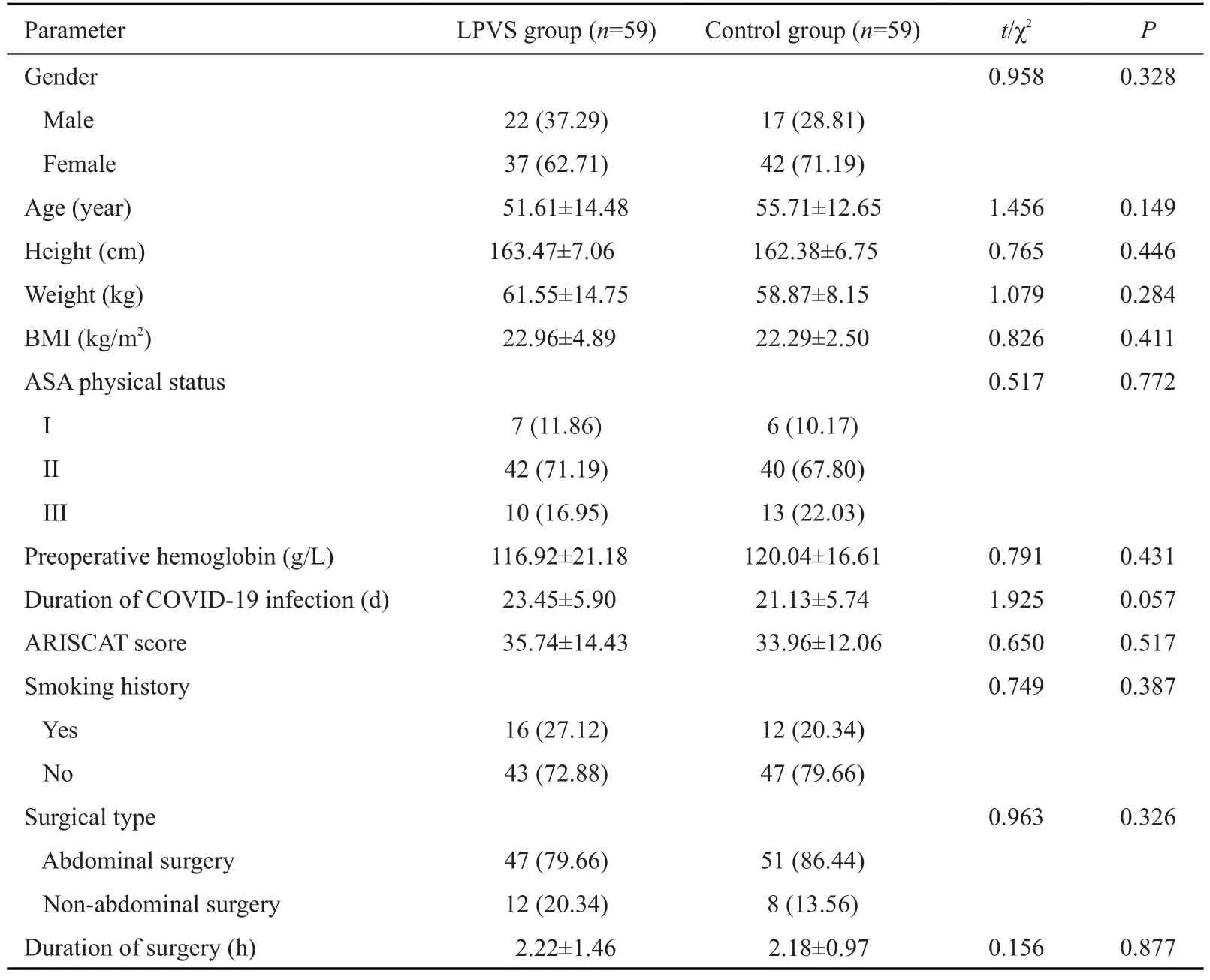
表1 两组患者一般资料比较Tab.1 Comparison of baseline characteristics of the patients between the two groups[n(%)or Mean±SD]
2.2 术中机械通气参数比较
两组患者术前SpO2和术中PetCO2水平差异无统计学意义(P>0.05);LPVS组患者PEEP值、气道压及平台压均高于对照组(P<0.05),但驱动压和潮气量低于对照组,差异有统计学意义(P<0.05,表2)。
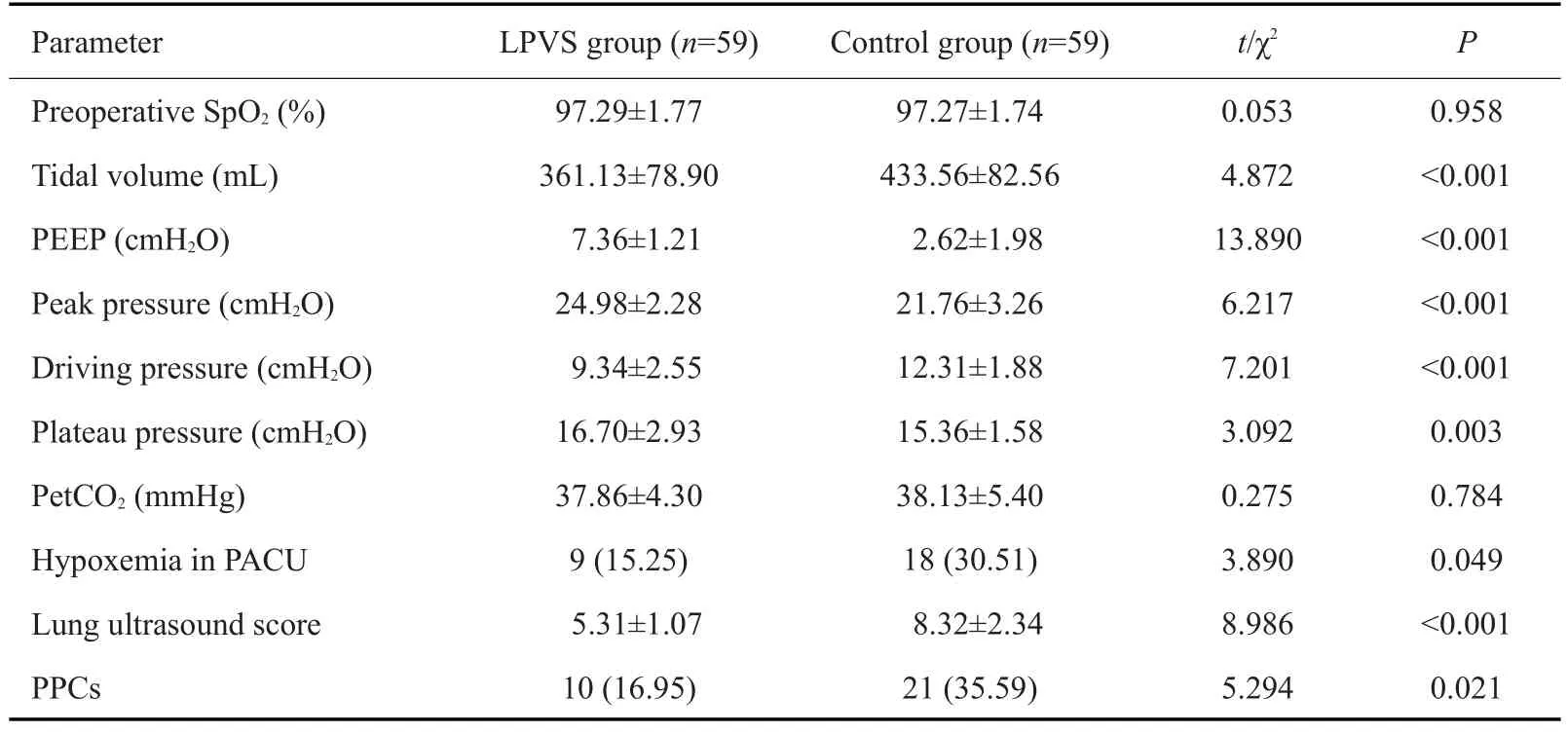
表2 两组患者通气参数及结局指标比较Tab.2 Comparison of ventilation parameters and outcomes in the two groups[n(%)or Mean±SD]
2.3 术后并发症发生风险
交互作用分析结果显示,不同通气策略与年龄、手术类型、吸烟史及术前ARISCAT评分无交互效应(表3)。合并效应后分析显示,LPVS组患者肺部超声评分,小于对照组,差异具有统计学意义(t=8.986,P<0.001);LPVS组发生PPCs 患者10 例(16.95),低氧血症患者9 例(15.25%),对照组发生PPCs患者21例(35.59%),低氧血症患者18例(30.51%),LPVS组术后肺部并发症发生风险低于对照组,差异有统计学意义(χ2=5.294,P=0.021,表2)。
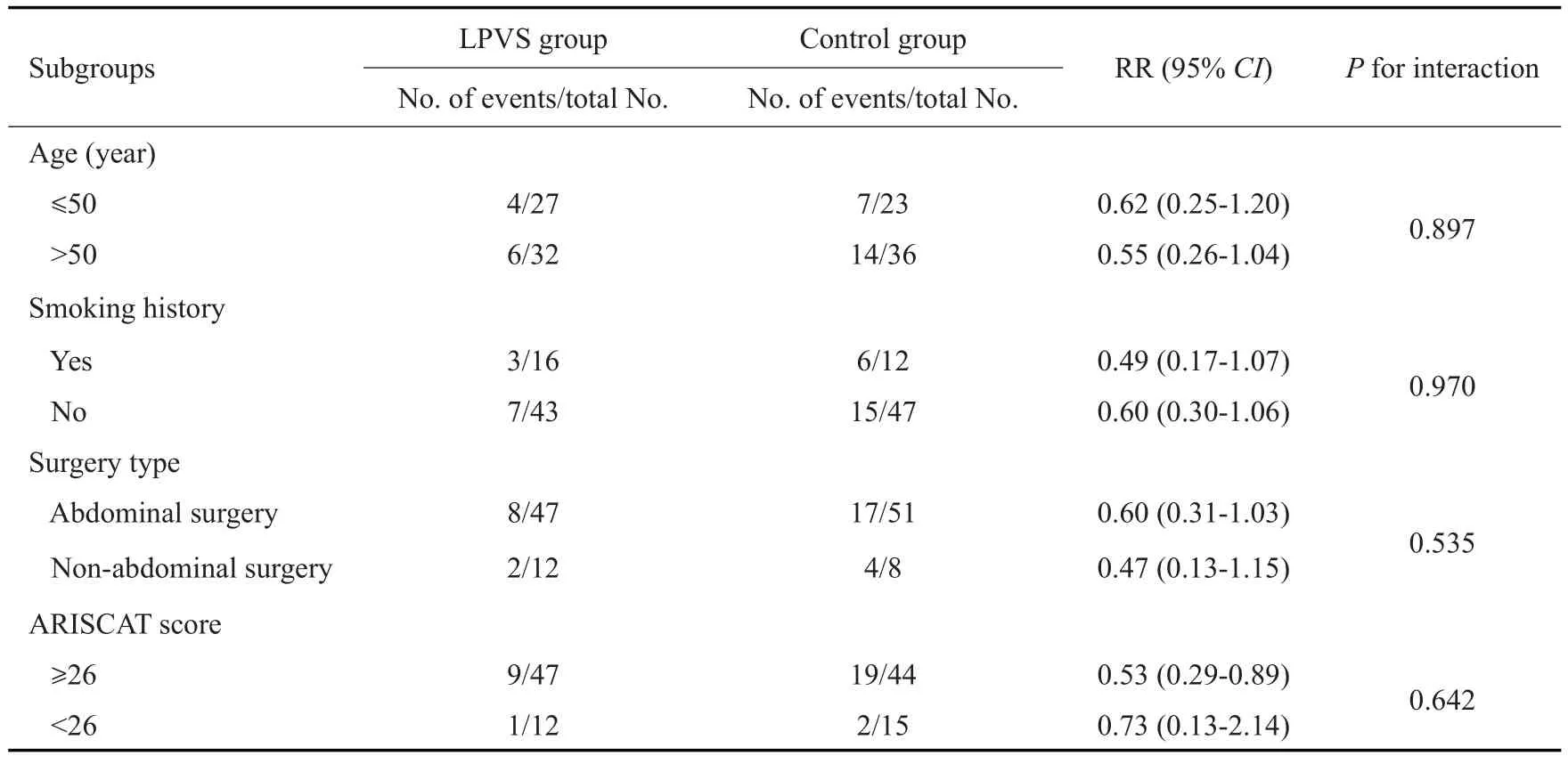
表3 亚组患者PPCs发生风险交互作用分析Tab.3 Interaction effects on the risk of PPCs in the subgroups
3 讨论
术后肺部并发症是全麻机械通气后患者最常发生的呼吸系统并发症,包括肺部感染、肺不张、胸腔积液、呼吸衰竭及急性呼吸窘迫综合征等[1,2]。2019冠状病毒病是由严重急性呼吸综合征冠状病毒-2引起的新型肺炎。病毒感染后,患者可出现发热,咳嗽,胸闷等症状,严重者可诱发ARDS发生,该症状可持续至康复后6周[15,16]。手术和机械通气可激发机体炎症和免疫应激反应,新冠康复患者体质变得虚弱,更易伴发术后肺部并发症,其PPCs发生率可高达51.2%[7,17],给医师围术期呼吸管理带来了新的挑战。本研究将驱动压力指导的个体化PEEP复合小潮气量通气策略用于COVID-19感染康复期患者的全麻手术中的呼吸管理,结果发现保护性肺通气策略可降低患者肺超声评分、PACU低氧血症及术后PPCs的发生风险。
自2000 年ARMA 试验发现,与传统通气设置相比,使用潮气量6 mL/kg和平台压小于30 cmH2O的保护性通气策略可降低患者ARDS患者死亡率以来,肺保护性通气策略被深入探究,作为指南被推荐用于成人ARDS患者的呼吸管理[18,19]。现阶段肺保护性机械通气概念已被广泛延伸至术中患者呼吸管理,但全麻期间的最佳呼吸机参数设置仍未明确,虽有部分试验对此进行了探究,可结果仍不一致[20-23]。研究认为并非所有手术患者均需要实施肺保护性通气策略,如对正常肺功能的手术病人、术后PPCs发生风险低、非上腹部或胸部外科手术的病人,实施常规机械通气并未造成肺的损伤,肺保护性通气策略并不能降低PPCs的发生率[10]。因此,麻醉期间应有针对性对肺功能脆弱患者实施这一保护措施。新冠感染患者肺部受累最为明显,可表现为包括弥漫性肺泡上皮破坏、透明膜形成、毛细血管损伤和出血、肺泡间隔纤维增生和肺实变[5,24]。本研究纳入新冠肺炎康复患者,手术后肺部并发症风险评分(ARISCAT评分)为34.89±13.32,均为中、高危风险患者。SARSCoV-2感染后6周内进行手术仍与术后肺炎风险增加相关[25],因此探究肺保护策略对该类人群的应用效果,具有较大的临床价值。
与“经典”ARDS相比,COVID-19-ARDS病理生理进展存在不同的改变,关于COVID-19-ARDS肺保护性通气的证据较少。一项针对1503例COVID-19重症患者的队列研究发现入住ICU后24 h内使用保护性通气设置可降低患者28 d死亡率[26]。最新指南也建议对于新冠患者实施肺保护性通气策略(潮气量:6 mL/kg,平台压力<30 cmH2O,驱动压<15 cmH2O)仍能取得较好的临床结局[27]。低潮气量的保护作用已被广泛接受,但高或低呼气末正压的好处以及设置呼气末正压的最佳方式一直存在争议,即是说在保护性通气中PEEP水平并非越高越好,对一些手术患者来说,高水平PEEP并未发现可降低术后肺部并发症的发生[23]。另外,值得注意的是在维持ARDS患者同样氧合条件下,COVID-19患者通常需要PEEP水平是高于“经典”ARDS患者的[28],表明COVID-19患者更易发生气压伤,提示医师术中实施肺保护性通气时更应该关注PEEP个体化问题。
驱动压(ΔP)是驱动整个呼吸系统扩张的直接动力,是死亡的一个强有力的预测因素,事实上从生理学的角度来看,驱动压力是将潮气量正常化到肺容积的更精确的方法。对于术中进行机械通气的病人来说,吸气屏气时ΔP=Pplat-PEEP,从呼吸力学的角度分析,平台压与肺顺应及潮气量有关,而其中的可控部分为潮气量与PEEP[29]。当设置合适的潮气量与PEEP时可获得最低的ΔP,此时呼吸系统的顺应性也最大。研究表明,与固定PEEP(5 cmH2O)肺保护性通气模式相比,驱动压指导设置个体化的PEEP通气策略可提高术中患者呼吸顺应性,改善氧合,降低肺不张等肺部并发症发生风险[30,31]。在本研究中,我们得到最适PEEP大多为中等水平(7~9 cmH2O)的PEEP(7.36±1.21 cmH2O),个体化PEEP组PPCs的发生率与对照组PPCs的发生率相比降低。这也与之前研究相佐证[32]。不过,腹腔镜会对腹内压和胸壁顺应性造成影响,随着腹内压增加,驱动压亦增加。此时,与肺顺应性密切相关的跨肺压可能更利于指导机械通气。但有研究表明跨肺压和驱动压呈线性关系,驱动压指导下PEEP水平接近于跨肺压监测下PEEP值。因此,限于监测条件,临床上仍常以驱动压作为指导去设置个体化的PEEP来抵消腹腔镜对驱动压升高的幅度,增加肺顺应性,发挥肺保护效应[33]。
同时,本研究也具有一定的局限性。(1)虽然不同通气策略与手术类型、是否吸烟、不同年龄组间无交互效应,但本研究仍为小样本单中心临床试验,未能统一手术类型,仍需大规模多中心证据支持;(2)出于伦理及安全考虑,本研究排除了中、重度以及仍具有明显症状的轻度新冠感染患者,因此结果是否适用于该类人群尚不明确,且需谨慎把握该类患者手术时机;(3)文献报道术后患者PPCs发生率可高达51.2%[7],但本试验无论是对照组还是肺保护通气策略组PPCs发生率均低于该值,一方面与术中实施肺保护性通气策略有关,另一方面这可能与本研究只纳入新冠感染轻度患者以及不同国家地区新冠病毒毒株,毒力不同有关。
对于感染后仍处于恢复期需要接受急诊或限期手术患者呼吸管理仍是当前一段时间内所面临的麻醉难点,本研究发现驱动压指导的肺保护性通气策略能够改善患者氧合,降低术后肺部并发症发生风险,值得临床推广应用。
- 南方医科大学学报的其它文章
- 高表达分泌颗粒蛋白II增加结直肠癌细胞对奥沙利铂的耐药性
- Neutrophil-lymphocyte and platelet-lymphocyte ratios for assessing disease activity in patients with rheumatoid arthritis receiving tofacitinib treatment
- 淫羊藿素通过调控铁死亡增加鼻咽癌细胞的放射敏感性
- 靶向结直肠癌的小白菊内酯脂质体纳米颗粒诱导程序性坏死并改善T细胞耗竭
- 二甲双胍减轻阿霉素诱导的心脏毒性:基于AMPK通路
- 甲基转移酶样3抑制剂STM2457通过调节线粒体功能改善代谢相关脂肪性肝病