碱渣的热分解特性及动力学分析*
宗永兰,吴泳霖,龚建涛,蒋 明,张继来
(云南农业大学 资源与环境学院,云南 昆明 650201)
碱渣又俗称白泥,是氨碱法生产纯碱中所产生的白色固体废物,每生产1t Na2CO3约副产0.3t 碱渣[1]。统计表明[2],截止2020 年我国每年的碱渣产量达1000 万t,且年增长达3%以上,目前利用率仅为3%~4%。近年来,大量的碱渣堆存不仅占用土地,且对海洋流域也产生极大的影响,形成大片“白海”,污染环境[3]。
碱渣为白色粉末细颗粒,其主要物相组分为CaCO3、Ca(OH)2、CaCl2、Mg(OH)2及NaCl。此外,还有极少量的CaSO4、SiO2、Al2O3等[4]。由于其特有的理化性质和高钙性,目前,碱渣主要应用于烧制水泥、碱渣-矿渣-粉煤灰复合胶凝材料的制作、制备免烧砖等[5]。利用碱渣生产建筑材料前对于碱渣的理化性质、热分解特性及动力学的研究极其重要,对产品的性能有直接影响。
热分析法是研究固体分解、相变、分解、升华等化学物理特性的一种重要方法,能较好的揭示碱渣热分解特性。Yan[6]等报道了煅烧碱性残渣对废水中磷酸盐的吸附,研究结果表明,碱渣煅烧到800°C 有很好的潜力作为吸附剂去除蚀刻废水中的磷酸盐。Li 等[7]探究了CaO-CaCO3循环过程中造纸碱渣的热化学储能性能,结果表明,改性后的碱渣比原始碱渣有更高的价值,改性碱渣是一种合适的储能材料。张雷[8]等对碱渣进行了热重分析,发现了碱渣在空气气氛下的热分解为多阶段分解模式,且其活化能随转化率的增大而增大。本文采用热重/差热法(TG-DTA)研究了N2气氛下碱渣的热分解特性及动力学特征,为碱渣综合资源化利用提供理论依据和参考。
1 实验部分
1.1 实验材料
碱渣取自山东省某氨碱厂,将其研磨、过筛至80 目备用。
1.2 实验方法
采用北京恒久实验设备有限公司HCT-1 型同步TG-DTA 热分析仪测定碱渣样品的TG-DTG 和TG-DTA 曲线。
实验条件 样品质量为(7±0.2)mg,动态无水N2气氛,气流流量均为50mL·min-1,升温速率分别为5、10、15 和20°C·min-1,温度范围为50~800℃。
1.3 热分解动力学方法
1.3.1 热分解动力学基本理论 碱渣的热分解属于固体热分解反应,故可遵循方程(1)[9]:
式中 α:碱渣热分解过程中某一个时刻t 时的转化率,%;定义α=(m0-mt)/(m0-mf),m0、mt、mf分别为样品的初始、任一时刻t、终止时的样品质量,g;t:热分解时间,s;A:反应指前因子,s-1;E:热分解活化能,kJ·mol-1;R:普适气体常数,取值8.314J·(mol·K)-1;T:热分解温度,K;f(α):根据碱渣的反应类型所决定的动力学微分机理函数。
1.3.2 热分解活化能计算 根据TG/DTG 曲线,分别采用Kissinger 法[10]、Flynn-Wall-Ozawa(FWO)峰值转化率近似相等法[11]、Flynn-Wall-Ozawa(FWO)等转化率法[12]对比求解活化能E,从而探讨不同气氛下碱渣热分解过程反应速率的快慢。Kissinger 方程和FWO 方程分别见式(2)和式(3)。
式中 Tmax:峰值分解温度,K;β:升温速率,K·min-1或°C·min-1;G(α):由反应类型所决定的积分动力学机理函数;Tα:不同升温速率下达到相同转化率时的温度,K;其余参数的物理意义与方程式(1)相同。具体求解方法见文献[13]。
2 结果与讨论
2.1 N2 气氛下碱渣热分解特性
N2气氛下碱渣热分解的TG-DTG 和TG-DTA曲线分别见图1、2。
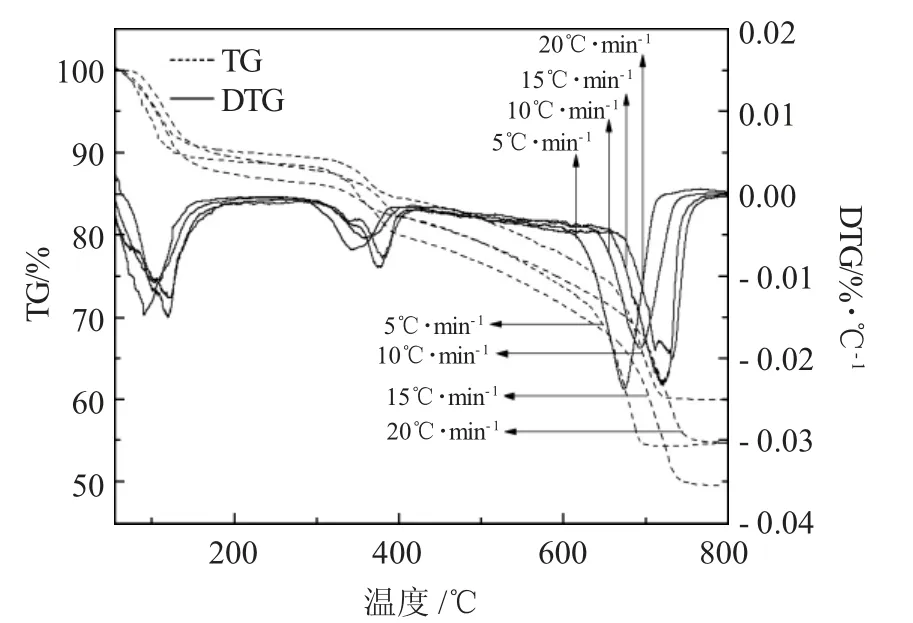
图1 N2 气氛下不同升温速率时碱渣的TG-DTG 曲线Fig.1 TG-DTG curves of alkali slag at different heating rates in N2 atmospheres

图2 N2 气氛下不同升温速率时碱渣的TG-DTA 曲线Fig.2 TG-DTA curves of alkali slag at different heating rates in N2 atmospheres
由图可知,升温速率分别为5、10、15、20°C·min-1时,碱渣的热分解呈现出3 个阶段,见表1。

表1 不同升温速率下碱渣的失重率(%)Tab.1 Weight loss rate of alkali slag under different heating rates
由图1、2 可见,DTG 曲线中有3 个阶段失重峰值的温度随着升温速率的增加而升高。DTA 曲线有3个向下的吸热峰,可知碱渣的3 个失重阶段均为吸热反应,其失重峰值的温度随着升温速率的变化规律与DTG 曲线相同,第一峰在80~130°C 之间,该阶段可能为碱渣中表面吸附水的释放;第二峰在300~400°C 之间,该阶段为碱渣中Ca(OH)2、Mg(OH)2的分解;第三峰在600~800°C 之间,表现为CaCO3的分解。随着升温速率增高,TG、DTG 和DTA曲线都向高温区移动。
2.2 碱渣热分解动力学
2.2.1 Kissinger 法求解热分解动力学 碱渣的动力学基础数据见表2,结合Kissinger 法拟合得到直线方程见图3。
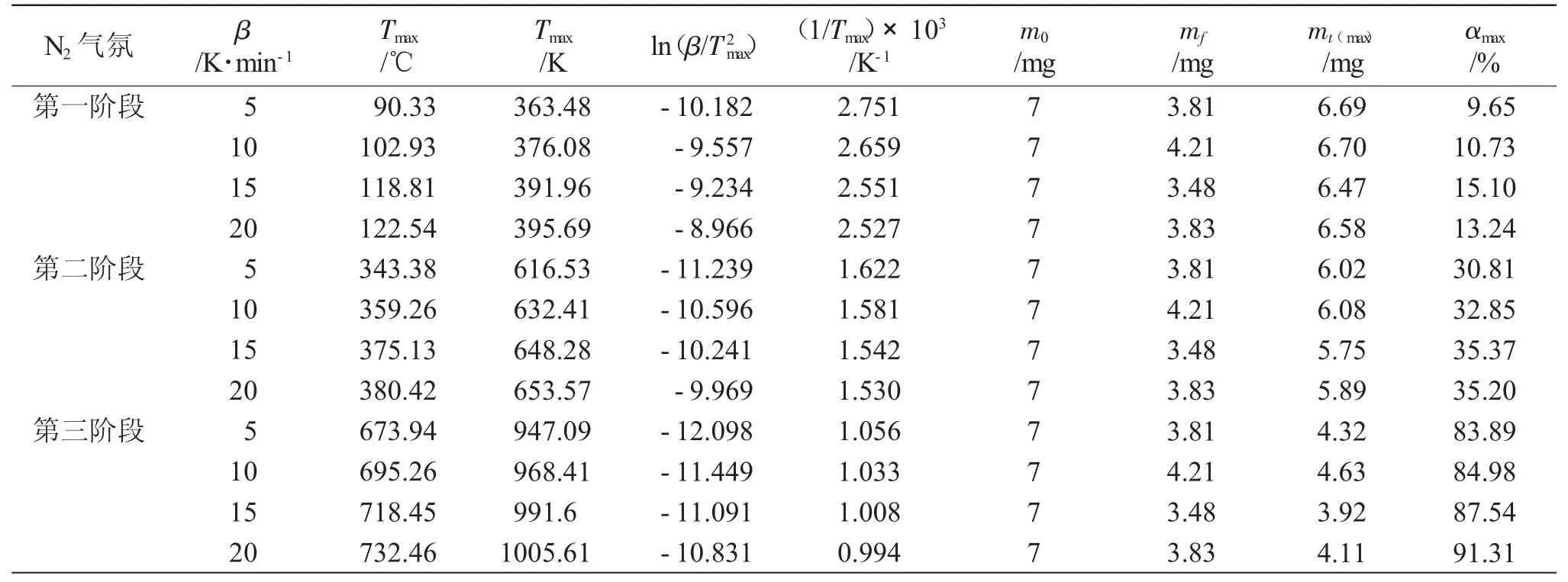
表2 TG/DTG 曲线分析得到的动力学基础数据Tab.2 Basic data of the kinetics by TG/DTG curves
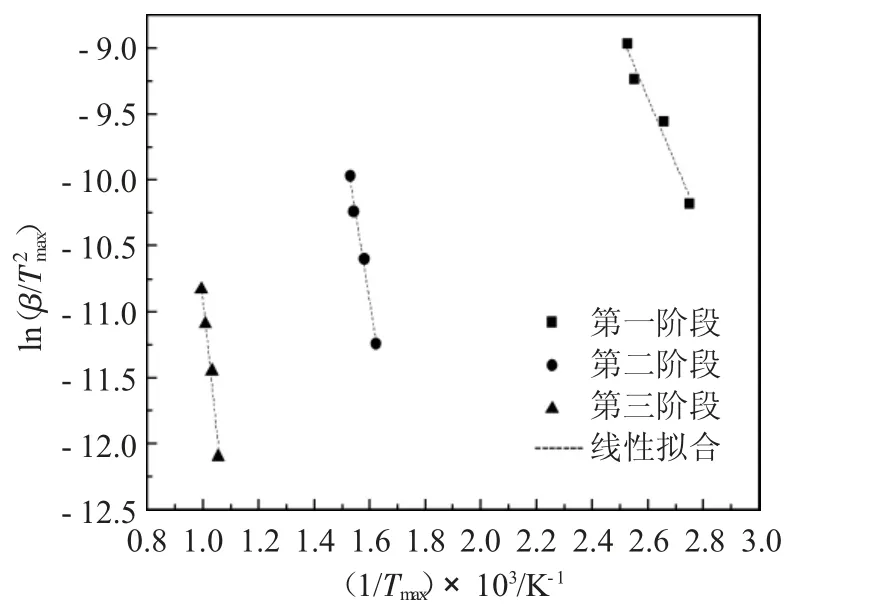
图3 N2 气氛下ln(β/T2max)-1/Tmax 的拟合曲线Fig.3 Fitting curves of ln(β/T2max)-1/Tmax in N2 atmospheres
根据图3 的拟合结果得到拟合方程为:
第一失重阶段 Y=-4.98X+3.58,相关系数R=0.9489,计算得到热分解活化能E=41.34kJ·mol-1,指前因子对数lnA=5.19;
第二失重阶段 Y=-13.12X+10.07, 相关系数R=0.9775,计算得到热分解活化能E=109.05 kJ·mol-1,指前因子对数lnA=12.64;
第三失重阶段 Y=-20.05X+9.14 , 相关系数R=0.9685,计算得到热分解活化能E=166.72kJ·mol-1,指前因子对数lnA=12.14。
随着温度的升高碱渣在N2气氛下的热分解活化能也逐渐增大。
2.2.2 FWO 峰值转化率近似相等法求解热分解动力学 FWO 峰值转化率近似相等法计算所得的峰值转化率αmax数值见表2。
由表2 可见,碱渣在N2气氛下同一分解阶段内αmax随升温速率的升高而呈逐步上升趋势,同时不同阶段总体也呈现上升趋势,表明碱渣的热分解程度不断升高。此外,不同升温速率时的αmax不近似相等,表明该法不适用于碱渣的热分解活化能E 的求解。
2.2.3 FWO 等转化率法求解热分解动力学 FWO等转化率法得到的拟合直线和结果见表3 和图4。

表3 不同转化率下碱渣的热分解活化能(E)Tab.3 Thermal dehydration Activation energy(E)of alkali slag at different conversion rates
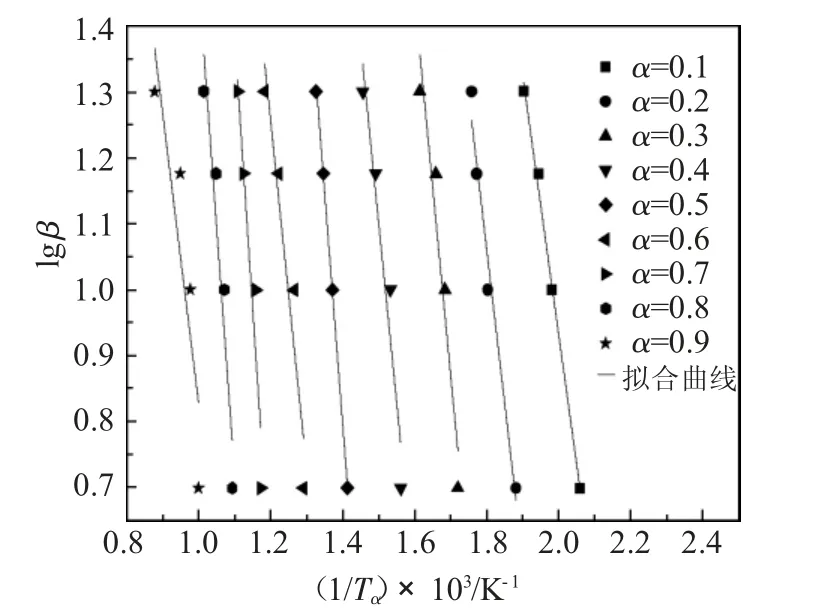
图4 N2 气氛下lgβ-1/Tα 的拟合曲线Fig.4 Fitting curves of lgβ-1/Tα in N2 atmospheres
由表3 和图4 可见,N2气氛下直线拟合良好,它的热分解活化能E 与转化率α 无明显相关性。同时,碱渣在N2气氛下的最大热分解活化能与最小热分解活化能的差值为77.9kJ·mol-1,小于其平均热分解活化能(105.4kJ·mol-1),表明碱渣在N2气氛下的热分解符合国际热分析协会的标准(由α 所得的最小与最大活化能差值应小于平均值[14]),说明FWO等转化率法可用来求解N2气氛下碱渣的热分解活化能。
3 结论
(1)升温速率越快,碱渣完全热分解需要的温度越高。
(2)碱渣热分解共有3 个阶段:在80~130°C 阶段是碱渣脱去结晶水;300~400°C 阶段是碱渣中Ca(OH)2和Mg(OH)2的分解;600~800°C 阶段是碱渣中CaCO3分解。
(3)由Kissinger 法计算得到碱渣,第一阶段热分解活化能E 为41.34kJ·mol-1,指前因子对数为5.19;第二阶段热分解活化能E 为109.05kJ·mol-1,指前因子对数为12.64;第三阶段热分解活化能E为166.72kJ·mol-1,指前因子对数为12.14。
(4)FWO 等转化率法其平均活化能均为105.41 kJ·mol-1,而FWO 峰值转化率近似相等法不适用于碱渣热分解活化能的计算。

