天然染料红花黄色素的提取工艺及其稳定性
王利平,聂文山,缪其桁,张 鑫
(1.内蒙古工业大学 轻工与纺织学院,内蒙古 呼和浩特 010080; 2.内蒙古鹿王羊绒有限公司, 内蒙古 包头 014040;3.东华大学 纺织学院,上海 201620)
当前,纺织产业处于以绿色低碳为引领的转型发展关键时期[1]。天然染料无毒无害,在提取及染色过程中仅有少量废水产生,具有环保、健康、安全等特点[2],在纺织品染色中得到进一步应用,如可通过对红花的提取获得红花黄色素用作纺织品染色的染料[3]。水提取法是一种绿色的提取方式,使用水作为溶剂提取红花黄色素,可有效减少有机溶剂和金属离子的使用及排放[4-5]。
目前,关于红花黄色素的报道大多集中于医药和食品领域[6-7],对红花黄色素的提取及在纺织品染色方面的应用研究不够系统,工艺优化有待进一步完善[8]。本文以红花为原料,分析水提取红花黄色素过程中的影响因素,并通过响应面法优化提取工艺,对色素的稳定性开展初步的探究,以期为后续的研究提供理论参考。
1 试验材料及仪器
材料:红花(市购,原产地新疆)。
药品:无水乙醇、硫酸锌、硫酸亚铁、氯化钙(天津永晟精细化工有限公司);乙酸、硫酸铜(天津市致远化学试剂有限公司);氢氧化钠(天津福晨化学试剂有限公司);氯化镧(上海阿拉丁生化科技股份有限公司),以上均为分析纯。
仪器:HH-6型恒温水浴锅(金坛市友联仪器研究所);9070型电热鼓风干燥箱(南京沃环科技实业有限公司);SHB-IIIG型循环水式真空泵(郑州长城科工贸有限公司);IR Affinity-1型傅里叶变换红外光谱仪(岛津试验器材有限公司);TDZ5-WS型台式离心机(湖南湘仪试验室仪器开发有限公司);UV1750型紫外-可见分光光度(岛津试验器材有限公司);YF3-5型高速万能粉碎机(温州市永历仪器设备有限公司);LGJ-12A型真空冷冻干燥机(河南信陵仪器设备有限公司)。
2 红花黄染料的提取工艺
2.1 单因素试验
取5份红花粉末,每份10.00 g,以固液比、温度、时间为3个因素,进行单因素试验,试验安排如表1所示。

表1 单因素试验表Tab.1 Single factor experiment table
采用分光光度计测定溶液的吸光度,比较有色溶液对某一波长光的吸收情况,进而确定物质溶液浓度[9]。将染液冷却后进行过滤,定容至500 mL,取适量提取液稀释10倍,测试其在403 nm处的吸光度,并比较不同条件对提取效果的影响。403 nm是红花黄色素对应的一个特征峰,这个峰值高说明色素溶解的多,故后续主要在403 nm处测试不同条件下溶液的吸光度。
2.2 响应面工艺优化
使用Design-Expert V8.0.6软件对提取工艺进行响应面试验设计[10]。
2.3 结果与讨论
2.3.1 固液比的影响
在不同的固液比条件下,根据表1试验条件,对不同溶液进行吸光度测试,试验结果如图1所示。

图1 固液比对红花黄色素提取效果的影响Fig.1 Effect of solid-liquid ratio on extraction of safflower yellow pigment
由图1可知,随着固液比的增大,403 nm处的吸光度先增大后减小。在固液比1∶25时,吸光度达到最大,这是因为在提取红花黄色素的过程中,溶剂进入到红花内部,将色素溶解的内驱力是浓度梯度,溶剂增多有利于这个过程,太多溶剂进入过程受阻,效果变差,故选择的固液比为1∶25。
2.3.2 温度的影响
在不同温度下,根据表1条件对不同溶液进行吸光度测试,试验结果如图2所示。
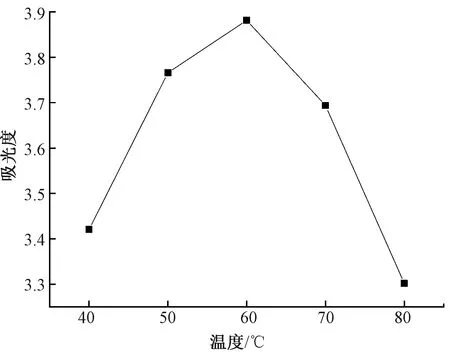
图2 温度对红花黄色素提取效果的影响Fig.2 Effect of temperature on extraction of yellow pigment from safflower
由图2可知,在一定温度范围内,随着温度的升高,吸光度逐渐增大。温度在60 ℃时吸光度最大,说明此温度下提取效果最好,这是由于中低温时温度的升高有利于体系内分子运动加速。随着温度的进一步升高,吸光度明显降低,可能是因为在温度升高的过程中,色素逐渐遭受破坏造成的。因此最佳提取温度选择60 ℃。
2.3.3 提取时间的影响
在不同提取时间下,根据表1条件,对不同溶液进行吸光度的测试,试验结果如图3所示。

图3 时间对红花黄色素提取效果的影响Fig.3 Effect of time on extraction effect of safflower yellow pigment
由图3可知,当提取时间较短时,色素在水中的溶解量较低,当提取时间为60 min时吸光度值达到最大,而继续延长提取时间时,提取液吸光度值出现下降,这是因为太长时间的提取破坏了色素本身的结构,进而影响色素的提取效果,故最佳提取时间选用60 min。
2.3.4 响应面法优化红花黄色素提取工艺
根据单因素试验所确定的优选工艺条件,选用合适的试验条件范围,设计红花黄色素提取工艺的因素水平表,具体见表2。

表2 因素与水平设计表Tab.2 Analysis factors and horizontal design table
红花黄色素提取工艺的响应面试验结果见表3。方差分析结果见表4。

表3 响应面试验结果Tab.3 Response surface experiment results
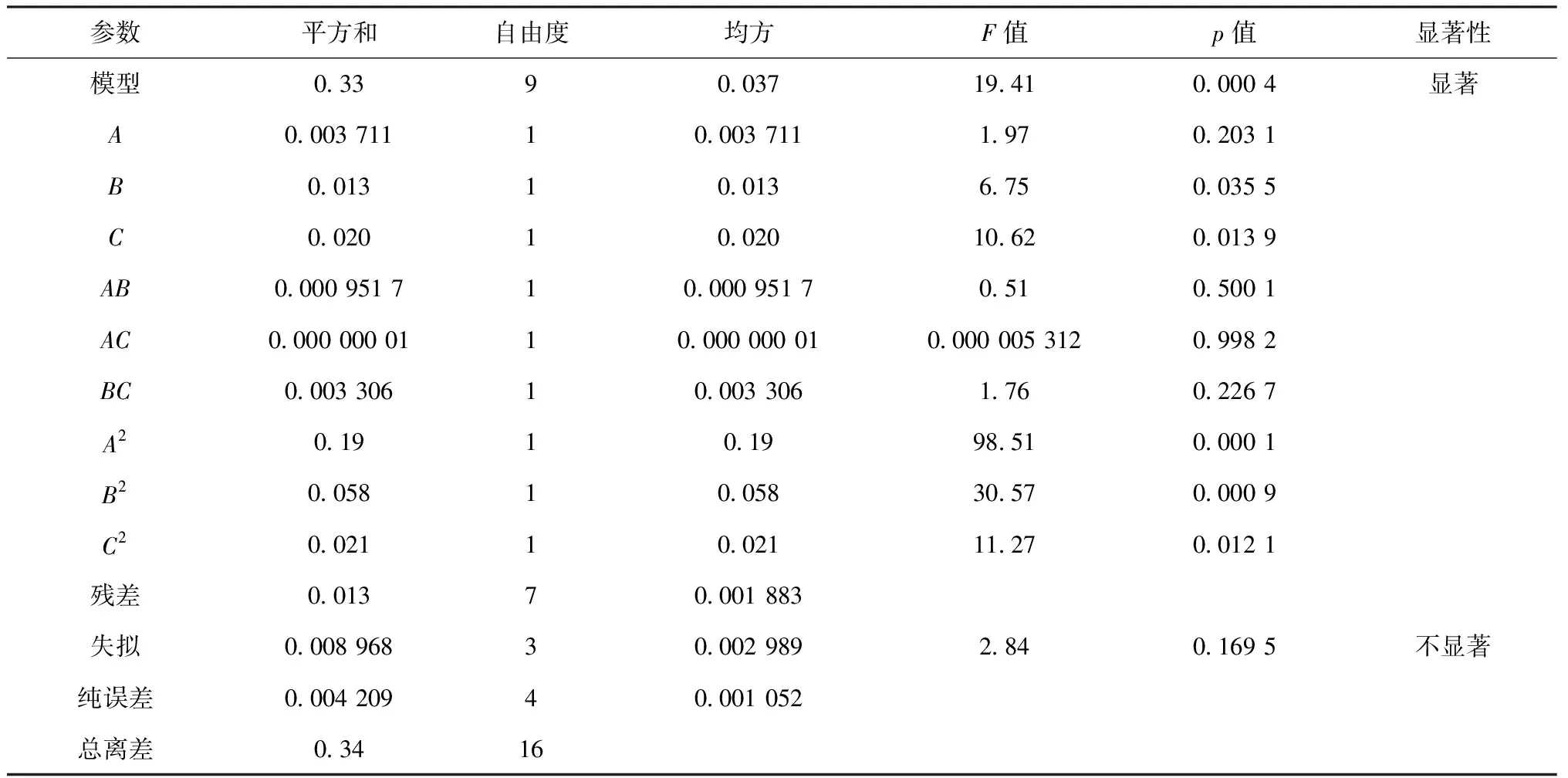
表4 方差分析Tab.4 Variance analysis
根据方差分析结果可知,模型的F值为19.41(P<0.001),说明该回归模型极显著。模拟项不显著(P=0.169 5>0.05),表明模型选择合适,可用此模型对试验进行分析和预测。显著性检验表明,提取时间C对红花黄色素提取液吸光度极显著(P=0.0139<0.05),提取温度B对提取液吸光度显著(P=0.0355<0.05),而固液比A对提取液吸光度不显著(P=0.203 1>0.05)。故红花黄色素的最佳提取工艺为固液比1∶25,提取温度60 ℃,提取时间60 min。
3 红花黄染料的稳定性分析
3.1 pH值对稳定性的影响
配制pH值分别为3、5、7、9、11的缓冲液50 mL,每份溶液中加入2 g红花黄粉末,待全部溶解后,静置溶液60 min后测试溶液在403 nm处的吸光度,绘制吸光度谱图如图4所示。

图4 不同pH值下的红花黄色素紫外光谱图Fig.4 Ultraviolet spectrum of safflower yellow at different pH value
由图4可知,溶液为酸性时,染料吸光度值比溶液pH值为碱性和中性时的值高。在酸性环境下的吸光度值相近,此时溶液呈黄色。由此可见,pH值对于红花黄染料的稳定性有很大影响,染液中部分成分在酸性条件下溶解度较大,故为达到高的增色效应,在后续染色过程中需要确保染色环境pH值在酸性范围内。
3.2 温度对稳定性的影响
配制5份50 mL质量分数为10%的红花黄染液,分别在50、60、70、80、90 ℃下保温60 min后测试溶液的吸光度,绘制吸光度图如图5所示。

图5 不同温度红花黄色素紫外光谱图Fig.5 Ultraviolet spectrum of safflower yellow at different temperatures
由图5知,随着温度的增加,溶液的吸光度先增加后减小,温度高于70 ℃后,溶液吸光度急剧减少,说明温度升高对染料的结构有明显的影响,可能会造成染料的分解,故为达到更好的上染效果,使用温度应低于70 ℃。
3.3 金属离子对稳定性的影响
配制浓度为0.1 mol/L的CaCl2、CuSO4、FeSO4、LaCl3、MgCl2溶液各1份,每份溶液中加入5 g红花黄粉末,待全部溶解后,静置溶液60 min后测试溶液在403 nm处的吸光度,绘制吸光度如图6所示。
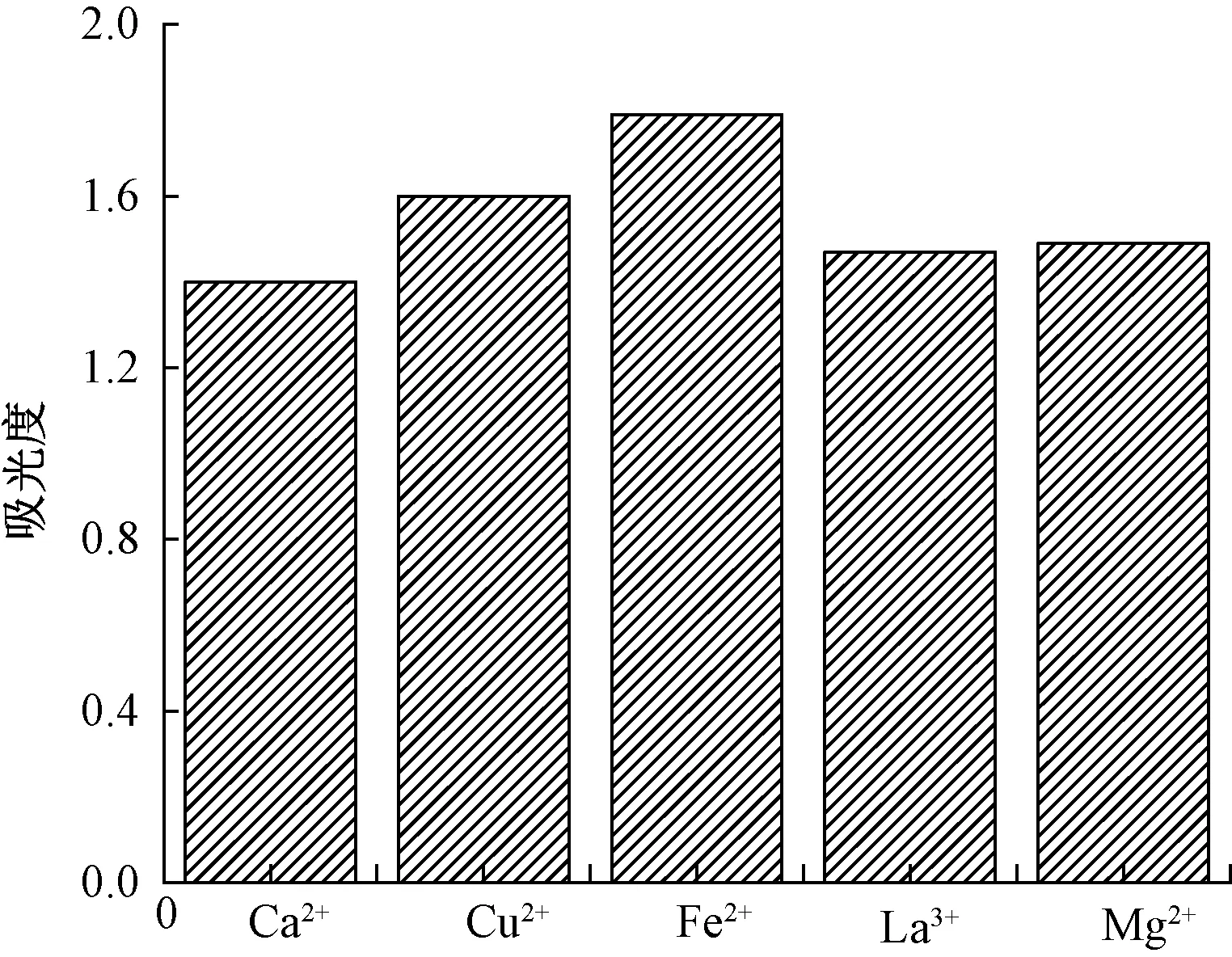
图6 不同金属离子红花黄紫外光谱图Fig.6 Ultraviolet spectrum of safflower yellow with different metal ions
由图6可知,加入不同的金属离子后,染液发生了不同程度的变化。其中Cu2+和Fe2+对溶液的影响较大,加入Cu2+后,溶液的颜色由黄色变为黄绿色,溶液的吸光度值略微上升。加入Fe2+后,溶液颜色由黄色转变为黄褐色,溶液的吸光度值明显升高,这是因为Fe2+与红花黄色素发生了络合反应,生成配位化合物,从而破坏了色素的结构。加入Ca2+、Mg2+和La3+后溶液吸光度的变化较小。
4 结 论
通过单因素试验与响应面法优化相结合的研究方法,从提取效果及稳定性方面,对水提取红花黄色素的工艺进行研究,同时对其稳定性进行探讨,得出以下结论:
①红花黄色素染液在特征峰(波长403 nm)处的吸光度随着固液比的增大先增大后减小,随着提取温度的升高先增大后减小,随着提取时间的增加而缓慢减小。在固液比1∶25,提取温度60 ℃,提取时间60 min时吸光度最大,提取效果最好。
② 提取条件对红花黄色素染液的吸光度显著性检验表明,提取时间极显著,提取温度显著,固液比不显著。红花黄色素的最佳提取工艺与试验结果一致。
③ 红花黄色素在pH值为3~5的酸性条件、环境温度在70 ℃以下时比较稳定;红花黄色素会与Cu2+和Fe2+反应,并发生颜色变化,Ca2+、Mg2+、Zn2+和La3+对红花黄色素的稳定性几乎无影响。

