S-100吸收性止血绫在体外循环心脏直视手术中的应用
朱一林(兰州大学第二医院,甘肃 兰州 730030)
ECC心脏直视手术术后出血是临床常见且严重的并发症之一[1]。出血量过多可引起其他严重并发症,大大升高了患者的死亡率。体外循环手术涉及心脏表面、大血管多个切口。因心腔及血管腔压力高,故此类切口缝合后渗血均较多,一般表现为广泛的针眼渗血。对此,临床应用结扎、补针、电凝等其他传统止血方法无法有效止血[2-3]。S-100吸收性止血绫由再生纤维素织物经化学变性而成,生物相容性好。遇针眼渗出血液后,可以即刻溶解为透明凝胶状。因此学界认为,在临床手术中,S-100可被用于贴敷于心脏表面切口及主动脉吻合口处。基于此,笔者在临床ECC心脏直视手术中应用S-100吸收性止血绫,获得了较为理想的临床效果。现报道如下。
1 资料与方法
1.1 临床资料 本研究是对临床资料的回顾性分析。纳入兰州大学第二医院心脏外科2020年1月-2022年12月诊治的实施ECC心脏直视手术患者106例。本研究经医院伦理委员会审批通过。纳入标准:18-70岁;术前接受经胸心脏血管超声、计算机断层扫描、核磁共振检查,确诊为心脏疾病,具有ECC心脏直视手术指征[4]并完成手术;患者术前血小板、凝血功能指标、血常规均正常;术前既往病史、在院接受手术的临床资料、随访资料(术后至少1年)完整,符合本研究统计分析对数据的要求。排除标准:术前有既往心脏手术史者;术前肝、肾功能和凝血功能异常者;术前体内脏器、组织已存在活动性出血者;术前(10d内)接受过抗凝治疗者;出现术后出血合并心脏压塞等病情危急、复杂病情者;特殊人群:处于妊娠期、哺乳期,或合并精神疾病、严重感染者;住院期间死亡病例。根据术中是否应用S-100将其分成两个组,对照组(n=37)和观察组(n=69)。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。
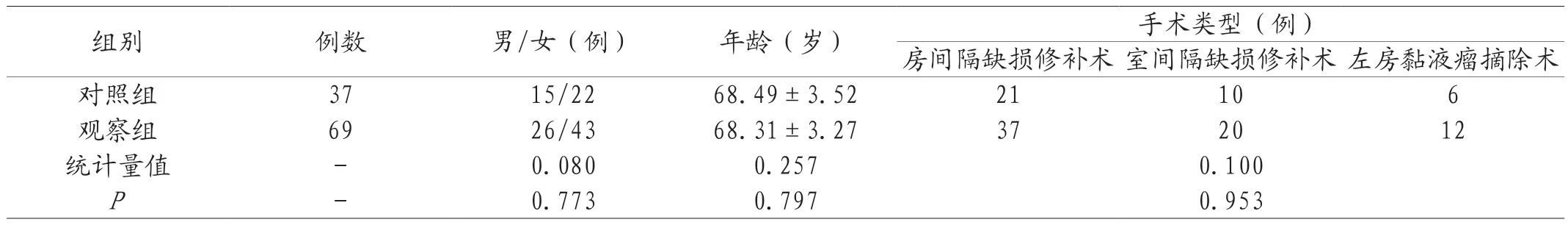
表1 两组患者一般资料比较
1.2 方法
1.2.1 主要的设备仪器 德国索林公司的StockertS 5型CPB机、变温水箱,意大利索林公司的中空纤维膜式氧合器、血液浓缩器,美国西科瑞公司的空气-氧气混合器,美国勃林格殷格翰公司的负压调节器,美国美敦力公司的混合静脉血氧饱和度监测仪,美国沃芬公司血凝分析仪。
1.2.2 麻醉与手术 (1)麻醉。在心脏停跳下进行手术。所有患者采用静吸复合麻醉、气管内插管,麻醉后放置食管超声探头。术前常规开放静脉通路,间歇正压通气,监测心电图,桡动脉穿刺监测动脉血压,监测肺毛细血管楔压,常规监测脑电双频谱指数/脑氧饱和度,放置体外电击除颤片。(2)手术。①建立CPB插管,经肋间单独造口放置左心减压管,主动脉开放前经灌注针处抽吸排除左心气体。确定心脏小切口入路,选用胸骨上段切口入路,在平胸骨第2肋间皮肤做一小的横切口,第2-4肋间以反“Z”字形锯开胸骨。房间隔缺损修补术或室间隔缺损修补术:右侧胸骨旁第3肋间、右侧腋中线/腋前线第3肋间为操作孔,于右侧锁骨中线第5肋间置入胸腔镜。②实施心脏手术。③经食管超声确定心脏手术效果满意后,停机,拔出静脉引流管。股动静脉外科重建,颈内静脉冰袋压迫30min。④鱼精蛋白中和(3mg鱼精蛋白中和1mg肝素),拔出动脉插管。⑤血液保护:术前肝素化后经静脉引流管放血500-1000mL,低温下保存,停机后复温、回输。
1.2.3 S-100的应用 ①在建立体外循环、进行股动静脉插管时,于游离股动静脉时、撤除股动静脉插管后,在腹股沟切口内放置S-100(北京泰科斯曼科技发展有限公司生产)以预防手术损伤及术后淋巴瘘。②术中用针管等笔式器械深入小切口或腔镜孔对手术创面喷洒S-100,以解决深部出血、止血难以控制等临床问题。见图1。③胸骨断端止血。a.术中在关胸阶段,将S-100卷为长条状填塞于双侧骨髓腔内进行止血。b.于钢丝拉起时直接将S-100放置于胸骨锯开处。
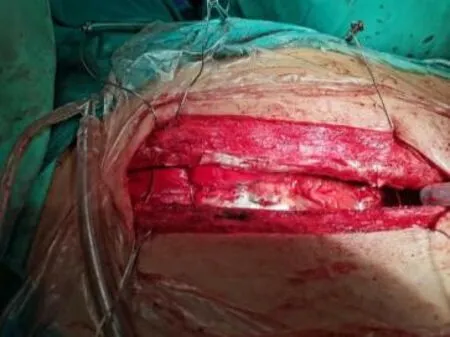
图1 术中用针管等笔式器械深入小切口或腔镜孔对手术创面喷洒S-100
1.2.4 围术期检查和监测 ①术前:纠正贫血和心、肝、肺、肾等重要脏器功能指标;术前1周停用抗凝或血小板抑制药物,术前10d停用阿司匹林。术前预充液中加入乌司他丁以减轻肺部炎性反应。连续动态监测ACT,对于术后有机血回输患者要完全中和肝素、预防肝素反跳现象。②术后:监测生命体征;小剂量持续负压吸引,确保引流通畅,血压不低于术前±10mmHg。定时行床旁胸片或B超检查;监测并积极处理术后各种并发症。
1.3 观察指标及评价标准 参照文献[5],统计并比较两组的围术期相关指标,包括:CPB转流时间、超滤量、心脏停跳时间、胸腔引流量、术后机械通气时间、重症监护时间。两组不良事件发生情况,包括术后心脏复跳情况(自动复跳比例、安置临时起搏器比例)及二次开胸比例。
1.4 统计学方法 采用SPSS19.0医学统计软件进行数据分析。计量资料以(±s)表示,比较采用t检验。计数资料以[n(%)]表示,比较采用χ2检验。等级资料采用Mann-Whitney U秩和检验。取α=0.05,P<0.05表示差异有统计学意义。
2 结果
2.1 围手术期指标比较 观察组术后胸腔引流量少于对照组,重症监护时间较对照组缩短,两组比较,差异有统计学意义,P<0.05。见表2。
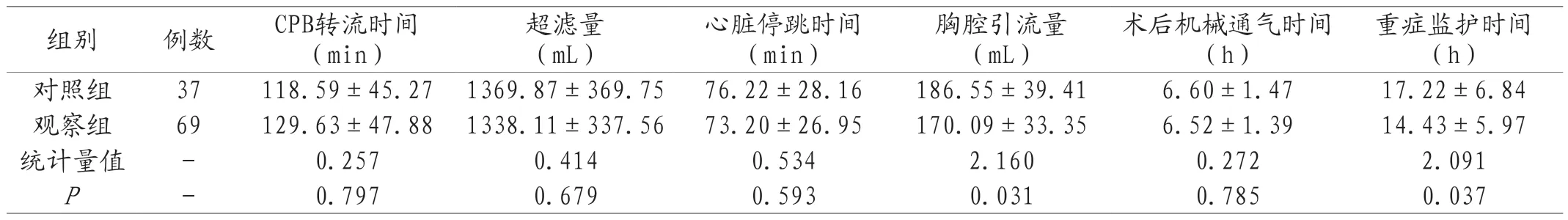
表2 两组围手术期指标比较
2.2 不良事件发生情况比较 观察组:1例手术创面广泛渗血,行再次开胸手术,术中未发现明显的出血点,考虑患者为60岁以上、年龄偏大,其可能合并胸骨的骨质疏松,其弥漫性出血推测为术后可见胸骨断面、胸骨上下层组织创面的渗血。对照组:5例出现手术创面广泛渗血,行再次开胸手术,3例术中未发现明显的出血点,推测是由于手术中处于低温、低血压,在术毕复温、升压后,部分已凝结出血点或者已闭塞血管被重新开放而引起出血。2例出血部位为大血管吻合口针眼。观察组术后出血率低于对照组,两组比较,差异有统计学意义,P<0.05。两组术后心脏复跳情况无统计学意义(P>0.05),观察组二次开胸比例低于对照组(P<0.05)。见表3。
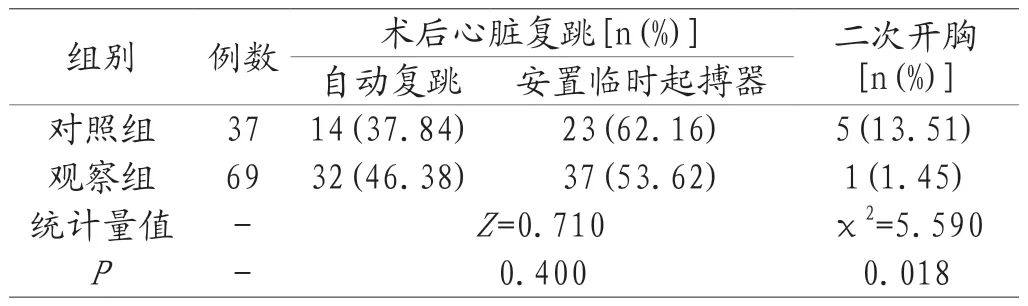
表3 两组不良事件发生情况比较
3 讨论
引起ECC心脏直视术后出血的主要原因包括:术中止血不彻底、肝素未完全中和,手术创伤所致凝血物质减少等。术中止血不彻底将显著增加术后出血概率。通常将ECC心脏直视术后出血分成弥漫性出血及活动性出血两种类型[6]。
引发弥漫性出血的原因包括:患者既往手术史、存在手术区域组织器官的粘连,术前心脏功能不全、使用抗凝药物,术中体外循环温度较低,肝素中和不足、止血不彻底,术后出血处理不及时、继发多脏器功能不全,体外循环导致凝血机制紊乱等多方面的因素。具体来说:一方面,多数心脏病患者术前有不同程度的心功能不全,由此可累及肝、肾、肺等多脏器功能。肝脏是多种凝血因子及凝血酶的合成场所。肝、肾功能不全是术后失血非常重要的影响因素。微循环灌注不足、低心排量可加重肝、肾的损害。另一方面,体外循环本身可能对凝血机制造成破坏[7]。比如:低温可致血液黏稠度增加、引起组织缺氧和酸性物质积聚,造成血液成分被破坏;体外循环可引起代谢紊乱、酸中毒,后者可直接损伤微血管内皮细胞,激活因子Ⅻ与内源性凝血途径;体外循环可相应稀释血液及血液循环中的血小板和血浆因子,影响术后早期凝血功能;体外循环的管道、泵形成的机械性挤压、心内吸引可对血小板造成直接损伤;与血液直接接触,激活、损伤、破坏血小板,可导致血小板功能异常。第三方面,临床在ECC心脏直视手术术中采用鱼精蛋白中和肝素,对患者正常凝血功能的恢复有帮助。但应用肝素和鱼精蛋白本身有损害血小板功能、引起血小板减少的可能,也会因抗凝作用而增加术后出血的概率。第四方面,血库提供的是非新鲜血液,血液来自不同的献血者,存在免疫差异[8]。ECC心脏直视手术患者输入大量库血,可能造成不同程度的输血反应,加重了其术后出血的风险。
引发活动性出血的原因包括:ECC心脏直视手术中,如心脏大血管切口缝合不当,则可导致活动性出血;术中胸骨后与粘连心包的分离可导致术后广泛渗血。如果ECC心脏直视术后出血或渗血较多,则可引起低血容量性休克、心脏压塞、低心排血量综合征、急性肾功能衰竭、严重心律失常等并发症,也可导致肺不张或呼吸窘迫综合征。对这类患者如处理不当,轻者会延长住院时间,重者则将危及生命安全。一般程度的弥漫性出血临床使用止血药物等综合治疗,可以获得良好的效果。如出现内脏、血管破损后导致的活动性出血,符合手术指征的需紧急实施二次开胸止血手术[9-11]。
随着胸腔镜心脏手术的逐渐普及,心脏手术快速发展为微创、小切口及创伤小的手术。但心脏手术术中仍存在出血量大影响手术视野、止血困难等临床难题。
资料[12]报道ECC心脏直视术后患者中约1.61%(10/620)因出血需再次行开胸手术。一般认为,成人ECC心脏直视手术患者如出现如下情况,均应再次开胸止血[13-15]。①纵膈、心包和/或胸腔引流量>4mL/[(kg•h)]或>2mL/(kg•h),持续4-6h以上、无减少趋势;排出鱼精蛋白不足;应用止血药物无效。②临床高度怀疑存在活动性出血:从引流管流出大量鲜红色血液,经临床评判为非心包腔内积聚所致。引流量每小时>4mL/kg且持续≥3h,颜色由淡红、暗红转为鲜红色,逐渐加深,经充分输血补液后血压仍不稳定。③紧急胸片检查结果提示一侧或双侧胸腔大量积液或纵膈明显增宽。④急性心脏压塞的先兆或症状。ECC心脏直视术后因出血而再次开胸手术中如进行大量输血或代血浆治疗,可能引起凝血功能紊乱、肺栓塞或呼吸功能不全等[16-17]。总之,ECC心脏直视手术术后出血、再次开胸手术对患者的预后都十分不利。体外循环心脏手术术后出血水平与预后不良和死亡率明显相关[18]。所以ECC心脏直视手术关胸阶段的止血处理至关重要。术中止血和防范术后出血均十分重要,其关系到手术的成功率。
近年来,通过对止血通路及止血材料的深入研究,越来越多的医用可吸收止血材料被应用于临床。S-100吸收性止血绫由再生纤维素织物经化学变性而成,其主要成分为羧甲基纤维素钠。相比于明胶海绵,S-100体积小,应用时无需过度压迫(止血),因此一般不会引起血压下降等不良反应。S-100的生物相容性较好。其可通过黏附、封闭、堵塞作用达到快速止血效果。通常心脏手术中,骨膜及骨髓腔的出血难以控制,电凝效果不佳。尤其是骨质疏松的老年病人,其骨髓腔较大,出血较多。S-100具有较强的组织黏附力,可于组织表面形成一层保护层,有效保护并封闭创面,减少渗出。本研究中观察组患者在ECC心脏直视术中应用S-100,对照组未应用。对两组的围术期相关指标比较分析后,结果显示:观察组术后胸腔引流量、重症监护时间较对照组少。这一结果显示,ECC心脏直视术中应用S-100有助于减少手术创面的渗出、降低胸腔引流量,故术后患者恢复快,在重症监护室的停留时间缩短。
已有文献[19-20]报道了ECC心脏直视手术患者因止血不彻底而发生术后出血和心脏压塞等,需再次施行手术。本研究中,观察组患者在ECC心脏直视术中应用S-100进行胸骨断端止血。术中于钢丝拉起时直接将S-100放置于胸骨锯开处行胸骨断端止血。术中在关胸阶段,将S-100卷为长条状填塞于双侧骨髓腔内,通常在30秒内能够有效控制创面渗血,止血效果可靠。
ECC心脏直视手术术后再次开胸,显著增加了患者出现手术切口感染、呼吸道、肾脏和神经系统等方面并发症的风险。术后纵膈感染、胸骨哆开是体外循环心脏直视手术的灾难性并发症,往往会导致多种不良后果产生,如病人死亡、医疗成本增加、住院时间延长等,而医用止血材料的应用是导致其发生的原因之一[21]。术后一旦发生感染,应用抗生素无法直接到达止血材料表面发挥杀菌及抑菌作用,一些止血材料反而成了细菌的温床。常用的止血方法有骨蜡填塞,但骨蜡不被人体吸收。研究[22]发现,在心脏外科手术术中胸骨断面使用骨蜡并不能减少术后出血量,反之可能增加术后胸骨不稳定愈合、愈合延迟的风险。S-100可通过浸泡变为透明凝胶,可最大限度保护手术视野不被遮挡。相比于明胶海绵,S-100体积小,无需压迫,一般不会引起血压下降等不良反应。S-100在体内14-21天则可被完全吸收,并直接降解为水和二氧化碳,相当于被机体完全吸收,无残余成分,可有效避免术后出现纵膈感染等不良事件。有效的止血可降低需大量输血、术后二次开胸手术、纵膈感染等不良事件发生率[23]。本研究对ECC心脏直视术后患者发生术后出血等不良事件情况进行随访观察和比较,结果显示:观察组中1例出现手术创面广泛渗血,对照组为5例。两组中的术后出血患者均接受了再次开胸手术,在术中均未发现明显的出血点,其中,1例观察组患者推测为胸骨的骨质疏松所致术后出血,故在第二次术中应用S-100,并获得了满意的止血效果,术毕评估达到彻底止血。对照组中3例患者推测为止血不彻底,故在第二次术中应用S-100并获得了满意的止血效果,术毕评估达到彻底止血。本研究如上述结果显示,ECC心脏直视术中应用S-100对于彻底止血是有效且安全的。
ECC心脏直视手术止血难度大,极具挑战性。在ECC心脏直视手术中实施有效的血液保护,对患者预后具有重要意义。S-100作为医用可吸收止血材料中的一员,具有生物相容性良好、吸附性强、止血迅速且持久、体积小、可塑形性强、可完全降解等独特优势。应用S-100能良好地解决ECC心脏直视手术的出血问题,具有临床应用推广的可行性。此外,笔者对实施ECC心脏直视手术操作有如下几个方面的建议。如:手术医生根据患者家庭情况和意愿,尽可能为其选择适合的体外循环机、变温水箱,生物相容性佳、预充量小的膜式氧合器等设备。尽可能安排有经验的手术医生,确保术中精准化操作、降低手术操作意外所致出血的风险;尽量缩短手术时间及体外循环时间;通过手术医生的手术经验和技巧,尽量规避常见的注意事项,如术中止血须彻底、停机前复温须到位等问题;有条件尽可能为患者施行术中及术后自体血回输;尽可能为患者使用进口膜肺,以保护血小板,减少血液有形成分的破坏。
综上所述,ECC心脏直视手术术中止血及时应用S-100吸收性止血绫,对于彻底止血、避免出血量过多及提升患者的预后水平非常重要。S-100在ECC心脏直视手术中有其独特的应用价值。

