胃苏颗粒联合四联法治疗Hp阳性慢性萎缩性胃炎患者的疗效
郑秀金,陈长旦,张炜
(宁德师范学院附属宁德市医院消化内科,福建 宁德 352100)
慢性萎缩性胃炎(chronic atrophicgastritis,CAG)是一种常见的消化系统疾病,其主要特征为黏膜腺体萎缩、破坏和不典型增生[1],已被临床证实为胃癌癌前疾病[2]。临床中以根除幽门螺旋杆菌(helicobacter pylori,Hp)、改善胃肠蠕动以及抑酸治疗为主,但受抗生素耐药性、饮食约束等因素影响,西医治疗效果普遍不理想[3]。近年来,Hp(+)CAG的发病率逐渐增长,且呈年轻化趋势[4],提高Hp(+)CAG治疗疗效十分重要。随着中医药学发展,中医对胃肠疾病的治疗逐渐得到重视。中医认为CAG属“胃脘痛”“嘈杂”范畴,因饮食痰积、气机壅滞导致,应给予和胃止痛、消胀理气治疗[5-6]。胃苏颗粒由紫苏梗、陈皮、香附等中药制成,可有效健脾和胃、化痰消肿[7]。目前临床中虽存在中药辅助治疗Hp(+)CAG的相关研究,但如何进一步提高CAG治疗疗效仍是临床研究热点。本研究拟探讨胃苏颗粒联合四联法治疗对Hp(+)CAG患者机体炎症、胃肠功能及血清缺氧诱导因子1α(hypoxia inducible factor 1 α,HIF-1α)、降钙素基因相关肽(calcitonin gene related peptide,CGRP)的影响。
1 资料与方法
1.1 一般资料
选取2021年1月至2022年12月宁德师范学院附属宁德市医院收治的119例Hp(+)CAG患者作为研究对象。根据治疗方法不同分为观察组(n=58)与对照组(n=61)。纳入标准:(1)符合CAG的诊断标准[8],结合患者体征、症状、消化内镜以及病理组织检查确诊;(2)具有Hp感染;(3)无过敏反应;(4)具备一定的理解能力,可正常沟通;(5)自愿参与本研究。排除标准:(1)合并有其他消化道系统疾病或其他器质性疾病;(2)合并有心脏疾病、肝肾功能疾病、恶性肿瘤或精神疾病;(3)入组前一个月进行过其他相关治疗;(4)不配合治疗者;(5)合并重度肠上皮化生或不典型增生,怀疑癌变者。本研究经医院伦理委员会审批通过。两组患者一般资料比较,差异均无统计学意义(P>0.05)。见表1。
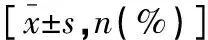
表1 两组患者一般资料的比较
1.2 方法
(1)对照组:采用四联法治疗。给予口服阿莫西林克拉维酸钾分散片(7∶1)(盛西凯)(陕西恒诚制药有限公司),2片/次、3次/d;艾司奥美拉唑镁肠溶片(石药集团欧意药业有限公司),20 mg/次、2次/d;克拉霉素分散片(宁夏启元国药有限公司)500 mg/次、2次/d;枸橼酸铋钾胶囊(济南恒基制药有限公司)300 mg/次、4次/d,于三餐前0.5 h及睡前口服。持续治疗10 d。(2)观察组:采用胃苏颗粒联合四联法治疗。四联法方案同对照组,同时给予胃苏颗粒扬子江药业集团江苏制药股份有限公司)口服治疗,15 g/次,3次/d。持续治疗10 d。
1.3 观察指标
1.3.1 胃粘膜病理严重程度评估 治疗前后对所有患者进行胃镜检查,根据炎症、肠上皮化生、腺体萎缩、病变活动度4个方面评估疾病进展。每项分值均为0~3分,表示无、轻度、中度及重度。最终得分越高,患者疾病越严重。
1.3.2 血清指标 治疗前后,采集所有患者晨起外周静脉血3.0~5.0 mL,离心、取上层清液处理,再利用生化分析仪检测血气中炎症指标白细胞介素32(IL-32)、白细胞介素6(IL-6)、HIF-1α、CGRP、胃蛋白酶原Ⅰ(pepsiongen Ⅰ,PGⅠ)及PGⅡ表达水平。
1.3.3 不良反应 观察记录两组患者治疗后不良反应的发生情况,并计算总发生率。
1.3.4 C-UBT 对患者行尿素呼吸试验(urea breath test,C-UBT)检查,C-UBT检查步骤:采用集气袋收集第1次气体(维持正常呼吸后屏住呼吸10 s,将末段气体吹进袋内):后马上服用尿素13C试剂,后应保持静坐,禁食,禁烟等待30 min;收集第2次气体(方法同第1次),采用尿素呼气试验检测仪(江苏德朗电子设备有限公司)检测。
1.4 统计学分析
2 结果
2.1 两组胃粘膜病理评分比较
治疗前,两组胃粘膜病变活动度、炎症、腺体萎缩、肠上皮化生评分比较,差异均无统计学意义(P>0.05)。治疗后,两组胃粘膜病理指标得分均降低,且观察组低于对照组,差异有统计学意义(P<0.05)。见表2。
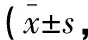
表2 两组胃粘膜病理评分比较分)
2.2 两组机体炎症水平比较
治疗前,两组患者的IL-32、IL-6浓度比较,差异均无统计学意义(P>0.05)。治疗后,两组血清IL-32、IL-6水平均降低,且观察组低于对照组,差异有统计学意义(P<0.05)。见表3。
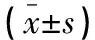
表3 两组患者血清炎症指标水平比较
2.3 两组血清HIF-1α、CGRP以及PGⅠ/PGⅡ水平比较
治疗前,两组HIF-1α、CGRP、PGⅠ及PGⅡ均无统计学差异(P>0.05)。治疗后,两组HIF-1α、PGⅡ均下降,且观察组低于对照组;PGⅠ、CGRP均升高,且观察组高于对照组,差异有统计学意义(P<0.05)。见表4。
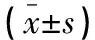
表4 两组治疗前后HIF-1α、CGRP以及PGⅠ/PGⅡ水平比较
2.4 两组不良反应发生情况比较
观察组不良反应总发生率为18.97%,对照组为14.75%,差异无统计学意义(P>0.05)。见表5。
2.5 两组Hp清除率比较
观察组Hp清除率为96.55%(56/58),对照组为83.61%(51/61)。观察组高于对照组,差异具有统计学意义(t=5.495,P<0.05)。
3 讨论
Hp(+)CAG患者胃粘膜上皮受到反复损伤,固有腺体数量减少,因此病程易于迁延,难以治愈[9]。患者可能存在胃部胀满不适,胃出血,胃溃疡,贫血及心理障碍等症状,严重影响其生活质量。虽然采用促进胃肠动力的药物和抗生素,可以改善胃肠道蠕动,但该治疗方案易出现复发和耐药性等问题[10]。因此,本研究引入胃苏颗粒和四联法联合治疗方案,旨在探索更为有效的Hp(+)CAG治疗方案。
本研究显示,两组患者治疗后胃粘膜病变活动度、肠上皮化生以及腺体萎缩均较治疗前改善,且观察组改善程度大于对照组。由此可见,胃苏颗粒辅助治疗可进一步改善Hp(+)CAG患者的机体功能。分析其原因可能是因为胃苏颗粒的主要成分为紫苏梗、香橼、香附、陈皮、佛手、枳壳、槟榔以及炒鸡内金[11],其中紫苏梗归肺、脾经,性温,属于理气药,可理气宽中、止痛;香橼舒肝理气、宽中化痰,现代医学发现香橼挥发油(香叶醛、柠檬烯等)对胃肠道有温和刺激作用,促进胃肠蠕动和消化液分泌,排除积气[12];香附行气化湿、活血化瘀,陈皮理气开胃,燥湿化痰,可治脾胃病,调节消化系统功能;佛手、枳壳合用可疏肝理气、和胃止痛,槟榔降气行滞、行水化湿,炒鸡内金消食化积,健运脾胃,以上诸多药材共奏和胃理气之效。此外,阿莫西林克拉维酸钾、枸橼酸铋钾胶囊、克拉霉素分散片等为CAG的常用治疗药物,如阿莫西林克拉维酸钾有效抑制Hp的生长,有助于抑制炎症;艾司奥美拉唑镁肠溶片可以调节肠道功能,缓解恶心、消化不良等症状,同时也可以抑制Hp繁殖[13]。因而中西医联合治疗可从不同层面改善Hp(+)CAG疾病症状,有效促进患者胃肠功能恢复。本研究还显示,观察组治疗后外周血炎症因子IL-32、IL-6均低于对照组,提示联合方案对Hp(+)CAG患者机体炎症改善作用更为显著。炎症因子参与胃粘膜内皮细胞损伤过程,对于慢性炎症性疾病而言,血清炎症因子表达水平与其疾病进展相关。联合方案对Hp(+)CAG患者炎症水平的改善,可能与该组患者胃肠功能修复、免疫功能增强有关。
本研究中,观察组HIF-1α较对照组降低,同时CGRP水平较后者显著升高。HIF-1α属于促血管生成因子,可通过编码血管内皮生长因子(vascular endothelial growth factor,VEGF)基因而刺激机体VEGF表达,可刺激血管新生、增加血管通透性。王坤等[14]表示,HIF-1α在胃癌患者中高度表达,且其血清浓度与CAG病变进展相关。同时,CGRP是一种小分子肽脂蛋白,可以发挥微血管扩张和保护血管的作用,调节血压、排钠元素、抗炎作用、促进新陈代谢和减少氧化应激,并减少心脑血管病发作发作及发展。CGRP可作为舒血管活性肽以介导一氧化碳、前列腺素合成分泌,同时还能调节胃肠激素和胃酸的分泌,保护胃粘膜[15]。胃苏颗粒联合四联法可显著促进Hp(+)CAG患者胃肠功能改善,这可能与香橼、陈皮和炒鸡内金等可调节胃肠功能的药物作用有关。本研究还显示,观察组治疗后PGⅠ高于对照组、PGⅡ低于对照组。PGⅠ、PGⅡ具备多种生理功能,可帮助身体维持正常的胃酸分泌水平、保护胃黏膜免受粘液内细菌的侵害,以及保护胃壁免受消化液的腐蚀。同时还能增强消化系统的免疫反应,促进消化和吸收营养物质,联合方案对消化系统功能的改善作用可见一斑。此外,本研究还表明,两组患者的不良反应发生率无明显差异,且均为轻微症状,在得到及时救治后均缓解,两种治疗方案的安全性均较高。同时观察组治疗后Hp转阴率高于对照组,这可能与机体免疫功能增强有关。
综上,胃苏颗粒联合四联法可有效改善Hp(+)CAG患者临床症状,下调血清HIF-1α、CGRP及炎症因子表达,有利于提高Hp转阴率,改善患者预后。

