STAT3 调控炎症因子分泌抑制脑梗死细胞凋亡机制研究
贾丹丹 陈蓉 马琳 李其富
脑梗死是一种严重的脑缺氧缺血性组织坏死疾病,它源于脑血管的堵塞,致使大脑遭受严重的氧气供应不足[1]。各种疾病(如高血压、糖尿病等)和不健康的生活习惯(如吸烟等)都可能导致脑梗死。神经元细胞死亡过程中,凋亡相关因子BCL2-Associated X蛋白(BCL2-Associated X,Bax)[2]和B 细胞淋巴瘤-2(B-cell lymphoma-2,Bcl-2)[3]的作用至关重要,它们会加速脑梗死的进程。多种炎症因子在急性脑梗死患者的血清中表达上调,其在脑梗死的诊断和治疗中具有重要的价值[4]。炎症因子及其激动剂或拮抗剂可能在脑梗死的调节中发挥重要作用。
核苷酸结合NOD 样受体热蛋白结构域相关蛋白3(NLR family pyrin domain containing 3,NLRP3)在调控人癌细胞的增殖、分化、侵袭和迁移等各种生物学过程起调控作用。胃癌相关成纤维细胞分泌的白细胞介素-6(Interleukin-6,IL-6)[5]通过信号转导及转录激活蛋白3(Signal transducer and activator of transcription 3,STAT3)促进胃癌上皮-间质转化和转移[6]。STAT3还可以抑制肺癌细胞增殖,促进细胞凋亡。此外,JAK/STAT 通路在缺血性脑卒中诱导的炎症性神经元损伤中起着重要的调控作用[7]。本研究将重点研究STAT3在脑梗死中的功能和作用机制。
1 材料与方法
1.1 主要材料
1.1.1 实验动物
类型为C57BL/6 的雄性小鼠,6~8 周,体重范围为28~30 g;6~8 周雄性SD 大鼠,体重范围为260~300 g。动物来源及饲养于SPF 级中国科学院动物中心,并获得海南医学院第一附属医院动物伦理批准。
1.1.2 实验试剂
胎牛血清、酶联免疫吸附测定(Enzyme linked immunosorbent assay,ELISA)及Tunel 凋亡检测试剂盒(美国Sigma公司);RNase-free DNase I、青霉素/链霉素混合液、RIPA 蛋白裂解液、苯甲基磺酰氟(PMSF)(凯基生物公司);RNeasy Mini 试剂盒(天根生化科技公司);RPMI-1640 培养基、B-27 培养基(康宁生物公司);0.05%胰蛋白酶(Gibco 公司);Trizol、SYBR Green qPCR Master 混合液、BCA 蛋白定量试剂盒(TAKARA 公司);Pierce™蛋白酶和磷酸酶抑制剂(赛默飞世尔中国公司);Bax、Bcl2、NLRP3 和GAPDH 抗体(武汉爱博泰克公司);AAV9 腺相关病毒及慢病毒(汉恒生物公司)。
1.2 方法
1.2.1 小鼠脑梗死模型(middle cerebral artery occlusion,MCAO)构建
10%水合氯醛以3.5 mL/kg 腹腔注射麻醉小鼠。用碘溶液清洗皮肤,使用手术剪剪开颈中部,找到颈总动脉和颈外动脉,用缝合线结扎,血管钳夹住颈内动脉。然后切开颈总动脉,插入金属丝塞后缝合,然后结扎。2 h 后再灌注。小鼠麻醉恢复后,站立不稳、出现左侧偏瘫等症状说明脑梗死模型构建成功。假手术组小鼠除结扎操作外,其余操作均进行。小鼠造模成功后麻醉处死,取脑标本作进一步分析。
1.2.2 神经元细胞培养和氧-葡萄糖剥夺模型(oxygenglucose deprivation,OGD)构建
新生3 d 大鼠麻醉后处死,将海马或皮质组织切开,用0.05%胰蛋白酶消化30 min。离心后,用含5%胎牛血清的DMEM 培养基重悬。以1×106细胞/mL 的密度培养细胞24 h,更换DMEM 培养基成B-27 培养基。5 d 后进行OGD。将OGD组培养基逐渐替换为无糖培养基,葡萄糖浓度低于1 mM,细胞培养在含95% N2和5% CO2的培养箱中,对照组细胞培养在含5% CO2的培养箱中。4 h 后,所有细胞更换为含5%胎牛血清的DMEM培养基,放回含5%CO2的培养箱中培养。
1.2.3 实验分组及处理
1.2.3.1 动物分组及处理 将40 只C57BL/6 的小鼠随机分为4 组:AAV9-con+Sham 组小鼠脑组织注射107TU/mL AAV9 对照病毒并进行假手术,AAV9-con+MCAO 组小鼠脑组织注射107TU/mL AAV9 对照病毒并进行MCAO 手术,AAV9-sh-STAT3+Sham 组小鼠脑组织注射107TU/mL 的AAV9-sh-STAT3 腺相关病毒并进行假手术,AAV9-sh-STAT3+MCAO 组小鼠脑组织注射107TU/mL 的AAV9-sh-STAT3 腺相关病毒并进行MCAO 手术。
人工智能的大多数应用需要“大数据”支持。在云计算和快速增长的数据量推动下,人工智能已在越来越多的领域得到应用。为执行任务,人工智能要大量地搜集、存储和分析数据。从数据隐私的角度来看,人工智能对数据的大量使用,使得妥善保护数据变得越来越重要。随着人工智能系统越来越多地被整合到基础设施、生产制造、商业运营和日常生活中,在医疗、交通、金融、娱乐、购物、执法等各个领域得到应用,特别是与物联网(IoT)和相关的生物物联网(Bio-IoT)的相互融合,关于个人的基因、面孔、财务、偏好等数据将无处藏匿。无所不在的数据捕获和优化对数据隐私和安全构成了威胁 [6,7] 。
取30 只C57BL/6 小鼠随机分为3 组:Control+MCAO 组小鼠注射对照慢病毒后进行MCAO 手术,AAV9-Sh-STAT3 +MCAO 组小鼠脑组织注射107TU/mL AAV9-Sh-STAT3 腺相关病毒并进行MCAO 手术,AAV9-OE-NLRP3+MCAO 组小鼠脑组织注射107TU/mL AAV9-OE-NLRP3 腺相关病毒并进行MCAO 手术。
1.2.3.2 细胞分组及处理 取生长融合至70%左右的脑神经元细胞随机分为4 组:Scramble 组细胞给予对照慢病毒Scramble 处理48 h,Sh-STAT3 组细胞给予抑制STAT3表达慢病毒处理48 h;Fugw 组细胞给予对照慢病毒Fugw 处理48 h,OE-STAT3组细胞给予过表达STAT3慢病毒处理48 h。
取生长融合至70%左右的脑神经元细胞随机分为4 组:Control+OGD 组细胞给予对照慢病毒处理48 h 后OGD 建模,Sh-STAT3+OGD 组细胞给予抑制STAT3表达慢病毒处理48 h 后OGD 建模,OE-NLRP3+OGD 组细胞给予过表达NLRP3 慢病毒OE-NLRP3处理48 h 后OGD 建模,Sh-STAT3+OE-NLRP3+OGD 组细胞给予抑制STAT3表达慢病毒和过表达NLRP3 慢病毒处理48 h 后OGD 建模。
1.2.4 RNA 提取和实时荧光定量PCR(Real-time Quantitative PCR Detecting System,qPCR)
使用TRIzol 提取总RNA,经RNase-free DNase I 处理后,使用RNeasy Mini Kit 纯化RNA。使用NanoDrop ND-1000 测定RNA 的浓度和纯度,使用Bioanalyzer 2100(Agilent Technologies)测 定RNA 的完整性。使用RT-PCR 试剂盒将mRNA反转录成cDNA。采用SYBR Green qPCR Master试剂盒,用PCR 检测仪进行扩增,以cDNA 为模板。条件:温度95℃,预变性30 s;温度95℃,变性5 min,60℃进行退火,延伸37 s,循环40 个。RTPCR 引物设计为:STAT3上游序列为:5'-GACCCAGGAACAAGGTGA-3',下游序列:5'-GCCAAGGAGAGGGAAAGT-3';NLRP3上游序列为:5'-GACTGGCAAAAGGCTGTG-3',下游序列:5'-AGTTTCTCCAAGGCTACCG-3';内参均为18S,使用2-ΔΔCt进行分析。PCR 引物由上海生工生物工程有限公司合成。
1.2.5 蛋白免疫印迹(Western Blot,WB)
将小鼠大脑或神经元细胞置于苯基甲基磺酰氟缓冲液(PMSF,10 μL/mL 缓冲液)冰上裂解30 min。将溶解后的组织或细胞悬液在4℃下离心5 min(11 000×g),收集上清液。样品电泳转移到聚偏二氟乙烯膜(PVDF)。将封闭后的膜与Bax(兔抗小鼠,1∶1 000)、Bcl2(兔抗小鼠,1∶1 000)、NLRP3(兔抗小鼠,1∶1 000)、GAPDH(兔抗小鼠,1∶5 000)一抗孵育过夜,温度为4℃。随后,TBST 清洗膜并与辣根过氧化物酶结合的二抗孵育。滴加ECL 发光液进行曝光、拍照,使用Image J 软件进行分析。
1.2.6 ELISA
1.2.7 Tunel 染色
使用TUNEL 染色试剂盒进行细胞凋亡检测。37℃蛋白酶K 孵育15 min,PBS 洗涤5 min。然后与酶液和标记液在黑暗中37℃(1∶9)混合孵育60 min。浸泡在标签溶液中的切片作为阴性对照。最后用DAPI 染色10 min。使用荧光显微镜进行拍摄统计。Tunel 阳性核以占每个视野总核的百分比表示。
1.3 统计分析
采用SPSS 25 统计软件进行统计分析,计量资料用()表示,两组间比较采用独立样本t检验。以P<0.05 表示差异具有统计学意义。
2 结果
2.1 STAT3 在大鼠MCAO 模型和细胞OGD 模型中的表达
qPCR 实验结果显示,MCAO 组与假手术组相比,小鼠脑组织中STAT3mRNA 和蛋白表达升高,差异有统计学意义(P<0.05)。见图1A。OGD 组大鼠脑神经元细胞中STAT3mRNA 和蛋白表达同样升高(P<0.05)。见图1B。
2.2 敲低STAT3 后MCAO 小鼠中STAT3、Bax 和Bcl2 的表达
qPCR 检测结果显示,与注射对照AAV9 腺相关病毒行假手术的AAV9-Con+Sham 组小鼠相比,MCAO 组小鼠脑组织中STAT3 表达明显升高,差异有统计学意义(P<0.05),敲低STAT3 AAV9 后其表达降低(P<0.05),再进行MCAO 手术则STAT3表达升高(P<0.05)。见图2A。此外,MCAO 组Bax 蛋白表达升高,Bcl2 蛋白表达明显降低。注射敲低STAT3AAV9 腺相关病毒后,Bax 蛋白表达明显降低,Bcl2 蛋白表达明显升高。见图2B。Tunel 染色结果验证,敲低STAT3能够抑制MCAO 手术诱导的脑组织细胞凋亡。见图2C。
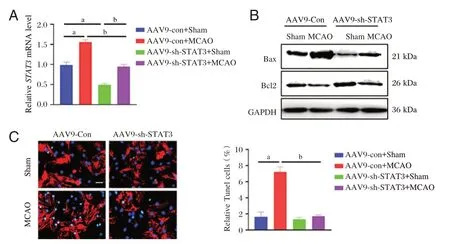
图2 注射敲低STAT3 AAV9 腺相关病毒后进行MCAO诱导的各组小鼠脑组织中STAT3、Bax 及Bcl2 表达以及细胞凋亡情况Figure 2 Expression of STAT3,Bax,and Bcl2,as well as cellular apoptosis in the brain tissue of different groups of mice after injection of AAV9 adenovirus targeting STAT3 followed by MCAO induction
2.3 STAT3 调控下的NLRP3 表达与炎症因子的关联
与转染对照组Scramble 病毒相比,脑神经元细胞转染抑制STAT3表达慢病毒组中NLRP3mRNA 和蛋白表达降低,差异有统计学意义(P<0.05)。见图3A。与转染对照组Fugw 病毒相比,脑神经元细胞转染过表达STAT3慢病毒组中NLRP3mRNA 和蛋白表达升高,差异有统计学意义(P<0.05)。见图3B。此外,动物水平ELISA实验结果显示,敲低STAT3表达降低了MCAO 导致的促炎因子IL-1β 和TNF-α 表达,并促进抗炎因子IL-10β 和TGF-β 表达。然而,敲低NLRP3表达只促进MCAO 引起的促炎因子IL-1β 和TNF-α 表达,对抗炎因子IL-10 和TGF-β 的表达没有影响(P<0.05)。见图3C、3D。
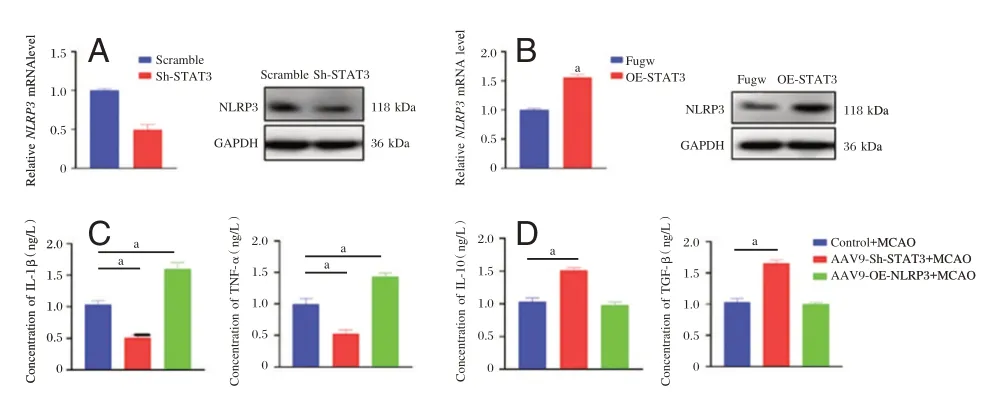
图3 脑神经元细胞转染抑制或过表达STAT3 慢病毒后NLRP3 的mRNA 和蛋白、炎症相关因子表达Figure 3 Expression of NLRP3 mRNA and protein,as well as inflammatory factors,in brain neuronal cells transfected with inhibitory or overexpressing STAT3 lentiviruses
2.4 敲低NLRP3 表达抑制OGD 诱导的脑神经元细胞凋亡
qPCR 结果显示,与OGD 刺激组相比,转染抑制STAT3表达慢病毒后,STAT3和NLRP3的mRNA表达降低,差异有统计学意义(P<0.05),转染过表达NLRP3慢病毒后,STAT3和NLRP3mRNA 表达升高(P<0.05)。见图4A。WB 实验结果显示,OGD 刺激组转染抑制STAT3表达慢病毒后,凋亡相关蛋白Bax 表达降低,Bcl2 表达升高;转染过表达NLRP3慢病毒后,凋亡相关蛋白Bax 表达升高,Bcl2 表达降低。见图4B。同样的,Tunel 染色结果表明,OGD 刺激组转染抑制STAT3表达慢病毒后可抑制细胞凋亡,OGD 刺激组转染过表达NLRP3慢病毒后促进细胞凋亡(P<0.05)。见图4C。
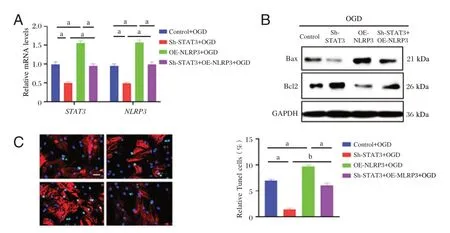
图4 脑神经细胞转染抑制和过表达STAT3 慢病毒后给予OGD后STAT3和NLRP3 mRNA、Bax 和Bcl2 表达及细胞凋亡情况Figure 4 Expression of STAT3 and NLRP3 mRNA,Bax and Bcl2 proteins,as well as cellular apoptosis,in brain neuronal cells transfected with inhibitory or overexpressing STAT3 lentiviruses followed by OGD treatment
3 讨论
NLRP3 是多肽链或蛋白质相互作用的复合物,其激活可以直接导致炎症因子的增多[8]。研究发现,NLRP3 是miRNA 的靶点[9],miRNA 可以通过调控NLRP3 的表达来影响其炎症活性[10]。一些学者曾对STAT 家族中最主要的STAT3通路进行深入研究[11],发现通过抑制JAK2/STAT3通路可以有效减少白细胞中的中性粒细胞等炎症细胞数量的增加[12]。本研究证实,STAT3通过正向调控凋亡小体NLRP3 介导的炎症因子分泌,影响脑梗死组织的细胞凋亡过程。抑制STAT3表达在一定程度上逆转了MCAO 诱导的细胞凋亡作用,过表达NLRP3 可以阻碍抑制STAT3表达对OGD 诱导的神经元细胞凋亡的作用。
Bcl-2 蛋白是抗凋亡分子,其调控机制与细胞凋亡因子的组成密切相关,这些因子包括促凋亡因子Bax[13]和凋亡抑制因子Bcl-xL[14]等。当Bcl-2 的表达水平升高时,它与Bax 结合形成异源二聚体,从而阻碍细胞凋亡的发生[15]。通过提高Bcl-2 的表达水平,细胞可以形成Bcl-2/Bax 复合物,从而抑制Bax 的活性,阻止细胞凋亡的进程。因此,Bcl-2/Bax 的平衡比例对于细胞凋亡的调控至关重要。这一机制在内源性凋亡途径中起着重要的调节作用。本研究表明,抑制STAT3表达的模型小鼠脑组织和神经元细胞表现出抗凋亡作用,同时上调Bcl2 和下调Bax 表达,而敲低STAT3能够抑制MCAO 手术诱导的脑组织细胞凋亡。本实验验证了STAT3在脑梗死中的作用,并提示STAT3可通过调控Bcl2 和Bax 发挥调控神经元细胞凋亡的潜在机制。
炎症因子在人原发性黑色素瘤细胞系中具有剂量依赖性,抗炎因子的分泌具有抗凋亡作用[16]。STAT3可调控炎症小体NLRP3 介导的炎症因子分泌,在炎症过程和疾病的发病过程中发挥重要作用。NLRP3 炎症小体与IL-1β 相似,是炎症反应的重要启动子,也是炎症反应的核心介质。有报道称激活的NLRP3 炎症小体在维持肠黏膜稳态中至关重要,结肠炎小鼠结肠中NLRP3 炎症小体激活量最高,血清IL-1β 水平最高[17]。STAT3的激活还受多种生长因子和细胞因子的调控,例如,STAT3的酪氨酸磷酸化可受p53 抑制和IL-4 以及janus 酶的诱导[18]。本研究发现,敲低STAT3表达降低了MCAO 导致的促炎因子IL-1β 和TNF-α 的表达,并促进抗炎因子IL-10β 和TGF-β 表达。结果表明NLRP3 炎症小体介导的炎症因子分泌在脑梗死中发挥重要的调控作用,提示NLRP3 可以作为防治脑梗死发生的重要干预靶点。
综上所述,本文通过对小鼠脑梗死模型和体外分离培养的神经元细胞进行检测,发现凋亡相关蛋白Bax 和Bcl2 的表达以及细胞凋亡率变化,表明抑制STAT3表达对模型小鼠脑组织和神经元细胞凋亡有抑制作用。STAT3通过调控NLRP3 介导的炎症因子分泌来抑制脑梗死组织细胞凋亡,进而抑制脑梗死的发生。

