利用铝灰和微硅粉制备4A分子筛的研究
欧玉静,彭 莉,李春雷,赵海涛,苏鹏程,高 鹏
(1.兰州理工大学 石油化工学院,兰州 730050;2.中国水利水电第六工程局有限公司,沈阳 110000)
铝灰是铸造铝过程中形成的残渣,主要含有铝(Al)、氧化铝(Al2O3)、氮化铝(AlN)、其他金属氧化物及无机盐等物质[1],氮化铝遇水受潮释放出氨气、氟化盐渗入土壤致使氟浓度超标、无机盐使得土壤盐碱化等问题会造成对环境的严重危害;微硅粉是硅铁合金和金属硅冶炼过程中,硅热电炉中产生的硅气体与空气中的氧气结合形成的一种球形粉尘,该粉尘中含有大量的二氧化硅(SiO2)和少量的碳(C),微硅粉质量轻,颗粒细小,排入空气会危及人体健康。目前,铝灰和微硅粉的处理方式主要为堆积或填埋[2-3],这种方法不仅会造成有价物质的浪费,也会对环境造成严重的危害。
4A分子筛是一种硅铝酸盐,化学式为Na2Al2Si2O8·4.5H2O,其晶型为铝氧四面体和硅氧四面体交错排列而成[4-5],具有晶体的结构和特征。4A分子筛具有独特的吸附、催化和离子交换作用[6-7],广泛应用于气体、液体的干燥、洗涤助剂、污水处理[8-10],特别是在洗涤助剂的制造方面。常用的洗涤助剂为三聚磷酸钠(STPP),但存在水质富营养化等问题,因此用4A分子筛代替STPP,可以实现洗涤剂的无磷化。本文以铝灰和微硅粉为原料,制备出高性能的4A分子筛,探究硅铝比(n(SiO2)/n(Al2O3))、碱度(n(Na2O)/n(Al2O3))、晶化温度、晶化时间对4A分子筛性能的影响,为实现铝灰和微硅粉的高值化、资源化利用提供新的方向。
1 实 验
1.1 原料与试剂
铝灰来源于中国铝业兰州分公司,微硅粉来源于嘉峪关大友铁合金有限公司,其余试剂均为分析纯。
1.2 材料制备
1.2.1 制备铝酸钠溶液
称取30.00 g铝灰于三口烧瓶中,缓慢加入150.00 g水,在40 ℃下水洗2 h,过滤烘干后得到28.80 g脱盐铝灰。称取脱盐铝灰4.80 g,加入2倍质量的碱,混合均匀置于马弗炉,以5 ℃/min的升温速率在600 ℃下焙烧120 min,得到铝酸钠熟料。将得到的铝酸钠熟料用水溶出,溶出条件为液固比4∶1,温度60 ℃,时间30 min,随后用EDTA滴定法滴定铝酸钠溶液中氧化铝的含量。
1.2.2 制备硅酸钠溶液
称取5.00 g微硅粉,加入2倍质量的碱,混合均匀后置于高温箱式炉中,以5 ℃/min的升温速率在650 ℃下焙烧240 min,得到硅酸钠熟料。将得到的硅酸钠熟料用水溶出,溶出条件为液固比5∶1,温度60 ℃,时间30 min,用分光光度法测定硅酸钠溶液中氧化硅的含量。
1.2.3 制备4A分子筛
将上述铝酸钠溶液和硅酸钠溶液按一定比例混合,并不断搅拌,会产生白色的凝胶,将凝胶转入反应釜中,在100 ℃下晶化8 h,过滤,烘干得到白色粉末,即为4A分子筛。实验的工艺流程示意图如图1所示。

图1 工艺流程示意图
1.3 材料表征及钙离子交换量的测定
采用X射线荧光光谱仪(XRF,XRF1800,岛津,日本)分析铝灰和微硅粉的主要元素及含量;采用元素分析仪(EA,FLASH EA 1112,THERMO,美国)测定微硅粉中C元素的含量;采用X射线衍射仪(XRD,D/max-2400,RIGAKU,日本)对铝灰、微硅粉及产物的主要物相和晶型结构进行分析;采用冷场发射扫描电子显微镜(SEM,MIRA3,TESCAN,捷克)观察铝灰、微硅粉和产物的形貌;采用傅里叶红外光谱仪(FTIR,NEXUIS-470,Nicolet Co,美国)测定产物分子骨架;采用比表面积分析仪(BET,Autosorb-iQ,美国)进行产品孔结构等信息测试;采用电感耦合等离子体原子发射光谱(ICP-OES,730/720,安捷伦,美国)测定溶液元素含量;采用QB/T 1768-2003中所述方法测定产物的钙离子交换能力,测定过程中的化学反应方程式为
Na2Al2Si2O8+CaCl2=CaAl2Si2O8+2NaCl
计算公式为
(1)
式中:E为钙离子交换能力,mg CaCO3/g;cE为EDTA标准滴定溶液的浓度,mol/L;V0为空白滴定中消耗的EDTA标准溶液的体积,mL;VE为试样滴定中消耗的EDTA标准溶液的体积,mL;m为4A分子筛的质量,g;X为灼烧失量,%;100.08为碳酸钙的毫摩尔质量,mg/mmol。
灼烧失量X以质量百分数表示,计算公式为
(2)
式中:m0为灼烧前试样质量,g;m1为灼烧前试样质量,g。
2 结果与讨论
2.1 铝灰成分分析
从表1可以看出,铝灰中主要含有Al、O、Mg、Na、Cl等元素,相对质量分数分别为38.52%、26.62%、13.71%、9.68%、4.26%,并含有少量的K、F、Ca、Si、Fe等元素。
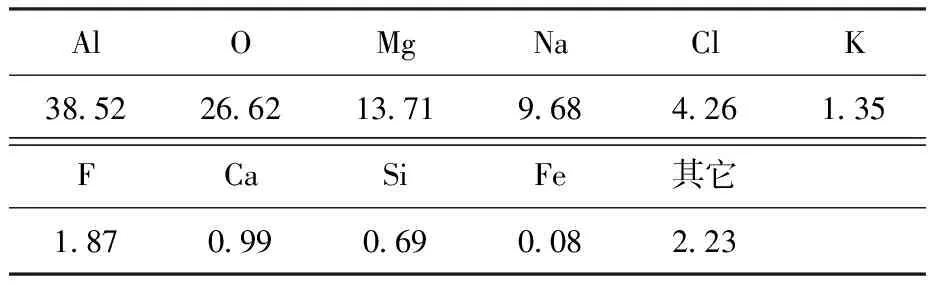
表1 铝灰元素组成及含量(质量分数/%)
铝灰的物相组成及晶型结构分析如图2所示。从图2可以看出,位于27.366°、31.703°、45.448°、76.548°、84.923°的衍射峰为NaCl的特征峰,28.345°、40.507°、50.169°的衍射峰为KCl的特征峰;位于19.007°、36.861°、59.926°的衍射峰为MgAl2O4的特征峰,36.916°、59.926°、65.369°的衍射峰为Mg2(SiO4)的特征峰;位于25.566°、35.136°、38.243°、43.336°、57.638°的衍射峰为Al2O3的特征峰,铝灰中主要物相为Al2O3、NaCl及其他金属氧化物,成分较为复杂。这是因为实验中所用的铝灰为铝-镁-硅系列铝合金产生的铸造铝灰,因此会存在MgAl2O4、Mg2(SiO4)物相,且在电解过程中通常会加入少量的无机盐作为助熔剂,因此会存在NaCl、KCl物相。

图2 铝灰的XRD谱图
铝灰的SEM图及元素面扫如图3所示。从图3可以看出,铝灰主要由块状、片层状及小颗粒物质组成,团聚现象严重。结合微区面扫(图3)可知,块状物和片层状物质主要为Al、O、Mg元素,小颗粒物质为Cl、Na、K元素,结合XRD分析可知,块状物质和片层状物质为Al2O3、MgAl2O4、和Mg2(SiO4)的覆合物,小颗粒物质为NaCl、KCl,这是因为在高温铸造的过程中,金属物质会以熔融态的形式存在,会夹杂包覆其他物质,形成Al2O3、MgAl2O4、和Mg2(SiO4)的覆合物。

图3 铝灰的SEM及面扫描图
2.2 微硅粉成分分析
微硅粉的元素组成及相对含量如表2所示。由表2可知,微硅粉中主要为硅元素,由于在金属硅和硅铁冶炼过程中会加入大量的焦炭用作还原剂[11],因此微硅粉中会含有部分游离碳,含量为1%~4%,除此之外,还含有少量K2O、CaO、Fe2O3、Na2O、MgCl2等杂质。通常,微硅粉的颜色为灰白色,但由于C的存在,微硅粉呈褐色或深灰色。
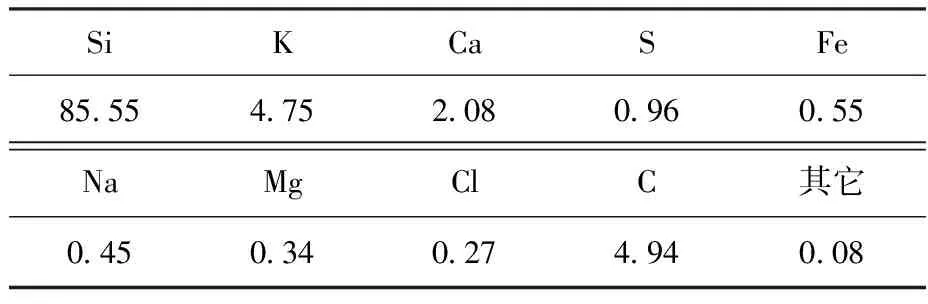
表2 微硅粉的元素及其含量(质量分数/%)
微硅粉的物相组成如图4所示。从图4可以看出,微硅粉的X衍射谱图为典型的玻璃态特征弥散峰,在衍射角2θ=20°~30°处有明显的特征弥散峰,说明微硅粉中的SiO2主要以非结晶相(无定形)存在。这是因为微硅粉在冷凝的过程中,冷却速度极快,且受到表面张力的作用,SiO2来不及形成晶体结构,因此呈现非结晶相结构。
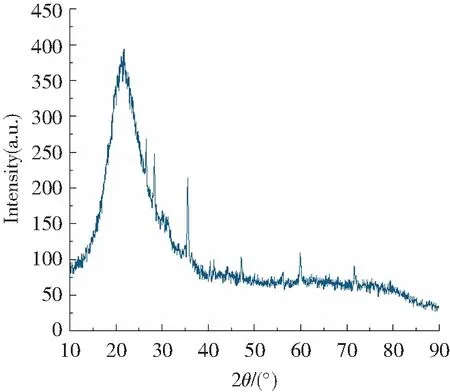
图4 硅粉的XRD谱图
微硅粉的微观形貌如图5所示。从图5(a)、(b)可以看出微硅粉为大小不一的类球形颗粒,颗粒表面光滑,粒径主要分布在0.1~0.3 μm之间,大颗粒占到80%,这是由于微硅粉在冷凝时,在从气相到固相的过程中受到表面张力作用。同时还可以看到类球状颗粒表面有一些絮状物,是由较细的微硅粉颗粒团聚而成附着在大颗粒表面形成疏松多孔结构,微硅粉的这种团聚特性在宏观上表现出密度低、易吸水、具有吸附性等特征。

图5 微硅粉的SEM图(a)和TEM图(b)
2.3 参数对钙离子交换量的影响
为了确定制备前驱体铝酸钠溶液和硅酸钠溶液中铝和硅的含量,对溶液中的铝、硅、钠元素进行ICP-OES测试,测试结果如表3所示。
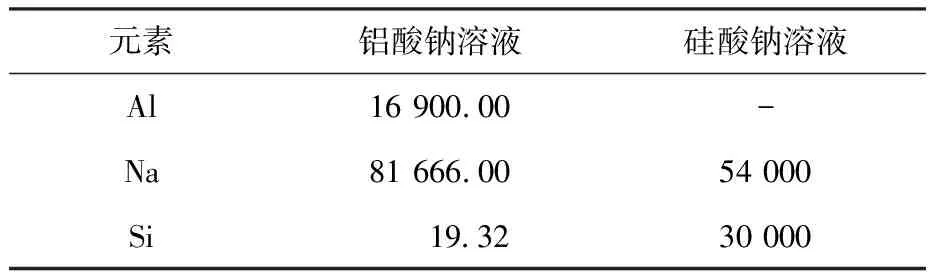
表3 溶液中的元素含量表
2.3.1 硅铝比的影响
硅铝比实验固定碱度为2.5,晶化温度100 ℃,晶化时间10 h,改变反应硅铝比1.6、1.8、2.0、2.2、2.4,制备产物的钙离子交换量和XRD谱图如图6所示。

图6 不同硅铝比的4A分子筛的钙离子交换量(a)和XRD谱图(b)
由图6(a)可知,4A分子筛的钙离子交换量随着硅铝比的增大而增大,在比值为2.0时达到最大,这是因为4A分子筛晶体是在较低的硅铝比体系中形成的,硅铝比的增大有利于硅铝凝胶的解聚并形成晶核,使得成核速率高于晶体生长速率[12],此时体系中为4A分子筛的晶体,钙离子交换量达到最大。当硅铝比大于2.0时,晶体生长速率大于成核速率,晶体长大,4A分子筛会转变为X型分子筛,导致钙离子交换量有所下降。从图6(b)中也可以看出,硅铝比较小时,结晶度小,晶型不完整,此时钙离子交换量低,随着硅铝比的增加,晶型逐渐完整,钙离子交换量随即增大,当硅铝比增加到2.0以后,除了4A分子筛的晶体还出现了X型分子筛的晶体,晶型发生了改变。因此,为保证良好的钙离子交换量,应使硅铝比为2.0。
2.3.2 碱度的影响
碱度实验固定硅铝比为2.0,晶化温度100 ℃,晶化时间10 h,改变反应碱度为2.4、2.5、2.6、2.7、2.8,制备产物的钙离子交换量和XRD谱图如图7所示。

图7 不同碱度的4A分子筛的钙离子交换量(a)和XRD谱图(b)
由7(a)可知,当碱度小于2.5时,随着碱度的增加钙离子交换量增加;当碱度大于2.5时,随着碱度的增加钙离子交换量降低。这是因为4A分子筛的晶化过程需要在强碱条件下进行,在反应初期体系中的碱度较大,在OH-离子的作用下,NaAlO2和Na2SiO3逐步形成铝氧四面体[AlO4]和硅氧四面体[SiO4],并通过氧桥联结成初级结构单元,Na+以水合阳离子形式与骨架结合以保证电中性,随后成核并长大。当碱度过低时,成核速率较慢,结晶速率也慢,反应不彻底,且较容易生成八面沸石分子筛[13],所以在一定范围内增加碱度能提高分子筛的结晶速度,使产物具有较高的钙离子交换量;如果碱度过大,硅铝凝胶中阴离子集团的溶解速度会加快,4A分子筛晶相会转变为羟基方钠石(Na8[Al6Si6O25]·H2O)[14],而羟基方钠石晶体在碱度较高的环境中更稳定,从图7(b)中也可以看出随着碱度的增大,出现了杂峰,即为羟基方钠石峰,所以在碱度大于2.5以后,4A分子筛的钙离子交换量会降低,因此应选择碱度为2.5。
2.3.3 晶化温度的影响
晶化温度实验固定硅铝比为2.0,碱度为2.5,晶化时间10 h,改变反应晶化温度为80、90、100、110、120 ℃,制备产物的钙离子交换量和XRD谱图如图8所示。

图8 不同晶化温度的4A分子筛的钙离子交换量(a)和XRD谱图(b)
在温度升高的过程中,无定形凝胶会溶解形成硅酸根水合离子和铝酸根水合离子,在碱性环境的催化下形成硅铝酸钠阴离子骨架,最终凝结成核形成4A分子筛。从图8(a)可知,当晶化温度低于100 ℃时,钙离子交换能力较低,说明当温度较低时,体系中的硅铝凝胶未能凝结成核,导致晶化过程太慢;当温度为100 ℃时,钙离子交换能力360 mg CaCO3/g,说明体系中的硅铝凝胶完全晶化,形成4A分子筛;当温度高于100 ℃时,钙离子交换能力有所下降,此时,晶化速度过快,导致4A分子筛的晶型发生变化或生成杂晶[15],因此,最佳晶化温度为100 ℃。
2.3.4 晶化时间的影响
晶化时间实验固定硅铝比为2.0,碱度为2.5,晶化温度100 ℃,改变反应晶化时间为8、9、10、11、12 h,制备产物的钙离子交换量和XRD谱图如图9所示。
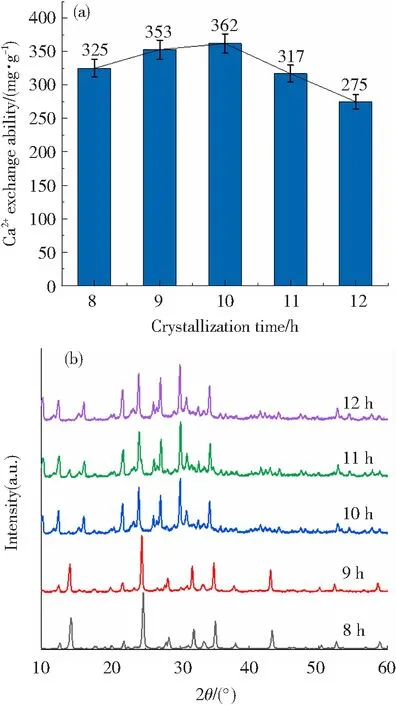
图9 不同晶化时间的4A分子筛的钙离子交换量(a)和XRD谱图(b)
从图9(a)可知,随着晶化时间的延长,4A分子筛的钙离子交换能力逐渐增大,这是因为在晶化初期,由于晶化不足,晶粒小,钙离子交换能力低,随着时间的延长,晶粒逐渐长大成为4A分子筛晶体,在此过程中钙离子交换能力随之增大,在10 h时达到最大。当10 h以后,钙离子交换能力会下降,原因是当4A分子筛晶体形成后会处于一种亚稳态[16],此时溶液仍为碱性,碱性溶液会促使4A分子筛晶体向稳定态转变,即晶体间相互集结。从图10(a)、(b)、(c)中可以看出,在晶化时间为8、9、10 h的条件下,4A分子筛颗粒多为立方晶型,大小较为规整,没有明显的堆叠,当晶化时间大于10 h后(图10(d)、(e)),分子筛颗粒发生了明显的堆叠,且有较多粒径小的圆球状颗粒产生,说明晶化时间过长容易引起晶体的堆叠及转晶,因此最佳晶化时间应为10 h。

图10 不同晶化时间下4A分子筛的SEM图
2.4 4A分子筛的表征
选取最佳条件,即硅铝比为2.0,碱度为2.5,晶化温度100 ℃,晶化时间10 h,制备4A分子筛并进行表征。由图11(a)可知,在角度2θ=10.2°、12.5°、16.1°、21.6°、23.9°、27.1°、29.9°、34.1°时出现强衍射峰,与洗涤剂用4A分子筛标准卡片PDF#11-590吻合,且没有杂峰出现,说明在最佳条件下制备的4A分子筛晶化程度好,晶化度高。
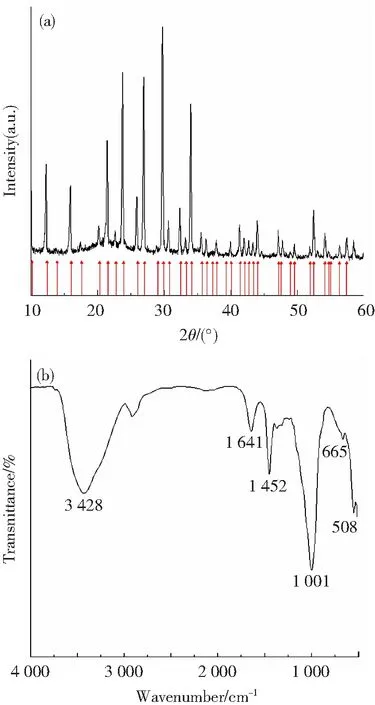
图11 4A分子筛的XRD谱图(a)和FTIR谱图(b)
从图11(b)可以看出,在501 cm-1左右处的吸收峰为Al—O键的弯曲振动峰,665 cm-1处的吸收峰为Si—O键的弯曲振动峰,说明有AlO4四面体和SiO4四面体形成;1 001 cm-1处的吸收峰为Si—O—Si键的不对称伸缩振动峰,表明非对称的Si—O—Si及聚合多面体聚合形成分子筛的骨架结构;1 641 cm-1处的吸收峰为H—O—H键的弯曲振动峰;3 650~3 200 cm-1区域内为—OH的伸缩振动峰,而在3 428 cm-1处有一个较宽的峰,说明产品中含有结合水[17-18]。以上表明所制备的产物符合4A分子筛的骨架特征,为4A分子筛。
图12为最佳工艺制备的4A分子筛的晶体SEM图。从图12可以看出,4A分子筛的晶体颗粒为规整的立方型晶体,晶粒棱角圆滑,大小均一,粒径略小于2 μm,存在部分堆叠。结合图9(a)、图10可知,晶粒堆积会使产品钙离子交换量下降,因此,在制备过程中,应选定合适的晶化时间,避免晶化时间过长使产品性能降低。

图12 4A分子筛晶体SEM图(a)和图(a)中方框位置的放大图(b)
4A分子筛的氮气吸附-脱附等温线如图13所示。从图中可以看出,产品的氮气吸附-脱附等温线为IV型等温线,属于介孔材料,具有一定的吸附性能。从图中还可以看出在P/P0为0.7至1.0范围内吸附曲线与脱附曲线不重合,存在滞后回环。根据IUPIC分类可知,属于H1滞后环,这种滞后环表明产品为接近球状的颗粒,且颗粒均匀分布。
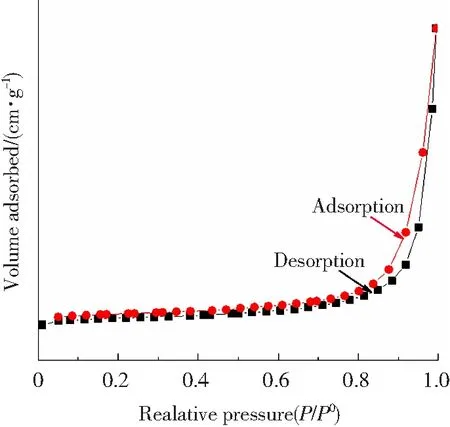
图13 4A分子筛氮气吸附-脱附等温线图
3 结 论
1)以铝灰和微硅粉为原料成功制备了4A分子筛,且最佳工艺条件为硅铝2.0、碱度2.5、晶化温度100 ℃、晶化时间10 h。
2)最佳工艺条件制备的4A分子筛的钙离子交换量为362 mg CaCO3/g,符合国家行业标准(>295 mg CaCO3/g)。
3)最佳工艺制备的4A分子筛晶粒清晰完整,粒径为2 μm左右,分子骨架符合4A分子筛的骨架特征,且具有一定的吸附性能。

