茶多酚对马氏珠母贝外套膜组织和细胞培养的影响
方 伟,丁瑞霞,陈明强,王 雨,赵 旺,温为庚,马振华
1.三亚热带水产研究院/海南省深远海渔业资源高效利用与加工重点实验室,海南 三亚 572000
2.中国水产科学研究院南海水产研究所/农业农村部南海渔业资源开发利用重点实验室,广东 广州 510300
3.中国水产科学研究院南海水产研究所热带水产研究开发中心,海南 三亚 572018
马氏珠母贝 (Pinctadamartensii) 又称合浦珠母贝,隶属于软体动物门、瓣鳃纲、珍珠贝目、珍珠贝科、珠母贝属,是世界上生产海水珍珠的主要贝种,也是我国生产海水养殖珍珠—“南珠”的主要贝类之一[1]。马氏珠母贝主要分布在热带和亚热带海域[2-4],从日本千叶县以南至菲律宾、越南、缅甸、印度尼西亚、斯里兰卡、澳大利亚等均有分布[5-6],我国主要分布在海南、广东、广西、台湾等省沿海。
我国是世界海水珍珠养殖大国,马氏珠母贝是人工插核育珠的主养贝种[7-9]。近年来马氏珠母贝种质退化,育珠贝病害严重,插核后的死亡率和吐核率增加,且优质珠率下降[10]。为了突破插核技术的局限性,人工将供体珍珠贝的外套膜组织块或细胞小片一起移植到受体珍珠贝体内,诱导其组织大量分泌珍珠质,以实现无核珍珠的培育[11-13]。当前国内许多学者对珍珠贝细胞、组织体外培养进行了大量研究,而国外相关的研究报道较少。Lei等[14]对马氏珠母贝珍珠囊进行了培养研究;李勇和孟立霞[15]研究了贝类细胞的生存环境,总结了当前贝类细胞培养中存在的问题,为建立细胞系提供了指导;靳雨丽等[16]对三角帆蚌 (Hypriosis cumingii) 外套膜细胞培养进行了研究,优化了外套膜细胞培养及育珠的生产条件;岑妍慧和林江[17]改进了马氏珠母贝外套膜组织细胞体外培养技术和培养条件。
茶多酚是从茶叶中提取的多羟基酚类物质的总称,主要包括黄烷醇类 (儿茶素类) 、黄酮、花色苷类等[18-19]。已有研究表明,茶多酚作为天然抗氧化物质具有抗氧化、防辐射、抗衰老、抑菌、抗过敏、抗血栓和解毒等作用[20]。茶多酚不仅广泛应用于畜产品加工和贮藏、食物的防腐保鲜、饲料添加剂等,还可以调节前列腺癌[21]、乳腺癌[22]以及鼻咽癌[23]等多种肿瘤的生物学活性。刘芳君等[24]研究发现,质量浓度低于0.05 g·L-1的茶多酚对小鼠 (Musmusculus) 黑色素瘤细胞的体外增殖无明显的抑制作用,而当其质量浓度提高至0.15 g·L-1时对该细胞迁移具有抑制作用。田梦秋等[25]研究发现,10~320 μg·mL-1的茶多酚对Hep2 细胞的体外增殖具有抑制作用,并诱导细胞凋亡,当茶多酚的质量浓度大于160 μg·mL-1时表现出较强的细胞毒性。王海琴等[26]研究了茶多酚对人牙槽骨成骨细胞增殖和凋亡的影响及分子机制。但茶多酚应用于马氏珠母贝外套膜组织和细胞培养的研究却鲜有报道。本研究通过在马氏珠母贝外套膜组织和细胞培养液中添加不同浓度的茶多酚,利用其抗氧化性、抑菌及解毒等特性来达到促进细胞生长增殖、提高细胞生物活性的目标,从而进一步优化组织和细胞培养,探索最适完全培养液,以提高组织和细胞体外培养的成功率,为人工无核育珠提供理论参考。
1 材料与方法
1.1 实验材料
实验用马氏珠母贝由三亚热带水产研究院陵水试验基地提供。本次实验随机选取生长状态良好的马氏珠母贝,壳长为 (5.80±0.32) cm,平均体质量为 (26.50±0.13) g。暂养于室外遮阳陆基玻璃池 (直径2 m,高1.2 m 的圆筒形),换水量为100%·d-1,投喂期间的饵料主要为牟氏角毛藻 (Chaetoceros mulleri),水温27~30 ℃,盐度27‰~31‰,pH 7.6~8.1,溶解氧质量浓度≥7.0 mg·L-1,亚硝酸盐(NO-2)质量浓度≤0.02 mg·L-1,氨氮 (NH+4-N) 质量浓度≤0.2 mg·L-1。
1.2 实验方法
1.2.1 茶多酚的提取
根据前人对茶多酚提取工艺的研究[27-28],采用溶剂提取法对茶多酚进行提取。称取研细的苦丁茶末3.0 g,加100 mL 体积分数为70%的乙醇作为溶剂,在75 ℃下回流浸泡1.5 h,趁热抽滤,取滤液旋转蒸发,待其呈膏状时,用热水溶解,并用无菌蒸馏水定容至50 mL 备用,通过吸光度法测定茶多酚的质量分数为20%。
1.2.2 完全培养液的配制
基础培养液配方:RMI-1640 培养基10.4 g·L-1、Hepes 缓冲液2.7 g·L-1、珍珠贝体液10.0 mL·L-1、青霉素100 000 IU·L-1、链霉素100 000 IU·L-1、氯化钙 (CaCl2) 200 mg·L-1、灭活小牛血清200 mL·L-1、平衡盐溶液50 mL·L-1、葡萄糖100 mL·L-1,pH 7.2。
自制珍珠贝体液:每次取10 个马氏珠母贝的外套膜周边黏液,经2 000 r·min-1离心10 min,取上清液置于56 ℃水浴锅中灭活处理20 min,并在紫外灯下灭菌20 min。加入培养液前需经过0.2 μm 的滤膜过滤。
将获取的茶多酚溶液稀释为0%、5%、10%、15%和20% 5 种体积分数,各取10 mL 溶液,分别加入到90 mL 的基础培养液中,配置成5 组含不同体积分数茶多酚的完全培养液 (0%、0.5%、1.0%、1.5%和2.0%组),其中0%组为对照组。
1.2.3 外套膜的获取
选取健康且活力较强的马氏珠母贝,用0.3%(w) 肥皂水反复洗刷,去除贝壳表面的附着物。割断闭壳肌、取出外套膜,用双蒸水反复冲洗,并在0.01% (w) 高锰酸钾溶液中浸泡30 min 进行初步消毒。将已消毒处理的外套膜边缘部位分离出来,并在抗菌溶液 (青霉素4 000 U·mL-1,链霉素5 000 U·mL-1) 中浸泡15 min,期间反复冲洗。最后用灭菌的双蒸水再次冲洗2~3 次后待用。
1.2.4 外套膜细胞的体外培养
将处理过的外套膜组织小片通过撕膜法获取外套膜外表皮,用无菌单面刀片切成碎块,放入含有300 mL 消化液 (0.25%胰蛋白酶,pH 7.2~7.4,预配好的胰蛋白酶消化液经0.22 μm 除菌膜进行除菌后再使用) 的培养瓶中,置于37 ℃恒温摇床上以120 r·min-1的速率消化30 min,后移至2.5 mL 离心管中以1 000 r·min-1的速率离心5 min,弃上清液。在留有沉淀物的离心管中加入平衡盐溶液继续以1 000 r·min-1的速率离心2 min,重复操作3 次,获取外套膜细胞。将相同数量的外套膜细胞放入5 组含不同浓度茶多酚的培养液中,置于25 ℃的恒温培养箱中持续培养。实验共设置5 组,每组3 个平行,每2 d 更换一次新鲜培养基。
观察组使用CT检查诊断准确率明显高于对照组使用B超检查诊断准确率,两组数据差异明显。有统计学意义(P<0.05)。见附表。
1.2.5 外套膜组织的体外培养
将处理过的外套膜放入无菌培养皿中,先用脱脂棉吸收表面的液体残留,然后用无菌双面刀片将其切割成1 mm2大小均匀的组织小片。每个培养瓶 (225 cm2) 内贴片30 个组织小片,待组织小片附着于瓶壁后,将培养瓶反转并加入5 mL 完全培养液。放入恒温箱中25 ℃培养24 h 后,将培养瓶再次反转,使组织小片完全浸没在培养基中,继续培养和观察。通过前期开展利用不同浓度的茶多酚对细胞活性影响的实验,得出当茶多酚添加量为1.0%时,相对细胞生物活性最高,细胞生长效果最佳,因此在开展外套膜细胞和组织培养观察实验时仅采用1.0%组培养液,每2 d 更换一次新鲜培养基。
1.3 测定指标
1.3.1 外套膜细胞的生长曲线
每隔48 h 对5 组分别取样,按常规方法消化后各取1 mL 细胞悬液至EP 管中计数细胞量,统计分析结果。
1.3.2 生物活性检测
将收集的外套膜细胞悬浮液加入 96 孔培养板(Corning,美国),每孔100 μL。为确保每孔细胞的数量及活性一致,每批实验都使用同一管混合均匀的细胞悬液,并确保细胞密度约为5×104个·mL-1。向细胞悬液中分别加入5 种不同浓度的茶多酚。设置两组对照分别为:仅含 100 μL 培养基的空白对照组和仅含100 μL 细胞悬液的对照组,每组3 个平行。添加完茶多酚后,将细胞置于细胞培养箱 (25 ℃) 中培养24 h。
细胞活性检测方法:使用 Cell Counting Kit-8(CCK-8) 试剂盒 (东仁化学) 按照说明书进行检测。在100 μL 的细胞悬液中加入10 μL CCK-8 试剂,放回25 ℃培养箱孵育4 h 后,用酶标仪测定波长450 nm 处的吸光度。
相对细胞活性计算方法:相对细胞活性=(实验组吸光度-培养基吸光度)/(对照组吸光度-培养基吸光度)。
1.3.3 细胞形态和钙离子 (Ca2+) 浓度测定方法
采用倒置显微镜观察组织细胞的形态与生长状况,并做好记录。采用血气分析仪测定马氏珠母贝外套膜组织及细胞培养液中的Ca2+浓度。
1.3.4 数据分析
采用SPSS 26.0 软件进行统计学分析,采用t检验,P<0.05 表示差异显著。结果均以“平均值±标准差 ()”表示。
2 结果
2.1 不同浓度的茶多酚对细胞活性的影响
不同浓度的茶多酚对马氏珠母贝外套膜细胞活性的影响见图1。在不同浓度的茶多酚刺激下,5 组间的细胞活性均存在显著性差异 (P<0.05),同时各组对细胞活性的影响差别较大。当茶多酚的浓度为1.0%时,细胞的相对活性提高至3 倍,对细胞活性的促进作用最大,其次为1.5%、0.5%、2.0%组。马氏珠母贝外套膜细胞在5 组培养液中的生长曲线如图2 所示,均呈现“S”型,分为4 个阶段:潜伏期 (第0—第2 天)、对数生长期(第3—第5 天)、平台期 (第6—第14 天) 和衰退期 (第16—第30 天)。其中1.0%组峰值最高,在培养第12 天时细胞密度达6.9×105个·cm-2,其他4 组峰值高度依次为1.5%组>0.5%组>2.0%组>0%组。在细胞培养第30 天,细胞密度最高的为1.0%组,最低的为0%组。结果表明,茶多酚对马氏珠母贝外套膜细胞的活性具有显著的促进作用,有利于细胞的增殖生长,当浓度为1.0%时,促进效果最佳。
2.2 外套膜细胞的培养观察
由2.1 中结果可知,1.0%组完全培养液对于马氏珠母贝外套膜细胞的培养优于其他组。因此采用1.0%组培养液对马氏珠母贝外套膜细胞进行培养,并利用倒置显微镜观察不同时期的细胞生长状况 (图3)。培养至第5 天时,细胞呈分散状态,形态为圆形或椭圆形,其中数量最多的为近圆形的上皮细胞,大小为40~50 μm,分裂过程中上皮细胞呈现多种形态。当培养至第10 天时,细胞贴壁效果较好,少量细胞悬浮于培养液中,瓶壁出现少量晶体颗粒。第20 天时,细胞相互聚集,呈现岛屿状分布。第30 天时,细胞聚集生长现象更为明显,培养瓶中可观察到在细胞群周边出现絮状结晶。

图3 马氏珠母贝外套膜上皮细胞培养观察 (400×)注:a.培养第5 天的细胞; b.培养第10 天的细胞;c.培养第15 天的细胞; d.培养第20 天的细胞;e.培养第25 天的细胞;f.培养第30 天的细胞。Fig.3 Observation on cells of P.fucata mantle (400×)Note: a.Cell cultured on Day 5; b.Cell cultured on Day 10; c.Cell cultured on Day 15; d.Cell cultured on Day 20;e.Cell cultured on Day 25; f.Cell cultured on Day 30.
2.3 外套膜组织培养观察
采用1.0%组培养液对马氏珠母贝外套膜组织进行培养,并利用倒置显微镜观察不同时间组织的生长状况 (图4)。外套膜组织培养第5 天时,组织块周边逐渐有细胞迁移出来,且组织块有细胞迁移留下的痕迹 (图4-a)。迁移出的细胞形态以圆形和椭圆形为主,呈颗粒状分散。当培养第10 天时,组织块生长晕上的细胞生长旺盛且细胞排列紧密,周边细胞数量进一步增加,并出现透明形态的细胞,胞体周边有突起,且贴壁效果明显,瓶底出现微小的颗粒状晶体。培养第15—第20 天,组织块周边细胞密集分布形成细胞片,上皮细胞的分泌作用使瓶底颗粒状晶体进一步增多。培养第25 天,组织块周边出现很多纤维状的突起,上皮细胞继续分泌大量颗粒状物质,在瓶底形成明显的白色块状物质。培养第30 天,组织块已变成了茶褐色,大部分组织和细胞仍然存活,但活力明显减弱,细胞分泌能力停止。

图4 马氏珠母贝外套膜组织培养观察 (400×)注:a.培养第5 天的组织;b.培养第10 天的组织;c.培养第15 天的组织;d.培养第20 天的组织;e.培养第25 天的组织;f.培养第30 天的组织。Fig.4 Observation on tissue of P.fucata mantle (400×)Note: a.Tissue cultured on Day 5; b.Tissue cultured for on Day 10; c.Tissue cultured on Day 15; d.Tissue cultured on Day 20;e.Tissue cultured on Day 25; f.Tissue cultured on Day 30.
2.4 外套膜组织和细胞培养对Ca2+吸收的影响
采用1.0%组培养液对马氏珠母贝外套膜组织和细胞进行培养,其组织和细胞培养液中的Ca2+质量浓度变化如表1 所示。在组织和细胞培养的整个过程中,培养液中Ca2+的质量浓度随着培养时间的延长均呈现先减后增的趋势,且培养液中的Ca2+质量浓度均在第10 天达到最低,分别为 (163.58±8.40) 和 (148.98±6.58) mg·L-1。培养第0—第5 天,细胞培养液中的Ca2+质量浓度低于组织培养液,且存在显著性差异 (P<0.05),表明在培养前期细胞对Ca2+的吸收能力明显强于外套膜组织;培养第5—第15 天,细胞培养液中的Ca2+质量浓度在同期略低于组织培养液,但两者之间无显著性差异;培养第0—第15 天,组织和细胞培养液中的Ca2+含量均呈现递减的趋势,说明在组织和细胞培养过程中均吸收了培养液中的Ca2+。培养第15—第25天,随着培养时间的延长,组织和细胞培养液中的Ca2+质量浓度均呈现递增趋势,但始终低于初始质量浓度 (200 mg·L-1),两者之间存在显著性差异(P<0.05)。
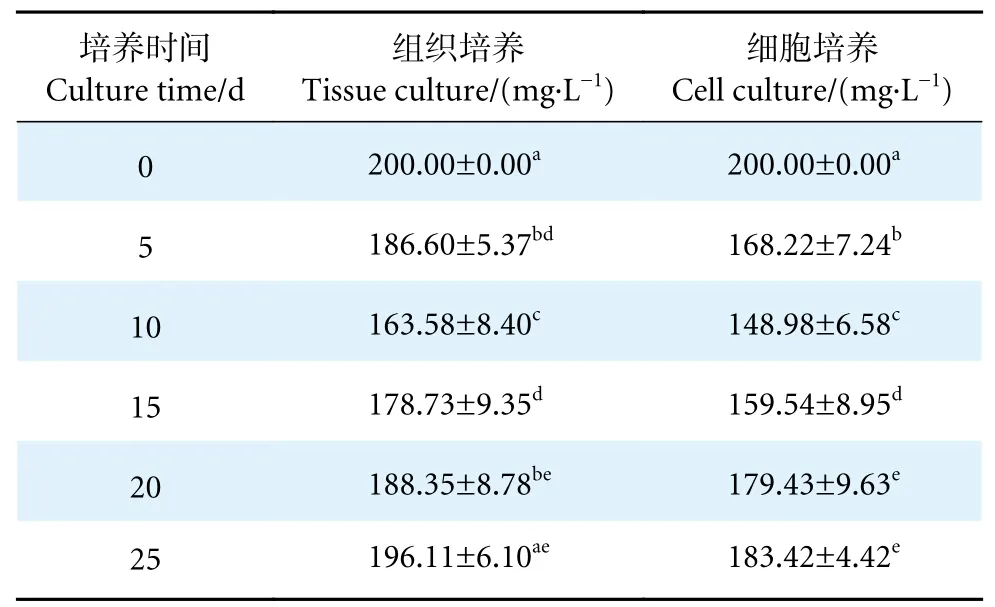
表1 马氏珠母贝外套膜组织和细胞培养液中的Ca2+质量浓度变化Table 1 Change of Ca2+ mass concentration in mantle tissue and cell culture medium of P.fucata
3 讨论
3.1 茶多酚对马氏珠母贝组织和细胞培养的影响
马氏珠母贝属于双壳类软体动物,作为低等动物,其外套膜组织细胞的培养有别于哺乳动物及其他脊椎动物。当前马氏珠母贝外套膜组织和细胞培养还未取得突破性进展,培养液的优化一直处在不断探索中[29]。常规的细胞培养液具有良好的借鉴作用,但局限性比较明显,通常情况下细胞的生物活性会随着培养时间逐渐降低,影响细胞的体外培养效果[30]。茶多酚作为一种天然提取物,具有显著的调节生物学活性、消除自由基、抗氧化、抑菌等功效[31]。在马氏珠母贝细胞培养液中添加适量的茶多酚,其酚羟基提供的大量H+与培养液中的氧自由基发生反应,从而提高培养液的抗氧化能力,促进细胞新陈代谢,改善细胞活性,可进一步优化组织细胞培养效果。本研究发现当培养液中添加茶多酚的体积分数为1.0%时,对细胞活性的促进作用最优,细胞的相对活性提高至3 倍。茶多酚在一定程度上消除了细胞微环境中的自由基,增强了机体抗氧化性,进一步释放了细胞的生物活性。曹东维等[32]研究发现,茶多酚在体外高糖环境下可延缓人肾小球系膜细胞 (Human glomerular mesangial cells,HGMCs) 衰老,提高细胞生物活性,这与本研究得出的结果相似。本研究共设置了含5 个体积分数梯度茶多酚 (0%、0.5%、1.0%、1.5%、2.0%) 的培养液,各组的细胞生长曲线均呈“S”型,说明茶多酚在细胞培养过程中未产生抑制或其他不良反应。通常细胞在生长过程中伴随着新陈代谢会排泄出二氧化碳、尿酸及其他有害物质,容易滋生有害细菌,引起培养环境的恶化,长期积累的毒素甚至会导致细胞死亡。在培养液中添加适量的茶多酚,其抗氧化、抑菌等功效可以维持培养环境的稳定,从而促进马氏珠母贝外套膜细胞的新陈代谢,起到延缓衰亡的功效。本研究结果发现所有添加茶多酚的实验组培养效果均优于对照组,其中茶多酚体积分数为1.0%时,培养效果最优,与其他4 组存在显著性差异 (P<0.05)。实验结果进一步表明了在细胞培养液中添加适量的茶多酚,对细胞增殖具有良好的促进作用。也有研究发现不同剂量的茶多酚对癌细胞的增殖生长具有抑制作用,这可能与癌细胞的增长和凋亡机制相关[33-34]。在培养液中添加过量的茶多酚是否对马氏珠母贝外套膜组织和细胞培养产生抑制作用有待进一步研究。
3.2 马氏珠母贝外套膜组织与细胞培养观察
在培养液中添加1.0%的茶多酚时,马氏珠母贝外套膜组织和细胞均可正常分裂增殖。培养第5 天,组织块周边出现细胞迁移,呈颗粒状分布,而细胞培养液中也相应的出现大量细胞分裂增殖,两者均观察到了近圆形的上皮细胞。培养第10 天,组织和细胞培养液中均观察到了细胞贴壁现象,且晶体颗粒初现。王爱民等[35]研究发现在马氏珠母贝外套膜组织培养中,最先迁移出来的是颗粒状细胞,紧随其后的是透明细胞。本实验在细胞培养前期发现了大量的颗粒状细胞,而透明细胞的数量相对较少,说明在茶多酚的刺激下细胞活性增强,前期以大量分裂增殖为主,当细胞增殖到一定数量后,开始逐渐分化为其他形态的细胞。Machii 和Wada[36]在对褶纹冠蚌 (Cristariaplicata) 的研究中,以外套膜组织块上部或边缘部位观察到褐色或茶色来判定其分泌作用,表明组织块而非独立的上皮细胞分泌了珍珠质。本研究在培养第20 天后发现组织和细胞培养液中均出现了晶体颗粒,说明马氏珠母贝上皮细胞也具有分泌珍珠质的功能。这可能是不同物种贝类的外套膜组织和细胞在不同的培养条件下,其功能表达存在差异。
3.3 组织和细胞培养液中的Ca2+浓度变化
培养液是维持动植物组织生长的人工配制养料,细胞培养成功的关键在于培养液中含有充足的营养组分,可提供细胞生长所需的能量、微量元素及未知的生物因子等。由于珍珠的化学成分与产珠贝壳类似,均由超过95%的碳酸钙和4%的固体蛋白质生物矿化而来[37-38],因此在马氏珠母贝外套膜组织和细胞培养液中添加适量的Ca2+,可保障其正常的分泌功能。本研究在完全培养液中添加了200 mg·L-1的Ca2+,随着组织和细胞的培养,组织液中Ca2+质量浓度在前10 d 呈递减趋势,说明组织和细胞增殖的过程中吸收了大量的Ca2+,同时镜检发现在瓶壁上存在颗粒状晶体也进一步给予证实。陈勇富和钱国英[39]对三角帆蚌外套膜离体上皮组织珍珠质分泌能力的研究也得出相似结论。在培养第15 天后,培养液中的Ca2+浓度随着培养时间的延长逐渐升高,说明在培养后期马氏珠母贝外套膜组织和细胞同正常的活体一样,具有旺盛的钙质吸收和分泌功能。这与唐敏和石安静[40]对外套膜外表皮细胞钙的分泌研究结果一致。通过对培养液中Ca2+浓度变化的研究可知,当培养液中添加适量的茶多酚、Ca2+及其他营养成分后,马氏珠母贝外套膜组织和细胞可正常增殖分化,且分泌珠质的功能并未受到影响。在茶多酚的刺激下,细胞的氧化代谢能力增强,培养前期可吸收大量的Ca2+,为珍珠质的分泌提供充足的钙源。在马氏珠母贝无核育珠的实践生产中,既要保证细胞培养液中含有充足的Ca2+,同时也要确保外套膜细胞在茶多酚的刺激下对其充分吸收,以加快珠质的分泌,提升珍珠的质量和产量。
4 结论
本研究探索了茶多酚对马氏珠母贝外套膜组织和细胞体外培养的影响。当培养液中茶多酚的添加量控制在0.5%~2.0%时,均可增强马氏珠母贝外套膜细胞的生物活性,其中添加量在1.0%时的增殖效果最优;进一步优化了马氏珠母贝外套膜细胞培养液 (1.0%茶多酚、RMI-1640 培养基10.4 g·L-1、Hepes 缓冲液2.7 g·L-1、珍珠贝体液10.0 mL·L-1、青霉素100 000 IU·L-1、链霉素100 000 IU·L-1、CaCl2200 mg·L-1、灭活小牛血清200 mL·L-1、平衡盐溶液50 mL·L-1、葡萄糖100 mL·L-1,pH 7.2);马氏珠母贝外套膜组织和细胞在添加适量茶多酚后均可正常增殖分化,且培养液中的Ca2+浓度随着培养时间的延长呈现先减后增的趋势。马氏珠母贝外套膜组织和细胞培养液作为无核育珠的关键技术之一,可通过添加1.0%的茶多酚进行优化和改良,这不仅填补了茶多酚在贝类细胞培养研究中的空白,也为贝类育珠的实际生产提供了重要的参考依据。

