新生儿腹膜后寄生胎1例并文献复习
杜青,金祝,郑泽兵,汤成艳,黄露,刘远梅
患儿,男,25 d,因发现腹腔占位于2022年1月18日入院。既往患儿祖母有双胎妊娠史。患儿母亲孕6个月彩色超声定期产检,发现胎儿腹腔有一占位性病变,产检考虑先天性腹膜后囊性病变或畸胎瘤可能,于围产医学科及小儿外科门诊就诊,建议定期规律产检至预产期内,再次彩色超声提示:患儿腹内占位未明显进行性增大,寄生胎或畸胎瘤等可能。产妇于妊娠38+2周顺产,患儿生后无窒息,皮肤色红,Apgar评分9分,正常哺乳无腹胀、呕吐,大小便正常。入院查体:T 36.8℃,HR 138次/min,R 26次/min。反应尚可,神清,无消瘦,腹部稍膨隆,腹软,于上腹部深压触诊扪及9.0 cm×7.0 cm×6.0 cm大小包块,实性感,较固定,无压痛及肌紧张,肝脾未触及,肠鸣音5次/min。腹部CT(图1):上中腹部腹膜后见椭圆形混杂密度团块,大小9.6 cm×8.5 cm×6.3 cm,内见骨质、软组织、脂肪、水样密度影,骨性结构构成脊柱、四肢形态;增强扫描部分实性成分似轻度强化,病变位于双肾、腹主动脉及下腔静脉前方,紧贴肝脏、胃、脾脏,门静脉、肠系膜上静脉紧贴肿块右缘走行,上中腹部腹膜后占位性病变,系寄生胎。肿瘤标志物:AFP 3 000.0 μg/L。排除相关禁忌证,取上腹部横切口行剖腹探查术,术中见(图2~3):肿块来源于腹膜后,包膜完整,囊实性,大小12.0 cm×10.0 cm×9.0 cm,压迫肠系膜动静脉,与腹膜后组织粘连致密,滋养血管来源于肠系膜上动脉;于横结肠下方切开横结肠系膜,暴露腹膜后肿块边缘,结扎肿块滋养血管,沿肿块包膜钝性分离,完整切除肿块,手术完毕后剖开肿块见羊膜包裹一成形胎儿,脐带可见,约3个月胎龄大小,四肢、脊柱均可见。术后病理(图4):送检肿块内可见皮肤、胰腺、肠管、软骨等结缔组织,符合寄生胎。术后随访至今,查AFP 7.20 μg/L,患儿未见复发,生长发育正常。
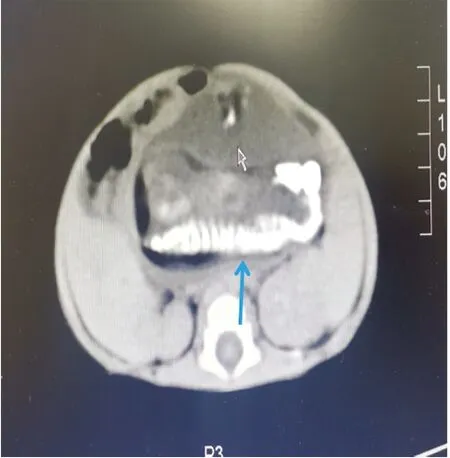
图1 CT示腹膜后混杂密度团块,见脊柱、四肢形态
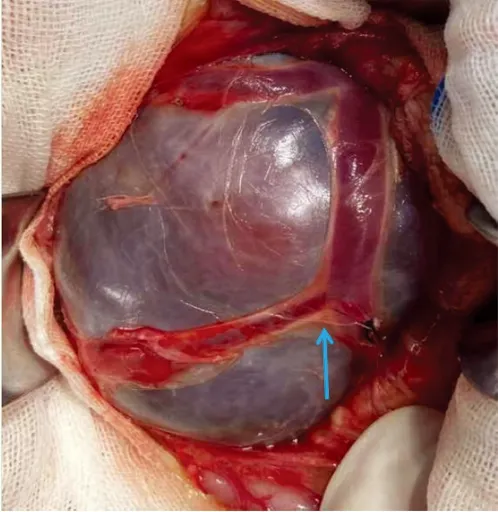
图2 术中示肿块包膜完整,囊实性,滋养血管包绕

图3 囊膜切开见一成形胎儿,脐部血管与宿主相连

图4 肿块镜检见结缔组织成份(HE染色,×100)
讨 论寄生胎(fetus-in-fetu,FIF)又称胎中胎,是一种胚胎发育异常形成的罕见先天性疾病,发病率约为1/50万[1],根据其寄生覆着部位分为内寄生胎和外寄生胎。内寄生胎胎外包裹有一层纤维囊壁膜,囊内有液体、发育缺如或发育停滞的胎块,且寄生胎有一支血管蒂与宿主血管相连接;而外寄生胎则是覆着于胎儿体表,男女发病率无明显差异[2-3]。FIF寄生部位通常以腹膜后和腹腔最多见[1,4],也有发生在骶尾部、胸部、阴囊、口腔等部位的报道[5-7]。本例其母亲孕期产检彩色超声发现,提示其为腹腔或腹膜后寄生胎或畸胎瘤可能,未明确定性,且患儿祖母遗传双胎产育史,患儿手术后明确为寄生胎,且脐部有支血管与宿主相连,因而本例为内寄生胎,较罕见,与文献报道相符。
FIF的临床表现主要与寄生的部位有关,表现为占位压迫效应,多以内寄生胎表现更为突出,以腹胀、呕吐、腹部肿块、肠梗阻及黄疸等出现。从影像学分析上看,FIF和畸胎瘤影像表现特征相似,有时难以鉴别;FIF在影像上可见成形的四肢及脊柱,畸胎瘤则是散在的不规则钙化灶;CT检查有助于FIF和畸胎瘤鉴别,因CT具有辐射风险性,适用于手术前的诊断[8];超声有无创、无辐射、操作简单方便等优点,是FIF首选检查,但产前诊断率不足20%[5]。FIF常发育成形或发育缺如成胎块,有学者指出MR检查可以鉴别FIF与宿主周围脏器、血管及软组织的关系,更有利于手术方案的制定及选择[5]。
对于FIF的诊断,至少需以下特征之一[1,3]:(1)有完整的纤维囊包裹; (2) 胎块表面有部分或完全的皮肤覆盖; (3)与宿主有相连血管;(4) 具有可识别的解剖结构,不一定有阶段性脊柱轴骨。由于产前诊断率较低,FIF还需与神经母细胞瘤、胎儿胎粪性囊肿等疾病相鉴别[9-10],但是,FIF最终的确诊需病理检查,病检可发现发育成熟或不成熟的器官组织[4]。
对于FIF,产妇孕期管理及早期诊断非常重要,若合并严重畸形、染色体异常及严重并发症,预后差,产妇应早期终止妊娠。产妇分娩方式的选择取决于产前影像学的诊断,若肿块较小,腹腔内或腹膜后肿块小于5 cm,且胎儿体质量小于或符合胎龄的,可选择经阴道自然分娩[11-12];反之,FIF形态不规则、肿块较大、外生形,且胎儿体质量大于胎龄和颈部、胸腔、口腔内等寄生位置异常时[13],为保证胎儿的出生安全,应到产科、新生儿科、儿外科专业实力较强的医院行剖腹产。
FIF的治疗方式是早期手术,若无明显压迫症状,可在婴儿足月后行手术较为安全;但如果肿块较大,影响婴儿生命,手术时机可不必局限于年龄,有文献报道,右上腹部FIF与胆道粘连引起胆道穿孔可导致婴儿死亡[14],故更应早期手术;若寄生于胸腔、颈部等部位严重威胁婴儿生命体征,应急诊手术解除病变,术后转新生儿进一步监护治疗。手术分为微创手术或开腹手术,术前影像学检查对于手术方式的选择有重要作用,若囊性成分占50%以上FIF可选择腹腔镜微创手术[6,15],可在微创下针穿刺抽出囊性液体,增大操作空间,利于手术分离切除囊膜及肿块。无论采用何种手术方式,应仔细解剖分离周围重要血管,完整切除囊膜及寄生胎。绝大部分FIF为良性,预后良好,因宿主血清AFP和母体血清含量有同时升高的报道[5,8],所以FIF切除术后AFP和人绒毛膜促性腺激素作为随访观察和确定恶性FIF复发的关键依据。本例患儿术前影像提示位于腹膜后,肿块巨大,术中肠系膜血管相连,选择开腹手术,完整切除囊膜及寄生胎,术后随访至今,复查AFP和人绒毛膜促性腺激素位于正常范围,患儿生长发育良好。
综上,FIF虽罕见,但只要经过合理的临床孕产前管理,同时需产科、儿外科、影像科、麻醉科、护理团队多学科合作,产前、产时、产后良好的精准治疗,会给FIF患儿带来良好的预后。

