面向高电压固态锂电池的明胶/聚氧化乙烯复合电解质的制备与性能
郑衍森,王泳茵,桂久青,谢卓豪,徐 越,曹巧英,徐悦华,刘应亮,梁业如
(生物基材料与能源教育部重点实验室,华南农业大学材料与能源学院,广东 广州 510642)
固态锂电池因选用不易燃的固态电解质,可降低甚至消除电池自燃的风险而显著提高安全性,成为下一代理想的电化学储能技术。特别是,采用固体电解质有望解决基于锂金属为负极的锂电池因锂枝晶带来的安全隐患,有望在提升安全性的同时,大幅度提升电池的能量密度[1-3]。高性能固态电解质是研发固态锂电池核心技术之一。在各类固态电解质中,聚氧化乙烯(PEO)电解质是目前被研究最为广泛的一类电解质材料,具有柔性高、成本低、界面电阻低以及与锂金属负极具有良好相容性等优势[4-5]。然而,PEO 电解质表现出较低的离子电导率(10-8~10-6S/cm)和较窄的电化学稳定窗口,限制了其进一步应用[6]。
为解决这些问题,研究者主要采用共聚、共混等方法在PEO 中引入其他材料,降低了PEO 结晶度,增强了其链段的运动能力,由此有效提高PEO基电解质的离子电导率和电化学稳定性[7]。然而,在实际高电压应用中,PEO 基电解质与正极产生的界面副反应更加突出[8],当充电电压超过4.05 V 时,PEO 链端的羟基基团易失去电子而被氧化。随着充电电压的升高,不可逆的氧化分解导致界面结构稳定性恶化,造成界面电阻快速增长和严重极化,使Li+输运的局部路径失效[7],最终导致固态锂电池失效[9-10],制约着固态锂电池能量密度的进一步提升。近年来,为拓宽PEO 聚合物基电解质电化学稳定窗口,研究者们提出锂盐添加剂或无机涂层等策略有效抑制聚合物电解质在高电压下的电化学氧化[11-12],由此建立稳定的正极电解质界面层,最终提升了高电压固态锂电池的循环性能[13]。然而,这些方法通常涉及到复杂的制备工艺,而且原料价格昂贵,导致制备成本较高,具有一定的局限性[14]。开发简单高效、条件温和、环境友好的新型工艺路线,设计合成具有高电压稳定性的PEO基电解质,仍然是聚合物固态电解质领域重要的科学问题。
为此,本工作将明胶与PEO 电解质进行物理共混,利用明胶的羧基与PEO链端羟基形成氢键,减缓高电压下PEO 端羟基氧化,由此发展出一种简单制备可耐高电压的明胶/PEO(Gelatin/PEO,G/PEO)复合电解质。研究结果表明,明胶的加入不仅降低了PEO电解质的结晶度,提高了复合电解质的离子电导率,而且得益于明胶与PEO端羟基之间的氢键作用,G/PEO复合电解质在4.0~4.3 V下的氧化副反应得以抑制。另外,明胶的主要成分氨基酸具有较低的HOMO能级从而提高了复合电解质的高电压耐受性,将其电化学稳定窗口提升至4.8 V。基于此,由G/PEO复合电解质组装的Li|LiNi0.8Co0.1Mn0.1O2(NCM811)固态电池,放电容量达186.1 mAh/g,100次循环后具有73.3%的容量保持率,明显优于基于传统PEO 电解质在相同条件下组装和测试的Li|NCM811 固态电池。相比于传统PEO 电解质在高于4.0 V 电压下因易氧化而导致容量快速下降的情况,G/PEO复合电解质的可逆循环性显著增强,其具有更好的实际应用潜力,为简单制备方法提升聚合物基固态电池的能量密度提供了新思路。
1 实验材料和方法
1.1 材料
PEO (分子量为600000)、明胶(纯度>99%)、双三氟甲磺酰亚胺锂(LiTFSI,纯度>98%)、N-甲基吡咯烷酮(纯度>99%)均购自上海阿拉丁生化科技有限公司;LiFePO4(LFP)、LiNi0.8Co0.1Mn0.1O2(NCM811)、聚偏二氟乙烯(PVDF)、导电炭黑(Super P)、锂金属片均购自广东烛光新能源科技有限公司;铝箔、CR2032扣式电池壳均购自深圳科晶智达股份有限公司。
1.2 仪器和试剂
傅里叶变换红外光谱仪(Vertex 70,布鲁克公司)用于表征样品的化学结构、粉体广角X 射线衍射仪(Rigaku-Ultima,株式会社理学)用于表征样品的结晶度、扫描电子显微镜(SU8220,日本日立高新技术公司)用于观察样品的表面形貌、能量色散光谱仪(X-Max,英国牛津仪器公司)用于观察样品的元素分布、X射线光电子能谱仪(Axis Supra,日本岛津)用于表征电极表面的化学组分、扣式电池封装机(MSK-110,深圳市科晶智达科技有限公司)、扣式电池拆卸机(MSK-110,深圳市科晶智达科技有限公司)、电化学工作站(CHI660E,上海辰华仪器有限公司)、电池测试系统(BTS7.6.x,深圳新威电子有限公司)、手套箱(STX-2,湖北米开罗那公司)。
1.3 固态电解质的制备
(1)PEO基电解质的制备
按照比例称取PEO、LiTFSI至搅拌瓶中(PEO∶LiTFSI质量比5∶2),并加入去离子水在60 ℃下搅拌12 h,直至得到均匀的溶液。随后,将分散均匀的溶液倒入聚四氟乙烯模具中并在常温静置36 h,随后在60 ℃条件下真空干燥10 h后转移到手套箱中静置,得到PEO基电解质。
(2)明胶/PEO复合电解质的制备
按照比例称取明胶、PEO 和LiTFSI 加入搅拌瓶中(明胶∶PEO∶LiTFSI 质量比3∶7∶2.8),加入去离子水在60 ℃下搅拌12 h。随后,将均匀分散的混合溶液倒入聚四氟乙烯模具中并在常温静置36 h,随后在60 ℃条件下真空干燥10 h 后转移到手套箱中静置,得到G/PEO复合电解质。
1.4 正极的制备和电池的组装
将正极活性材料(LFP 或NMC811)和Super P导电剂以质量比8∶1加入玛瑙研钵内研磨30 min,后将黏结剂与研磨后的粉末加入搅拌瓶中,正极活性材料∶Super P∶PVDF 三者组成的质量比为8∶1∶1,将以上混合物均匀分散在N-甲基吡咯烷酮中搅拌形成均匀分散的浆料。电极片涂布时将均匀浆料涂布在铝集流体上,将涂有正极浆料的电极片放置在真空干燥箱中80 ℃干燥12 h,扣式电池电极片使用冲片机切成直径为12 mm 的圆形电极片,最后称量以及计算正极活性材料质量。全电池采用CR2032型电池壳依次以正极、电解质、负极的次序在水氧含量均<0.1×10-6的手套箱中组装。
1.5 电化学测试
离子电导率测试通过组装不锈钢(SS)|聚合物电解质(PEO 或G/PEO)|不锈钢(SS)对称电池,利用CHI660D 电化学工作站测试电解质在不同温度下的交流阻抗值,并计算出电解质膜的电导率,计算公式如式(1)所示
式中,d为聚合物电解质的厚度;A为电解质膜的有效面积;R为电池的本体阻抗。
活化能由Arrhenius 方程计算得出,计算公式如式(2)所示
式中,σ为离子电导率;Ea为活化能;T为热力学温度;R为通用气体常数8.314;A为指前因子。通过研究不同温度下的离子电导率,研究lgσ与温度的倒数的线性关系,获得斜率k×(-8.314)×ln10÷96.5 kJ/mol 得出活化能(eV)。
电化学稳定窗口测试采用Li|聚合物电解质(PEO 或G/PEO)|SS 纽扣电池,在Modulab XM DSSC型光电化学测试系统上对电解质进行线性扫描伏安法测试,电压扫描范围为2~6 V,扫描速率为0.1 mV/s。交流阻抗测试:采用上海辰华仪器有限公司生产的CHI660E 型电化学工作站和英国输力强精密测量公司生产的Modulab XM DSSC 型光电化学测试系统进行交流阻抗(electrochemical impedance spectroscopy,EIS)测试。测试条件如下:频率范围为100 kHz~100 mHz,振幅为5 mV/s。充放电循环测试:采用深圳新威电子有限公司产生的BTS7.6.x 型电池测试系统对纽扣电池进行恒流充/放电测试以获得相应的充/放电比容量、循环性能和倍率性能等信息。对于使用LFP正极片所组装的全电池,其测试条件为2.5~4.2 V。对于使用NCM811 (深圳科晶智达股份有限公司)正极片的电池,其测试条件为3.0~4.3 V。
2 结果与讨论
2.1 明胶/PEO复合电解质的制备与结构
G/PEO 复合电解质的制备流程如图1(a)所示。得益于PEO 与明胶良好的相容性,其形成的复合电解质具有优异的成膜性,且由于明胶具有较强的硬度,所制备的G/PEO 电解质具有显著的机械强度和柔韧性。即使多次折叠,电解质膜的形态仍保持完好,这表明其具有良好的柔韧性[图1(c)]。
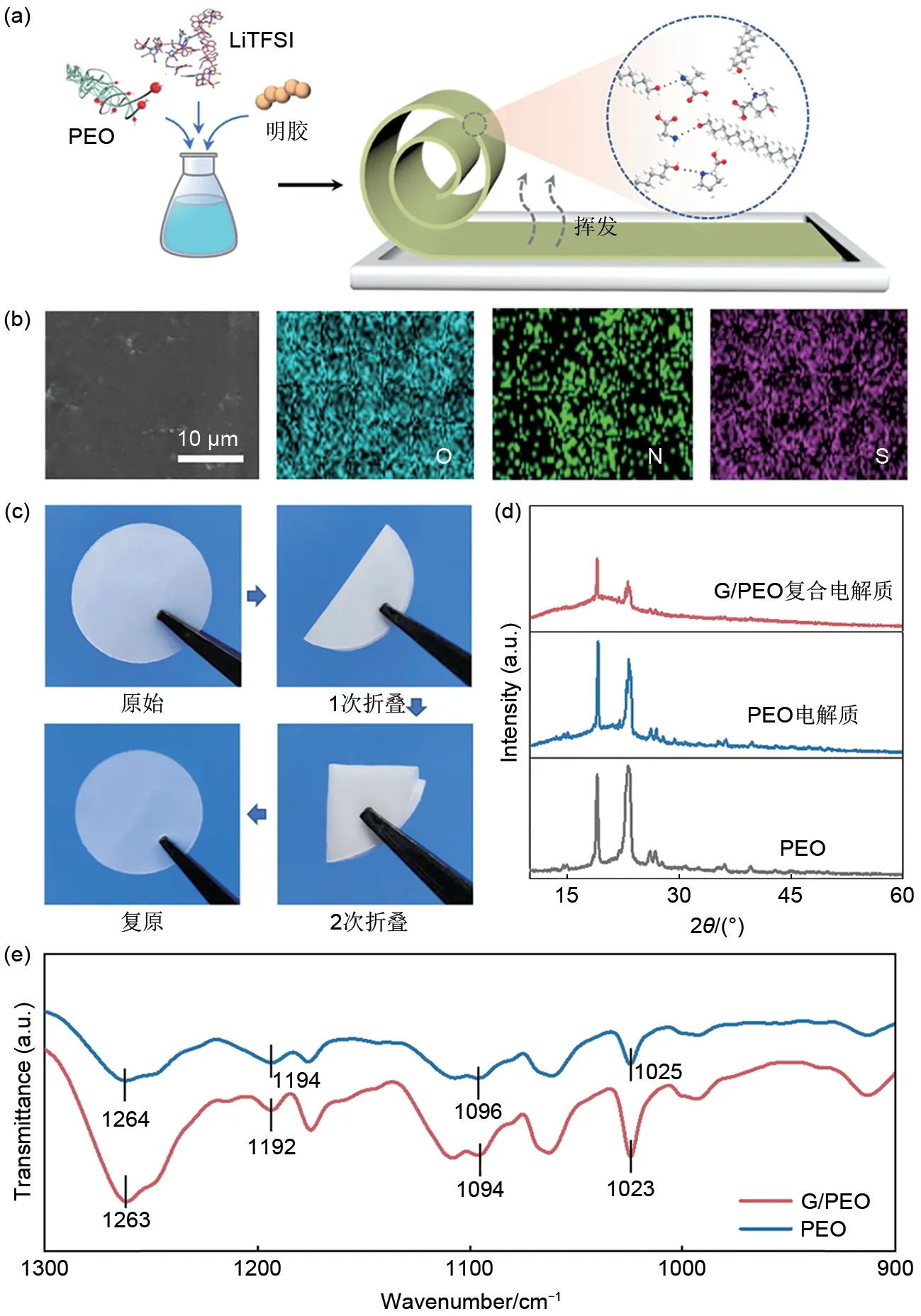
图1 (a) G/PEO电解质的制备工艺示意图;(b) G/PEO电解质SEM和EDS元素图像;(c)光学数码照片显示了G/PEO的柔韧性;(d) PEO、PEO电解质和G/PEO复合电解质的XRD图谱;(e) PEO、G/PEO电解质的红外光谱Fig.1 (a) Schematic diagram of the preparation process of G/PEO electrolyte; (b) SEM and EDS elemental images of G/PEO electrolyte; (c) Optical digital photos show the flexibility of G/PEO; (d) XRD patterns of PEO,PEO electrolyte, and G/PEO electrolyte; (e) FTIR spectrum of PEO and G/PEO electrolyte
为了考察所制备复合电解质的表面形貌,通过扫描电子显微镜(SEM)和能量色散光谱仪(EDS)对G/PEO 电解质膜进行形貌表征。SEM 图像显示[图1(b)],G/PEO 电解质膜表面平整,平整的表面有利于电解质与电极的界面接触以及使锂离子更加均匀地沉积,从而减少锂枝晶的产生。EDS图谱显示O、N、S 元素均匀地分布于电解质中,表明明胶及无机锂盐均匀分散于PEO 中[图1(b)]。PEO、PEO 电解质和G/PEO 复合电解质的X 射线衍射(XRD)测试结果如图1(d)所示。PEO 在19.1°和23.3°展示出两个尖锐的衍射峰,表明了其具有高结晶度。当添加LiTFSI 后,所形成PEO 电解质的衍射峰位置向低角度方向轻微移动[15-16],且峰值强度降低[图1(d)]。当进一步加入明胶后,特征峰的强度降低[17],表明明胶与PEO 的混合降低了PEO的结晶度,有利于锂离子在聚醚链上跳跃传输[16]。图1(e)展示了PEO 电解质与G/PEO 电解质的红外光谱,可以看出在加入明胶后,PEO 的特征峰(1300~900 cm-1段)吸收峰都有所增强,并且特征峰都向低波数移动,这说明了明胶与PEO 之间有氢键作用。
2.2 明胶/PEO复合电解质的电化学特性
为研究明胶的加入对复合电解质电化学性能的影响,对制备的复合电解质进行电化学表征。组装SS对称电池(SS|G/PEO|SS及SS|PEO|SS)并进行EIS测试。根据图2(a)的测试结果可以发现,G/PEO的本征阻抗比PEO更小,表明G/PEO电解质具有更低的电阻。从图2(b)的离子电导率柱状图可得知,G/PEO和PEO电解质在60 ℃下的离子电导率分别为3.51×10-4S/cm 和2.43×10-4S/cm,意味着明胶蛋白质大分子的加入能够提高PEO 基电解质的离子电导率,这是由于明胶大分子的加入有利于降低PEO的结晶度,明胶/PEO开辟形成的聚合物快速传导锂离子导电路径有利于锂离子跳跃传输,从而提高了离子导电性,复合固态电解质具备高的离子传输速率,促进了电池电化学性能的提升。

图2 (a) PEO和G/PEO电解质在60 ℃下的电化学阻抗谱和 (b) 离子电导率; 25~80 ℃下 (c) G/PEO与 (d) PEO的离子电导率;(e) PEO和G/PEO的活化能和 (f) LSV曲线Fig.2 (a) Electrochemical impedance spectroscopy and (b) ion conductivity of PEO and G/PEO electrolytes at 60 ℃; The activation energies of (c) G/PEO and (d) PEO were calculated using the Arrhenius equation at 25—80 ℃; (e) Activation energy and (f) LSV Curve of PEO and G/PEO
PEO 和G/PEO 电解质在不同温度下的离子电导率如图2(c)、(d)所示,随着温度的提升,两种电解质的离子电导率相应提升。值得注意的是,在不同温度下G/PEO 复合电解质的离子电导率均高于传统PEO 电解质。通过对不同温度下的离子电导率进行线性拟合,结合Arrhenius公式算出离子跃迁活化能。随着明胶的引入,复合电解质的离子跃迁活化能(Ea)相比于传统PEO 电解质从0.63 eV 降至0.43 eV [图2(e)],有利于锂离子在聚合物链中的跃迁。为了解复合电解质的电化学窗口及耐压性能,采用线性扫描伏安法(LSV)进行表征,PEO和G/PEO电解质的LSV测试结果如图2(f)所示。相比于PEO电解质的低电化学稳定窗口(4.0 V左右),G/PEO电解质的电化学稳定窗口由4.0 V扩展到4.8 V,可能是明胶与PEO链之间的相互作用使复合电解质具备更宽的耐压窗口。具有4.5 V 以上的高分解电压是G/PEO复合固态电解质能较好兼容匹配高压正极材料的前提条件,有效提升了固态锂电池的能量密度。
2.3 基于明胶/PEO复合电解质的高电压固态锂电池性能
为了验证G/PEO 在高电压固态锂电池中的实际应用潜力,研究了Li|LFP 和Li|NMC811 全电池的电化学性能。众所周知,为保证固态电池的循环稳定性,LFP 正极与PEO 匹配的测试电压窗口不高于4.0 V。为了证明G/PEO的耐高电压性能,设置Li|G/PEO|LFP电池截止电压为4.2 V进行恒电流充放测试。Li|G/PEO|LFP 在3.0~4.2 V 和2.5~4.2 V测试窗口下(60 ℃,0.1 C)分别提供110.3 mAh/g和130.1 mAh/g 的可逆放电比容量,180 次循环后依然具有稳定的电压分布特性和126.0 mAh/g的放电比容量,表明电池具有较好的高压稳定性[图3(a)]。为了对比,在相同的条件下组装了匹配传统PEO电解质的Li|PEO|LFP电池。如图3(b)所示,Li|PEO|LFP电池在首次循环中提供113.0 mAh/g的容量后逐渐衰减,这是因为PEO 电解质在高电压下的氧化分解导致的。相比之下,Li|G/PEO|LFP电池在0.1 C下100 次循环后显示出114.2 mAh/g 的平均可逆容量和超过92.2%的平均库仑效率[图3(b)],这表明基于G/PEO 复合电解质的高电压固态锂电池循环稳定性取得了实质性的提升。

图3 (a) 3.0~4.2 V和2.5~4.2 V下的Li|G/PEO|LFP电池;(b) 2.5~4.2 V下的Li|PEO|LFP和Li|G/PEO|LFP电池;(c)3.0~4.3 V下Li|PEO|NCM811和Li|G/PEO|NCM811电池;(d) Li|PEO|LFP和 (e) Li|G/PEO|LFP电流密度为0.1 C时的电压分布图Fig.3 (a) Li | G/PEO|LFP batteries at 3.0—4.2 V and 2.5—4.2 V; (b) Li|PEO|LFP and Li|G/PEO|LFP batteries at 2.5—4.2 V; (c) Li|PEO|NCM811 and Li | G/PEO|NCM811 batteries at 3.0—4.3 V; (d) Voltage distribution diagram of Li|PEO|LFP and (e) Li|G/PEO|LFP at a current density of 0.1 C
为进一步验证复合电解质在高电压全电池体系中的电化学性能,将G/PEO 复合电解质与高压三元正极材料相匹配,当G/PEO与高压正极材料(例如NCM811)配对时仍可以获得良好的可逆放电比容量,由此进一步证实了明胶的加入提升了PEO电解质的高电压性能。结果表明,Li|G/PEO|NCM811 电池在3.0~4.3 V下提供144.9 mAh/g的初始放电比容量[图3(c)]。活化后,放电比容量达到186.1 mAh/g,并在100次稳定循环后具有73.3%的容量保持率,这明显优于在相同条件下组装和测试的Li|PEO|NCM811全电池。与PEO 电解质形成鲜明对比的是,Li|G/PEO|LFP 和Li|G/PEO|NCM811 全电池的充电曲线没有检测到“电压噪声”行为[图3(d)和3(e)],证明了G/PEO在循环过程中的高电压稳定性。
2.4 明胶/PEO复合电解质的耐高电压机理
通过分析G/PEO和PEO在长期高电压环境下的稳定性,对深入理解电解质失效及耐压特性具有重要意义。分别对G/PEO和PEO电解质组装的SS|Li电池进行了电压浮动测试。
如图4(a)所示,两种电解质体系在低于4.0 V时均呈现出相似的电流泄漏分布。然而,当电压超过4.2 V 时,PEO 电解质组装的SS|Li 电池展现出泄漏电流增加与较大波动,这表明PEO 电解质发生氧化副反应[18],这种不稳定的反应导致容量迅速衰减[19]。相比之下,由G/PEO 电解质组装的电池保持稳定的低响应泄漏电流至4.4 V,这种极小的漏电流证实了G/PEO 的高压稳定性,保证了电池的长循环寿命。为进一步评估复合电解质在高电压下长期运行的电化学稳定性,在图4(b)和4(c)中记录了G/PEO 和PEO 电解质在60 ℃、4.6 V 下施加恒定直流偏压后的阻抗谱。在12 h 和24 h 后,SS|G/PEO|Li电池的阻抗没有明显变化。相比之下,SS|PEO|Li电池的阻抗明显增加,这表明,G/PEO电解质具有较高的氧化电位,有效减少界面氧化副产物,可以与高压正极相匹配。

图4 (a) G/PEO和PEO在3.8~4.4 V下的高电压浮动测试;(b) SS|G/PEO|Li和 (c) SS|PEO|Li电池在60 ℃下在4.6 V偏压下不同时间的EIS变化;(d) PEO和G/PEO的FTIR光谱;(e) PEO、甘氨酸、脯氨酸、羟脯氨酸和丙氨酸的ESP表面静电势(红色区域和蓝色区域分别表示负电荷和正电荷)Fig.4 (a) High voltage floating test of G/PEO and PEO at 3.8—4.4 V; (b) The EIS changes of SS|G/PEO|Li and(c) SS|PEO|Li batteries at different times under 4.6 V bias at 60 ℃; (d) FTIR spectra of PEO and G/PEO; (e) ESP surface electrostatic potentials of PEO, glycine, proline, hydroxyproline, and alanine (red and blue regions represent negative and positive charges, respectively)
通过傅里叶变换红外光谱(FTIR)研究了G/PEO的结构变化[图4(d)]。在PEO 和G/PEO 的电解质中都检测到2880 cm-1的主峰,对应于主链重复单元中碳-氢键(C—H)的拉伸振动[17]。值得注意的是,加入明胶后,PEO链的端—OH基团(3446 cm-1)的红外吸收峰显著减弱[20]。这表明明胶的加入极大地抑制了PEO 链段中的—OH 端基氧化,这与Yang等人[21]使用稳定的—OCH3基团代替PEO 中的末端—OH将聚合物电解质的电化学稳定窗口从4.05 V增加到4.3 V的结果一致,同时与G/PEO高电压电化学测试结果相呼应。
为了进一步理解G/PEO 复合电解质在分子水平上结构与性能的关系,采用密度泛函理论(DFT)从分子轨道能级的角度计算了PEO、明胶的主要组分(甘氨酸、脯氨酸、羟脯氨酸和丙氨酸)的静电势面(ESP)、最低未占据分子轨道(LUMO)和最高已占据分子轨道(HOMO)能级。ESP计算研究了各分子的电荷分布[图4(e)],结果表明甘氨酸、脯氨酸、羟脯氨酸和丙氨酸分子的负电荷集中在羧基的氧原子上,PEO 链的正电荷集中分布于链端的羟基的氢原子中,分子表面静电势正值区域倾向于接触负值区域,而且正值越正、负值越负时这种倾向越强[22]。具体地,PEO的正电势中心(1.18 eV)与明胶中组分占比最多的甘氨酸分子的负电势中心(-1.24 eV)能量的绝对值趋同,表明两分子间存在较强的氢键作用力[23]。HOMO能级计算表明(图5),PEO矩阵具有较高的最高已占据分子轨道(HOMO)能级(-6.75 eV),证明了其在高电压下的不稳定性。甘氨酸(-7.56 eV)、脯氨酸(-7.29 eV)、羟脯氨酸(-7.02 eV)和丙氨酸(-7.56 eV)的HOMO 能级均低于PEO,表明电子难以跃迁[24],由多种氨基酸组成的明胶及G/PEO电解质具有优异的高电压耐受性。

图5 DFT理论计算得到的PEO、甘氨酸、脯氨酸、羟脯氨酸和丙氨酸的HOMO和LUMOFig.5 HOMO and LUMO of PEO, glycine, proline, hydroxyproline, and alanine calculated by DFT theory
理解G/PEO 在高电压环境中电解质/正极界面相的演变同样重要,为此对搁置于不同高电压状态下的电池进行了研究。具体地,将组装好的Li|G/PEO|NCM811搁置于60 ℃烘箱环境中,分别施加4.3 V、4.6 V的高电压并保持15 h。为了对比,在同样条件下组装了Li|PEO|NCM811 全电池,给予同样强度和相同时间的电压施加。在施加15 h的高电压后,对Li|G/PEO|NCM811、Li|PEO|NCM811全电池进行了拆卸,用X射线光电子能谱技术(XPS)分析了NCM811 正极与电解质界面相的化学特征。如图6(a)、(d)所示,高分辨率C 1s 谱表明C—C(284.8 eV),C=O (286.5 eV),—CF2(290.7 eV)均出现在PEO和G/PEO高电压搁置前的正极/电解质界面处[17],在给定高电压搁置后PEO和G/PEO匹配的正极界面均出现O—C=O (288.6 eV),—CF3(293.1 eV)新特征峰,且施加电压前出现的C—C、C=O、—CF2特征峰的峰强度和峰面积都有所增加[25]。G/PEO 样品的新特征峰强度均弱于PEO 匹配的NCM811正极[图6(b)、(e)],这可能是电极/电解质固相萃取剥离后含有LiTFSI 及其PEO 分解产物黏附在NCM811 电极表面所致。值得注意的是,在4.3 V搁置15 h后,PEO匹配的NCM811电极界面相上出现HOOC(CH3)(C6H5)CH3(286.1 eV)相关的新峰[17,26][图6(b)],且随着搁置电压升高至4.6 V,该特征峰的峰强度和峰面积均有所增加[图6(c)],这些峰属于不饱和短链醚羰基、酯等基团,其可能是NCM811三元正极与电解质界面之间的氧化分解产物,PEO 电解质在高电压下易氧化分解形成离子电导率差且不稳定的CEI层,导致高的电池内阻和低的库仑效率。相反,无论在4.3 V 还是4.6 V时,G/PEO电解质匹配下的NCM811电极表面形成的分解产物均较少[图6(e)、(f)],这意味着G/PEO电解质匹配的Li|G/PEO|NCM811 电池在正极/电解质界面上的副反应较少,提升了界面稳定性。

图6 (a)~(c) Li|PEO|NCM811和 (d)~(e) Li|G/PEO|NCM811高电压搁置15 h后正极界面组分C1s的XPS图谱Fig.6 (a)—(c) XPS spectra of positive electrode interface components C1s after high voltage storage for 15 hours for Li|PEO|NCM811 and (d)—(e) Li|G/PEO|NCM811
3 结 论
本文设计制备了一种可耐高电压明胶/PEO 复合电解质,通过实验分析并结合理论计算,评估了电解质匹配高压正极NCM811的电化学稳定性,并揭示了界面化学特征。结果表明,在大于4.0 V 时PEO 电解质链端羟基氧化分解是充放电曲线产生“电压噪声”行为的主要原因,加入明胶后,结合傅里叶变换红外光谱表征、XPS和理论计算,揭示了明胶中的氨基酸分子与PEO 链之间的氢键作用力提高了聚醚链段端羟基结构稳定性,使电解质在4.0~4.3 V状态下的氧化副反应得以减缓。同时,大分子明胶改变了PEO电解质的结晶度,G/PEO电解质中形成了快速的Li+导电路径,从而提高了离子导电性。本工作为简便构建耐高电压固态电解质及高能量密度固态锂电池的合理设计提供了有价值的指导。

