氯化钠-硫酸钠/硅基相变材料的热物性研究
袁子鸥,王 峰,祁星朝,张 琦,马剑龙,唐忠锋
(1.内蒙古工业大学能源与动力工程学院,内蒙古呼和浩特 010051;2.中国科学院上海应用物理研究所,上海 201800)
随着工业快速发展和环保政策不断收紧,工业废盐(主要是NaCl和Na2SO4)排放量剧增,引发严重的环境问题[1-3]。工业废盐主要采用填埋、中高温热解碳化、中高温氧化和高温熔融等无害化或资源化处置方法,其中将工业废盐在高温热解下碳化,再经过滤和蒸发结晶最终制得纯度高的NaCl 和Na2SO4等无机盐产品成为未来废盐处置的主要方式[4-6]。但该处置工艺复杂,单位质量废盐处置能耗高、成本高,不满足未来工业快速发展的要求,已成为制约废盐资源化利用的瓶颈问题。随着“双碳”目标的提出和新能源快速发展,使用温度范围宽、热容量高、热稳定性和化学稳定性优异的熔盐成为研究的热点[7-10]。如能将工业废盐中含有的NaCl或Na2SO4的高温碳化与熔盐制备同步处置无疑是具有重要意义的,该工艺既能缩短工艺流程、节能环保,又能提高废盐的附加值,为废盐的资源化利用提供一条新途径,具有重要的意义。
研究者将NaCl 或Na2SO4与MgCl2、Na2CO3、CaCl2、KCl、ZnCl2等单盐制备成熔盐,该方法为废盐或固废处置提供了一种新的思路[11-16]。由于NaCl-Na2SO4熔盐本身的腐蚀性极强,对结构材料的耐腐蚀要求高,将其直接用作传蓄热工质容易出现泄漏等一系列问题。为解决以上问题,采用耐熔盐腐蚀的氧化物、碳化物等多孔无机材料与熔盐复合制备成相变材料是实现储能应用和废盐处置的有效方法[17-19]。MILIOZZI等[20]将硅藻土和NaNO3-KNO3混合制备了复合材料,得到了能量密度高和成本低的复合储能材料。MITRAN 等[21]将NaNO3-KNO3与介孔SiO2负载制备相变材料,研究发现2.76 nm的纳米孔限制效应导致其结晶相的熔点和结晶点降低,该复合材料具有单一的熔点和结晶相。吴建锋等[22]将NaCl 与SiC 泡沫复合制备高温复合相变材料,研究发现NaCl 与SiC 化学相容性好,相变温度为801.6 ℃,其相变潜热为157.9 kJ/kg。QIAN等[23]将硅藻土和Na2SO4混合制成的相变材料具有高潜热和高热稳定性的特点,工作温度区间宽且其腐蚀性得到大幅度改善。综上所述,目前未见采用NaCl-Na2SO4共晶熔盐与无机多孔材料制备相变材料的研究,关于该相变材料的热物性及结构变化更是未见报道。
本研究主要目的是实现工业废盐中NaCl 和Na2SO4的无害化或资源化处置。考虑到直接以工业废盐中的NaCl 和Na2SO4为原料制备共晶熔盐的过程包含有机物去除、脱碳、除杂等一系列问题,工艺过程冗长、影响因素复杂且有机物去除和脱碳等机制还不清晰,因此,本研究主要集中在NaCl-Na2SO4共晶盐制备和负载多孔材料方面。以分析纯NaCl和Na2SO4为原料,开展NaCl-Na2SO4共晶盐制备工艺研究,分别采用介孔MCM-41 和微孔13X 硅基材料作为NaCl-Na2SO4共晶盐的载体,制备出NaCl-Na2SO4/硅基相变复合材料。通过对比不同硅基多孔材料负载NaCl-Na2SO4前后的结构及热物性变化,分析载体孔结构对共晶盐熔融及相变过程的影响,探究微纳尺度下限域效应对共晶盐热物性的影响机制。本文为NaCl 和Na2SO4等工业废盐的无害化或资源化处置提供重要的理论数据和支撑,具有重要的实际应用价值。
1 实验部分
1.1 原料
NaCl(纯度>99%)、Na2SO4(纯度>99%)。选择介孔MCM-41 和微孔13X 硅基材料作为载体,其组分及结构参数见表1。

表1 硅基多孔材料Table 1 Porous silicon-based materials
1.2 制备方法
在100 ℃下分别将NaCl和Na2SO4干燥2 h,称取干燥后的NaCl 6.39 g 和Na2SO413.61 g 进行混合研磨,在650 ℃下熔融并恒温保持6 h,自然冷却结晶后将NaCl-Na2SO4研磨成粉末,放置在恒温干燥箱中干燥待用。称取两份7.0 g NaCl-Na2SO4分别与3.0 g MCM-41和3.0 g 13X混合研磨,将其放置在加热炉中升温至680 ℃并恒温8 h,自然冷却结晶后取出样品,并将其标记为MCS(MCM-41 为载体)和XCS(13X为载体)。
1.3 样品表征及性能测试
采用BRUKER D8 型X 射线粉末衍射仪对样品进行表征,测试条件为Cu靶、衍射角范围为2θ=10°~80°、扫描速率为15(°)/min。
采用SU8020 型场发射扫描电镜和FEI Talos F200X 型场发射透射电镜对样品进行测试,结合EDS能谱面扫对样品进行分析。
利用同步热分析对样品进行TG-DSC 测试,在N2气氛、温度范围为室温~800 ℃、升温速率为10 ℃/min条件下进行测试。
2 结果与讨论
2.1 物相及晶体结构变化
图1 为NaCl-Na2SO4共晶盐及负载熔盐前后样品的XRD 谱图。从图1 可知,对NaCl-Na2SO4共晶盐而言,其中2θ在19.03°、28.02°、28.99°、32.12°、38.61°、48.78°处的峰为Na2SO4结晶峰,2θ在27.33°、31.69°、33.82°、45.44°、56.47°、66.22°、75.30°处的峰为NaCl结晶峰;无定型相MCM-41硅基多孔材料在20°~30°为无序宽峰;2θ在11.78°、15.46°、18.43°、20.13°、23.23°、26.64°、30.93°、33.65°、40.85°、42.66°处的峰为硅基多孔材料13X 的X 型沸石特征峰;与NaCl-Na2SO4熔盐共混高温煅烧后,MCS及XCS样品主要衍射峰没有出现明显的减弱,结果说明MCS和XCS 中存在结晶盐相,该共晶盐与多孔硅基复合材料共存,高温负载过程中无化学反应变化,复合材料中无新物质生成。

图1 NaCl-Na2SO4共晶盐及相变复合材料的XRD谱图Fig.1 XRD patterns of NaCl-Na2SO4 eutectic salt and composites
2.2 微观形貌
图2为熔盐及硅基材料负载熔盐前后的SEM和EDS 图。图2a 是NaCl-Na2SO4共晶盐的SEM 图,从图2a 可以得出,颗粒表面光滑,有明显晶界和稳定的结构;从图2b 可以看出,MCM-41 呈细颗粒团簇状;负载NaCl-Na2SO4共晶盐再经过煅烧后(图2c),MCM-41 表面的细颗粒团簇状结构被破坏,表面平整度降低,熔盐进入硅基材料孔隙中,两者形成致密结构。与EDS1 相比,EDS2 中出现了Na,这在一定程度上表明该熔盐已经成功地负载在MCM-41表面形成致密结构。从图2d可以看出,硅基材料13X呈规则的八面笼状、颗粒分散均匀;负载NaCl-Na2SO4共晶盐再经过煅烧后(图2e),13X 的八面笼状结构被破坏,表面平整度降低,表面形成熔盐负载的结构。通过EDS3和EDS4的对比发现,EDS4中清晰观察到Na,说明钠基盐已成功负载在多孔材料上。产生以上现象的原因主要是共晶盐与硅基材料高温煅烧到680 ℃后,液态熔盐与硅基材料的润湿性好,通过孔的毛细作用进入到不同的孔径中,填充了原硅基材料MCM-41 和13X 间的间隙,原有孔隙被致密的熔盐覆盖形成以上的SEM 形貌。对负载熔盐后的不同硅基材料进行对比发现,由于MCM-41 的比表面积大、孔径尺寸大且具有长程有序的孔道结构,导致熔盐更容易进入到负载材料中,形成均一的复合材料结构,这在一定程度上能有效地降低高温熔盐在高温相变过程中的泄漏,减小对结构材料的腐蚀[24]。

图2 NaCl-Na2SO4(a)、MCM-41(b)、MCS(c)、13X(d)和XCS(e)的SEM微观形貌图及MCM-41(EDS1)、MCS(EDS2)、13X(EDS3)和XCS(EDS4)的EDS图Fig.2 SEM micrographs of(a)NaCl-Na2SO4,(b)MCM-41,(c)MCS,(d)13X and(e)XCS,EDS images of(EDS1)MCM-41,(EDS2)MCS,(EDS3)13X and(EDS4)XCS
图3为MCM-41、13X和负载熔盐后样品的TEM照片。从图3a 可以观察到硅基材料MCM-41 具有明显的有序孔结构[25]、孔径均一、孔隙形貌明显;从图3b 可以看出,MCS 基本保持了介孔结构,熔融盐均匀分布在其孔道内;从图3d观察到13X颗粒表面粗糙,但由于13X其孔径微小和笼形孔道的限制,观察到的孔结构不明显,在以往关于13X的TEM形貌表征测试中可以观察到相似的结果[26];以13X 为载体的复合材料XCS的TEM图见图3e,同样可以观察到熔融盐分布在孔结构内,与13X 骨架明显不同的是XCS 堆叠方式发生了改变。图3c、f 分别为MCS和XCS 在高分辨率透射电子显微镜(HRTEM)下的晶格条纹图和选区电子衍射图。图3c 显示MCS 的Na2SO4面心立方结构(FCC)的(313)和(131)晶格面特征间距为0.173、0.276 nm;图3f 显示XCS 的Na2SO4的(220)晶格面的特征间距为0.220 nm。与MCS相比,XCS只存在一种晶格面,同时熔盐在负载材料中的分布不如MCS 均匀。这主要是因为在烧结过程中,载体材料的熔化温度高于相变材料的相变温度,熔融状态下的共晶盐变成液态,在毛细管作用下进入多孔材料颗粒间的孔隙,同时由于硅基材料本身的稳定性高,可依靠多孔骨架保持形状的稳定,因此熔盐未对孔结构造成破坏,硅基多孔材料仅起到了定型和支撑的作用。

图3 MCM-41(a)、MCS(b)、13X(d)和XCS(e)的TEM图及MCS(c)和XCS(f)的晶格条纹和选区电子衍射图Fig.3 TEM images of(a)MCM-41,(b)MCS,(d)13X and(e)XCS and Lattice fringes and selected area electron diffraction patterns of(c)MCS and(f)XCS
2.3 熔点、比热容及热稳定性变化
图4 是NaCl-Na2SO4、MCS、XCS 样品的DSC 曲线。从图4可以看出,NaCl-Na2SO4盐有单一的熔融尖峰,其熔点为623 ℃,与相图预测的理论共晶熔点626 ℃基本一致,表明制备的NaCl-Na2SO4为共晶熔盐[27]。共晶盐和复合材料的热物性数据汇总见表2,MCS 熔点为618 ℃、XCS 熔点为607 ℃,表明硅基材料的加入使共晶盐的熔点略有降低。其中MCS维持单一熔融峰,载体的引入对熔盐相变结晶过程影响不大,NaCl-Na2SO4与硅基材料两者同时结晶或者熔化,表明负载后材料稳定性更好[28-29]。XCS 的熔融峰出现双重峰,表明XCS 中载体与盐出现了两相结构,不具备良好的共晶性[30],这主要是由于硅基材料13X的微孔级的孔径和笼状孔道结构产生的限域效应,限域效应在一定程度上阻碍了孔道内NaCl-Na2SO4的共晶,导致XCS在相变过程中的动力学过程缓慢,未形成更好的共晶结构[21,31]。
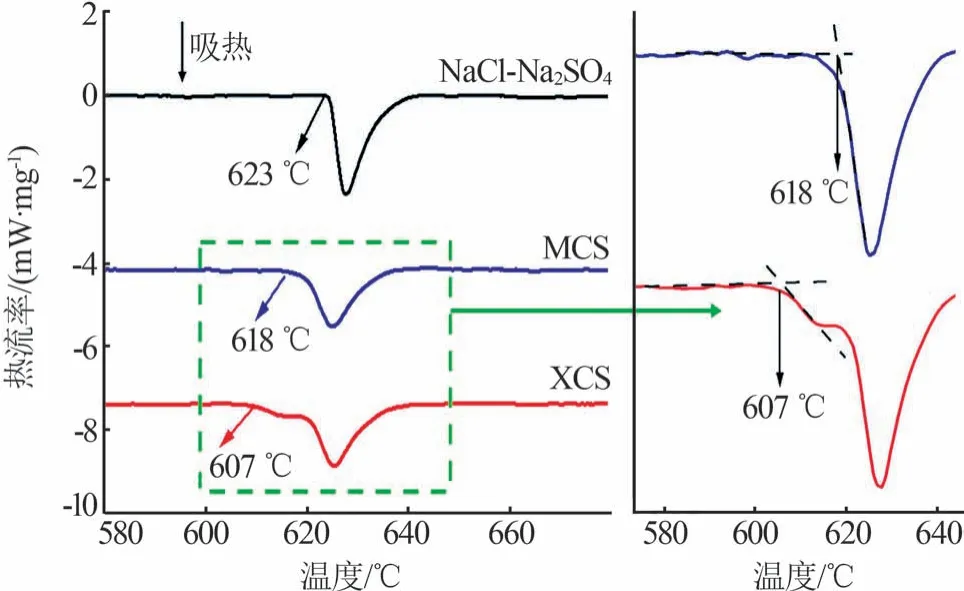
图4 NaCl-Na2SO4共晶盐及复合材料的DSC曲线Fig.4 DSC curves of NaCl-Na2SO4 eutectic salts and composites

表2 共晶盐和复合材料的热物性数据Table 2 Thermal properties of eutectic salt and composites
图5 是NaCl-Na2SO4共晶盐及复合材料的比热容随温度的变化规律,样品的平均比热容见表2。从图5可以看出,在350~500 ℃时,硅基材料负载熔盐后的固态比热容随温度的增加呈逐渐下降趋势,在相同温度下共晶盐的比热容高于MCS 和XCS。对比表2 中复合材料MCS 和XCS 的平均比热容,发现随着硅基材料的孔径减小,其比热容呈降低的趋势。这主要是由于硅基材料的热传导性差,硅基多孔骨架结构阻碍材料内部的传热速率。其中MCS的比热容略大于XCS样品,主要归因于MCM-41较大的孔径和长程有序孔道结构更有利于内部的热传导过程,这一结果与EDS结果相吻合。

图5 NaCl-Na2SO4共晶盐及复合材料的比热容曲线Fig.5 Specific heat capacity curves of NaCl-Na2SO4 eutectic salts and composites
图6a 为NaCl-Na2SO4共晶盐及复合材料的TG曲线。由图6a 可知,NaCl-Na2SO4的分解点温度为756 ℃、MCS 的分解点温度为840 ℃、XCS 的分解点温度为797 ℃,分解温度由高到低依次为MCS、XCS、NaCl-Na2SO4。图6b 为样品在700、800、900 ℃时质量损失随温度变化图。由图6b 可知,NaCl-Na2SO4的质量损失较为严重,在900 ℃下质量损失率为14.11%;MCS在高温700~900 ℃下基本没有发生明显的质量损失,稳定性高。多孔硅基复合材料在高温下的分解温度高于NaCl-Na2SO4且质量损失率低于NaCl-Na2SO4,这主要是由于多孔硅基材料的热稳定性高,孔结构的存在可以阻碍体系内热量的传递,共晶盐在多孔硅基材料的微孔道中不易发生分解,从而提高了复合相变材料的热稳定性[32-35]。
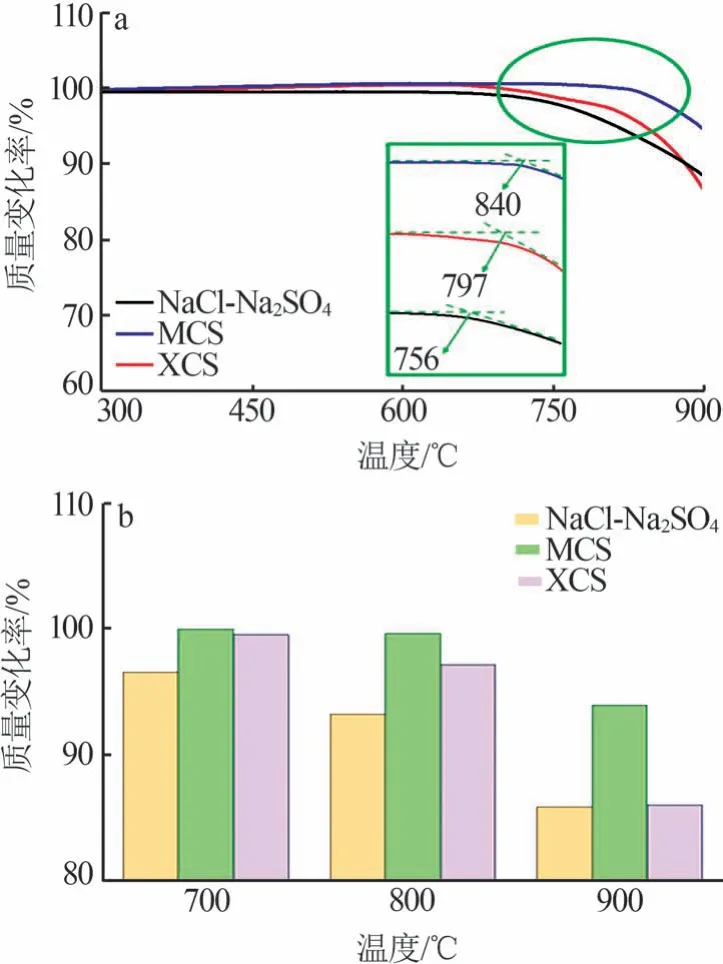
图6 NaCl-Na2SO4共晶盐和复合材料的TG曲线(a)及高温下质量损失随温度的变化(b)Fig.6 (a)TG curves of NaCl-Na2SO4 eutectic salts and composites,(b)bar plot of weight loss as a function of temperature at elevated temperatures
根据样品的质量损失情况可知,与MCS 相比,XCS 在700 ℃和800 ℃下的质量损失率明显低于NaCl-Na2SO4,但在900 ℃出现了与NaCl-Na2SO4相同的质量损失现象。这主要归因于13X 的孔径较小,笼状孔结构不易于吸附更多的熔盐导致盐的负载量少(与EDS结果相对应),其中一部分盐聚集在孔道内,另一部分盐吸附在孔表面边界处。附着在硅基材料表面的盐在700 ℃和800 ℃时先发生了分解,900 ℃时孔道内的盐也逐渐分解。MCS 的长直孔和相对较大的孔径可负载更多熔盐,表现出在高温下更低的质量损失率。
3 结论
针对主要成分为NaCl 和Na2SO4的工业废盐废弃量大、腐蚀性强,后处理成本高的问题,以NaCl和Na2SO4为基盐制备了NaCl-Na2SO4共晶盐,并将其与不同尺寸的硅基材料制备复合材料,以实现熔盐在储能领域中的应用。研究发现,NaCl-Na2SO4熔盐成功负载到硅基材料中,负载熔盐后的硅基材料MCS和XCS 中存在结晶盐相,负载过程中硅基材料和熔盐均未发生化学变化。与NaCl-Na2SO4共晶盐相比,制备的MCS 熔点为618 ℃、分解温度为840 ℃,XCS 熔点为607 ℃、分解温度为797 ℃,复合材料的熔点略有降低,高温下热稳定性大幅度提升,复合材料的温域扩大。负载熔盐后的硅基材料在高温下结构稳定,高温下多孔硅基材料骨架能改善熔盐的热稳定性并起到定型作用。本研究通过简单的制备方法降低了NaCl-Na2SO4熔盐服役过程中强腐蚀性,为强腐蚀性废弃盐在储能领域中的应用提供一种研究方法。后续将逐步研究含不同杂质离子单盐对熔盐共晶及相变材料制备的影响,解释复合材料的热物性变化规律,进而逐步实现工业废盐在储能领域中的应用。本文为工业废盐的无害化高温处置技术提供新的发展路径,具有重要的科学意义和实际应用前景。

