不同养殖阶段的大口黑鲈肠道结构和肠道微生物组成变化的比较
李鸣霄 强 俊,* 徐钢春 周国勤 张茂友 陶易凡 路思琪 李 岩 陆 健 徐 跑,*
(1.南京农业大学无锡渔业学院,无锡 214081; 2.中国水产科学研究院淡水渔业研究中心,农业部淡水渔业与种质资源利用重点实验室,无锡 214081;3.南京市水产科学研究所,南京 210036;4.苏州水产技术推广站,苏州 215008)
过去20年里全球对水产品的需求量迅速增长,而过度捕捞导致了天然渔业资源急剧下降,这就促使水产养殖的快速发展[1]。随着对水产动物营养需求的研究不断深入,人工饲料的配方越来越完善,营养越来越全面,具有生产周期短、成本低、安全性高等优点,饲喂人工配合饲料可以减小对养殖水体的污染,改善水产动物肌肉营养水平、提高免疫力、降低疾病发生率等[2-3]。目前大口黑鲈养殖模式可以分为4个阶段,分别为仔鱼期卤虫诱导开口、稚鱼期使用微量配合饲料驯化转食、幼鱼期投喂人工配合饲料直至成熟个体[4-5]。然而,在苗种培育阶段依旧存在死亡率高的问题,成为制约鱼类苗种产业发展的主要瓶颈之一[6-7]。
近年来,许多专家学者针对鱼类苗种培育的影响因素开展了相关研究,包括饲料的喂养方式、转食的开始时间和持续时间等。例如,梭鲈(Sanderlucioperca)鱼种可在孵化后第15天开始饵料驯化,降低了对消化能力或消化道发育的不利影响[4];而海鲈鱼(Dicentrarchuslabrax)应在第20天进行驯化工作,有助于提高鱼种的发育、存活和消化酶活性[8]。此外,转食成功率也受到配方饲料营养成分的影响[9]。大口黑鲈(Micropterussalmoides),又名加州鲈,属鲈形目、太阳鱼科、黑鲈属,原产于北美洲。大口黑鲈拥有快速的生长速度、广泛的温度耐受性和对新环境的适应可塑性,被认为是优质食物来源而引入中国,并成为中国重要的水产养殖鱼类之一。2021年年产量近70.21万t[10],相比于2020年增长了13.33%。目前,针对满足大口黑鲈营养需求的人工配合饲料的开发已经较为完善,但有关苗种饲养和食性转变的认知深度有限,苗种培育阶段的大口黑鲈死亡率和生产成本仍然很高,极大地限制了产业的快速发展。因此,进一步研究大口黑鲈对于饵料改变的适应与调控有助于优化苗种培育过程,提高养殖存活率。
研究表明,在鱼类仔稚鱼养殖过程的高死亡率可能是由病原微生物引起的高发病率疾病所造成的[11-12],而关于改善水产养殖中鱼种健康状态的研究大多集中在益生菌调控[13-14]和加强养殖水处理[15]上,很少研究鱼类养殖中与宿主相关微生物的多样性和功能[11],这阻碍了我们对鱼类发育阶段中微生物群落建立的理解。在动物肠道中,微生物群落处于一种不断动态变化的状态,而其组成结构受到宿主特征(如年龄、免疫和遗传特征等)[16-17]、环境(如水体、饮食和药物等)[18-19]以及微生物(如黏附能力、酶和代谢能力)等因素的影响[20]。因此,针对动物肠道微生物群组成及结构特征的变化情况将备受关注。16S rDNA是一种对特定环境样品中所有细菌进行的高通量测序技术,以研究环境样品中微生物群体的组成,解读微生物群体的多样性、丰富度以及群体结构,该技术被认为是最适于细菌系统发育和分类鉴定的指标[21]。本研究通过16S rDNA高通量测序技术,对不同养殖阶段的大口黑鲈肠道微生物群进行分析,并通过组织切片观察和消化酶活性测定比较不同养殖阶段之间大口黑鲈肠道发育和消化功能的改变,有助于更好地了解大口黑鲈食性转变的肠道生理过程,也为大口黑鲈的苗种培育提供理论依据和参考。
1 材料与方法
1.1 饲养与管理
试验用鱼选自中国水产科学研究院淡水渔业研究中心宜兴基地的刚孵化2 d的卵黄囊仔鱼,在圆形水泥池中饲养。参考大口黑鲈苗种培育模式,出膜平游后第3天开始投喂丰年虫,也称为卤虫(含有41%~62%粗蛋白质,2%~8%粗脂肪),持续到第11天。该阶段选择在04:00—22:00进行投喂,第1天间隔2 h投喂1次,幼鱼开口后逐渐延长间隔时间至6 h投喂1次。鱼苗摄食后头部往后均为红色,可以此判断鱼苗的饥饱情况,日投饵料为鱼体重的40%~70%,前期高,后期低。
从第12天开始,对鱼苗投喂卤虫和商品饲料(含有48%粗蛋白质,5%粗脂肪)的混合饮食,其中商品化微量饲料的比例缓慢增加(每天增加4%的商品饲料),持续到第36天,此时的大口黑鲈已完全使用商品饲料投喂。随后大口黑鲈在循环水系统中继续使用商品饲料饲养,直至成长为成熟个体(试验周期为6个月),期间根据鱼体大小及时调整饲料的口径。该阶段每天在07:00、12:00和17:00 3个时间点投喂。商品饲料购自无锡某生物科技有限公司。
整个适应和养殖期间水质参数如下:温度为(28±1) ℃;溶解氧含量>6.0 mg/mL;pH为7.2~7.6;氨氮含量<0.1 mg/L;亚硝酸盐含量<0.01 mg/L。
1.2 试验设计及样品采集
在养殖第5、25、45和180天,随机选取20尾大口黑鲈样本,分别代表开口摄食期、转食人工配合饲料期、适应人工配合饲料期以及成鱼养殖期4个不同阶段。用100 mg/L MS-222预先麻醉,快速解剖取出肠道组织(第5天仔鱼由于体积太小,不能完整的取出肠道组织,故将整条鱼作为1个样本),立即置于液氮中快速冷冻并储存在-80 ℃冰箱中,用于后续肠道消化酶活性测定。在4个阶段再各挑选大口黑鲈16尾,麻醉后采集肠道组织,置于液氮中快速冷冻并-80 ℃保存,用于肠道微生物16S rDNA测序。另外,再随机挑选共20尾大口黑鲈(每个阶段5尾),麻醉后解剖,截取肠道中段,保存于4%多聚甲醛中,用于制作肠道切片(第5天仔鱼采用整鱼纵切的方式,而对第25、45和180天的大口黑鲈肠道进行截面横切)。
1.3 肠道组织切片
肠道样品在4%多聚甲醛固定24 h后,酒精梯度脱水,二甲苯透明,石蜡包埋后,使用YD-202型切片机切片,厚度为6~8 μm,苏木精-伊红(HE)染色,中性树胶封片,在Eclipse Ci-L(Nikon,日本)拍照显微镜下观察并摄像。成像完成后使用Image-Pro Plus 6.0分析软件(Media Cybernetics Corporation, 美国)统一以毫米作为标准单位,分别测量每张切片中4根完整绒毛高度。
1.4 肠道消化酶活性测定
取约1.0 g肠道样品在冷冻的磷酸盐缓冲液(PBS,50 mmol/L,pH=7.4)中研磨,然后在4 ℃下3 000×g离心20 min,吸取上清液用于测定肠道消化酶活性。淀粉酶、胰蛋白酶和脂肪酶活性参照Qiang等[22]方法进行测定。
1.5 肠道微生物16S rDNA测序
1.5.1 DNA的提取和高通量测序
按照DNA提取试剂盒E.Z.N.A.®Water DNA Kit(Omega Bio-Tek,Norcross,美国)的说明,从采集的4个阶段,共64个肠道样本中提取总基因组DNA,使用1%琼脂糖凝胶电泳检测提取的DNA。将各个阶段每2个肠道DNA混合成为1个样本,建立4组文库,分别命名为5dph(孵化后天数)、25dph、45dph和180dph,选用特定引物341F(5′-ACTCCTACGGGAGGCAGCAG-3′)和806R(5′-GGACTACHVGGGTWTCTAAT-3′)进行PCR扩增。PCR扩增过程如下:98 ℃预变性30 s;接着98 ℃变性10 s,54 ℃退火30 s,72 ℃延伸45 s,持续进行35个循环;循环结束后72 ℃最终延伸10 min。将PCR产物利用琼脂糖凝胶电泳进行检测,判断扩增后的DNA浓度是否达到了试验扩增要求。测序在杭州联川生物技术股份有限公司Illumina(Kapa Biosciences, Woburn,美国)的平台上进行。
1.5.2 高通量测序结果初筛和数据分析
样品在Illumina Nova-Seq平台上进行测序,使用FLASH合并匹配端读取。在特定的过滤条件下根据FQTRIM(v 0.94)对原始数据进行质量过滤以获得高质量的clean data。所有数据统计分析均使用QIIME2软件和R软件(v 3.5.2),调用Vsearch9(v 2.3.4)软件检查并剔除嵌合体序列。通过SILVA(release 132)分类器对所得到的特征序列(features)进行分类比对,使用QIIME2软件,获取各样本在门、纲、目、科、属5个分类水平上的组成和丰度分布,对feature丰度矩阵中每个样本的序列总数在不同深度下随机抽样,以每个深度下抽取到的序列数及其对应的feature数绘制稀疏曲线,并对每个样本计算α-多样性指数,包括Chao1、Observed species, Shannon、Simpson指数及覆盖率。采用Blast进行序列比对,每个代表性序列用SILVA数据库对特征序列进行注释。
1.6 统计分析
本试验中使用SPSS 22.0软件进行分析。用The Shapiro-wilk和The Levene检验肠道绒毛高度和消化酶活性的正态性和方差的同质性,再应用one-way ANOVA进行单因素方差分析,根据Duncan氏法进行多重比较确定组间差异。此外,使用R包绘制稀疏曲线,使用QIIME2软件进行β-多样性和主坐标分析(PCoA)以评估样品之间物种复杂性的差异,再使用Kruskal-Wallis H检验确定4个阶段之间α-多样性和分类水平上丰度差异的显著性,使用Galaxy平台(https://galaxyproject.org)对所有检测到的细菌类群的丰度进行线性判别分析(LDA)效应大小(LEfSe)分析。在所有分析中,P<0.05表示为差异显著,数据均以平均值±标准差表示。
2 结果与分析
2.1 不同养殖阶段的大口黑鲈肠道结构变化
4个阶段的肠道切片如图1-A所示,其中第5天(a-1)肠道壁结构界限模糊,黏膜下层没有发育完全,杯状细胞等数量稀少,而第25(b-1)、45(c-1)和180天(d-1)肠道组织结构清晰,均由黏膜层、黏膜下层、肌层和浆膜组成,杯状细胞等黏液细胞数量显著增多,且主要分布于肠绒毛前端或近前端。此外,如图1-B和表1所示,4个阶段大口黑鲈的肠道绒毛高度存在显著差异(P<0.05),对比于开口摄食阶段的大口黑鲈,转食、适应人工配合饲料和成鱼养殖3个阶段的大口黑鲈的肠道绒毛高度分别增加105%、218%、1 248%。

A图中,BB:纹状缘;CM:环肌;GC:杯状细胞;IV:肠绒毛;LM:纵肌;SCE:单层柱状上皮;Se:浆膜;SM:黏膜下层;TP:固有膜。B图中,红色箭头标注的红色细线代表肠道绒毛高度。In the figure A, BB: brush border; CM: circular muscle; GC: goblet cell; IV: intestinal villus; LM: longitudinal muscle; SCE: single columnar epithelium; Se: serosa; SM: sub mucosa;TP: tunica propria. In the figure B, the thin red line marked by the red arrow represents the height of the intestinal villus.

表1 不同养殖阶段的大口黑鲈肠道绒毛高度的变化
2.2 不同养殖阶段的大口黑鲈肠道消化酶活性变化
如表2所示,与开口摄食(第5天)卤虫相比,转食人工配合饲料阶段(第25天)的大口黑鲈3种消化酶活性都出现了显著下降(P<0.05),而在第45天,适应了人工配合饲料的大口黑鲈肠道消化酶活性又出现回升,显著高于第25天(P<0.05),但其中淀粉酶活性要显著高于第5天大口黑鲈仔鱼(P<0.05)。到了第180天成鱼养殖期,大口黑鲈肠道中3种消化酶活性均达到最高值,但蛋白酶活性与第5天大口黑鲈相比并未表现出显著差异(P>0.05),淀粉酶活性与第45天大口黑鲈相比也未表现出显著差异(P>0.05)。

表2 不同养殖阶段的大口黑鲈肠道消化酶活性的变化
2.3 肠道微生物
2.3.1 16S rDNA测序数据与排序
在过滤、质量控制、引物、嵌合体和低置信度的数据去除后,本研究使用了来自4个文库,32个样本的总共1 721 562个clean data,平均每个样品约有53 799个序列读数。32个样本中的特征序列features数量达到了1 825,各组的features数分别为599(5dph)、841(25dph)、402(45dph)、550(180dph)。基于读数之间97%的相似性阈值对其进行聚类,鉴定出19个细菌门,34个纲,73个目,146个科和336个属。如图2所示,每个样品中肠道菌群的测序深度都被完全捕获,因此证实本研究数据的真实可靠,所有样品都适合进一步分析。
2.3.2 不同养殖阶段的大口黑鲈肠道微生物α-和β-多样性分析
本研究计算了4个α-多样性指数(Chao1、Observed species、Shannon和Simpson指数)(图3),这些指标代表了微生物群落的丰富度和多样性。结果发现,第25天大口黑鲈稚鱼肠道中微生物的α-多样性指数显著高于其他3组(P<0.05)。
此外,通过评估β-多样性,以量化4个阶段之间肠道微生物群落组成的差异,采用基于加权和未加权矩阵的PCoA,根据肠道微生物群落组成研究样品间的关系。如图4的PCoA图所示,每个符号代表了样品的肠道微生物群,其中第1主成分和第2主成分的贡献率分别为15.55%和10.56%,37.00%和27.82%。图中4组样本之间的圆点分布离散,样本95%置信区域距离较大,表明随着食性的改变和个体的发育,4个阶段大口黑鲈的肠道微生物群组成呈现显著的不同。

图2 不同养殖阶段的大口黑鲈肠道样品的

*:P<0.05;**:P<0.01。下图同 the same as below。

a:未加权距离矩阵主坐标分析 PCoA of unweighted UniFrac distance matrix;b:加权距离矩阵主坐标分析 PCoA of weighted UniFrac distance matrix。
2.3.3 不同养殖阶段的大口黑鲈肠道细菌门相对丰度变化
为了探究不同养殖阶段的大口黑鲈肠道内菌群组成之间的变化差异,从门水平进行了分析。肠道菌群中12个最丰富features的相对丰度由累计柱状图(图5-a)表示。其中变形菌门(Proteobacteria)相对丰度最高,占所有肠道微生物的90.61%。其他如厚壁菌门(Firmicutes)、梭杆菌门(Fusobacteria)、软壁菌门(Tenericutes)和拟杆菌门(Bacteroidetes)这4种细菌门分别占比为4.38%、2.34%、1.88%、0.44%。与第5天相比,第25天厚壁菌门相对丰度更丰富(图5-b)。此外,拟杆菌门(图5-c)和软壁菌门(图5-d)分别是第5和45天肠道菌群组成中特有的,它们在其他3组中相对丰度极低甚至没有(图5-b~图5-d),但梭杆菌门相对丰度(图5-e)在4组之间并未表现出显著差异。

图5 不同养殖阶段的大口黑鲈肠道中细菌门相对丰度
2.3.4 不同养殖阶段的大口黑鲈肠道细菌属相对丰度变化
在属(图6-a)水平上,比较了12个优势菌群的相对丰度,发现第5天大口黑鲈肠道内,气单胞菌属(Aeromonas)处于最优势地位,占所有肠道微生物的93.45%,而随着大口黑鲈的不断发育和食性的改变,肠道菌群组成中该属的占比不断减少,分别为33.72%、23.52%和1.72%(图6-b),在第180天大口黑鲈肠道中完全退出优势地位。假单胞菌属(Pseudomonas)是第25和45天大口黑鲈肠道中共有的优势菌群,却在另外2组大口黑鲈肠道中相对丰度占比极低(图6-c)。第25天大口黑鲈肠道中还出现了37.64%的不动杆菌属(Acinetobacter)和5.83%的乳球菌属(Lactococcus)(图6-d),虽然第45天肠道中也出现了不动杆菌属,但相对丰度较低。此外,第45天大口黑鲈肠道中还存在7.42%的支原体(Mycoplasma)、5.82%的芽孢杆菌属(Bacillus)和16.99%的肠杆菌属(Enterobacter)。发育成为成熟个体(第180天)后,在大口黑鲈肠道内发现了多个新优势菌群,分别为邻单胞菌属(Plesiomonas)、大肠埃希菌属-志贺氏菌属(Escherichia-Shigella)、克雷伯氏菌属(Klebsiella)、鲸杆菌属(Cetobacterium)和柠檬酸杆菌属(Citrobacter),占比分别为37.85%、23.21%、17.19%、9.00%和6.23%。

图6 不同养殖阶段的大口黑鲈肠道中细菌属的相对丰度
2.3.5 不同养殖阶段的大口黑鲈肠道细菌种类变化
LDA效应大小LEfSe方法用于比较4个阶段之间大口黑鲈肠道中所有检测到的细菌类群的相对丰度。经多次试验调整后的Kruskal-Wallis秩和检验(P<0.05)和效应量分析(LDA评分>4)后检测所有特征物种,确定了31、20和36个细菌分类群在3个比较组(LB5dph vs. LB25dph、 LB25dph vs. LB45dph、 LB45dph vs. LB180dph)中有显著差异(图7~图9)。其中相比于第5天大口黑鲈,大多数变形菌门(61.90%)和所有的厚壁菌门在第25天的相对丰度更高(图7);在食性转变过程中,厚壁菌门和变形菌门在第25天相对丰度更高,而第45天软壁菌门的相对丰度更高(图8);到了第180天成鱼阶段,肠道中厚壁菌门和软壁菌门相对丰度降低,未表现出显著差异,而存在半数的变形菌门在该阶段的相对丰度更高(图9)。

a:LEfSe分析产生的分类学分支图,图中亮度和每个分类单元的丰度成正比;b:通过Kruskal-Wallis检验(P<0.05),LDA评分>4,直方图中显示的分类群丰度显著不同。绿色:变形菌门中的细菌;红色:厚壁菌门中的细菌;蓝色:软壁菌门中的细菌;紫色:放线菌门中的细菌;黄色:其他门中的细菌。下图同。a:taxonomic cladogram produced from LEfSe analysis, brightness is proportional to abundance of each taxon;b: taxa shown in histogram are determined to differ significantly by Kruskal-Wallis (KW) sum-rank test (P<0.05) and have LDA score>4, the abundance of taxa shown in the histogram is significantly different. Green: bacteria in Proteobacteria; Red: bacteria in Firmicutes; Blue: bacteria in Tenericutes; Purple: bacteria in Actinobacteria; Yellow: bacteria in other phyla. The same as below.
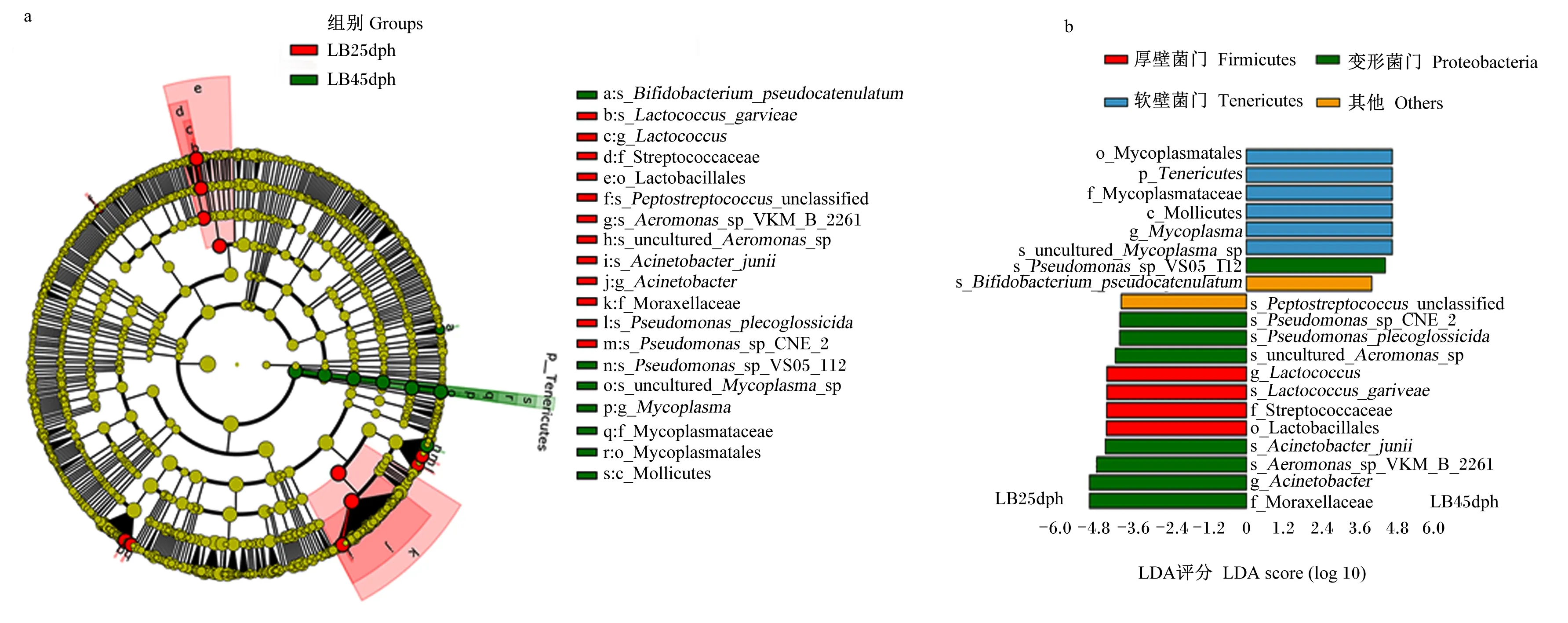
图8 线性判别分析效应大小分析比较了第25和45天2个阶段之间大口黑鲈肠道中已确定的细菌类群的丰度

图9 线性判别分析效应大小分析比较了第45和180天2个阶段之间大口黑鲈肠道中已确定的细菌类群的丰度
为了确定哪些细菌受到转食人工配合饲料的影响,我们计算了变形菌门、厚壁菌门和软壁菌门下细菌物种的相对丰度(图10、图11)。试验发现,在第5天大口黑鲈中相对丰度更高的是变形菌门中的3个细菌物种,分别是粪杆菌属某种(Faecalibacterium_sp.)、豚鼠气单胞菌(Aeromonas_caviae)和维氏气单胞菌(Aeromonas_veronii);第25天大口黑鲈中相对丰度更高的是变形菌门中3个细菌物种,分别是琼氏不动杆菌(Acinetobacter_junii)、假单胞菌属某种-CNE-2(Pseudomonas_sp._CNE_2)和变形假单胞菌(Pseudomonas_plecoglossicide),以及厚壁菌门中的1个细菌物种,格氏乳球菌(Lactococcus_garvieae);第45天大口黑鲈中相对丰度更高的是变形菌门中的2个细菌物种,分别是不动杆菌属某种(Acinetobacter_sp.)和蒙氏假单胞菌(Pseudomonas_monteilii),以及软壁菌门中的1个细菌,未培养-支原体属某种(uncultured_Mycoplasma_sp.);第180天相对丰度更高的是变形菌门中的3个细菌物种,分别是弗氏柠檬酸杆菌(Citrobacter_freundii)、克雷白氏杆菌属-未分类(Klebsiella_unclassified)、邻单胞菌属-未分类(Plesiomonas_unclassified)和大肠埃希菌-志贺氏菌属-未分类(Escherichia_Shigella_unclassified),但细菌Escherichia_Shigella_unclassified相对丰度在4组之间并未存在显著差异(P>0.05)。另外,气单胞菌属某种-VKM-B-2261(Aermononas_sp._VKM_B_2261)和未培养-气单胞菌属某种(uncultured_Aeromonas_sp.)在第5和25天大口黑鲈肠道中都存在,相对丰度显著高于其他2组(P<0.05),而未培养-不动杆菌属某种(uncultured_Acinetobacter_sp.)和假单胞菌属某种-VS05-112(Pseudomonas_sp._VS05_112)在第25和45天大口黑鲈肠道中都显著表达(P<0.05),但两者之间不存在显著差异(P>0.05)。

图10 不同养殖阶段的大口黑鲈肠道中变形菌门下选定细菌物种的相对丰度
3 讨 论
3.1 不同养殖阶段的大口黑鲈肠道发育及3种消化酶活性变化
肠道是鱼类整个消化系统里最长的一段区系,是鱼类消化吸收营养物质的主要场所[23-24],肠道形态结构的正常发育是鱼类肠道消化吸收功能和免疫屏障功能正常的重要保证。在本试验中,从肠道组织切片观察发现,开口摄食阶段(第5天)大口黑鲈肠道刚刚开始发育,各层结构界限模糊,但第25、45和180天肠道形态结构可以明显的区分,且随着养殖时间的推移,黏膜层中柱状上皮细胞和杯状细胞显著增加,肠道绒毛高度也显著增加,其中微绒毛结构的完善大大增加了柱状上皮细胞的吸收能力,杯状细胞能分泌消化酶和黏液来水解食物和保护上皮细胞[25]。这些结果表明,随着养殖周期的延长,大口黑鲈肠道结构逐渐发育完善,褶皱增多,绒毛高度增加,接触表面积增大,对食物的消化吸收能力不断增强,有助于满足大口黑鲈生长发育的营养所需。

图11 不同养殖阶段的大口黑鲈肠道中厚壁菌门和软壁菌门下选定细菌物种的丰度
研究表明,消化酶随着鱼类生长发育而不断变化,消化酶的活性高低直接影响动物对饲料营养的利用程度,因此鱼类肠道中消化酶活性的变化能很好地反映鱼类生长状况[26]。在本试验中,从第5天开口摄食卤虫到适应人工配合饲料的第45天大口黑鲈,其肠道中淀粉酶、胰蛋白酶和脂肪酶活性均表现为先下降后上升的趋势,说明苗种培育过程中大口黑鲈肠道消化能力减弱,对摄入的营养物质吸收利用率降低,可能是由于第25天大口黑鲈稚鱼对摄食饲料的改变处于适应阶段,其中配合饲料的营养物质不易被直接消化吸收。而第5天大口黑鲈肠道消化酶活性高可能是因为摄入的卤虫通过自溶或作为激活大口黑鲈仔鱼内源性消化酶的酶原“供体”来协助消化过程[27]。因此,不同阶段的大口黑鲈肠道消化酶活性的改变可能是导致仔稚鱼死亡的原因之一[28]。此外,第45天大口黑鲈肠道淀粉酶活性显著高于第5天仔鱼,可能与肠道逐步发育和人工配合饲料中一定比例的淀粉含量对淀粉酶分泌具有的诱导作用有关[8]。
第180天大口黑鲈成鱼肠道消化酶活性最高,这可能是因为商品化配合饲料中各营养成分搭配合理,能够很好地满足大口黑鲈生长所需,有利于消化和吸收;以及大口黑鲈成鱼的可消化能需求量大,摄食量增加,肠道结构发育成熟,可以分泌大量的消化酶来分解食物[29-30]。但胰蛋白酶活性相比于第5天大口黑鲈未有显著差异,可能是因为卤虫富含大量动物蛋白质,在大口黑鲈生长发育中最优先被利用,需要更高的胰蛋白酶活性。
3.2 不同养殖阶段的大口黑鲈肠道中微生物群组成结构变化
肠道是一个复杂的系统,肠道中微生物与宿主之间存在专性共生和兼性寄生关系[31],它们在宿主的生长发育、营养代谢、免疫功能和抵抗病菌的入侵方面有着不可或缺的作用[32]。鱼类肠道菌群的数量和组成结构受许多因素的影响,其中摄食饲料对肠道微生物的影响最大[32]。因此,研究不同养殖阶段的大口黑鲈肠道中微生物群落组成的变化,可以了解大口黑鲈鱼种对食性转变的适应过程,以及肠道微生物在维持大口黑鲈肠道健康中的作用。
鱼类对饲料营养的需求与肠道菌群的组成密切相关[33]。人工配合饲料所使用的阶段及配比,在鱼体里面的消化吸收、中间产物以及自身携带的微生物等都不同,这些都显著影响着鱼类的肠道微生物种群结构[34]和肠道健康状况[25]。本试验中,第5、25、45和180天4个阶段的大口黑鲈肠道样本中微生物丰富度差异显著,开口摄食、转食和适应人工配合饲料,成鱼养殖4个阶段大口黑鲈的肠道微生物多样性也表现出明显的差异,其中第25天大口黑鲈肠道中有着最高水平的微生物多样性和丰富度,可能是因为摄食混合饲料的大口黑鲈肠道内环境适合更多的菌群定植。第45天的大口黑鲈肠道的微生物多样性和丰富度都要低于第5天仔鱼,这代表着人工配合饲料改变了大口黑鲈肠道中微生物群落的组成。郁二蒙等[35]研究也观察到类似的结果,对大口黑鲈鱼苗投喂冰鲜杂鱼和人工配合饲料,发现饲料组大口黑鲈肠道微生物多样性显著降低。多项研究表明,β-多样性指数随着饲料成分的改变而变化[36-37]。在本试验中,第5、25、45和180天大口黑鲈肠道样本的PCoA结果显示,食性转变和生长发育对大口黑鲈肠道微生物群落有着一定的影响,4个阶段的大口黑鲈样本之间距离较远,微生物组成结构差异性较大,这表明转食过程会影响到大口黑鲈肠道微生态结构,在其他受到摄食饲料变化影响的动物研究中也观察到类似的结果[38-39]。同时,本研究中某些微生物类群组成差异可能是我们使用了不同的采样方法(第5天仔鱼为整鱼样本,而第25、45和180天为肠道样本)所造成的。
在本试验中,4组大口黑鲈肠道中共鉴定出5个主要的细菌门类:变形菌门、厚壁菌门、梭杆菌门、软壁菌门和拟杆菌门。Desai等[40]对饲喂用植物蛋白质替代水产饲料中鱼粉的虹鳟(Oncorhynchusmykiss)肠道微生物组进行了鉴别,发现主要的细菌门为变形菌门、厚壁菌门、放线菌门和拟杆菌门。Zhu等[36]研究饲料蛋白质水平对吉富罗非鱼(Oreochromisniloticus)肠道菌群组成的影响时发现梭杆菌门、拟杆菌门、变形菌门和厚壁菌门4种主要的细菌门类。此外,李英英等[41]发现大黄鱼(Pseudosciaenacrocea)肠道中的主要菌门是变形菌门、厚壁菌门、梭杆菌门和拟杆菌门。不同研究鉴别出的细菌门类的相对丰度各不相同,这些差异的原因可能与饲料、性别、年龄、生长环境等有关[42-44]。
研究表明,肠道虽然是机体抵御病原体的第1道防线,但也被认为是病原微生物入侵的主要门户[45],因此,肠道功能和结构的完整性和稳定性对动物体健康至关重要。肠道中的细菌、真菌、原生动物和病毒等微生物以协同、拮抗或共生关系相互作用,形成稳定的肠道内环境[46]。稳定的肠道细菌群落是宿主抵抗病原菌入侵并发挥各种生物学功能的先决条件[47-48],但如果肠道微生物群失调,会引起肠道屏障通透性改变,内毒素分泌增加,诱导微生物群与宿主之间的稳态平衡向促炎状态转变[49-50]。在本试验中,细菌门分类水平上,4个阶段的大口黑鲈肠道微生物群组成差异不大,其中80%以上为变形菌门,这与Larsen等[51]研究结果类似,认为变形菌门是大口黑鲈“核心肠道微生物群”中最重要的一部分。但在细菌属分类中,4个阶段的大口黑鲈肠道微生物群组成表现出明显的差异,表明转食人工配合饲料引起了肠道微生物群的改变。大口黑鲈开口摄食卤虫,肠道内环境处于相应的稳态平衡,各系统和器官之间相互协调,肠道特有的屏障功能保护机体免受其他细菌和有毒物质的危害[52],但由于人工配合饲料的加入,肠道微生物群组成发生了改变,微生态平衡被打破,引起肠道屏障功能受损和免疫力下降,进而增加对病原菌的易感性[53-54],这可能是大口黑鲈苗种培育工作难度大、死亡率高的原因之一。
变形菌门是鱼类肠道中主要微生物门之一,在鱼类营养代谢中发挥重要的作用,而它们的生态失调与肠道代谢和炎症疾病有关[55-56]。在本试验中,大口黑鲈肠道中鉴定出属于该门的7个属类,分别是气单胞菌属、假单胞菌属、不动杆菌属、肠杆菌属、领单胞菌属、克雷伯氏菌属和柠檬酸杆菌属。其中气单胞菌属的相对丰度随着食性转变和发育在大口黑鲈肠道内发生了极显著的变化,第5天大口黑鲈仔鱼肠道中气单胞菌属相对丰度最高,且该属下2个菌种,豚鼠气单胞菌和维氏气单胞菌相对丰度显著高于第25天大口黑鲈稚鱼。Zhu等[57]发现,维氏温和气单胞菌、豚鼠气单胞菌和嗜水气单胞菌的混合感染会引起潘阳湖野生花鼓鱼(Hemibarbusmaculatus)的不断死亡。Van Zwetselaar等[58]研究也表明,尽管气单胞菌的致病性和毒力在该属物种之间有着较大的差异,但往往都与动物体胃肠道感染有关。因此,我们认为大口黑鲈仔鱼期死亡可能是高相对丰度的气单胞菌群引起的肠道感染所导致的。
在大口黑鲈的4个养殖阶段之间,第25天大口黑鲈肠道内变形菌门下假单胞菌属(变形假单胞菌)、肠杆菌属和不动杆菌属(琼氏不动杆菌)相对丰度表现更高。而变形假单胞菌是常见的水产生物致病菌,会诱发香鱼(Plecoglossusaltivelis)的岀血性腹水病[59]和斜带石斑鱼(Epinepheluscoioides)的内脏白点病[60]等;不动杆菌属也是一种重要的条件致病菌,当动物体抵抗力降低时易引发机体感染[61],其中琼氏不动杆菌可以与其他病原菌一起对石鲽(Kareiusbicoloratus)和牙鲆(Paralichthysolivaceus)有着较强的致病作用[62]。此外,其他肠道细菌如肠杆菌数量的上升也会使得肠道炎症反应持续存在[63]。因此,苗种培育过程中食性改变引起了第25天大口黑鲈肠道微生物的生态失调,进而诱导大口黑鲈对肠道炎症的易感性,而在这种受损的肠组织中,肠道细菌如假单胞菌和肠杆菌等可能会通过从成熟细胞中获取营养来快速生长,降低鱼体免疫力,从而使炎症反应持续下去[64],导致大口黑鲈的持续死亡。此外,本试验中,第25天大口黑鲈稚鱼肠道内厚壁菌门的相对丰度显著高于第5天大口黑鲈仔鱼,而厚壁菌门被证实在代谢紊乱的病理变化中发挥重要作用[65]。其中厚壁菌门下乳球菌属中格氏乳球菌在第25天大口黑鲈肠道中表现出较高相对丰度,它是乳球菌病的病原体,常常引起虹鳟[66]、梭鱼(Lizahaematocheila)[67]和牙鲆[68]的组织病变和出血性败血症等病症。
在本试验中,相比于第5和25天大口黑鲈,第45和180天鱼肠道中气单胞菌属相对丰度极低。其中第45天鱼肠道中蒙氏假单胞菌和软壁菌门中细菌相对丰度更高。蒙氏假单胞菌是革兰氏阴性菌,它产生的活性物质能对病毒产生钝化作用,使病毒粒体缺乏完整性,从而无法在寄主体内增殖,降低病毒的侵染能力[69],并具有利用多种油脂生长增殖的能力[70]。此外,第45天幼鱼肠道中还存在芽孢杆菌属,该属中某些种类在鱼体内能起到抗氧化的作用[71]。这些结果表明,适应了人工配合饲料的大口黑鲈,肠道中有益菌群相对丰度增加,有助于提高鱼体免疫力,抵御病原体的侵袭。虽然第180天和第45天大口黑鲈都饲喂人工配合饲料,但肠道微生物群落组成结构依旧具有一定的差异,这可能是受到饲料粒径、肠道发育和生理状态[72]等因素的影响。
4 结 论
本研究利用16S rDNA微生物多样性和肠道组织切片以及酶活性检测等手段,比较分析不同养殖阶段的大口黑鲈肠道结构和肠道微生物群组成。结果表明,随着大口黑鲈的养殖周期的延长,肠道结构不断完善,绒毛高度增大,褶皱增多,消化吸收功能增强。此外,食性转变和生长发育显著改变了大口黑鲈肠道消化酶活性和微生物群落组成,苗种培育初期转食人工配合饲料导致了肠道内环境稳态失调,变形假单胞菌、琼氏不动杆菌和格氏乳球菌等容易诱发肠道炎症和败血症的细菌相对丰度显著升高;但随着人工配合饲料的适应,大口黑鲈会调整进入新的稳态。本研究有助于更好地了解大口黑鲈苗种培育过程,但是关于人工配合饲料成分、肠道微生物和大口黑鲈代谢之间的复杂关系还需要进一步的研究来阐述。

