人参皂苷Rg3 抑制肿瘤微血管形成的研究进展
姜楠美,张源
(延边大学农学院,吉林 延吉 133002)
1 人参皂苷Rg3 概述
人参(Panax ginseng C.A.Mey.)属五加科多年生草本植物,也是一味药食同源的中药材,在亚洲一般被用作滋补剂。人参在现代医学中的治疗潜力已被广泛研究,人参皂苷是人参中的有效成分之一,是一种三萜皂苷类化合物,可影响机体多重代谢通路,也可抑制肿瘤微血管形成。研究发现,人参皂苷有广泛的抗癌、抗衰老、提高免疫力等功效[1],人参皂苷可以分成原人参二醇型、原人参三醇型和齐墩果酸型[2],人参皂苷Rg3为原人参二醇型人参皂苷。近几年,人参皂苷Rh1[3]、Rg1[4]、Rg3[5]、Rd[6]常被众多学者研究,人参皂苷Rg3可以抑制肿瘤细胞的增殖和转移。人参化学成分中有皂苷类物质,适当食用人参可以有效的预防肿瘤生成[7]。人参皂苷Rg3可以有效的被人体吸收,从而发挥增强人体免疫力、抑制肿瘤生长等作用[8],对于人体健康有很大益处。人参皂苷Rg3的主要提取方法有水提取法、超声波提取法、有机溶剂提取法、超临界流体萃取法等[9,10]。人参皂苷Rg3分子式为C42H72O13(图1)。人参皂苷Rg3还具有广泛的药理活性[11-13],例如抗肿瘤、抗心血管疾病、抗衰老、抗炎、抗病毒、抗疲劳和抗抑郁等作用。另外,人参皂苷Rg3可以作用于肿瘤细胞周围微血管,有效抑制肿瘤细胞有丝分裂前期ATP 的合成,阻断营养供给。也可作用于肿瘤细胞生长周期的G2 期[14],能够有效减缓肿瘤细胞生长速度,因此,人参皂苷Rg3具有抑制肿瘤细胞生长、抑制肿瘤细胞侵袭、抑制肿瘤微血管形成、促进肿瘤细胞凋亡等作用,进而直击癌细胞[15]。本文主要综述了人参皂苷Rg3抑制肿瘤微血管形成的研究进展,旨在为肿瘤患者提供治疗方案及人参皂苷Rg3在肿瘤领域的应用提供一定的参考,以期在未来提高肿瘤患者的临床疗效。
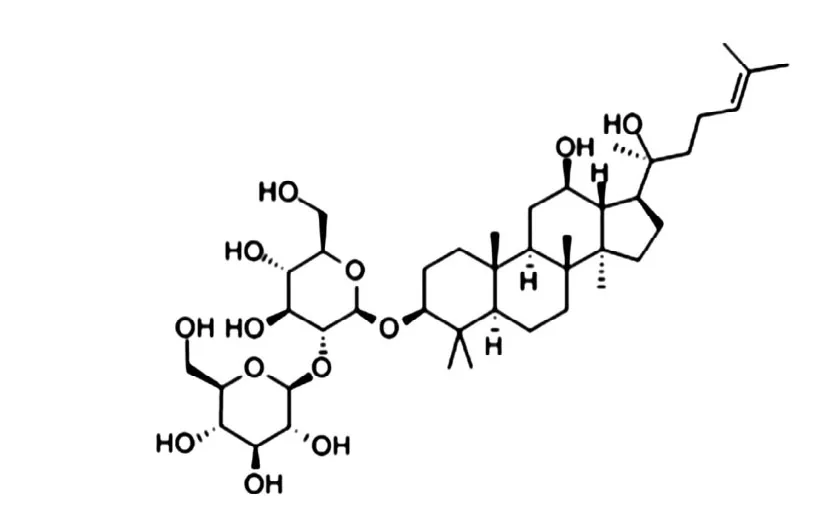
图1 人参皂苷Rg3 结构式Fig.1 Ginsenoside Rg3 structure formula
2 肿瘤微血管形成概述
微血管形成是肿瘤生长和转移较为重要的一步,因肿瘤细胞的生长离不开血液中的营养物质,微血管可以充当一个通道角色,为肿瘤传递营养物质,可见微血管的形成无疑有利于肿瘤细胞的生长繁殖。肿瘤微血管密度(MVD)是肿瘤微血管形成的标志之一,代表着肿瘤微血管形成强度[16]。血管内皮生长因子(VEGF)则是一种特异性有丝分裂原,与肿瘤的生长和转移也有一定联系,VEGF 信号是促微血管形成的重要调节因子之一,可以调节肿瘤微血管形成,进而促进肿瘤的生长。VEGF 对肿瘤微血管形成及通透性均有诱导效果[17]。肿瘤微血管形成是由与肿瘤相关的上皮细胞、内皮细胞和基质细胞释放的正负调控分子介导的。基质金属蛋白酶(MMPs)在肿瘤侵袭转移中发挥着关键作用,破坏肿瘤细胞侵袭的组织学屏障[18]。在肿瘤生成的早期,VEGF 可以诱导内皮细胞生成组织因子和MMPs,形成凝血酶并促进肿瘤细胞的增殖。肿瘤需要通过肿瘤微血管获得充足的血液及氧气,并将代谢产物排出[19]。肿瘤微血管形成的方式有很多,例如出芽式血管生成、套入式血管生成、募集内皮基质细胞的血管生成、血管生成拟态等[20]。肿瘤微血管生成首先要求开启血管生成开关,随后MMPs 表达,通过这一方式降解基底膜后,内皮细胞在促血管因子的作用下移至相应的部位后快速增殖,最后通过肿瘤基质细胞的支持形成肿瘤微血管。在这一复杂过程中,肿瘤细胞和肿瘤基质细胞发生相互作用,二者共同形成适合肿瘤微血管形成的微环境[21]。肿瘤微血管的形成过程非常复杂,其需要肿瘤细胞分泌肿瘤细胞基质金属蛋白酶等降解细胞外基质,然后释放促进微血管生成因子,让促血管因子的基数大于抑血管因子,从而促进肿瘤微血管的形成。还能募集宿主细胞至肿瘤部位,通过这些细胞分泌的各种促微血管形成因子来帮助肿瘤微血管形成[22]。另外,肿瘤细胞募集肿瘤基质细胞之后,就成为促微血管形成因子在内的各种细胞因子的主要来源,肿瘤微血管在此基础上形成[23]。肿瘤微血管形成也是一个多因素作用的结果,其与肿瘤的生长相互促进,如果能较好的抑制肿瘤微血管形成,减少肿瘤所需营养供应,那么在一定程度上可以更好的抑制肿瘤生长。
3 人参皂苷Rg3 抑制肿瘤微血管形成
人参皂苷Rg3抑制肿瘤微血管形成可以应用于众多恶性肿瘤[24],例如肺癌、肝癌、胃癌、乳腺癌和结肠癌等。人参皂苷Rg3与常规肿瘤治疗的联合疗法被认为更有效[25],人参皂苷Rg3提高肿瘤细胞对化学药物的化学敏感性,逆转多重耐药性并降低毒性。人参皂苷Rg3抑制肿瘤微血管的形成,有效降低了营养成分的传递,降低了癌细胞的存活率。因此在肿瘤生长过程中,抑制肿瘤微血管形成是抑制肿瘤生长和转移的关键一步。几种促微血管形成因子、抗微血管形成因子和相关信号通路均有助于调节肿瘤微血管的形成。肿瘤微血管形成的关键是血管内皮生长因子受体2(VEGFR2)的信号传导,VEGFR2 在与其主要配体VEGF相互作用时被激活[26]。因此,VEGF 或VEGFR2 的下游信号传导包括PI3K/AKT,可能是抑制肿瘤微血管形成药物开发的潜在关键点[27,28]。目前,临床批准的抗血管生成药物是针对VEGF 的抗体[29],限制肿瘤治疗。因此,开发有效的低毒性治疗方法可能具有更少的脱靶效应,临床副作用更少。人参皂苷Rg3可以抑制肿瘤微血管形成,对肿瘤及其细胞的生长起到干预作用,这些结果使人参皂苷Rg3成为一种很有潜力的肿瘤预防和治疗候选物[30]。
3.1 肺癌
人参皂苷Rg3抑制肿瘤微血管形成防治方法已被用于肺癌。陶涛等[31]通过动物试验证明了人参皂苷Rg3对于晚期或淋巴转移肺癌具有治疗作用。王柯等[32]通过建立Lewis 肺癌小鼠移植瘤模型,评估人参皂苷Rg3联合GP 的抗肿瘤作用,其抑瘤作用可能与干预Nrf2 信号通路和CD62P 的表达相关,也证实了人参皂苷Rg3可增强GP 对Lewis 肺癌小鼠肿瘤生长及肿瘤新生血管形成的抑制作用。Che 等[33]发现人参皂苷Rg3可延长裸鼠存活期,由于肿瘤组织生长致密且内压高,肺癌药物不易输入,抑制肿瘤微血管的形成有利于药物的输入,对肺癌细胞生长具有很好的抑制作用,表明人参皂苷Rg3对肺癌治疗效果显著。Jung 等[34]归纳总结了人参皂苷抗肺癌分子信号机制,我们可以进一步了解人参皂苷Rg3通过抑制肿瘤微血管形成所发挥的抗肺癌作用。
3.2 肝癌
治疗早期肝癌的首选办法是手术切除,但手术切除不适用于较大的肿瘤,且不适用于晚期肝癌。当肿瘤微血管不受控制形成时,肝癌细胞会迅速生长。因此,抑制肿瘤微血管形成被认为是抑制肝癌增殖和迁移的有效手段[35]。王爱红等[36]通过建立小鼠肝癌模型,根据处理方式不同进行分组,记录各组小鼠瘤重并计算抑瘤率,记录肿瘤微血管密度,并使用蛋白质印迹法(Western blot)检测瘤基质金属蛋白酶2(MMP2)、基质金属蛋白酶9(MMP9)、血管内皮生长因子蛋白表达,研究发现各治疗组小鼠肿瘤组织中MMP2、MMP9、VEGF蛋白表达量较模型组均下降,得出人参皂苷Rg3可有效抑制肝癌细胞生长增殖结论,其机制可能是抑制肿瘤微血管形成。方煊等[37]研究发现人参皂苷Rg3通过抑制肿瘤微血管形成及调节机体免疫对小鼠肝癌发挥抑制作用。唐琳琳等[38]表述了人参皂苷Rg3的抗肝癌作用,可以通过抑制肿瘤微血管形成机制发挥抗肿瘤作用。郑淇予[39]研究发现人参皂苷Rg3抑制肝癌细胞增殖,为进一步开展人参皂苷Rg3抑制肿瘤微血管形成的临床前研究,提供了理论支持。总之,人参皂苷Rg3抑制肿瘤微血管形成对肝癌的发生及发展具有很好的抑制作用。
3.3 胃癌
由胃癌细胞产生的促微血管形成因子,引起许多新生微血管形成,并参与肿瘤生长和转移。因此,肿瘤微血管的形成可作为胃癌的预后因素。丁健[40]研究发现,人参皂苷Rg3在一定程度上抑制肿瘤微血管生成,抑制肿瘤转移。Heeok 等[41]对人参皂Rg3抑制肿瘤周围微血管形成,从而抑制胃癌的生长增殖进行了表述。Yang 等[42]研究发现人参皂苷Rg3可通过调节AKT等信号通路发挥抑制胃癌细胞增殖的作用。李烨婷等[43]以胃癌SGC7901 细胞进行试验,通过Western blot 等方法检测相关物质表达,证明了人参皂苷Rg3通过抑制Wnt/β联蛋白通路阻止胃癌SGC7901 细胞血管生成拟态形成。Hong 等[44]研究了MVD 与胃癌临床病理特征的相关性,表明在恶性肿瘤中,肿瘤微血管形成与肿瘤增殖和转移息息相关。从众多研究结果来看,人参皂苷Rg3可对胃癌细胞的增殖、侵袭及迁移起到良好的抑制作用。从作用机制分析,人参皂苷Rg3可以通过抑制肿瘤微血管形成来抑制肿瘤生长。
3.4 乳腺癌
人参皂苷Rg3可以通过抑制肿瘤微血管形成抑制乳腺癌细胞生长,发挥抗乳腺癌作用。王杰等[45]通过动物试验研究明,人参皂苷Rg3可抑制乳腺癌生长和转移,其机制可能与抑制MMP2、MMP9 和VEGF的表达及肿瘤微血管的生成有关。李红涛等[46]建立乳腺癌大鼠模型并进行分组,通过计算抑瘤率、记录MVD、检测VEGF 和MMP9 蛋白表达水平,发现人参皂苷Rg3对乳腺癌细胞增殖具有抑制作用,抑制肿瘤微血管的形成。黎国栋等[47]以MCF-7 对数生长期细胞进行对照试验和体外管道形成抑制试验,使用蛋白免疫印迹法检测人参皂苷Rg3对VEGF-A 和MMP9蛋白表达的影响,发现人参皂苷Rg3可以有效抑制MCF-7 细胞体外血管形成拟态的能力。更有试验研究表明,人参皂苷Rg3从不同方面发挥抗乳腺癌作用,抑制微血管的形成就是其中一种有效途径[48-50]。Zhang等[51]在试验中研究发现,人参皂苷Rg3通过抑制微血管的形成对乳腺癌生长产生抑制作用。
3.5 结肠癌
人参皂苷Rg3治疗结肠癌也具有显著疗效。胡倩华等[52]总结并分析了人参皂苷Rg3治疗结肠癌作用,如抑制结肠癌细胞生长、增殖、迁移,促进细胞凋亡及通过抑制肿瘤微血管形成改善肿瘤微环境。朱鸣等[53]开展临床研究发现,化疗联合人参皂苷Rg3治疗结肠癌,是通过调节血管内皮生长因子水平发挥作用,说明人参皂苷Rg3作为抗癌辅助药的显著功效。简捷等[54]研究也说明了人参皂苷Rg3显著的抗结肠癌功效,为其通过抑制肿瘤微血管发挥作用奠定理论基础。唐雨辰[55]总结了人参皂苷Rg3还可以通过抑制微血管生成和促进抗肿瘤免疫力的途径重新塑造肿瘤微环境,发挥抑制结肠癌细胞生长的作用。
4 前景与展望
在肿瘤的治疗方案中手术治疗、化疗和放疗最为常见,但手术治疗需要切开皮肤和组织,可能会导致出血、感染等并发症,而且并不会遏制某些肿瘤的转移。化疗和放疗对人体正常细胞具备较大杀伤力。由于手术切除治疗、化疗和放疗对患者的远期生存效果一般,找到防治恶性肿瘤新药物尤为重要。人参皂苷通过多种机制发挥抗肿瘤作用,其中,人参皂苷Rg3在体内外对不同类型的肿瘤均表现出显著的抗癌活性,人参皂苷Rg3抑制肿瘤机制主要包括抑制细胞增殖、转移和微血管形成。因为肿瘤的生长增殖需要营养的供给,所以人参皂苷Rg3通过抑制肿瘤微血管形成抗肿瘤应该被人们重视。人参皂苷Rg3无毒且耐受性良好,如能较好的应用在肿瘤领域,在未来将有望降低我国肿瘤发生率。
下一步应对人参皂苷Rg3的作用机制进行探索。例如,人参皂苷Rg3在人骨肉瘤细胞中诱导强烈的遗传毒性和DNA 损伤。这些遗传毒性作用是否与细胞周期停滞和细胞凋亡有直接相关。需要进一步研究确定协调不同信号通路的机制,来实现人参皂苷和常规肿瘤治疗的协同抗肿瘤活性机制,以便充分了解人参皂苷Rg3在治疗中的机制。对部分抗肿瘤药物水溶性差及口服生物利用度低提出了新的解决方法,例如,制备了载有人参皂苷Rg3的磁性人血清白蛋白纳米球[20(S)-Rg3/HSAMNP]。开发出具有改进功效、药代动力学和生物利用度特征的新型人参皂苷Rg3类似物,有效抑制肿瘤微血管形成,发挥更好的抗癌作用。目前,关于人参皂苷Rg3抑制肿瘤微血管形成的具体机制,尚需进一步研究。相关研究表明,单独使用人参皂苷Rg3或将人参皂苷Rg3与其他药物结合使用都可以抑制肿瘤微血管形成,达到良好的抑瘤效果。在后续研究中可以把人参皂苷Rg3开发成强有效的单体抗癌药物,也可以着重研究人参皂苷Rg3与其他抗癌药物的联合使用效果研发组合药物,并应用于恶性肿瘤治疗领域,将会有较好的发展前景。目前很多人参皂苷Rg3新药已在国内上市,而且含有人参皂苷Rg3的中药复方也已经应用于肿瘤的临床辅助治疗。
总之,人参皂苷Rg3在未来作为抗癌药和肿瘤治疗的有效辅助剂具有巨大潜力。以后还应更广泛的挖掘人参皂苷Rg3的药用价值,使人参皂苷Rg3更广泛地存在于我们的生活中,极大的发挥预防肿瘤、治疗肿瘤作用,从而造福人类。

