消化道肿瘤患者术中低体温预测模型构建与验证
罗梦佳,戴艳然,郎红娟(空军军医大学:护理系,西京医院胃肠外科,陕西 西安 7003)
在正常状态下,人体通过神经体液调节将体温维持在约37 ℃,以确保生理功能的稳定[1]。但在全身麻醉诱导下,由于内在补偿机制的丧失与麻醉药诱导的血管舒张相加,导致体内热量从核心重新分布到周围组织,因此热调节显著受损[2]。围术期非计划性低体温是指围术期由于各种原因而导致的机体核心体温低于36 ℃[3],是公认的围术期常见并发症[4]。体温过低会增强患者麻醉苏醒期的不适感,增加不良事件发生率,例如感染和伤口并发症、心脏和血液循环并发症、出血增加以及对输血的需求增加[5]。有研究报道,术中低体温发生率可高达90%[6]。目前,国内外有关低体温研究主要集中于泌尿外科、妇产科等,消化道肿瘤手术患者由于长期禁食、肿瘤消耗、手术创伤大等原因,导致其低体温率居高不下,而关于消化道肿瘤手术患者术中低体温及预测模型鲜有报道。本研究拟构建消化道肿瘤患者术中低体温的风险预测模型,旨在预测消化道肿瘤手术患者发生术中低体温的风险,为消化道肿瘤手术患者围术期体温保护提供理论依据。
1 对象与方法
1.1 对象
采用便利抽样法,选取2021年3月至6月在空军军医大学西京医院胃肠外科手术室接受消化道肿瘤手术的患者作为研究对象。纳入标准:①年龄≥18岁;②行择期手术;③全身麻醉;④术前均已确诊为肿瘤患者;⑤术中需要留置导尿管的患者。排除标准:①存在严重并发症(如出血、穿孔)的急诊患者;②术前体温>38 ℃或<35 ℃的患者;③孕期或哺乳期患者。本研究得到空军军医大学西京医院伦理委员会批准(许可证号:KY20202116-C-1),所有手术操作均由具有丰富手术经验的外科医师实施。纳入对象均自愿参与本研究。
通过查阅文献,专家咨询,共收集15个[性别、年龄、吸烟史、BMI、血糖、血红蛋白、白蛋白、美国麻醉协会(American Society of Anesthesiologists,ASA)评分、手术时间、是否灌肠、静脉入量、室温、手术类型、手术方式、是否采取主动保温措施]危险因素纳入本研究。根据样本量计算公式[7],每个自变量需5~10例患者,经西京医院胃肠外科30例小样本测得消化道肿瘤手术术中低体温的发生率为30%(9/30),考虑到10%~20%的样本可能不符合要求。因此,本研究所需的样本量为15×8×(1+0.2)/0.3=480例,最终入组495例。将其按2∶1比例分配,建模组330例,验证组165例。
1.2 方法
1.2.1 体温测量及判断 提前将手术室温度调至21~25 ℃,湿度为40%~60%。患者入室后,行常规保温措施,加盖棉被,放置护肩棉垫,静脉输入等体温的加热液体。患者全麻后插入14号测温导尿管,利用导尿管内置体温传感探头术中连续监测患者膀胱温度并作为中心体温[8]。由巡回护士记录麻醉开始时、手术1 h、手术结束时患者膀胱温度。术中患者任一时间点膀胱温度<36 ℃则定义为术中低体温。
1.2.2 资料收集 由巡回护士记录手术患者性别、年龄、吸烟史、BMI、血糖、血红蛋白、白蛋白、ASA评分、手术时间、是否灌肠、静脉入量、室温、手术类型、手术方式、是否采取主动保温措施等15项资料。手术结束后将数据录入电脑,双人核对。

2 结果
共纳入有效病例495例,其中,男340例(68.7%),女155例(31.3%);年龄20~85(59.64±11.31)岁;手术类型:食管癌根治术17例(3.4%),胃癌根治术270例(54.5%),结肠癌根治术107例(21.6%),直肠癌根治术101例(20.4%)。
2.1 建模组发生术中低体温的单因素分析
将建模组330例分为低体温组和非低体温组。其中术中发生低体温108例,发生率为32.7%;未发生低体温222例,占67.3%。组间比较,共7个变量具有统计学意义(P<0.05,表1)。
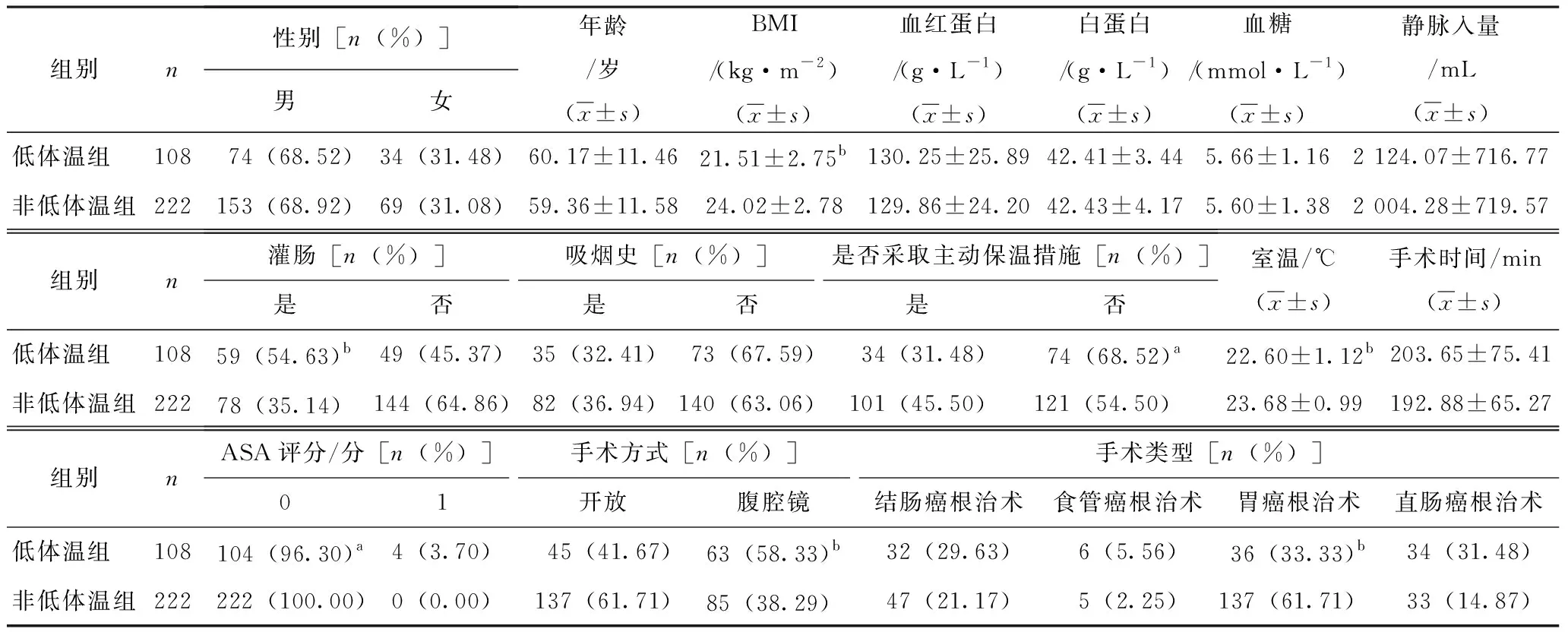
表1 消化道肿瘤手术患者术中低体温的单因素分析
2.2 建模组发生术中低体温的多因素分析
将单因素分析结果有统计学意义的7个因素(ASA评分、手术类型、手术方式、是否灌肠、是否采取主动保温措施、BMI、室温)作为自变量,以患者是否发生术中低体温为因变量,纳入二元logistic回归中进行分析,结果显示,手术类型、手术方式、室温、是否采取主动保温措施是术中低体温发生的独立危险因素(表2~3)。

表2 自变量赋值
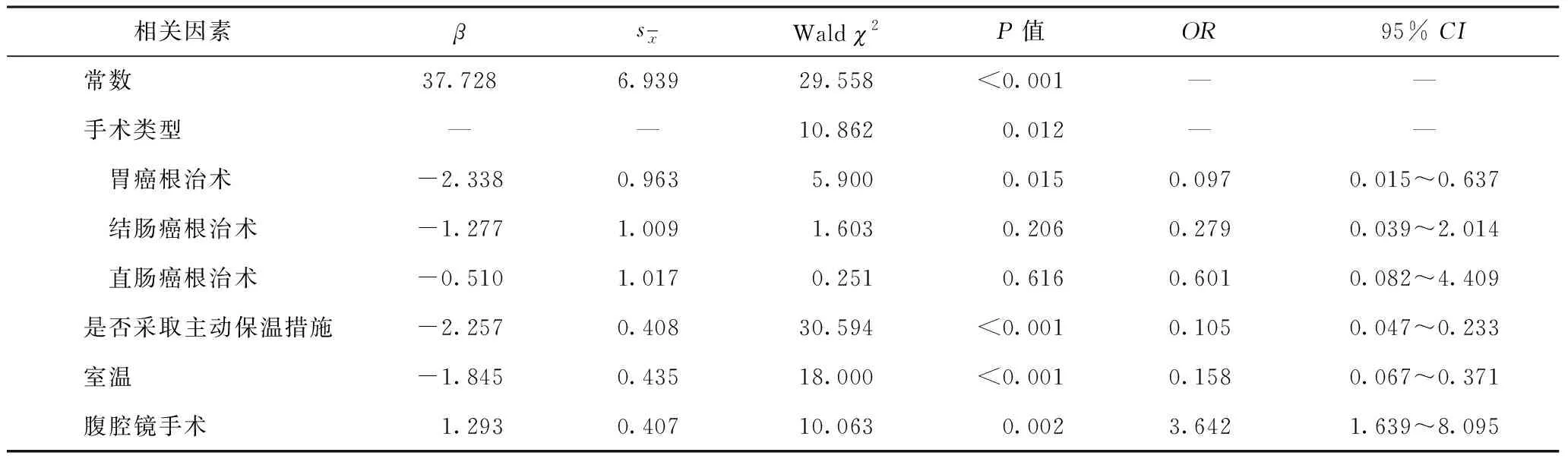
表3 消化道肿瘤手术患者术中低体温的多因素logistic回归分析
2.3 ROC曲线对消化道肿瘤手术患者术中低体温发生风险预测模型预测效果的分析
对预测模型进行Hosmer-Lemeshow检验验证拟合效果,P=0.589,表明拟合度良好。根据预测模型的公式计算出患者术中低体温的发生率,采用ROC曲线预测实际低体温的敏感度与特异度(图1)。以约登指数最大值为预测模型的最佳临界值。最终测得ROC曲线下面积为0.865,95%CI:0.823~0.906。此ROC曲线的约登指数为0.608,敏感度为0.806,特异度为0.802。
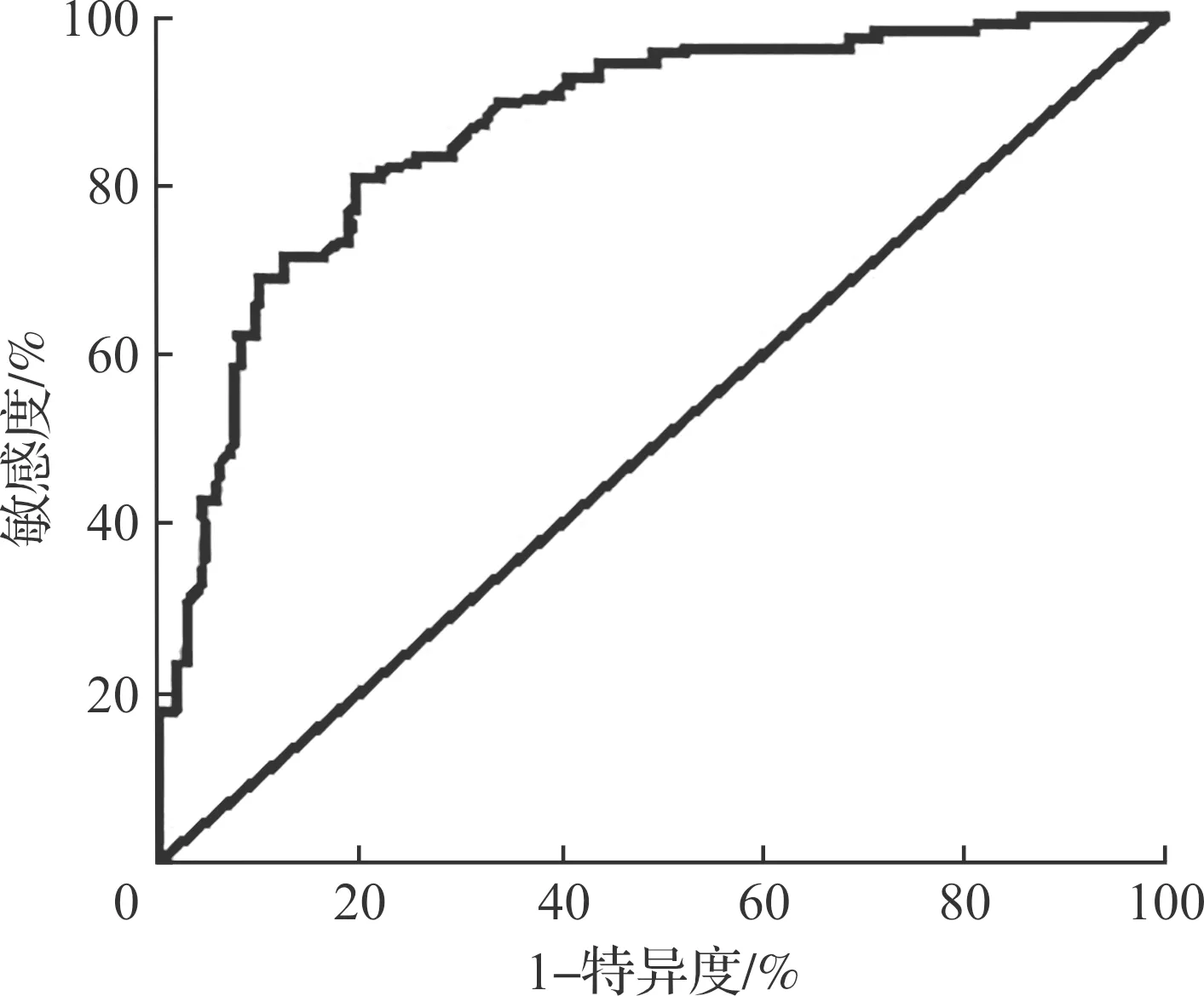
图1 预测组术中低体温预测ROC曲线
2.4 ROC曲线对消化道肿瘤手术患者术中低体温发生风险预测模型的临床应用
对验证组纳入的165例患者应用该模型,其中男112例(67.9%),女53例(32.1%);年龄20~82(59.68±10.89)岁。实际发生术中低体温60例,发生率36.4%,使用预测模型判断低体温发生52例,误判8例,敏感度为86.67%;实际未发生术中低体温105例,模型判断为85例,误判20例,特异度为80.95%。则模型总正确率为(52+85)/165=83.03%。建模组和验证组数据集之间的一般临床变量分布无显著差异(P>0.05),避免了由于临床变量分布不均而导致的结果偏差。
3 讨论
3.1 建立消化道肿瘤手术术中低体温预测模型具有重要意义
本研究根据2017版围术期患者低体温防治专家共识中围术期低体温标准[9],回顾性分析495例行消化道肿瘤手术患者术中发生低体温的情况,结果显示,其总体发生率与国内外其他研究基本一致[10-11]。本研究所有手术均由同一型号测温尿管进行膀胱温度监测,以避免因为监测方式、手段不同而导致的误差。本研究显示,手术类型为胃癌根治术、手术方式为腹腔镜、室温、是否采取主动保温方式是术中低体温发生的独立影响因素。对于高危患者,术前应采取提高手术间室温、加盖厚棉被、加热手术衣裤等措施;术中应采取使用复温毯、加热输液系统、加温加湿CO2气腹等主动保温措施[2,12-13]。对于低危患者,术前使用小于30 min的预热,亦可降低术中低体温的发生率[14-16],且更节约医疗资源。
3.2 消化道肿瘤手术术中低体温影响因素分析
LAI等[17]使用便利抽样法,通过观察和测量儿科手术患者体温进行的前瞻性队列研究结果,以及YANG等[18]通过分析接受计划手术的1 840例患者的资料,均显示手术类型是导致术中低体温的危险因素。本研究结果同样显示,以食管癌根治术作为参考,行胃癌根治术的患者较少发生术中低体温。分析原因可能与以下因素有关:①食管癌为三切口手术,手术创伤大、难度高、时间长。此外,术野暴露范围大小不一,内脏组织长时间体外暴露极易导致热量丢失;②由于消毒范围不同,食管癌根治术需要消毒颈、胸、腹部,而胃癌根治术仅需消毒腹部。麻醉诱导后1 h内是机体核心体温再分布期,麻醉剂导致外周血管扩张、肌肉产热减少、血液循环速度减慢等原因,致使患者核心体温迅速下降。同时,大范围的消毒使得患者体表暴露面积增加,加之消毒液刺激等则会使体温迅速下降;③不同类型手术术中腹腔冲洗量不同。在临床工作中,体腔冲洗液通常在常温下保存,在手术开始之前并未对液体进行加温至37~41 ℃,麻醉状态下患者很难在接触低温液体后进行自身体温调节。使用尚未进行加温的体腔冲洗液可降低冲洗部位周围的温度,已经降低的局部温度会通过血液循环致使全身核心体温下降[19]。本研究结果显示,腹腔镜手术为术中低体温的独立影响因素。MIYAZAKI等[20]回顾性分析了2 574例仰卧位接受择期腹部手术的成年患者的数据,PU等[21]对110例行腹腔镜胃肠手术的患者进行分析,结果均显示腹腔镜手术及CO2总量是发生术中低体温的独立危险因素。随着加速康复外科理念在外科医学的逐渐应用和发展,腹腔镜手术方式由于其创口小,恢复快等优点,已经作为一种常规的治疗手段。尽管其可以通过缩小切口大小来减少机体热量散失,但是内脏器官长期暴露于大量冰冷的CO2气体环境中,更易导致患者术中体温降低。JIANG等[22]研究结果显示使用温暖、湿润的CO2气体或在20 ℃,未加湿的CO2结合设定为38 ℃强制空气加热器均可减少术中体温过低。LEE等[23]研究结果显示术前10 min强制空气预热即可降低低体温发生率,与本研究室温为术中低体温的保护性因素结果一致。手术间空气过滤器的出风口根据手术室规范一般安装在手术床的正上方,快速、长时间的空气对流可通过对流散热的方式使得机体热量丢失,由此导致的体温丢失占总体热量散失的比例也不断增加,最高可达到61%。LAU等[2]通过分析200位患者资料证明术前至少30 min的强制空气对流加热降低了整个术中低体温发生率;ZEBA等[24]对30例接收腹部手术的患者进行资料分析,其结果显示使用热气床垫进行的外部加热能够减轻体温过低的现象;MUNDAY等[25]研究发现使用包括强制空气加热和碳聚合物床垫在内的加热装置可有效防止体温过低。这与本研究使用主动保温措施可降低术中低体温发生率的结果一致。主动保温措施主要是借助外部加温设备达到为机体提供额外热量以此避免患者术中体温降低的效果,其温度可以调节,能在患者周围形成热环境,阻止热量从核心向体表转移。
综上所述,手术类型为胃癌根治术、手术方式为腹腔镜、室温及是否采取主动保温措施是发生术中低体温的独立危险因素。建立术中低体温发生风险预测模型可有效预测消化道肿瘤手术患者术中低体温的发生风险。但该研究结果仍需前瞻性、大样本量研究进一步验证。

