磷石膏矿化CO2制备球霰石型碳酸钙试验研究
乔静怡,陈秋菊,刘卓齐,丁文金
(1.西南科技大学 固体废物处理与资源化教育部重点实验室,四川 绵阳 621010;2.西南科技大学 矿物材料及应用研究所,四川 绵阳 621010)
0 引言
碳酸钙是一种非常重要的无机非金属材料和化工原料,被广泛应用于化工、造纸、塑料、橡胶、医药等领域[1-2]。无水碳酸钙具有方解石、文石、球霰石3种晶型[3]。在热力学稳定性方面,球霰石的稳定性最差[4],仅存在于某些鱼类的耳石器官、海鞘的骨针、甲壳动物组织中[5]。与方解石和文石相比,球霰石具有独特的中空、多孔球形结构,生物兼容性和安全性较好,颗粒分布均匀[6-7]。因此,球形球霰石被广泛应用于化妆品、生物医药、光催化等高附加值领域。
目前制备球形球霰石的常用方法有碳化法、复分解法和热分解法,主要以天然矿物或纯的化学物质为原料,在制备过程中往往需添加晶型控制剂。范天博等[8]采用仿Solvay 氨碱法,以白云石为原料,在碱性环境下成功制备出了高球霰石含量的碳酸钙;对球霰石的形成机理分析结果表明,NH4+-NH3缓冲体系不仅可以增大碳酸钙的过饱和度,还可以为球霰石的生长提供一个良好的溶液环境,原料中微量的Mg2+起到了促进完好晶型形成的作用。任丽英等[9]以氯化钙为钙源、L-赖氨酸为模板,基于生物矿化过程,采用气相扩散法成功合成了球霰石碳酸钙微球,为碳酸钙药物载体材料的制备提供了合成方法与条件。陈传杰等[10]基于钙醇法,首先将CaCl2溶解于乙醇中,再将溶解后形成的络合物与Na2CO3水溶液反应制备球霰石型CaCO3,并系统讨论了陈化时间和反应温度对产物晶型与形貌的影响。LAI等[11]以甘氨酸作为晶型调控剂成功制备了球霰石型纳米碳酸钙,虽然得到的球霰石纯度较高,但是制备过程中需严格控制反应体系的各项因素,这在实际应用中很难实现。DING等[12]在不使用任何添加剂的情况下,仅通过控制反应温度便制备出了高纯球霰石型碳酸钙产品。ZHANG等[13]将碳酸氢铵分解产生的氨气和二氧化碳通入氯化钙溶液进行碳化反应,并采用复合添加剂(L-赖氨酸与无水对氨基苯磺酸)作为晶型调控剂,实验结果表明,当复合添加剂的复配比为5∶1时,球霰石在其与方解石的混合相中占主要成分。胡艳丽等[14]将碳酸铵分解产生的氨气和二氧化碳通入氯化钙溶液进行碳化反应,并用L-天冬氨酸作为晶型调控剂,实验结果表明,随着 L-天冬氨酸浓度的升高,碳酸钙晶体的生长速度明显变慢,体系中球霰石型碳酸钙占比降低,且随着碳化反应时间的延长,球霰石型碳酸钙逐渐转化为方解石型碳酸钙。
本文以氯化铵为助剂,首先浸取磷石膏中的硫酸钙,再以溶解态硫酸钙进行CO2矿化制备CaCO3,在矿化过程中不添加任何晶型控制剂,仅通过控制矿化条件制备球形球霰石型CaCO3。与国内外现有制备球形球霰石型碳酸钙相比,该方法以磷化工行业产生的固废磷石膏为原料,整个制备过程在低温、常压下进行,且无需添加晶型控制剂,所得球形球霰石的纯度和白度均较高,可为高纯碳酸钙的低成本制备与工业固废磷石膏的高值化利用研究提供参考。
1 试验原料与方法
1.1 试验原料
试验所用磷石膏取自四川绵阳某磷化工厂,原料的化学成分为:CaO占29.60%, SO3占39.36%, SiO2占5.03%, P2O5占1.60%, Al2O3占 1.85%, H2O占20.74%,其他组分占1.82%[15]。实验过程中所用氯化铵、氨水为分析纯;二氧化碳为工业级,纯度99%。
1.2 试验方法
准确称取10 g磷石膏原料,放入1 000 mL锥形瓶中,按一定液固比向锥形瓶中加入一定浓度、一定体积的氯化铵溶液;将锥形瓶放入恒温水浴摇床中,在240 r/min下反应一段时间后抽滤,将滤饼洗净、烘干后用于后续研究。滤液用于后续的碳酸钙制备试验。氯化铵浸出工艺条件为:NH4Cl盐溶液浓度1.65 mol/L,液固比60,盐洗时间30 min,盐洗温度10~30 ℃[15]。
量取400 mL含有钙离子的浸出液,倒入500 mL三口烧瓶中,将带有磁力搅拌子的三口烧瓶放入恒温水浴锅中,搅拌过程中加入不同量(6.25%、7.50%、10.00%)的浓氨水用于调节溶液pH,同时以一定速率通入二氧化碳气体,待反应液中出现白色沉淀后再反应15 min停止反应,固液分离后将固体产物在100 ℃下烘干12 h得到最终产品。
1.3 表征
用德国蔡司Sigma300型场发射扫描电子显微镜对试验过程中所得固体产物的显微形貌进行分析;用荷兰PANalytical公司X'Pert Pro型X射线衍射仪(X-ray Diffraction,XRD)对试验过程中所得固体产物的物相进行表征。
2 结果与讨论
2.1 正交试验结果分析
影响碳酸钙晶体形貌的因素有很多,根据前期所做的单因素试验及分析结果,决定考查碳化温度、氨水加入量、搅拌速度、CO2流速等4个因素对所得产物晶型与形貌的影响。
正交试验设计和试验结果分别见表1、表2。

表1 正交试验设计
分析试验结果可知:因子A取2水平最佳,因子B取3水平最佳,因子C取1水平最佳,因子D取2水平最佳,故指标达到最佳的条件是A2B3C1D2,即在碳化温度22 ℃、氨水加入量10.00%、搅拌速度650 r/min、CO2流速0.3 L/min的条件下产物中球霰石型碳酸钙的质量分数最高。
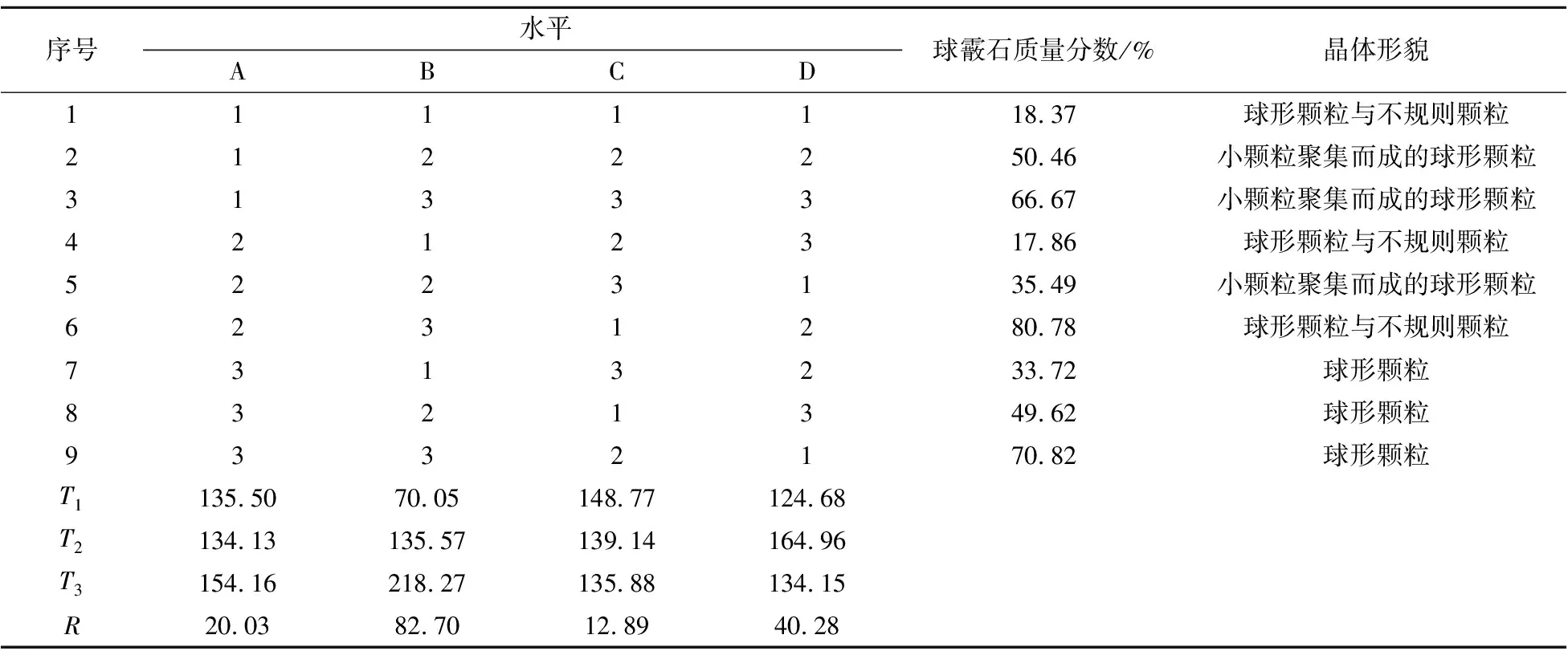
表2 正交试验结果
根据表2中的极差R可知:因子B对产物中球霰石质量分数的影响最大,因子D其次,再次为因子A,因子C影响最小。
2.2 不同碳化温度下氨水加入量对产物物相的影响
图1为正交试验产物对应的XRD图谱。
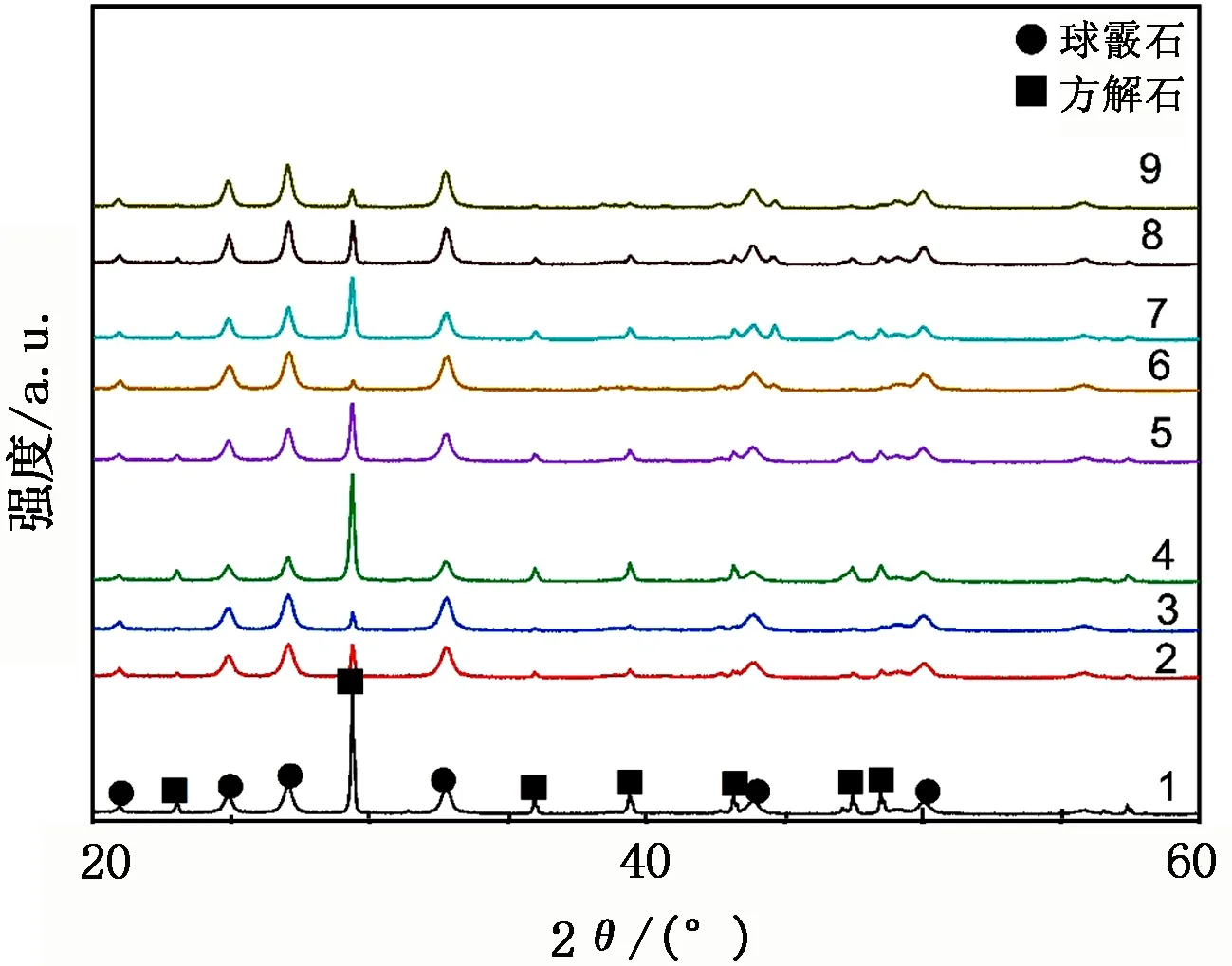
图1 正交试验产物CaCO3的XRD图谱
图1中的衍射峰位置均与球霰石标准衍射卡片(00-024-0030)和方解石标准衍射卡片(00-005-0586)的相结构一致。图中编号1、2、3对应的是碳化温度在18 ℃时,产物物相随氨水加入量的变化图谱;编号4、5、6为碳化温度在22 ℃时产物物相随氨水加入量的变化图谱;编号7、8、9是碳化温度在30 ℃时,产物物相随氨水加入量的变化图谱。由图1可知:无论何种温度下,随着氨水加入量的增加,方解石104、006、110、113、202、018、116晶面对应的特征衍射峰强度均逐渐减弱;当氨水加入量为10.00%时,方解石006、110、113、202、018、116晶面对应的特征衍射峰几乎消失,而球霰石101晶面的衍射峰强度逐渐增强。同时,从XRD图谱中物相的衍射峰尖锐程度可以看出,产物中方解石的结晶度高于亚稳定型球霰石。
由XRD图谱得到方解石104晶面与球霰石101晶面的特征峰强度Ic、Iv对应的值,根据Iv/(Ic+Iv)可计算出产物CaCO3中球霰石的质量分数。不同碳化温度下球霰石质量分数随氨水加入量的变化曲线见图2。由图2可知:同一温度下,随着氨水加入量的增加,产物中球霰石质量分数升高,这与文献[16]中的结论一致;不同的氨水加入量条件下,随着碳化温度的升高,球霰石质量分数变化趋势不同。
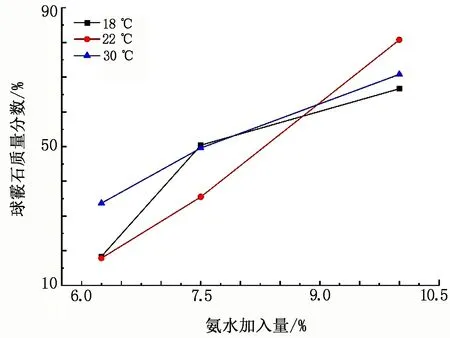
图2 不同碳化温度下球霰石质量分数随氨水加入量的变化曲线
在碱性溶液体系中,当钙离子和碳酸钙离子浓度达到一定值后两者会迅速反应,导致CaCO3快速成核;当反应体系中钙离子和碳酸根离子没有过量时,所得CaCO3晶体后续生长缺乏足够的钙源和碳源,生成的CaCO3一般为亚稳定型球霰石晶型。随着反应的进行,热力学亚稳定型球霰石会逐渐转变为热力学稳定的方解石晶型[17-19],从而很难得到纯球霰石型CaCO3。
磷石膏的NH4Cl盐浸液在无任何添加剂的情况下,碳化产物中球霰石型CaCO3的含量随着氨水加入量的增加(即溶液初始pH的增大)而升高。固碳反应初期,形成无定形CaCO3暴露(001)面的球霰石纳米片,该面仅由CO32-与Ca2+组成,能量较高,溶液中存在的NH4+可吸附于该面,从而降低其能量,稳定球霰石纳米片[20]。该纳米片通过堆积生长形成球形球霰石晶体,即氨水加入量越多,溶液中NH4+浓度越高,越有利于球霰石的形成。
相关研究[21]认为,球霰石的成核驱动力计算式为
ΔG= -RgTlnS,
(1)
式中,Rg为气体常数;S为溶液过饱和度。由式(1)可以看出,溶液的过饱和度越大,则形成球霰石的趋势越明显,而不是转化为方解石。氨水加入量的增加导致溶液初始pH增大,促进了CO2的溶解,使溶液中CO32-的浓度迅速升高,溶液的过饱和度增大,导致产物中球霰石型CaCO3含量升高。
碳化温度为18 ℃时,不同氨水加入量的产物SEM照片见图3。

图3 18 ℃碳化温度下不同氨水加入量产物SEM照片
由图3可知:氨水加入量为6.25%时,碳化产物以直径大小不等的空心球形颗粒为主,还含有少量不规则形状颗粒,其中粒径小于5 μm的颗粒居多;当氨水加入量增至7.50%时,产物中主要为团聚的球形颗粒,粒径较大,在10 μm左右;当氨水加入量增至10.00%时,产物中仍然为团聚的球形颗粒,其中小粒径颗粒数量增加。
碳化温度升至22 ℃时,不同氨水加入量的产物SEM照片见图4。

图4 22 ℃碳化温度下不同氨水加入量产物SEM照片
由图4可知:当氨水加入量为6.25%时,碳化产物为球形小颗粒,粒径较小,在4 μm左右,其中含有少量不规则形状颗粒;当氨水加入量增至7.50%时,产物大小较均匀,为团聚的球形颗粒,粒径在5~14 μm;当氨水加入量增至10.00%时,产物为小颗粒空心球状物,粒径均小于8 μm。
碳化温度升至30 ℃时,不同氨水加入量的产物SEM照片见图5。

图5 30 ℃碳化温度下不同氨水加入量产物的SEM照片
由图5可知:该组碳化产物的球形颗粒大小较均匀,且为空心球形,很少有团聚体出现;随着氨水加入量的增加,颗粒趋向于形貌完整的大小均匀的球形;当氨水加入量为7.50%时,产物颗粒粒径大多在5 μm以下;其他两种条件下的颗粒粒径相差不大,均在4~9 μm。
3 结论
a.通过4因素3水平正交试验,得到影响磷石膏盐浸液固碳制备球形球霰石最显著的因素为氨水加入量,其次为CO2流速,再次为碳化温度,搅拌速度的影响最小。获得的最佳试验条件为氨水加入量10.00%、CO2流速0.3 L/min、碳化温度22 ℃、搅拌速度650 r/min。
b.相同温度下,随着氨水加入量的增加,碳化产物中球霰石质量分数呈近似线性升高;不同温度下,随着氨水加入量的增加,产物的形貌变化规律不完全一致,但均向着球形颗粒多的方向发展;温度为30 ℃时,产物形貌较其他温度下的好。
c.氨水加入量影响球形球霰石质量分数的机理是溶液中增加的NH4+可吸附于无定形CaCO3暴露(001)面的球霰石纳米片上,从而导致球霰石质量分数升高。

