高分辨率对比增强锥形束CT在颅内支架成形术后评估中的应用价值
万程,王丹,潘文秋,易根发,胡继红,何波,汤志伟,赵卫
颅内支架具有将血流转向载瘤动脉而远离动脉瘤的导向作用,增强动脉瘤内血栓形成及瘤颈部内膜形成,从而减少动脉瘤复发,达到治愈动脉瘤的作用,被广泛用于颅内动脉瘤的辅助治疗[1],其主要技术包括支架辅助弹簧圈栓塞术、单独支架置入术及支架重叠技术等。由于支架金属覆盖率高、载瘤动脉迂曲、术者操作不熟练及术后未按规范用药等原因,可导致支架局部贴壁不良、内膜异常增生及血栓形成等,最终导致缺血性事件的发生[2]。研究报道,金属材料的使用量会增加血栓栓塞的风险,如支架长度、支架数量和重叠支架等[3]。然而,近三分之一的颅内动脉瘤患者在支架植入后发生非特异性症状的缺血事件,如情绪变化、慢性疲劳或难以恢复与工作相关的活动,这些表现在临床上容易被忽视,从而对患者生活质量产生不利影响[4]。因此,如何准确动态评估血管内支架贴壁情况、内膜增生及支架内血栓等情况,及时调整治疗方案,避免缺血事件的发生尤为重要。既往多采用2D-DSA及3D-DSA对颅内支架进行随访,但评估较困难并常常容易漏诊,因此有必要寻找更简便、准确的评估方法。笔者发现高分辨率对比增强锥形束CT(high-resolution contrast-enhanced cone beam CT,VasoCT)可快速、准确评估支架贴壁、内膜增生及血栓等情况,对颅内支架植入后的评估具有较大优势。本文旨在探讨VasoCT在评估颅内动脉支架植入术后支架贴壁、内膜增生及支架内血栓情况的应用价值。
材料与方法
1.病例资料
回顾性搜集2019年11月至2021年10月在昆明医科大学第一附属医院因颅内动脉瘤行支架植入治疗且术后3个月返院复查的患者共32例。排除颈动脉支架植入者及有严重心、肝、肾、肺功能障碍不能耐受检查者。32例患者中男19例,女13例,年龄19~75岁,平均(46.3±3.2)岁。前循环动脉瘤31例,后循环基底动脉尖动脉瘤1例。32例患者共植入34枚支架,单纯Pipline支架植入25枚,Pipline支架辅助弹簧圈栓塞动脉瘤患者7枚,LVIS及Solitaire支架辅助弹簧圈栓塞各1枚。单纯支架植入者在三维DSA及常规XperCT的基础上行VasoCT检查,支架辅助弹簧圈者结合去金属伪影(metal artifacts reduction,MAR)技术。
2.图像采集方法
影像采集均在Phlips FD20 DSA机上进行,XperCT Cereb.HD采集参数:120 kV,250 mA,视野48 cm×48 cm,采集时间20 s,采集速度40帧/s,注射对比剂总量40 mL,流率5 mL/s,压力200 psi,注射延迟时间为3 s。VasoCT采集图像,术中首先选择VasoCTIA,扫描视野则自动变为22 cm×22 cm,后将探测器升至最大射线源到影像板的距离(source to image receptor distance,SID),将感兴趣区调整至中心点,将所有物体从C臂旋转区域中移开,确定结束和开始位置,设置高压注射器联动延迟时间,嘱患者不要移动,则开始采集图像。采集图像前,所有前循环病变患者造影导管均超选至C1段,后循环病变患者导管置于V1段,采集参数:80 kV,260 mA,7 ms,30fps。对比剂为碘佛醇(320 mg I/mL),造影时将对比剂和0.9%氯化钠溶液按1:9稀释为浓度10%的低浓度对比剂,注射总量为60~70 mL,流率3 mL/s,压力为200 psi,注射延迟时间2~3 s,采集时间20~24 s。影像采集完成后传送至Philips工作站进行图像处理,采用放大重建、Stent、MAR、MIP等技术根据需要选取30%或50%空间容积及支架优化模式进行图像重建。
3.图像质量评价
由2位具有10年以上工作经验的神经介入医师对图像质量进行综合量化评分。支架贴壁情况评分标准:0分显示不清,1分不完全显示,2分完全显示。支架内内膜增生情况评分标准:0分显示不清,1分不完全显示,2分完全显示。支架内血栓形成情况评分标准:0分显示不清,1分不完全显示,2分完全显示。
4.统计学分析
采用SPSS 26.0软件进行统计学分析。采用 kruskal-Wallis秩和检验比较不同重建方法图像质量的差异。使用Kappa检验对2位医师评价图像质量进行一致性检验,0.75≤Kappa值<1.00表示一致性较好,0.40≤Kappa值<0.75表示一致性一般,Kappa值<0.40表示一致性差。以P<0.05为差异有统计学意义。
结 果
所有患者术后3个月或更长时间均成功进行随访,对9例支架辅助弹簧圈栓塞者,结合去金属伪影(MAR)技术去除金属伪影,1例大脑中动脉梭形动脉瘤单纯行Pipline支架植入治疗,复查显示支架近端出现内膜中度增生,管腔狭窄,经加强抗血小板治疗后1
年复查示内膜增生完全消失(图1)。结合MAR技术可得到不受金属伪影影响的清晰图像(图2)。

图1 患者,男,41岁,发现左侧大脑中动脉M1段梭形动脉瘤入院。a) DSA示左侧大脑中M1段梭囊状动脉瘤(箭);b)行Pipeline支架植入,VasoCT提示支架位置、贴壁良好(箭);c) 3个月后三维DSA复查示支架近端充盈缺损(箭);d) VasoCT提示支架贴壁良好,支架内可见充盈缺损(箭),考虑内膜增生,予加强抗血小板治疗;e) 与图1c相比,术后1年三维DSA复查示支架近端充盈缺损消失(箭),血流通畅;f) VasoCT提示支架近端内未见充盈缺损(箭),支架位置、贴壁良好。

图2 患者,女,50岁,因头痛入院。a)3D-DSA示左侧颈内动脉眼段巨大动脉瘤,行Pipline+弹簧圈栓塞。b)术后即刻VasoCT示支架位置、扩张良好,动脉瘤腔内弹簧圈金属伪影较重(箭);c)结合MAR后,消除弹簧圈金属伪影,清晰显示支架情况。
从表1秩和检验对应的秩次值可得出,VasoCT以及VasoCT结合MAR技术在评估支架贴壁、内膜增生及支架内血栓情况等方面可提供较好的图像质量;在支架贴壁情况(χ2=46.360,P<0.001)、内膜增生情况(χ2=46.460,P<0.001)及支架内血栓情况(χ2=45.539,P<0.001)等方面,与三维DSA及常规XperCT评估相比差异有统计学意义。为了验证两位医师对图像质量评价的一致性,选取VasoCT组及XperCT组分别进行Kappa一致性检验,Kappa值均大于0.75(表2、3),P<0.001,表明两位医师对图像质量评价的一致性较好。

表1 不同重建方法评估支架贴壁、内膜增生及支架内血栓情况
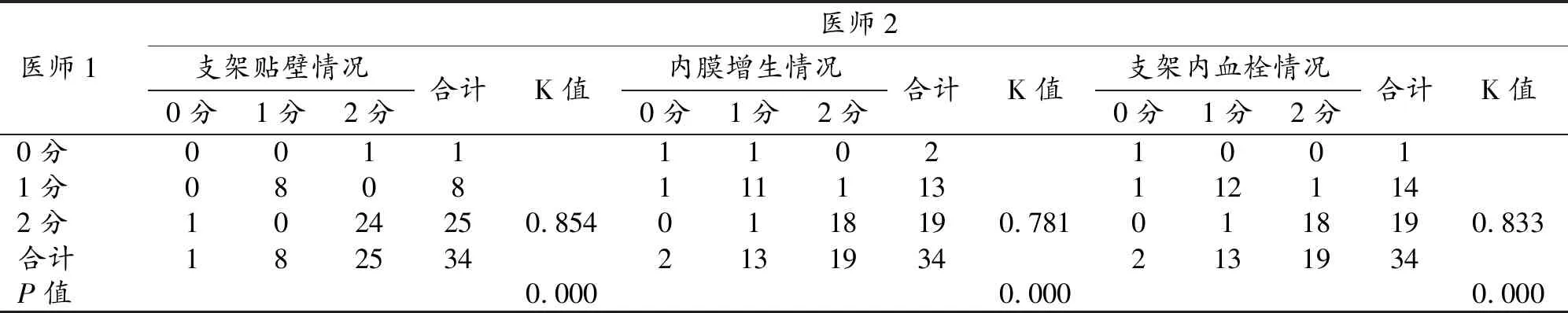
表2 VasoCT组一致性检验结果
术后依据DSA工作站辐射剂量表格中的剂量面积乘积(dose-area product,DAP)、累计空气比释动能(cumulative air kerma,CAK)、累计透视时间及手术时间等指标,使用辐射剂量软件空气比释动能计算辐射剂量。经统计本组患者的平均DAP为136.25 Gycm2(85.99~220.33 Gycm2),CAK为1171.67 mGy(366.28~2430.67 mGy),累计透视时间为77.92 min (25.63~112.32 min),手术时间为220.1 min(122~347 min)。使用辐射剂量评估软件计算的头部DAP为15.33 Gycm2,CAK为155.40 mGy,皮肤最大剂量峰值为0.784 Gy。
讨 论
当颅内支架尺寸选择不当、术中支架局部打开不良、支架头端因血管迂曲与载瘤动脉成角、过度栓塞动脉瘤腔至支架变形或弹簧圈部分脱出均可导致支架贴壁不良、血管内膜异常增生以及血栓形成。一篇关于不同类型支架的支架辅助弹簧圈的文献综述发现,手术等相关并发症的发生率为19%,死亡率为2%[5]。因此,及时准确评估、早期干预是降低并发症的关键。有研究报道术中使用VasoCT及时评估支架及弹簧圈情况,有助于降低术中并发症的发生率[6],降低血栓栓塞事件发生率[7]。
随着血流导向装置、编织EndoBridge等新兴材料在神经介入中的运用不断增加,简化了手术操作流程,并提高了手术安全性,但传统的评估技术往往受限。VasoCT采用非像素融合技术,具有超高的空间分辨率。与XperCT相比,其采用小视野(22 cm×22 cm)、低kV(80 kV)、Non binned读取方式,提供了最高的空间分辨率(体素大小为0.1~0.3 mm3)和适合的密度分辨率(10 HU),可清晰显示颅内支架以及支架与血管、支架与弹簧圈的关系[8]。对于支架辅助弹簧圈栓塞者,使用VasoCT 结合MAR技术可有效去除来自支架和线圈的金属伪影,清晰显示支架与弹簧圈、血管壁及瘤颈口的关系和弹簧圈栓塞填充的密度,改善图像质量,从而潜在地减少并发症和动脉瘤的复发[9]。在本组病例中,共有32枚支架为Pipline支架,由于金属覆盖率较高,常规成像方法金属伪影较重,难以准确评估支架情况。使用VasoCT检查,评估支架贴壁、内膜增生及血栓情况明显优于常规Xper-CT;与三维DSA相比,VasoCT图像可进行多方位、多角度显示,具有更高的对比度分辨率及较少的对比剂用量等优势。
目前,评估头颈部支架贴壁情况、内膜增生及血栓形成情况的影像学方法主要有VasoCT[10]、频域光学相干断层扫描(frequnce domain optical coherence tomography,FD-OCT)以及相关影像学重建技术[11]等。FD-OCT可清晰显示支架与内膜的关系、内膜异常增生情况及支架内血栓形成等情况[12],但脑血管树高度迂曲的解剖结构对OCT导管的导航提出了较大挑战[13];目前多用于颈动脉支架及较直的血管内[14],并多以体外实验及病例报道居多[15]。有学者采用MRI T1-mapping及T2-mapping技术对兔颈总动脉血栓进行定量评价,有望用于鉴别颅内不同类型血栓[16]。在我们前期的研究中,FD-OCT主要用于C5段以下血管,对于C5段以上血管及血管重度狭窄者,操作难度及风险较高。近年来,有学者介绍了一种神经血管高频光学相干断层扫描系统[17],在体内、外实验中获得成功,在颅内动脉中使用具有较大的潜力及优越性。
Caroff等[18]使用VasoCT评估经编织 EndoBridge (WEB)栓塞动脉瘤腔后,动态随访WEB的形状,可以精确定量评估WEB尺寸及其与靶血管的关系。术中对比剂的稀释比例、对比剂的总量、注射流率、注射压力及时间、造影导管位置均可影响VasoCT图像质量,目前没有统一标准。术中笔者将对比剂碘佛醇(320 mg I/mL)与0.9%生理盐水按1:9比例进行稀释,造影导管置于颈内动脉C1段进行VasoCT,可清晰显示支架整体形态、支架贴壁情况及内膜情况。对栓塞动脉瘤腔患者,结合MRA技术可明显减少瘤颈部的金属伪影,提高支架与瘤颈口的分辨率。本组患者中1例内膜异常增生致血管狭窄,未发现血栓形成及支架贴壁不良者,VasoCT可清晰显示支架内增厚的内膜伴管腔狭窄,图像质量较好,但本研究样本量较少,仍需进一步扩大样本量同时需延长随访时间行进一步研究。相关文献报道[19],VasoCT数据采集的CT辐射剂量指数在80 kV时为49 mGy,120 kV时XperCT数据采集的CT剂量指数为45 mGy,低于标准常规CT血管造影。本组患者的DAP、CAK及皮肤最大剂量峰值等均低于规定范围[20-21]。但检查方式的增加,辐射剂量也会相应增加,因此选择最佳成像技术及时进行评估,在缩短手术时间的同时可降低辐射剂量。
综上所述,VasoCT是一种高分辨率3D成形技术,在评估颅内支架贴壁、内膜增生及支架内血栓情况等方面具有明显优势,可用于术中及时评估及术后随访,但图像质量与执行注射协议明显相关。对支架辅助弹簧圈栓塞动脉瘤患者,VasoCT结合MAR技术可去除金属伪影,在评估支架与邻近结构的关系上具有独特优势。

