土壤中磺胺甲口恶唑吸附-解吸反应
蓝志鹏, 童 鑫, 黄 宇, 杨杰文
(仲恺农业工程学院资源与环境学院,广东 广州 510225)
磺胺甲口恶唑(SMX)具有疗效显著、成本低廉、广谱性强等优点,被广泛应用于畜禽疾病治疗中[1],在中国的使用量高达313 t[2]。SMX在畜禽体内无法完全代谢,30%~90%以母体分子或代谢物的形式随粪尿排出体外[3]。未经处理的畜禽粪便用作肥料还田时,将导致其中残留的SMX进入土壤,有研究结果表明,中国农田土壤中SMX的检出率和残留量均较高[4-6]。进入土壤中的SMX存在潜在风险,如:诱导产生抗性基因[7-10]、影响土壤微生物群落正常功能[11-12]、毒害非目标生物[13]以及通过作物或地下水进入食物链[14-15],这将威胁生态环境和人体健康[16-17]。
吸附-解吸反应对SMX在土壤中的环境行为和生物风险效应有决定性影响,因为该反应控制着SMX在土壤固-液两相中分配的相对数量[18]。SMX的辛醇水分配系数仅为0.89,因而在雨水冲刷、浸泡和渗滤的作用下容易在土壤中向下垂直迁移至地下水。一般而言,土壤中SMX吸附-解吸反应与土壤pH值、共存离子和有机质等因素密切相关。有研究结果表明,SMX的吸附系数与土壤pH值呈负相关,与土壤有机碳含量、水解性酸度和交换性酸度呈正相关[19-20]。随着离子强度的增加,SMX在土壤中的吸附量先增大后减小。反应热力学试验和傅里叶变换红外光谱分析结果证实土壤中SMX的吸附反应为自发的物理、化学吸附过程,主要通过氢键、静电相互作用等方式与固体表面结合[21]。类似研究结果还表明,土壤有机质含量越高,对同属磺胺类抗生素的磺胺氯哒嗪和磺胺甲嘧啶的吸附量越大,而磺胺甲嘧啶被解吸的数量则越低[22],总体上看,土壤组分的复杂性导致直接探测SMX与土壤表面相互作用的机制十分困难,但通过比较组分和性质差异较大的土壤对SMX的吸附结果,并借助有机探针分子的竞争吸附作用,仍可得到一些相对微观的机理。此外,现有研究侧重于吸附反应,对土壤表面吸附态SMX的解吸特性了解相对较少。
基于以上分析,本研究拟以菜园土和砖红壤(这2种土壤的有机质含量差异较大,有利于探明有机质对土壤中SMX吸附-解吸反应的影响)为试验对象,研究上述土壤中SMX的吸附动力学与吸附量,探究pH值、离子强度、陪伴离子的影响,在此基础上,研究2种土壤中SMX的解吸差异,揭示土壤对SMX的吸附机制,以期为了解SMX的环境行为和生态风险提供理论依据。
1 材料与方法
1.1 试验材料
SMX标准品购自西格玛奥德里奇(上海)贸易有限公司。试验用水为电阻率大于18 MΩ·cm的超纯水。乙腈和甲醇为色谱纯,其他化学试剂均为分析纯。试验土壤为菜园土和砖红壤0~20 cm土层样品,分别采自广东省韶关市曲江区马坝镇石堡村和广东省湛江市徐闻县曲界镇红星农场十七队。所有土样经风干、去除植物残体和石砾后研磨过100目筛,充分混匀,密封避光保存。为排除微生物对试验结果的影响,土样经高压灭菌消毒。此外,用H2O2氧化法去除土壤有机质。用超纯水将灭菌土壤润湿,加入30% H2O2,搅拌混匀状态下,75 ℃水浴加热氧化,若泡沫消失,则继续加入30%H2O2直至无泡沫产生,煮沸去除残余H2O2后,冷冻干燥后备用。灭菌原状土和去除有机质后土壤的理化性质见表1。
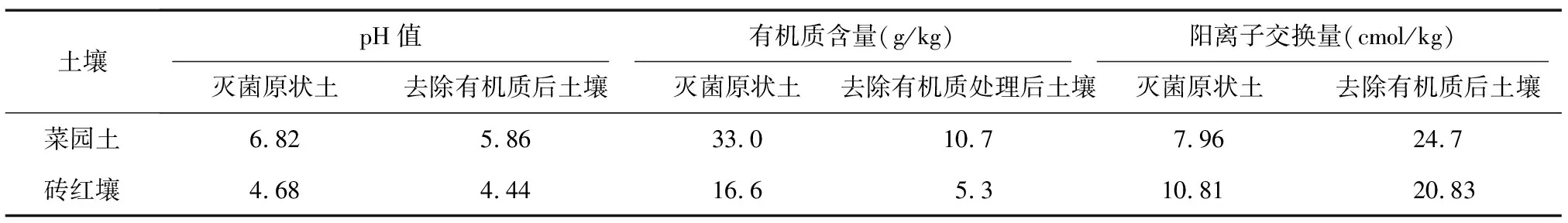
表1 原状及去除有机质处理后土壤理化性质
1.2 试验方法
1.2.1 吸附动力学 吸附动力学反应在用铝箔包裹的玻璃瓶中进行,体系总体积为200 ml,内含20 g土壤样品、2.00 mg/L SMX和0.01 mol/L NaCl背景电解质。首先,将土壤样品与已知体积超纯水在120 r/min转速条件下预先平衡24 h,在此期间添加预定体积的稀HCl或NaOH使悬浮液pH值维持在5.00±0.05。随后,向上述体系加入一定体积SMX与NaCl混合工作液以启动反应(体系pH值同样保持在5.00)。用注射器分别在0.25 h、1.00 h、4.00 h、12.00 h、24.00 h、48.00 h、72.00 h、96.00 h抽取约2 ml悬浮液,经0.22 μm聚醚砜过滤器过滤后,测定滤液中SMX的质量浓度。
1.2.2 等温吸附反应与溶液因素影响 等温吸附反应在用铝箔包裹的玻璃离心管中以室温条件进行。分别向玻璃离心管内加入2.0 g土壤、20.0 ml工作液(内含0.01 mol/L NaCl和0.5 mg/L、1.0 mg/L、2.0 mg/L、5.0 mg/L、8.0 mg/L、10.0 mg/L SMX),通过添加预定体积的稀HCl或NaOH调整pH。反应体系用旋转混匀仪在30 r/min转速下混匀72 h后达到吸附平衡,再在3 000 r/min转速下离心10 min以分离固-液两相。小心将离心管中的上清液倾倒完全,经0.22 μm聚醚砜滤膜过滤后,测定其pH值和SMX的质量浓度。
本研究还进一步考察了pH值、离子强度、Cu2+浓度、芳香胺浓度等溶液因素以及去除有机质对土壤吸附SMX的影响。在研究pH值和离子强度的影响时,pH值范围为3.5~7.0,3种NaCl背景电解质浓度分别为0.01 mol/L、0.10 mol/L、0.50 mol/L。具体步骤是:称取2.0 g土壤样品于离心管中,加入20.0 ml内含某种浓度NaCl和2 mg/L SMX的工作液,再用稀HCl或NaOH将体系pH值控制在预定范围,吸附平衡时间及固-液两相分离方法按等温吸附反应的方法进行。在研究Cu2+、芳香胺等陪伴离子浓度的影响时,Cu2+的浓度设定为2.0 mmol/L或5.0 mmol/L,苯胺、4-苯胺磺酸这2种芳香胺的质量浓度均设定为5 mg/L,试验步骤与研究pH值和离子强度的试验步骤基本相同,不同的是所加工作溶液还含有设定浓度的陪伴离子。按相同固液比和SMX质量浓度,参考上述步骤研究不同pH值条件下,去除有机质的土壤对SMX的吸附。
1.2.3 等温解吸反应 等温吸附反应结束后,小心去除离心管内上清液,向土壤残渣中加入20.0 ml 0.01 mol/L CaCl2进行解吸试验。反应体系在25 ℃下用旋转混匀仪平衡72 h后,3 000 r/min离心10 min,上清液用0.22 μm聚醚砜过滤器过滤,用于测定SMX的质量浓度。
1.3 分析方法
用1260 Infinity II HPLC系统[安捷伦科技(中国)有限公司产品]测定SMX的质量浓度,该系统配备ThermoFisher Scientific反相C18柱(150.0 mm×4.6 mm,5 μm,Hypersil GOLDTM)和紫外线检测器。流动相由30%乙腈和70% 0.01 mol/L乙酸组成。流速1.0 ml/min,柱温为30 ℃,进样量为10 μl,波长为265 nm。
1.4 数据处理
SMX的吸附量按公式(1)计算:
(1)
式中:q为土壤对SMX的吸附量(mg/kg);C0为体系中SMX的初始质量浓度(mg/L);Ct为反应时间t时刻溶液中SMX的质量浓度(mg/L);V为体系溶液的体积(L);m为体系中土壤的质量(kg)。
SMX的解吸量按公式(2)计算:
(2)
式中:qdes为解吸达到平衡时SMX的解吸量(mg/kg);qe(des)为解吸平衡时溶液中SMX的质量浓度(mg/L);qe(ads)为吸附达到平衡时溶液中SMX的质量浓度(mg/L);V1为解吸达到平衡时溶液的体积(L);V2为解吸试验前土壤保留的溶液体积(L);m为体系中土壤的质量(kg)。
采用拟二级动力学方程对土壤吸附SMX的反应动力学进行拟合,方程如下:
(3)
式中:t为吸附反应时间(h);qt为反应时间t时刻土壤对SMX的吸附量(mg/kg);qe为吸附平衡时土壤对SMX吸附量(mg/kg);K2为拟二级速率常数[g/(mg·min)]。
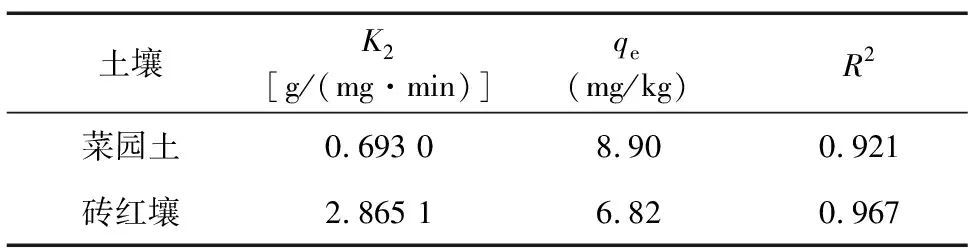
表2 菜园土和砖红壤吸附SMX的拟二级动力学方程拟合结果
采用Freundlich模型拟合SMX在土壤中的吸附解吸等温线,方程如下:
(4)
式中:Qe为平衡时土壤对SMX的吸附量(mg/kg);Ce为平衡时溶液中SMX的质量浓度(mg/L);Kf为Freundlich模型中代表吸附容量的常数(L/mg);n为Freundlich模型中代表吸附强度的常数。
2 结果与分析
2.1 吸附反应动力学
图1显示,菜园土和砖红壤对SMX的吸附速率在初始反应时较高(1 h内的吸附量分别达到平衡吸附量的69.4%和84.3%),随后逐渐降低。在反应初始阶段,土壤表面活性吸附位点比较充裕,SMX可被快速吸附至土壤表面。随着反应进行,吸附位点逐渐饱和,且吸附阻力增加,SMX吸附速率逐渐降低,最终在72 h基本达到吸附平衡。上述菜园土和砖红壤中的SMX吸附动力学特征与黄土、红土体系中的相同[23]。同时,菜园土和砖红壤这2种土壤中的SMX吸附动力学均可用拟二级动力学方程进行拟合(R2>0.920)(表2)。
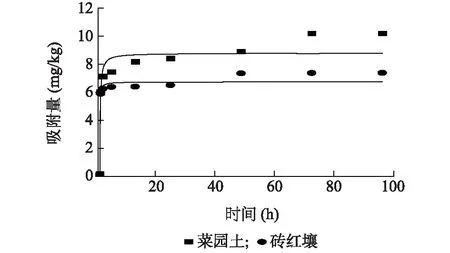
图1 菜园土和砖红壤中磺胺甲口恶唑(SMX)的吸附反应动力学Fig.1 Adsorption kinetics of sulfamethoxazole (SMX) in vegetable soil and latosol
2.2 吸附等温线
吸附等温线有助于了解吸附反应平衡后污染物在土壤固-液两相中的分配比例。图2显示,在本研究设定的SMX质量浓度范围内,2种土壤对SMX的吸附量整体随平衡质量浓度的增加而增加,且未达到土壤饱和吸附量。表3显示,本研究所得吸附等温线符合Freundlich模型(R2>0.970),2种土壤的Kf(Freundlich模型中代表吸附容量的常数)值均较低(菜园土为3.821~10.134 L/mg;砖红壤为1.083~2.674 L/mg),这表明SMX与土壤表面结合位点的相互作用较弱。一般而言,1/n(n为Freundlich模型中代表吸附强度的常数)值小于1意味着土壤表面SMX吸附位点是非均匀的,即:SMX先占据土壤中的易吸附位点,并随着吸附位点数量减少而逐渐降低吸附速率。同时,SMX辛醇水分配系数较低,且不具有强有机络合剂所特有的五环或六环结构[24],这将导致土壤对SMX的结合能力较弱。此外,由于砖红壤和菜园土在理化性质尤其是有机质含量方面的差异,也使得SMX的Kf值在2种土壤中明显不同。有研究结果表明,有机质和蒙脱石均对磺胺类抗生素吸附过程有贡献,但在质量相同的情况下有机质对磺胺类抗生素的亲和力高于蒙脱石[25]。菜园土和砖红壤对SMX的最大吸附量分别为31.7 mg/kg和9.3 mg/kg,菜园土对SMX的最大吸附量是砖红壤的3.41倍,这意味着有机质是土壤吸附SMX的重要载体。

图2 菜园土(a)和砖红壤(b)在不同pH值条件下对SMX的吸附等温线Fig.2 Adsorption isotherm for SMX under various pH by the vegetable soil (a) and latosol (b)
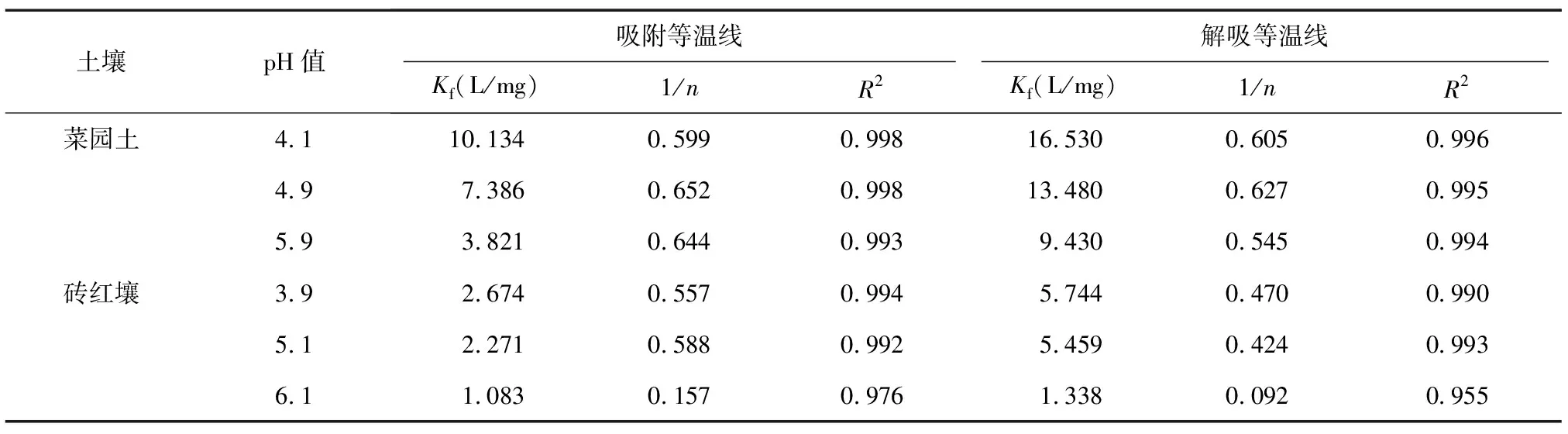
表3 SMX的吸附-解吸等温线拟合参数
2.3 pH值对土壤吸附SMX的影响
图3显示,pH值为3.5~7.0时,菜园土和砖红壤对SMX的吸附率随pH值增大而降低。在吸附等温试验中,SMX在菜园土中的吸附Kf值亦从pH值为4.1条件下的10.134 L/mg大幅度下降到pH值为5.9条件下的3.821 L/mg。一般而言,土壤吸附SMX机制主要有:①静电引力;②氢键;③SMX结构中的苯环与土壤有机质结构中的苯环之间的π-π共轭作用;④疏水性分布;⑤范德华力。其中,静电引力和氢键的作用强度易受pH值的影响,这是因为溶液pH主要改变SMX离子形态和土壤表面电荷性质。首先,在pH值为3.5~5.0时,SMX以中性形态为主(占总量的90%以上),而在pH值为6.0~7.0时,中性形态SMX百分比降至10%,阴离子形态(SMX-)增加到90%左右[21]。其次,随着pH值升高,2种土壤表面负电荷数量将逐渐增加。由此可见,pH值越高,土壤表面对SMX的静电斥力越强,SMX与土壤组分尤其是有机质之间也越不易形成氢键,从而表现出土壤对SMX的吸附量随pH值升高而降低的趋势[19]。

图3 离子强度和Cu2+对SMX在菜园土(a和b)和砖红壤(c和d)中吸附的影响Fig.3 The influences of ionic strength and Cu2+ on the adsorption of SMX by the vegetable soil (a, b) and latosol (c, d)
2.4 陪伴离子对土壤吸附SMX的影响
除溶液pH值外,陪伴离子可通过以下机制对土壤中SMX的吸附反应产生影响:①竞争吸附位点;②与SMX发生络合反应而改变后者形态;③改变表面电荷性质。首先,从图3可以看出,随着背景电解质NaCl浓度的升高,在所研究的pH值范围内,2种土壤对SMX的吸附率均未发生较大变化。这间接说明静电引力在SMX吸附反应中所起的作用较小,其理由是Cl-是典型的静电吸附阴离子,如果静电引力在SMX吸附反应中所起的作用较大,那么随着NaCl浓度的增加,土壤对SMX的吸附率应该降低,但试验结果却非如此。与此同时,提高背景电解质浓度,将对固体表面的静电场和库伦势能产生屏蔽效应,理论上也将导致SMX吸附量降低,但这也未被研究证实。
其次,加入Cu2+后,2种土壤对SMX的吸附率总体均有所上升,这个规律随着pH值和Cu2+浓度的升高越发明显。导致这种结果的原因主要是:①带正电荷的Cu2+可与SMX形成离子对,由此使得溶液中SMX阴离子的比例降低,进而使得土壤表面对SMX的静电斥力作用降低,有利于SMX向土壤表面接近;②Cu2+与土壤表面可发生专性吸附反应,并导致土壤表面正电荷数量增加,这也将有利于SMX与土壤表面结合;③借助于土壤表面吸附态Cu2+的桥梁作用,可形成土壤-Cu2+-SMX表面三元络合物,也可使得SMX的吸附量增加[26]。基于以上论述,可较好地解释当pH值较低时,Cu2+对SMX吸附反应的促进作用为何不明显。在低pH值条件下,一方面,土壤对Cu2+的吸附作用较弱;另一方面,SMX主要以中性形态存在,与Cu2+的络合程度较低,所受到的来自土壤表面的静电斥力作用也不强。在上述2种因素的综合作用下,Cu2+对SMX吸附反应的促进作用较小[27]。与之相反,随着pH值上升,土壤对Cu2+的吸附作用逐渐增强,会促进SMX吸附反应。
此外,加入苯胺和4-苯胺磺酸后,菜园土对SMX吸附量的下降较砖红壤明显(图4),且在低pH值条件下苯胺的抑制作用更强。通过上述试验结果可进一步推测土壤对SMX的吸附机理。苯胺中胺基N有孤对电子,可与H+结合。当pH值<4.6时,SMX以带+1价电荷的阳离子形态为主[28]。因此,在低pH值条件下,当土壤表面正电荷数量较多时,其对苯胺的吸附将不是以静电吸附、氢键和电子供体-受体复合等几种方式为主,这就意味着苯胺与SMX之间不可能发生对土壤表面正电荷吸附位点的竞争作用。与此同时,苯胺更多是通过π-π共轭作用或者疏水性作用与土壤表面结合[29],这说明SMX与土壤表面存在类似作用。与苯胺相比,4-苯胺磺酸的抑制作用较小,这是因为磺酸基团有较强的吸电子效应[30],降低了胺基和整个苯环的电子密度,从而降低了4-苯胺磺酸与土壤的相互作用及其对SMX吸附的抑制作用。

图4 苯胺、4-苯胺磺酸对SMX在菜园土(a)和砖红壤(b)中吸附的影响Fig.4 The influences of aniline and 4-aniline sulfonic acid on the adsorption of SMX by the vegetable soil (a) and latosol (b)
2.5 去除有机质对土壤吸附SMX的影响
H2O2氧化处理后土壤有机质含量明显下降,菜园土与砖红壤有机质含量分别下降67.6%和68.1%。图5显示,pH值为3.5~7.0时,2种土壤去除有机质后对SMX的吸附率均有所降低,且在低pH值条件下较为明显,最大吸附率下降约40.0%,这充分表明有机质是影响土壤吸附SMX能力的重要因素,进而也解释了为何菜园土对SMX的吸附量大于砖红壤。H2O2氧化法主要去除土壤中易氧化的有机质,剩余部分为难氧化有机质,如:胡敏素以及与土壤矿物质紧密结合的有机质。土壤经氧化处理后含有较多的长链烷烃化合物,而含氧、氮的有机物略微减少[31]。大量研究结果表明,有机质在土壤吸附SMX反应中有重要作用[32-33]。通过对比吸附SMX前后土壤的红外光谱,可知土壤有机质中C-H键发生拉伸振动,这表明有机质中烷烃或烯烃基团参与了土壤吸附SMX反应[21]。类似地,去除有机质后,土壤对磺胺甲氧嗪的吸附能力降低,吸附等温线Kf最高降低99%[34]。
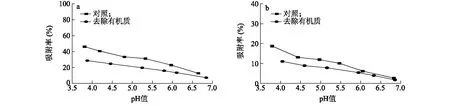
图5 去除有机质对磺胺甲口恶唑在菜园土(a)和砖红壤(b)中吸附的影响Fig.5 The influences of organic matter removal on the adsorption of SMX by the vegetable soil (a) and latosol (b)
2.6 解吸等温线
图6显示,解吸反应后,2种土壤中仍有SMX未被解吸。解吸等温线可以用来表示解吸试验结束后,单位质量土壤表面仍然吸持的吸附质数量与解吸液中吸附质平衡质量浓度的关系[22],表面吸持量越多,说明该吸附质越难被解吸。在本试验条件下,SMX解吸等温线可用Freundlich模型进行拟合(R2>0.950),具体拟合结果见表3。拟合参数1/n值均小于1.000,表明SMX在土壤中的解吸等温线是非线性关系。同时,如果土壤对有机污染物的解吸等温线Kf值越高于吸附等温线,则说明解吸过程结束后仍有相当多的有机污染物保留在土壤表面,两者越接近则表明有机污染物更易被解吸[35],且Kf值越大,土壤中有机污染物越不容易被解吸,解吸量越少。从本研究拟合结果来看,菜园土和砖红壤的解吸等温线Kf值均高于吸附等温线Kf值,这说明部分SMX与土壤表面之间存在紧密结合,因而导致土壤中SMX的吸附反应非完全可逆。菜园土Kf值高于砖红壤,表明有机质含量较高的土壤中SMX不容易被解吸,这与前人的研究结果一致[36]。此外,解吸等温线Kf值随pH值上升而逐渐降低,尤其以菜园土最为明显,即:pH值越低,SMX越不容易被解吸,反之则越容易被解吸,这与前述pH值越低土壤对SMX吸附量越大的研究结果一致。说明不同pH值条件下,土壤中存在SMX强吸附位点和弱吸附位点。也就是说,pH值越低,土壤与SMX之间可能越易产生氢键以及π-π共轭作用[37],结合越紧密,从而导致SMX难以被解吸。相比之下,pH值越高,土壤对SMX的静电斥力作用越大,阻碍了上述作用的产生,导致两者结合不牢固以及SMX易被解吸。
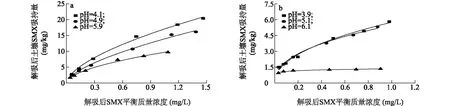
SMX:磺胺甲口恶唑。图6 菜园土(a)和砖红壤(b)对SMX的解吸等温线Fig.6 Desorption isotherm for SMX under various pH by the vegetable soil (a) and latosol (b)
3 结 论
本研究中,菜园土和砖红壤对SMX的吸附反应动力学符合拟二级动力学方程。Freundlich模型能较好地拟合这2种土壤对SMX的吸附等温线(R2>0.970)。有机质含量较高的菜园土对SMX的最大吸附量是砖红壤的3.41倍。土壤对SMX的吸附能力与pH值、陪伴离子(类型、质量浓度或浓度)以及土壤有机质含量有关。当pH值为3.5~7.0时,2种土壤对SMX的吸附能力随着pH值的升高而明显降低。Cu2+可促进SMX吸附,苯胺和4-苯胺磺酸等芳香胺类化合物均能与SMX竞争吸附,且苯胺的抑制作用较大。去除有机质后,土壤对SMX最大吸附率下降约40%,这说明土壤有机质是SMX的重要吸附载体。有机质含量较高的菜园土中,SMX的解吸率较低且SMX解吸过程中存在滞留现象,这表明其在土壤中存在不可逆吸附。

