化学平衡原理在高中化学教学中的应用
【摘要】本文论述化学平衡原理在高中化学教学中的应用,提出化学平衡原理在化学理论层面的应用、化学平衡原理在化学实验层面的应用、化学平衡原理在解题训练层面的应用等具体做法,旨在帮助学生牢固掌握判断化学平衡原理的方法,促进学生快速、准确地解答化学试题。
【关键词】高中化学 课堂教学 化学平衡原理
【中图分类号】G63 【文献标识码】A
【文章编号】0450-9889(2023)20-0125-04
化學平衡原理指的是在宏观条件一定的可逆反应中,化学反应的正、逆反应速率相等但不等于零,反应物与生成物各组分浓度不再发生改变的状态。如果一个已经达平衡状态的系统被改变,那么该系统会随之发生改变而对该改变进行抗衡,所以说这是一种动态平衡。在高中化学教学中,化学平衡原理有着十分广泛的应用,不仅被应用于方程式中,而且被应用在化学实验、解决化学问题中。学生只有掌握化学平衡原理的判断方法,才能快速解答化学问题。因此,教师应重视加强对化学平衡原理的应用,不断提高学生参与化学学习的积极性,帮助学生牢固掌握判断化学平衡原理的方法,为接下来的解题做好准备,从而促进学生快速、准确地解答化学试题。
一、化学平衡原理在化学理论层面的应用
(一)判断化学反应是否达到平衡状态
在高中化学教学过程中,学生会遇到大量的化学反应,运用化学平衡原理来判断化学反应是否达到平衡状态,既可以加深对化学平衡本质的理解,又可以借助所学知识准确判断出化学反应中两种或者多种化学物质是否达到平衡状态。在这种情况下,学生应精准掌握化学反应过程中存在的多种物质浓度及方法,假如可以发生可逆反应,不仅可以判断出多种反应现象,还可以对比反应值逆解读反应相关数据,最终判断出是否真正实现反应平衡。
例如,当判定密闭容器内的化学反应是否达到平衡状态时,假如反应体系中的气体总压强没有出现变化,即可判定该化学反应处于平衡状态。如在体积恒定容器中氮气和氢气发生反应:N2(g)+3H2(g)?2NH3(g),容器内产生的气体处于混合状态时,气体总质量没有出现变化,容器的体积在化学反应过程中同样没有出现变化情况,根据质量守恒定律相关知识,混合气体的总压强并没有因此再出现变化,所以该化学反应达到平衡状态。又如,在一些化学反应中,当有有颜色的化学物质参加反应,而该物质的颜色没有出现变化时,该化学反应也处于平衡状态。如在2NO2(g)?2NO(g)+O2(g)化学反应中,由于NO2(g)为有色物质,当该物质的颜色不变即浓度不变时,我们就能够判定这一化学反应处于平衡状态。
(二)运用平衡原理书写化学方程式
在整个化学教学中,无论是初中阶段,还是高中阶段,化学方程式都占据着极为重要的地位,是一项重点学习内容。在化学学习过程中,有不少化学题目都是围绕化学方程式展开的,学生不仅要学会正确写出化学方程式,还要真正理解化学方程式的含义,如此方能正确解答有关化学方程式的问题。在高中化学教学中,教师要运用化学平衡原理帮助学生深刻记忆、透彻理解并牢固掌握化学方程式,使学生进一步了解化学反应的原理,继而深刻分析化学平衡原理。
例如,对恒定容量的容器来说,当反应体系内的气体总压强保持不变时,我们可以确定化学反应达到平衡状态。如4NH3+5O2=4NO2+6H2O的化学方程式中,根据已学的质量守恒定律可知,容器内混合气体的总质量不变,容器内的体积也不变,说明当反应体系内的气体总压强保持不变时或混合气体的密度保持不变时,此化学反应达到了平衡状态。
二、化学平衡原理在化学实验层面的应用
(一)借助实验教学契机运用化学平衡原理
化学平衡是建立在可逆反应基础之上的,可逆反应则是在同一条件下,既能够正向进行还能逆向进行的一类特殊化学反应。大部分化学反应都具有可逆性,均能够在不同程度上达到平衡状态。实验教学是高中化学教学过程中最重要的环节之一,教师应当充分借助实验教学的契机运用化学平衡原理开展教学,通过现场演示或者播放案例的方式呈现可逆反应,指导学生以可逆反应为依托分析与研究化学平衡原理,使学生进一步理解化学平衡的内涵,增强学生的认知。
例如,在教学“浓度变化对化学平衡的影响”时,教师可以利用重铬酸根离子与铬酸根离子之间的转化实验来探究浓度变化对化学平衡的影响,指出实验原理是Cr2O72-+H2O?2CrO42-+2H+,具体实验步骤是先往K2Cr2O7溶液中缓缓滴入NaOH溶液,当溶液颜色由橙变成黄色时,化学反应平衡往正反应方向移动,然后往里面加入适量的酸,则溶液颜色由黄色变成橙色。通过观察这个实验现象,我们知道化学反应平衡往逆反应方向移动。接着,教师带领学生总结浓度变化对化学平衡影响的规律,即增大反应物的浓度或者减小生成物的浓度,平衡往正反应方向移动;减小反应物的浓度或者增大生成物的浓度,平衡往逆反应方向移动。由此可见,适当增加相对廉价的反应物或者及时分离出生成物,平衡向正反应方向移动,能够提高产物产量,减少生产成本。
(二)鼓励学生做实验探究体验化学平衡原理
在高中化学教学过程中,实验教学这一重要环节不仅是学生学习理论知识的主要途径,也是学生研究各种化学原理、规则与规律的关键方式,更是锻炼学生动手能力的常规手段之一。为更好地运用化学平衡原理,教师需要及时转变教育观念,坚持以“学生探究实验为主,演示实验为辅”的教学原则,尽可能为学生创设更多亲自动手操作实验的机会,鼓励他们依托实验深层次探究化学平衡原理,切实体会化学平衡原理的内涵,进一步提高学习效果。
例如,在“压强变化对化学平衡的影响”教学中,教师可以利用多媒体设备播放N2(g)+3H2(g)[]2NH3(g)这一可逆反应的视频,带领学生一起分析压强对合成氨的平衡的影响。学生在观察实验视频的过程中发现增大压强时,该化学平衡往正反应方向移动,减小压强时,化学平衡往逆反应方向移动。接着,教师播放可逆反应FeO(s)+CO(g)?Fe(s)+CO2(g)实验视频,并通过改变压强的大小,引导学生观察实验结果。学生发现针对该实验,通过改变压强的大小对反应的平衡没有影响。随后教师指导学生讨论探究其他条件不变,压强增大或者减小时,N2O4(g)?2NO2(g)反应平衡是否移动、移动方向如何?学生讨论后回答,并归纳总结出“在其他条件不变时,增大压强,化学平衡向着气体总体积减小的方向移动;反之,减小压强,化学平衡向着气体总体积增大的方向移动”的规律。
(三)转变实验方式内化化学平衡原理
在高中课程体系中,化学作为一门以实验为基础的自然科学类科目,涉及大量的实验研究,尤其是学生在学习化学平衡原理这一相对抽象的知识时,更是离不开实验的帮助,通过做实验学生可以更加深入地分析化学平衡原理,进而理解化学平衡原理的本质。对此,高中化学教师应该适当转变有关化学平衡原理的实验教学方式,利用发现问题的方式引导学生沿着正确的方向思考,让学生深入实验活动,认真观察实验程序与反应变化,进而内化化学平衡原理。
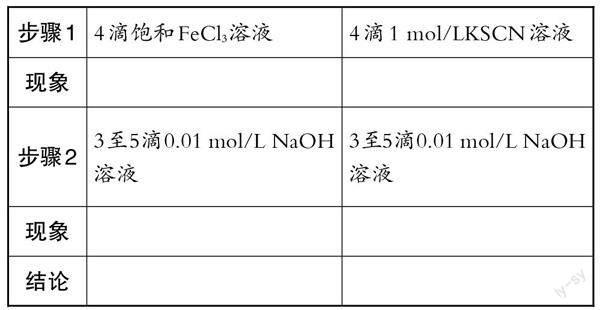
例如,以“化学平衡的移动”教学为例,本节课是以化学平衡状态为基础,通过实验进行验证,探究反应物的浓度对化学平衡状态的影响。课堂上,在探究反应物的浓度对化学平衡移动的影响时,教师可以转变实验方式,安排以下实验教学环节。教师事先准备好0.05 mol/L的氯化铁溶液、0.1 mol/L的硫氰化钾溶液、1 mol/L的硫氰化钾溶液、0.1 mol/L的氢氧化钠溶液,以及若干支试管。实验原理:FeCl3(aq)+6KSCN(aq)?Fe(SCN)3(aq)+6KCl(aq)。实验步骤:(1)向盛有5 mL 0.05 mol/L FeCl3溶液的试管中加入5 mL 0.1 mol/L KSCN溶液,溶液显红色;(2)将(1)中红色溶液分置于两支试管中;向其中一支试管中滴加4滴饱和FeCl3溶液,充分振荡,观察颜色变化;向第二支试管中滴加4滴1 mol/LKSCN溶液,观察溶液颜色变化;(3)向(2)的两支试管中各加入3至5滴0.01 mol/LNaOH溶液,观察实验现象,并要求学生完成下表。
接着,教师组织学生对上述实验进行深入思考、讨论,并且由学生代表来解释实验现象并得出结论:增大生成物浓度,平衡向逆反应方向移动;减小生成物浓度,平衡向正反应方向移动;增大反应物浓度,平衡向正反应方向移动;减小反应物浓度,平衡向逆反应方向移动。经过深入探讨,学生能够深刻记忆上述实验现象、实验过程和实验原理。这有助于他们在大腦中形成相对完善的知识体系,进一步加深他们对化学平衡原理的认识和理解。
三、化学平衡原理在解题训练层面的应用
(一)巧用化学平衡判定方法解答试题
在高中化学课程教学中,要想更好地运用化学平衡原理,教师不仅可以在理论知识讲授与实验操作两个环节运用化学平衡判定方法,还可以基于解题训练层面切入,围绕化学平衡原理的运用设计有针对性的训练习题,为学生创设运用化学平衡原理解题的机会,指导学生学会巧妙运用化学平衡判定方法解答试题。因此,高中化学教师在解题训练中,应带领学生在解题过程中不断通过练习与总结,进而牢固掌握化学平衡原理的要点,增强他们对化学平衡知识和判别方法的理解。
例1:在一个密闭的容器内,化学反应mA(g)+nB(g)?pC(g)+qD(g)达到平衡状态,不改变温度条件,将容器体积扩大1倍,当化学反应重新达到平衡时,物质B的浓度变为原来的45%,那么以下说法正确的有( )。
A.化学平衡往逆反应方向进行移动
B.物质A的质量分数提高
C.物质A的转化率降低
D.m+n 【分析】当容器体积增大时会对化学平衡产生影响,学生在解答本题时,可以假设容器体积变大后不会对化学平衡产生影响,那么物质B和C的浓度均为原来的50%,但反应达到平衡时,B的浓度是原来的45%,说明减小压强平衡向正反应方向移动,如此则可说明m+n (二)巧用化学平衡极限方法解答试题 从本质来看,化学平衡都属于可逆反应,即为化学反应中的反应物与生成物均不能完全消耗掉。在处理有关化学反应平衡类的选择题时,教师提示学生可以结合化学平衡原理的特点将一些不是可逆反应的化学反应直接排除,提高他们做题的正确率。此外,在有关化学平衡原理的计算题中,教师还可以指导学生使用极限法,即假设可逆反应的起始反应物均完全反应,以这种极限条件为假设将会得到生成物的最大值,这样学生在解决化学平衡原理的计算题时就可以快速计算出正确的结果。 例2:已知在一个恒容密闭的容器中,1 mol的水蒸汽与1 mol的一氧化碳气体在一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2(g)且达到平衡状态,生成0.68 mol的二氧化碳,假设其他条件不变,再把4 mol的水蒸汽充入到密闭容器中,当反应再次达到平衡状态时,那么生成物二氧化碳的量可能是( )mol。 A.2 B.1.4 C.0.52 D.0.94 【分析】在处理这类题目时,教师可以指导学生采用极限假设法进行计算,将1 mol的水蒸汽与1 mol的一氧化碳气体反应达到平衡时,有0.32 mol CO、0.32 mol水蒸汽、0.68 mol CO2、0.68 mol H2。在此基础上,再通入4 mol水蒸汽,化学平衡显然向右移动,假设反应完全进行,则生成的二氧化碳气体为1 mol,但是不可能到1 mol,因此只能处于0.68至1 mol范围之内,通过对比分析,只有选项D中的0.94在这一范围内,符合答案要求。 (三)巧用化学平衡分割方法解答试题 在化学可逆反应中,外界条件包括催化剂参与、温度变化、容器体积等,均会影响化学反应平衡,将正反应与逆反应速率的相等状态进行打破,无论遇到有关化学平衡原理的任何题型时,学生都要认真审题,仔细研究题干中涉及的环境变化条件,把起始量不一样的两个化学平衡进行适当分割,转变成一样的起始量,即对分割法的运用,再结合题干中提供的具体条件进行解题,从而帮助学生掌握运用化学平衡原理分割法解答试题的窍门。 例3:在恒容、恒温的条件下,有两个体积一样的甲、乙容器,往甲容器里面分别充入1 g的二氧化硫和氧气,往乙容器里面分别充入2 g的二氧化硫和氧气,那么下列说法不正确的有( )。 A.乙容器中的化学反应速率比甲容器的大 B.乙容器中的化学反应达到平衡状态后氧气浓度比甲容器的大 C.乙容器中的二氧化硫气体的转化率比甲容器的大 D.乙容器中的化学反应达到平衡状态后二氧化硫气体的体积分数比甲容器的大 【分析】本题主要考查化学平衡建立过程和化学平衡的影响因素。选项A为浓度越大反应速率越大;选项B为由于乙容器中的量是甲容器中的两倍,所以反应后乙容器中剩余的氧气多;选项C为由于乙容器中的量是甲容器中的两倍,气体物质的量越大,压强越大,因此乙容器中相当于增大压强,平衡正移,二氧化硫的转化率增大;选项D为由C选项可知,乙容器中二氧化硫的转化率变大,所以二氧化硫的体积分数小。综上可知,D选项错误,因此选D。 综上所述,在高中化学教学中,教师应充分认识化学平衡原理的重要性。虽然化学平衡原理学习起来有一定的难度,但是化学平衡原理是有特点、有规律可循的,教师应把握好教学契机,从理论知识讲授、化学实验操作与课后解题训练等多个方面加以运用,为学生创设更多运用化学平衡原理的机会,使学生在实际学习过程中不断积累与归纳运用化学平衡原理的经验,让学生深刻体会到化学平衡原理的实用性,不断增强自身的化学综合能力。 参考文献 [1]贺行武.关于探讨化学平衡原理在高中化学里的应用[J].中学生数理化(教与学),2020(10). [2]范德超.“化学坐标图像”教学探索[D].成都:四川师范大学,2022. [3]孙金凤.高中化学变化观念与平衡思想的教学实践探索[D].成都:四川师范大学,2021. [4]郑弘丽.高中化学建模教学的实践研究[D].芜湖:安徽师范大学,2020. [5]贺中金.浅析如何在高中化学教学中巧用化学平衡原理[J].天天爱科学(教育前沿),2019(7). 作者简介:陆采添(1990— ),广西钦州人,本科,学士,主要研究方向为高中化学教学。 (责编 林 剑)

