改性沸石用于人工湿地处理农村污水
孙剑平,扈师鸣,李绍峰
(1.沈阳建筑大学市政与环境工程学院,辽宁 沈阳 110168;2.深圳职业技术学院材料与环境工程学院,广东 深圳 518055)
近几年,人工湿地正在向着更绿色高效的方向发展,应用领域也愈发广泛[1]。人工湿地已用于处理农村生活污水中的氮磷等主要污染物[2]。白雪莹等[3]以锰砂为湿地填料进行脱氮除磷影响因素研究,去除率可达到90%以上,但材料本身含有的锰离子有可能微量转换为其他价态,进而对出水造成二次污染,且脱氮阶段污水初始浓度对吸附效果的影响较大。Xia Ruize等[4]以铁碳材料为基质,依靠铁质材料的磁性和活性炭的吸附性能,并利用铁碳原电池原理,实现物理化学共同作用,总磷去除率可达到94.3%,且还可以去除重金属离子等其他污染物,但本身的制作成本较高,且前中期的出水COD质量浓度较高[5]。D.Parde等[6]通过对各个行业的生产废料作为人工湿地基质来进行研究,发现锯屑、零价铁、LECA等材料是去除磷、硫酸盐和有机物的较好材料,最高去除率可达到80%,但材料的制作以及前处理较为繁琐,且去除效果受材料本身效果影响较大。人工湿地的优点在于,建造运行管理费用低,技术水平要求不高,易于维护,针对污水量不大的污水能有效处理;缺点为土地占有面积较大、处理效率缓慢,进水端污水需经过预处理等[7-8]。针对上述问题,笔者从填料的改性入手,将改性填料应用于人工湿地处理农村污水,通过实验研究确定填料的最优工艺条件,进而提高人工湿地的处理农村生活污水的效果。
1 实 验
1.1 实验材料
斜发沸石来自广东深圳,经过清洗过筛备用;玉米秸秆来自广东联丰农作物加工厂,过筛后取粒径小于0.85 mm的材料备用。
1.2 实验仪器
实验仪器包括:365-紫外可见分光光度计,DHG-9070A电热鼓风干燥箱,微波消解仪,ORION 5 STAR pH计,Milli-QA超纯水仪,UPW-20NE超纯水器,AL-204电子天平,VB 24 Plus磁力搅拌器。
1.3 模拟废水配制方法
实验原水采用实验室配制的模拟农村生活污水,主要有可溶性淀粉、葡萄糖、蛋白胨、氯化铵、磷酸二氢钾、氯化钙、氯化镁来进行配制[9]。此溶液中,总磷质量浓度6.73 mg/L,氨氮质量浓度46.45 mg/L,COD质量浓度394.12 mg/L。
1.4 填料材料选取
选取质量10g 、粒径为0.425~0.85 mm的斜发沸石和玉米秸秆,采用去离子水冲洗三次,去除孔隙中的杂质,烘干后各取5 g,室温下分别放入两个250 mL锥形瓶中,各加入1 mol/L的FeCl3溶液200 mL。转速100 r/min下恒温振荡24 h,反应后将材料用去离子水清洗三次至洗至中性,放入烘箱110 ℃烘干备用[10-11]。再分别取5 g未改性的以及铁离子改性后的斜发沸石和秸秆放入装有250 mL废水的锥形瓶中,转速100 r/min下恒温振荡60 h,反应后取上清液,经0.45 μm滤膜过滤,取滤后溶液上清液测定吸光度计算污染物质量浓度。
1.5 不同因素对处理效果的影响
投加5 g复合改性沸石于装有250 mL废水的锥形瓶中,150 r/min条件下恒温振荡反应60 h,测定反应前后污染物质量浓度,计算污染物去除率,对比沸石改性方式、粒径大小、投加量和溶液pH值等因素对去除效果的影响,得出改性沸石处理农村生活污水中污染物的最优条件。
2 结果与分析
2.1 不同填料基质对污染物去除效果的影响
分别在6 h、12 h、24 h、48 h、60 h取样,计算不同污染物的浓度和去除率,实验结果如图1所示。

图1 不同填料对水中污染物去除率影响Fig.1 Effects of different fillers on the removal rate of pollutants in water
由图1可知,无论是否改性,沸石的污染物去除效果都要比秸秆的去除效果要好,并且改性沸石较未改性沸石处理效果有较大提升。60 h时改性沸石总磷去除率达81.15%,较未改性沸石增加了15.3%;氨氮去除率为81.45%,较未改性沸石增加了13.67%;COD去除率为81.41%,较未改性沸石增加了4.39%。因此选择改性斜发沸石作为后续实验的基质材料。秸秆在去除氮磷污染物过程出现不稳定情况,可能是因为长时间的振荡处理过程中,玉米秸秆自身内部存在的氮磷元素被释放出来。
2.2 改性条件对污染物质量浓度的影响
对比分析天然沸石、碱改性沸石,Fe3+改性沸石以及NaOH-Fe3+复合改性沸石四种材料对水中污染物的去除效果,结果见图2。从图中可以看出,复合改性沸石去除效果最优,60 h后污染物质量浓度基本稳定不变吸附达到平衡。
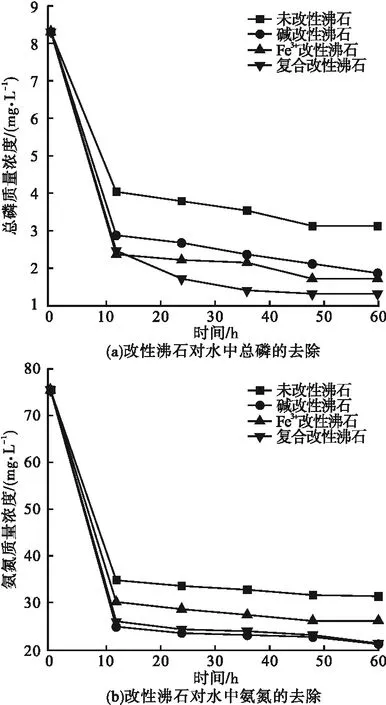
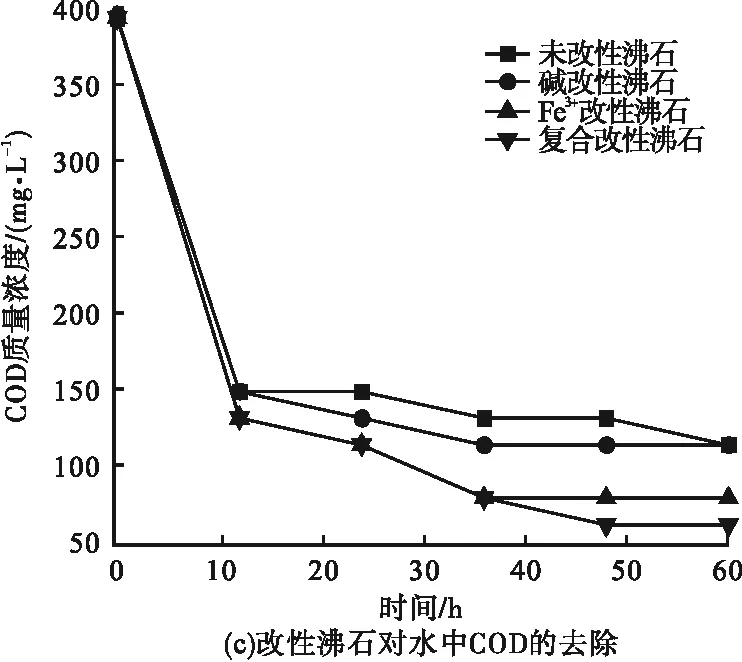
图2 改性方式对污染物去除效果的影响Fig.2 Influence of modification method on pollutant removal efficiency
2.3 沸石粒径大小对污染物去除率的影响
分别将5 g粒径为2~5 cm、0.2~1 cm、0.45~1 mm、0.2~0.4 mm的复合改性沸石放入250 mL的实验室模拟污水中恒温振荡48 h,取上清液测定吸光度计算污染物去除率,结果见图3。从图中可以看出,随着沸石粒径的减小,污染物去除效果都有所提高。分析原因是因为随着粒径变小,材料暴露出来的外比表面积增大,当沸石粒径从0.2~1 cm进一步减少时,对污染物去除率提升幅度变小,原因可能是粒径越小,振荡过程中沸石间颗粒碰撞也会越激烈,使已附着在沸石表面孔隙的污染物脱离沸石,导致污染物流失。

图3 沸石粒径大小对污染物去除率的影响Fig.3 Effect of zeolite particle size on pollutant removal rate
2.4 沸石投加量对污染物去除率的影响
分别将不同质量的复合改性沸石放入250 mL的模拟农村生活污水中,相同条件下在磁力搅拌器上进行48 h反应,取上清液测定吸光度计算去除率,结果见图4。从图中可以看出,总磷和氨氮在沸石投加量5 g时去除率达到82.4%和81.93%,COD在沸石投加量4 g时去除率为80.23%。再加大沸石投加量,去除率略有提升,分析原因是因为已达到吸附动态平衡。结合处理效果及成本分析,决定每250 mL污水投加5 g沸石的比例较为适宜。
2.5 pH值对污染物去除率的影响
实际农村生活污水的水环境比较复杂,pH值是水环境的一个重要指标,在不同pH值的环境下进行实验,水中污染物的去除率如图5所示。由图5可知,三种污染物的去除率都在pH=7的水环境下达到最大。当pH<7时,沸石表面铁的氢氧化物很难与水中磷酸根离子络合形成沉淀;氨氮以NH4+形式存在,与水中氢离子存在竞争吸附。当pH>7时,水中OH-与水中的磷酸根阴离子产生竞争关系;氨氮以NH3·H2O形式存在,极性吸附剂沸石对其吸附能力弱。而对于COD而言,实验配水主要是有机羧酸,不论pH大于或小于7,都主要以羧酸阴离子形式存在,沸石本身带负电,对羧酸阴离子产生排斥作用,所以pH=7时,三种污染物去除效率最高,经计算总磷去除率为84.12%,氨氮去除率为81.89%,COD去除率为83.41%。
3 数据处理和表征分析
3.1 吸附等温线

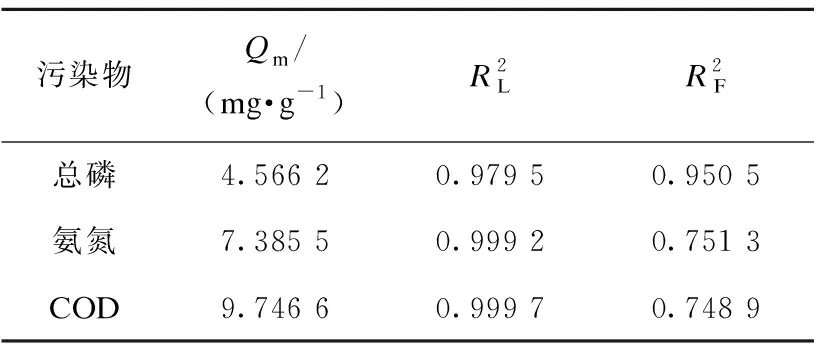
表1 Langmuir方程和 Freundlich方程拟合结果Table 1 The fitting results of Langmuir equation and Freundlich equation
从表1可以看出,对于三种污染物,都是Langmuir方程比Freundlich方程拟合结果更高。说明当温度不变时,吸附过程主要为单分子层吸附形式,吸附到沸石上污染物之间没有相互作用力。
3.2 吸附动力学过程
对复合改性沸石进行吸附动力学试验,拟合结果见表2。表中qe为吸附平衡时的吸附容量,K1、K2为吸附速率常数。

表2 准一级速率方程和准二级速率方程拟合结果Table 2 Fitting results of pseudo-first-order rate equation and pseudo-second-order rate equation
从表2可以得出,对于三种污染物,都是准二级动力学能更好地描述污染物在沸石上的吸附过程。说明复合改性沸石对三种污染物可能主要是化学吸附。
3.3 表征分析
3.3.1 SEM扫描电镜分析
采用HITACHI SU5000扫描电镜观察沸石表面微观状态,结果如图6所示。

图6 天然斜发沸石的表面全貌和复合改性沸石的表面全貌Fig.6 Surface overview of natural clinoptilolite and overall surface view of composite modified zeolite
从图中可以看出,改性前天然斜发沸石表面光滑,块状结构,形状整齐。复合改性后的沸石表面呈较为粗糙的海绵状,孔隙加深,这种粗糙颗粒表面使沸石更易与吸附质接触,故复合改性沸石可以增强对污水中污染物的吸附能力。
3.3.2 BET及孔隙度分析
改性前后沸石孔结构参数见表3。由表可知,天然沸石经过碱改性,比表面积、孔容和平均孔径有明显的提升。天然沸石经铁离子改性后,比表面积和孔容减小,可能是沸石表面形成的铁的氢氧化物会堵塞部分孔道,以至于沸石的比表面积有所减小[14]。先碱改性后铁改性沸石较天然沸石孔容和孔径都有所增大,虽然在沸石孔道内形成铁的氢氧化物沉淀减小了沸石的比表面积,但铁的氢氧化物可与污染物络合提高去除能力,因此复合改性更利于污染物的吸附。
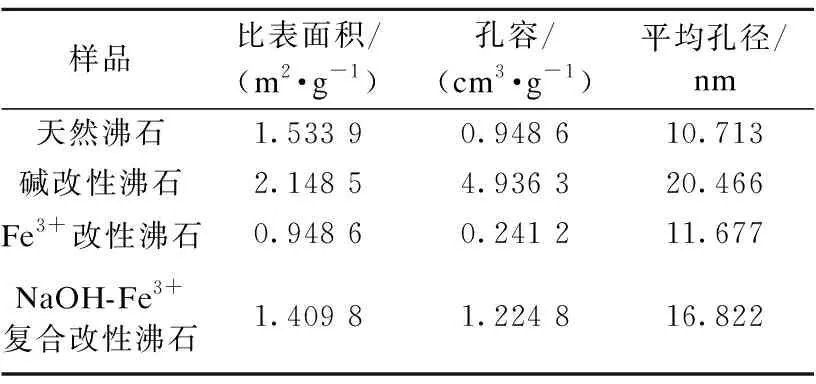
表3 四种状态沸石的BET结果Table 3 BET results of four states of zeolite
3.3.3 沸石改性前后能谱(EDS)分析
X射线光电子能谱是分析物质表面化学性质的一项技术,可以分析除H和He以外的所有元素。天然沸石与复合改性沸石的EDS分析结果见表4。从表中可以看出,天然沸石铁元素含量很少,复合改性后硅铝比下降,铁元素含量明显增加,表明铁离子成功进入了沸石孔隙结构。

表4 天然沸石与复合改性沸石的EDS分析Table 4 EDS analysis of natural zeolite and composite modified zeolite %
3.3.4 X射线光电子能谱(XPS)
复合改性沸石反应前后XPS谱图如图7所示。从图中可以看出,相比于吸附反应前的复合改性沸石,反应后的复合改性沸石出现P2p、N1s的特征峰,C1s特征峰强度升高,表明污水中的总磷、氨氮和COD被吸附到了沸石上。
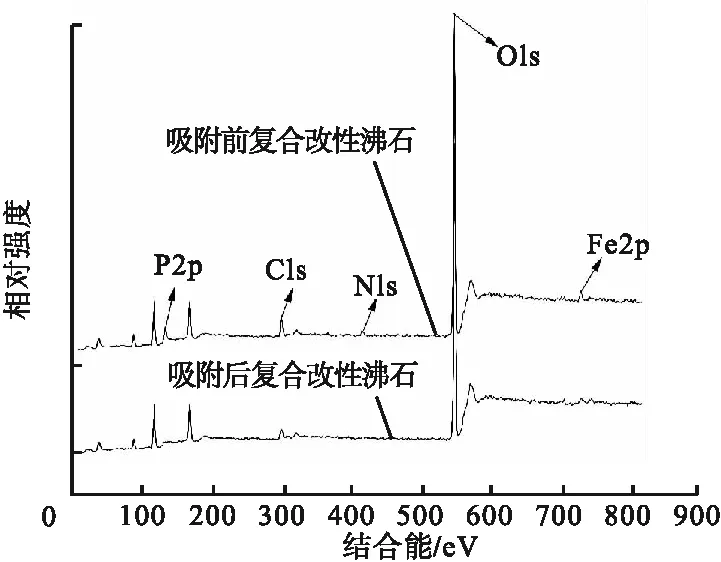
图7 复合改性沸石反应前后XPS谱图Fig.7 XPS spectrum of composite modified zeolite before and after reaction
3.4 机理分析
复合改性沸石孔隙内形成的铁的氢氧化物可以与磷酸根发生络合沉淀反应,提高了总磷的去除效果。复合改性后沸石中的铁离子可以与NH3·H2O发生反应生成氢氧化铁沉淀,促进生成游离态的氨根离子,而后沸石中阳离子与氨根离子发生离子交换反应提高氨氮去除率。以上过程存在的反应为
Fe3++NH3·H2O→Fe(OH)3↓+NH4+
复合改性沸石对COD的去除率较天然沸石仅提升了4.39%,可能是因为改性后分子筛孔体积和平均孔径增加,促进了COD在分子筛微孔内的传输,但提升效果有限。
4 结 论
(1)经过基质材料和沸石改性方式对比,确定复合改性沸石作为基质材料对污染物的去除效果最好,在沸石粒径0.2~0.4 mm、沸石投加量为20 g/L、pH=7的条件下,总磷去除率达84.12%,氨氮去除率达81.89%,COD去除率达83.41%。
(2)Langmuir方程和准二级反应动力学方程拟合结果更适用于复合改性沸石吸附过程。吸附过程主要为单分子层吸附形式,并主要体现为化学吸附。
(3)复合改性沸石内部铁的氢氧化物可与磷酸根发生络合沉淀反应,沸石中铁离子与NH3·H2O反应促进氨根离子被离子交换去除,改性后对总磷和氨氮去除率显著提高。

