金银合金发光纳米团簇研究进展
卞佳林,王学娟,刘国锋
同济大学化学科学与工程学院,上海 200092
金属纳米团簇是一种以几个至几百个金属原子为核、有机配体分子为壳,通过金属-金属相互作用、金属-配体相互作用组装形成的核壳型纳米结构[1-8]。由于其尺寸与电子的费米波长相当,具有类似于分子的离散能级,表现出类分子的光学、电学和化学等特性[9-10]。同时,由于金属的缺电子性质,金属原子可以和有机分子中含孤对电子的原子进行配位,获得有机配体分子的理化性质,例如,通过有机配体的手性诱导和手性转移,赋予金属纳米团簇独特的手性特性[11]。此外,基于纳米团簇原子级的精确结构,其内部的金属组成和排列方式可以被精准调控,也可以通过配体修饰和交换等策略,定向改变纳米团簇表面结构及理化性质。由于金属纳米团簇大的比表面积、较多暴露的活性原子以及不同于金属纳米粒子的电荷分布等特性,其在化工催化、能源环境、食品安全、农业加工、医学诊断、光电材料和信息存储等诸多学科领域具有广泛的应用前景[12-13]。
金、银和铜等贵金属发光纳米团簇已经得到了广泛的研究,近年来,关于金银合金发光纳米团簇的研究越来越受到科研工作者的青睐[12,14]。通常,单一金属纳米团簇发光效率较低,金银复合纳米团簇中的金银原子协同作用可以用来增强发光性能和手性[9],如以金原子为核、银作为媒介原子连接金原子和有机配体分子,获得的金银复合纳米团簇可以有效提升发光效率,同时更有效地实现手性传递和转移[15]。本文主要概述近年来金银双金属发光纳米团簇的制备方法、发光性质以及其应用于生物成像、分子识别与传感和作为光敏剂提升抗菌活性等方面的研究进展。
1 金纳米发光团簇
随着纳米材料与技术的发展,在生理环境下表现出高光稳定性的发光纳米颗粒,如镉或铅无机量子点被开发用作传统有机发光分子探针的替代品,但镉或铅对人体有严重的生理毒性,严重影响了此类纳米材料在生命医学领域的应用推广。因此,对生物环境耐受度高、毒性小的金纳米材料便成为研究者新的选择,特别是尺寸小于2 nm 的金纳米团簇,由于其优异的发光性能和精确的化学组成与拓扑结构,近年来备受材料学家和化学家的关注。
金纳米团簇(AuNCs)是以一个或多个零价的金原子作为核心,通过连接外部的Au(I)形成完整的核壳团簇结构。其中,核心Au(0)原子是在纳米团簇的合成过程中由三价金或一价金离子经谷胱甘肽(GSH)还原获得,其他常见的还原剂有硼氢化钠、CO、三乙胺和甲醛等。通常,外部的Au(I)不够稳定,采用硫醇分子或硫代硫酸盐等含硫有机配体,通过Au—S 键作用可进一步稳定金纳米团簇,同时也实现了金纳米团簇的表面功能化[5-7,16-17]。
目前已经报道的AuNCs 可实现从可见光到近红外二区的发光[18],主要基于两种发光机制。一是由于金纳米团簇的金原子被限制在分子尺度和特殊的离散能级中,能级差变大导致的量子限域效应(QCE)[19]。金纳米团簇纳米级的尺寸增加了表面金原子的无序性和缺陷,无序性会引起表面激子的形成,缺陷则会使能隙中产生更多附加能系,进而使金纳米团簇具有独特的发光性能。二是AuNCs通过配体金属电荷转移(LMCT)以及配体金属-金属电荷转移(LMMCT)产生可调的发光[20-21]。
Chen 等研究表明,AuNCs 的发光受配体种类、溶液的pH 以及反应温度等诸多外界因素的影响,其中AuNCs 的发光受有机配体的影响最为明显,因而有望通过配体的理性设计实现AuNCs 发光波长的精确调控[22]。Li 等以聚腺嘌呤为模板合成了AuNCs,当用290 nm 的光激发时,其在475 nm 处有较强的蓝光发射[23]。Sahoo等以双链脱氧核糖核酸(DNA)为模板合成了AuNCs,其激发波长为320 nm,在580 nm 处产生明亮的橙光[24]。Kawasaki 等以胃蛋白酶为模板,通过对反应溶液pH 的调节,合成了具有蓝色、绿色和红色发射的AuNCs,分别对应纳米团簇Au5(Au8)、Au13和Au25[25]。Song 等以巯基修饰的环糊精为配体,成功合成了近红外二区的发光AuNCs,其发射波长为1 050 nm,可作为体内蛋白质和抗体的标记物,实现靶向肿瘤药物在近红外二区(NIR-II)的可视化[26]。但是,早期报道的金纳米团簇的发光量子产率(PLQY)都较低,通常低于10%,限制了这类材料的实际应用。2012年,Luo 等利用聚集诱导发光(AIE)效应显著提升了金纳米团簇的发光性质,合成了发光量子产率达15%的金纳米团簇。该研究选择谷胱甘肽作为有机配体,同时谷胱甘肽在团簇合成过程中还兼具还原剂的作用,二者功能可以通过反应温度进行协调。其关键策略是诱导Au(I)-硫醇盐复合物在原位产生受控聚集的Au(0)核,形成Au(0)@Au(I)-硫醇盐核壳纳米团簇,研究发现其强发光主要由纳米团簇表面上Au(I)-硫醇盐复合物的AIE 效应所致(见图1)[27]。
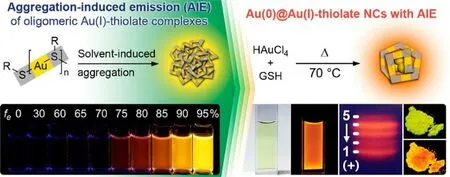
图1 聚集诱导发射实现超亮Au(0)@Au(I)-硫代酯核壳纳米团簇的构筑[27]Fig.1 Schematic of aggregation-induced emission of Au(0)@Au(I)-thiolate core-shell nanoclusters[27]
2014 年,Yu 等同样采用谷胱甘肽作保护剂,利用CO 作为还原剂,合成了一种较强发光的Au22(SG)18(SG 为谷胱甘肽基团),发光量子产率从0.1%提高到8%,并具有较大的斯托克斯位移和微秒级的发光寿命。通过比较具有强发光性质的Au22(SG)18纳米团簇和发光微弱的Au22(SG)16纳米团簇以及Au22(SG)17纳米团簇,发现Aun(SG)m纳米团簇对原子组成和构型高度敏感[28]。这为之后研究不同配体数对纳米团簇发光性质的研究奠定了基础[29]。在团簇壳层引入刚性的配体分子,可以有效减少表面配体因拉伸/振动引起的非辐射能量损失,从而增强团簇发光。Pyo 等基于这一策略,以谷胱甘肽为配体,同时使用大位阻的四辛基铵(TOA)阳离子刚化壳层,合成了发光量子产率大于60%的Au22(SG)18金纳米团簇。通过对Au22(SG)18进行的时间分辨和温度相关光学测量表明,在冰点以下存在高量子产率可见光发光,证明了壳刚度提高了发光量子产率[30]。除上述方法外,还可采用相转移剂使硫醇和Au(I)实现更充分的接触,使用CO 或者硼氢化钠作为还原剂,可得到粒径小、单分散性好的纳米团簇[31]。此外,精氨酸、多巴胺和脯氨酸等也可用作为金纳米团簇合成的配体分子。
2 银纳米发光团簇
银纳米团簇作为另一类重要的贵金属纳米团簇,既可以采用硫代硫酸盐或者硫醇做配体来保护银纳米团簇防止聚集和氧化,也可采用炔基化物和膦等有机物作为配体[32]。相比于金,银的稳定性较弱,在空气环境中更易被氧化和吸水,因此合成稳定高效的发光银纳米团簇仍存在挑战。目前,银纳米团簇主要由直接还原法、化学刻蚀法和配体交换法等合成方法来制备[1,10,33]。
直接还原法是现阶段采用较多的方法,可通过调整反应液的pH、还原剂的浓度、溶剂极性以及反应物浓度等来控制反应速率[34-35]。Zhang 等采用三乙胺作为还原剂与反应基质,将过量的三乙胺滴加在含有AgNO3和N-[(R/S)-1-(萘-4-基)乙基]丙基-2-炔-1-胺的二氯甲烷/甲醇混合溶剂中,在4 ℃下静置3 d 得到具有圆偏振发光(CPL)的深红色块状晶体的R/S-Ag17 纳米团簇[29]。
化学刻蚀法可获得一些尺寸较大且结构致密的纳米团簇[36]。Khatun 等采用硫醇刻蚀法合成了银纳米团簇[Ag59(2,5-DCBT)32]3-(2,5-DCBT:2,5-二氯苯硫醇),发现这一银纳米团簇可作为其他三类银纳米团簇[Ag44(4-FTP/4-CTP)30]4-(4-FTP:4-氟苯硫酚)、[Ag25(2,4-DMBT)18]-(2,4-DMBT:2,4-二甲基苯硫酚)和[Ag29(1,3-BDT)12(PPh3)4]3-(1,3-BDT:1,3-苯二硫酚,PPh3:三苯基膦)的前驱体[37]。
配体交换法可在不改变纳米团簇内核前提下实现部分或者完全的配体交换,是精细调控纳米团簇尺寸和结构的一种重要手段。Chang 等通过还原Ag—S 键和配体交换法将Ag21[S2P(OiPr)2]12和Ag20[S2P(OiPr)2]12成功制备并分离出Ag21[Se2P(OiPr)2]12和Ag20[Se2P(OiPr)2]12两类含Ag—Se 键的纳米团簇[38]。此外,还采用固态合成法获得了Ag9纳米团簇,在惰性气氛下或乙醇保存下其固态高度稳定,发现其还可在含水的混合溶剂中稳定存在[39]。
模板辅助合成也是化学合成纳米团簇的方法之一,主要基于模板/配体的保护合成金属纳米团簇。Alhilaly 等采用Cl-作为阴离子模板,合成了三种原子精度和维数控制的银纳米团簇。其中两种为联吡啶连接的纳米团簇节点(称为基于纳米团簇的框架,NCF)组成的一维和二维结构框架,展现了纳米团簇尺寸中单个Ag 原子差异在控制NCF 维数、调节光学性质和提高热稳定性方面的作用。并认为通过原子级精确组装和尺寸控制的纳米团簇可用于构建结构可调的簇基框架材料(见图2)[40]。
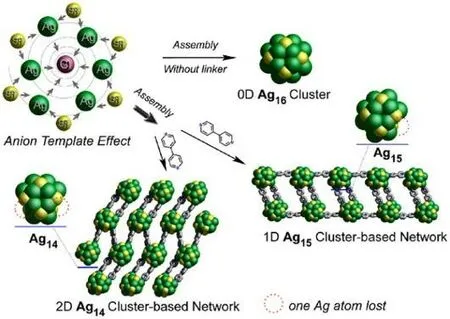
图2 阴离子模板法合成银纳米团簇并组装形成纳米团簇框架[40]Fig.2 The anions-directed synthesis of silver nanoclusters and their assembly of nanocluster-based frameworks [40]
银纳米团簇的发光特性也备受关注。2002 年,Zheng 等报道了第一例稳定的水溶性发光银纳米团簇[41]。之后还以寡核苷酸为配体,合成了系列具有从蓝光到近红外发光特性的银纳米团簇[42],这些纳米团簇还具有长的发光寿命以及耐光漂白的性质。Rao 等通过界面合成得到了蓝光发射的Ag7和近红外发光的Ag8纳米团簇,其中Ag8纳米团簇对温度和溶剂均表现出一定的响应特性[43]。当采用谷胱甘肽、半胱胺酸衍生物、青霉胺和DNA 等手性分子作为银纳米团簇合成的配体时,还可获得具有手性光学活性的银纳米团簇[44-46]。Kumar 等采用双齿α-二氢脂酸为配体合成了稳定的手性发光银纳米团簇,其在660 nm 处发出明显的红光,发光量子产率(7.6%)强于相应谷胱甘肽和半胱氨酸修饰的银纳米团簇。在圆二色吸收(CD)光谱中表现出区别于手性配体的团簇手性信号,基于该类配体对映体构筑的银纳米团簇呈现显著的镜像CPL 信号[44]。Luo 等设计了一对含手性炔烃配体的对映体银纳米团簇[Ag17(R/S-NYA)12](NO3)3,光致发光量子产率为8%[27]。该银纳米团簇的CD 光谱在波长为240~700 nm处显示出优异的CD 镜像信号,同时在745 nm 处可检测到明显的CPL 信号,被认为其CPL 的大斯托克斯位移主要是由Ag—Ag 键伸长引起的,此外炔基也具有不可忽略的贡献[29]。
3 金银合金纳米团簇
对于金属纳米团簇的合成,掺杂通常是指在不改变原有金属纳米团簇结构的前提下,通过不同金属原子间的替换或取代,获得新的双金属或多金属纳米团簇;合金化是指在纳米团簇框架中含有两种或两种以上金属原子的纳米团簇[47]。金属纳米团簇由于具有原子精确结构,掺杂或合金化已被证明是调整其理化性能的有效方法[48-49]。通常,将原子掺杂到母体纳米团簇中将提高它们的热稳定性和催化活性[50-51]。此外,纳米团簇的电子结构和光学性质也可以通过用异质金属替代来定制[52-53]。也就是说金银合金纳米团簇可以通过金银原子间作用来调整其性质[33,54]。目前金银合金纳米团簇的合成方法主要有三种。(1)共还原法(一锅合成法):将金银前驱体HAuCl4和AgNO3混合,然后引入特定的还原剂进行氧化还原反应,形成金银合金纳米团簇[55-56]。(2)氧化还原合成法(两步合成法):先利用AgNO3与配体形成银纳米团簇,在电置换的基础上加入HAuCl4氧化银纳米团簇,形成金银合金纳米团簇[57]。(3)反氧化还原法:先混合HAuCl4与配体,形成金纳米团簇后加入AgNO3来取代金纳米团簇中的金原子,形成金银合金纳米团簇[58]。其中共还原法最为常用[27-28,44,59]。
Negishi 等通过共还原法获得了Ag 掺杂的Au25-nAgn(SC12H25)18(n=0~11)双金属纳米团簇,并研究了Ag掺杂对稳定的硫代酸保护Au25纳米团簇Au25(SR)18电子结构的影响(SR为SC12H25同系物),结果表明Au25(SR)18的电子结构对Ag 掺杂敏感,并可通过掺入Ag 原子进行连续调制[52]。Udayabhaskararao 等采用了氧化还原合成法,以巯基丁二酸为配体,先合成银纳米团簇Ag7,8前驱体,再引入金原子,通过电交换反应合成得到13 核Ag7Au6合金团簇,其发射波长为650 nm[57]。Wu 等在2012 年首次报道了有关金抗电偶反氧化还原制备金银合金纳米团簇的方法,研究发现当金或银纳米粒子的尺寸减小到小于3 nm 时,还原活性大大增强[58]。这与经典的氧化还原理论相反,该理论认为金属离子可以很容易地被更多的活性金属还原。此外,抗电偶反氧化还原为在纳米尺度上制造合金或调整纳米结构的组成、结构和性能提供一种简单而温和的方法。
Pei 等在温和的条件下通过Au(I)-Ag(I)纳米团簇的C—H 活化,证明了氧鎓Au(I)簇氧离子的重要性,提出了一种用于乙腈C—H 活化的协同金属化/去质子化过程,从而在质子溶剂的帮助下实现乙腈双子四聚体双金属簇的构筑(见图3),为Ag2O 参与金催化过程提供了新的见解[60]。

图3 [(CCN)2Au8Ag4(dppy)8(CH3CN)2](BF4)6 双金属簇的结构[60]Fig.3 Illustration of cluster [(CCN)2Au8Ag4(dppy)8(CH3CN)2](BF4)6 [60]dppy: diphenyl-2-pyridylphosphine
配体交换法可选择性替换金属纳米团簇表面的配体,是实现合金纳米团簇后修饰的重要策略之一。Yang 等采用原位两相配体交换法制备合金纳米团簇,获得了一系列合金纳米团簇Au20Ag1(SR)15,Au21-xAgx(SR)15(x=4~8),Au21-xCux(SR)15(x=0,1)和Au21-xCux(SR)15(x=2~5)(R 为叔丁基)(见图4)[61]。有趣的是,这些双金属纳米团簇的光吸收光谱显示出明显的特征峰,表明金属掺杂显著影响了金属纳米团簇的内在电子结构。此外也可通过化学刻蚀方法获得合金纳米团簇[62]。
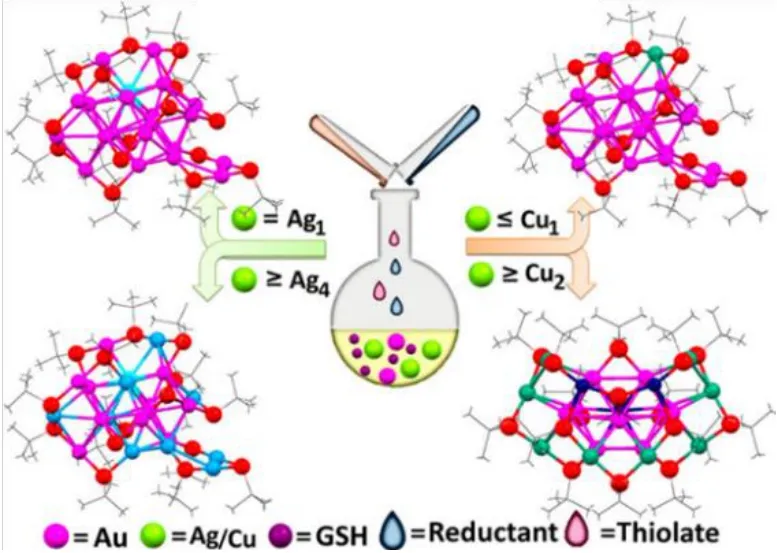
图4 原位两相配体交换法制备金银合金纳米团簇[61]Fig.4 Synthesis of Au-Ag alloy nanoclusters by the method of in-situ two-phase ligand exchange [61]
金属交换法是指在预合成的金属纳米团簇中掺杂其他金属,也是双金属纳米团簇合成的重要方法之一。Kazan 等利用Ag,Cu 和Cd 等金属作为掺杂金属源,通过在Au 中掺入Ag 和Ag-硫醇复合物来研究交换机制,并合成了双金属纳米团簇[63]。通过基质辅助激光解吸飞行时间(MALDI-TOF)质谱法验证硫醇配体在掺杂过程中的作用,发现掺杂反应在很大程度上取决于团簇类型和配体结构,且配体是合金化的关键因素。通过X 射线光电子能谱(XPS)研究显示,硫醇在其中充当媒介作用,在团簇和金属表面之间交换金属原子。
Chang 等采用密度泛函理论(DFT)对金银合金纳米团簇中金属与硫的相互作用进行了计算,结果表明Ag-Au 合金纳米团簇比裸露的Ag 或Au 纳米团簇具有更优异的性能,高的生物相容性、长期稳定性、无毒、低成本合成和良好的水溶性[64]。根据密度泛函理论计算Au 或Ag 对硫的吸附强度的差异,表明Au—S 键比Ag—S 键更强,在Ag-Au 合金纳米团簇中,Au 与Ag 原子有协同作用,用Au 代替Ag 核心中的Ag 原子集群,Ag 对硫的吸附变得更敏感,而随着团簇尺寸的增大,团簇对硫的吸附强度会减弱,所以Au 和Ag 对硫的吸附性可以通过改变化学顺序来调整。此外,配体多为硫代硫酸盐或含有巯基的结构,通过改变Au—S 键和Ag—S 键的强度可以改变整个团簇的稳定性和尺寸。
为获得具有手性光学活性的双金属簇,Jupally 等以谷胱甘肽为手性配体,Au 与Ag 物质的量比为3∶1,通过一锅法还原Au 和Ag 盐的混合物,经凝胶电泳分离提纯,得到了一系列幻数双金属Au-Ag纳米团簇[62]。XPS 研究表明,将Ag 杂原子掺入较小尺寸的Au 纳米簇中不太有利,且Ag 杂原子优先占据团簇核心(包括核心表面和中心)而不是外围的位点半环壳。结合光谱学得知,掺入Ag 原子对金纳米团簇的电子结构有显著的调控。值得注意的是,双金属Au-Ag 纳米团簇化合物表现出比相应Au 对应物更弱的CD 响应。这种手性减弱可以用纳米团簇中Ag 杂原子的统计分布形成的几何异构体的增加来解释,因为不同手性光学异构体构型的增加会导致平均的CD 响应相互抵消而减弱。
此外,金属原子和配体分子的不对称堆积也可导致纳米团簇手性的产生。Kobayashi 等采用相同的配体获得一对结构异构体,[Au9Ag12(SR)4(dppm)6X6]3+-C 和[Au9Ag12(SR)4(dppm)6X6]3+-Ac [dppm:二-(二苯膦)甲烷;SR:1-金刚烷硫醇/叔丁基巯烷;X:Br/Cl;C 代表结构异构体是手性的;Ac 代表另一个是非手性的][65]。通过单晶X 射线衍射(XRD)和高分辨率电喷雾电离(HESI)质谱确认,二者具有不同的结构和不同的手性。而且发现Au5Ag8@Au4金属核的不同排列不仅导致了异构体的产生,同时实现了手性纳米团簇的构筑。进一步研究发现,[Au9Ag12(SR)4(dppm)6X6]3+-C 的两种对映异构体可通过高效液相色谱法分离。该工作不仅有助于更深入地了解贵金属纳米团簇中的结构异构体,而且丰富手性纳米团簇的构筑[66]。
4 金银合金纳米团簇的发光性能
大多数配体保护的纳米团簇光致发光量子产率较低,阻碍了其作为发光材料在诸如细胞成像、智能显示、识别与传感领域的应用。增强PLQY 的常用策略有掺杂外来金属原子、配体壳修饰增强团簇的刚性以及AIE。
合金化通常可以显著增强金属团簇的发光性能。其中,受控掺杂因其保持了纳米团簇原有结构的完整性,被认为是最有前景的方法之一。2009 年,Jia 等通过Ag 原子掺入增加团簇的刚性,获得了具有超配位碳的光稳定Au(I)-Ag(I)团簇[Au6Ag2(C)(dppy)6](BF4)4,其核心结构为六个Au(I)组成的八面体,两个Ag(I)在两对面的顶端,其溶液和固态均可观察到显著的磷光,见图5[67]。
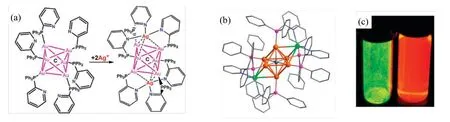
图5 [Au6(C)(dppy)6](BF4)2(a)与[Au6Ag2(C)(dppy)6](BF4)4 的阳离子结构(b)及AuAgNCs 在固态和溶液中的发光照片(c)[67]Fig.5 Structure of the cationic part of [Au6(C)(dppy)6](BF4)2 (a) and [Au6Ag2(C)(dppy)6](BF4)4 (b), and emission photos of AuAgNCs in the solid state and in the solution(c) [67]
Wang 等合成的棒状Au25(PPh3)10-(SR)5Cl2纳米团簇的固有发光量子产率较低(仅为0.1%),但是发现,采用Ag 原子代替部分Au 原子可以显著增强发光强度。获得的Au25-xAgx(x=1~13)纳米团簇表现出高光致发光量子产率(为40%),这与弱发射Au25-xAgx(x=1~12,发光量子产率为0.21%)形成鲜明对比[69]。进一步理论研究表明,其光致发光效率的增强源于第一激发态(S1)和相应的最高占据分子轨道-最低未占分子轨道(HOMO-LUMO)跃迁,而它们受Ag 掺杂程度的影响显著[70]。Au25和Au25-xAgx的超快弛豫动力学证明了顶点Ag 杂原子在稳定LUMO 上的电荷和增强Au25-xAgx纳米团簇刚性方面的重要性,这进一步导致了合金纳米团簇具有更强的发光量子产率[71]。Soldan 等通过在Ag团簇中掺入不同数量的Au 原子,显著提高了该类纳米团簇的发光量子产率[72]。在Ag29(S2R)12(PPh3)4纳米团簇结构中,Au 掺杂导致团簇光致发光增强了26 倍,即当引入多达五个Au 杂原子时,Ag29(发光量子产率小于0.9%)的发光效率增加到24%,Ag29纳米团簇的发射中心则从658 nm(Ag29-xAux,x为1~5,Au 相对于Ag 的物质的量含量为10%)红移到668 nm(Ag29-xAux,x为2~5,Au 相对于Ag 的物质的量含量为40%)。Xie 等通过DFT 计算揭示了Au 掺杂的Ag29-xAux纳米团簇中的光致发光增强的原因,即Au 原子引起的相对论效应对于增强高掺杂度的Ag26Au3,Ag25Au4和Ag24Au5的发光发挥着重要作用;异核Au—Ag 键可以增加这些金掺杂纳米团簇异构体的稳定性并提升其发光强度[73]。这些新发现有助于设计具有优异发光特性的金银合金纳米团簇。
AIE 增强被认为是另一种有效提升金属纳米团簇发光性能的有效策略[14,74]。Lu 等制备了少原子的七核和十核的金银双金属团簇(Au6Ag 和Au9Ag),并通过X 射线衍射和质谱法测定了它们的结构。通过能量分解分析证明Au(I)-Ag(I)相互作用远超出了典型的以色散相互作用为主的闭壳金属-金属相互作用,对Au 与Ag 的化学计量比调节是调控该合金纳米团簇的关键因素。建立了Au6Ag 聚集体粒径与其发光量子产率之间的正相关关系,证明了AIE 策略调控团簇发光的有效性[75]。Dou 等采用谷胱甘肽作为配体与HAuCl4反应,先合成金纳米团簇,再引入AgNO3,采用硼氢化钠为还原剂,合成了发光量子产率为6.8%、荧光发射峰值为667 nm 的金银合金纳米团簇,该团簇通过AIE 效应呈现出强烈的红色发光[15]。此外,Wang 等还通过Ag 掺杂来设计金纳米团簇壳中Au(I)-硫代氨酸基团的尺寸、结构和团聚状态,实现AIE 增强发光。通过延长反应时间,合成的AuAgNCs 发光可以从橙色调整为红色[59]。Jin 等在甲醇中合成了具有AIE 效应的Au4Ag5(dppm)2(SAdm)6-(BPh4)纳米团簇[dppm:双(二苯基膦)甲烷;SAdm:1-金刚烷硫醇]。该纳米团簇在良溶剂甲醇中不发光,只有在聚集态和固态(即薄膜或晶体)时才能发出明亮的红光(见图7)][76]。
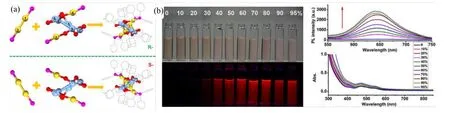
图7 Au4Ag5 纳米团簇的晶体结构(a)及其在不同比例下的光学照片和发光光谱(b)[76]Fig.7 Crystal structure of Au4Ag5 nanocluster(a), digital photographs and spectra of samples of with different fractions of water under visible light and UV light, respectively(b) [76]
2017 年,Chen 等合成的Au4Ag13(dppm)3(SR)9金银合金纳米团簇(SR 为2,5-二甲基苯硫醇)表现出了结晶诱导发射增强(CIEE)。Au4Ag13团簇结晶态在695 nm 处显示出强烈的发光,与无定形态的弱发射形成鲜明对比,并且在溶液相中几乎没有发射(见图8)。结构分析和密度泛函理论计算表明,晶态中C—H…π 作用显著限制了分子内旋转和振动,从而显著增强了晶态的辐射跃迁[77]。
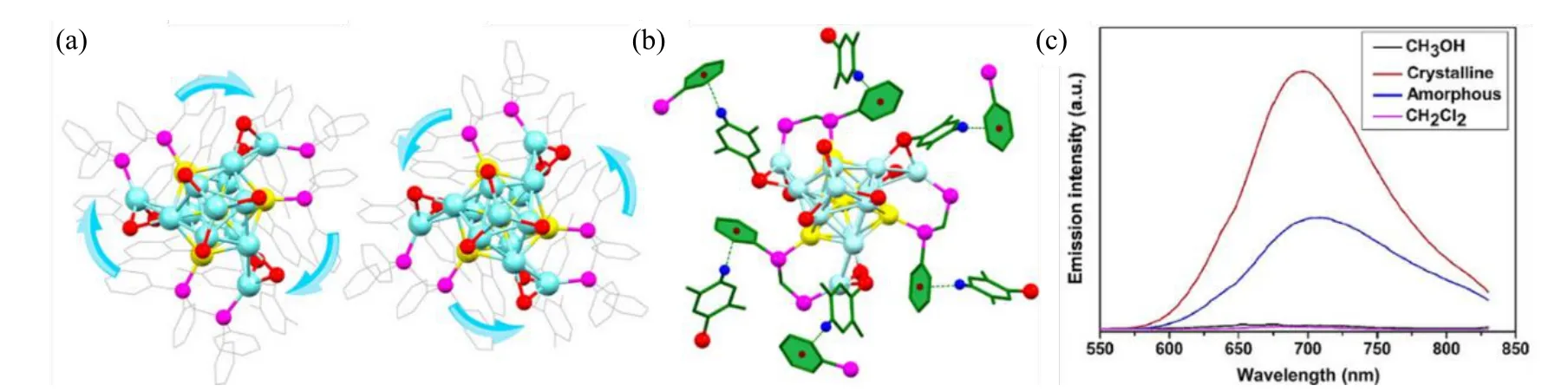
图8 Au-Ag 双金属纳米簇的晶体结构(a)及其单晶中的C-H…π(b)与相应的结晶诱导发射增强的光谱图(c)[77]Fig.8 Structure of one pair of enantiomers of Au-Ag NCs(a), the compact C-H…π interactions in the single crystal of Au-Ag NCs(b) and the corresponding CIEE property in spectra (c) [77]
与上述不同的是,Yin 等先单独合成Au-GSH 团簇和Ag-GSH 团簇,然后通过静电相互作用结合形成复合金属纳米团簇。研究发现Ag-GSH 纳米团簇发光非常微弱,甚至在紫外激发的情况下也无法观察到荧光。当Au 与Ag 的物质的量比(Au:Ag)为8:1 和1:1 时团簇显现出最强的荧光发射性质;当Au:Ag 大于8:1 时,过多的Au-GSH 纳米团簇会包裹在Ag-GSH 表面,此时主要显现Au-GSH 纳米团簇的吸收和发射性质;当Au:Ag 小于1:1 时,Au-GSH 纳米团簇被过多的Ag-GSH 纳米团簇包裹,此时主要显示单一Ag-GSH 纳米团簇的性质,荧光减弱[78]。
Jana 等采用多巴胺(Dopa)作为配体来制备合金纳米团簇。由于Ag—N 比Au—N 键合力强,所以先形成Ag-Dopa 团簇,再利用多巴胺还原Au(III)合成得到复合纳米团簇。与水溶液中的金纳米团簇相比,双金属纳米团簇的发射峰蓝移并伴随强度的增强。研究发现,发射强度的增加取决于双金属纳米团簇的银浓度,这一“银效应”通过荧光表征得到证实。在Ag 与Au 的物质的量比(Ag:Au)为0.25∶0.60 时,荧光增强最大,为单金属AuNCs 的5 倍。相比于单金属纳米团簇中仅存在Au(0),双金属纳米团簇中存在Au(I)/Au(0)-Ag(0)。此外,通过研究不同有机溶剂对双金属纳米团簇发光性能的影响发现,团簇在乙醇中的荧光发射强度最强[79]。
Zhang 等在巯基琥珀酸(MSA)和聚(N-乙烯基咪唑)(PVIm)的协同作用下,通过两步法合成了最大发光量子产率为23.6%的超亮金银合金纳米团簇(Au-AgNCs),几乎是相应单金属AuNCs 的两倍。研究发现Ag:Au 为0.1~0.4 时存在协同荧光增强效应,其中Au-Ag0.2的磷光发射主要分布在远红/近红外区域(发光中心约为718 nm),其磷光特性表现出明显的大斯托克斯位移(>400 nm)和2 μs 级的长寿命。当Au-AgNCs 中保持较高的Ag:Au 时,Au-AgNCs 的最大发射波长(λem)可以调节到约666 nm,但伴随着磷光发射的抑制[80]。
此外,金银合金纳米团簇的发光性能与孵育的温度、时间、pH 以及金银原子的化学计量比等均相关。不同化学计量比的金银会形成不同结构的团簇,通过团簇内部的Au:Ag 大小来调控其发光性能的研究相对较多。纳米团簇由于暴露较多的外部原子,因而存在不稳定和易聚集的特性。由于金、银与硫原子之间有强的金属-硫作用力,通常采用含巯基的有机配体分子对金属团簇进行保护,实现壳层刚化,以及通过AIE 等策略提升合金团簇的发光性能。值得一提的是,合金团簇间的金属-金属作用变化可导致团簇结构的整体发光性能的变化。Mo 等报道了一例溶剂诱导的团簇间Au-Au 作用重排,实现硫化物桥接的Au(I)-Ag(I)团簇对溶剂的可逆发光响应[81]。上述代表性Au-Ag 合金发光纳米团簇的结构组成、合成方法以及发光性能等列于表1。
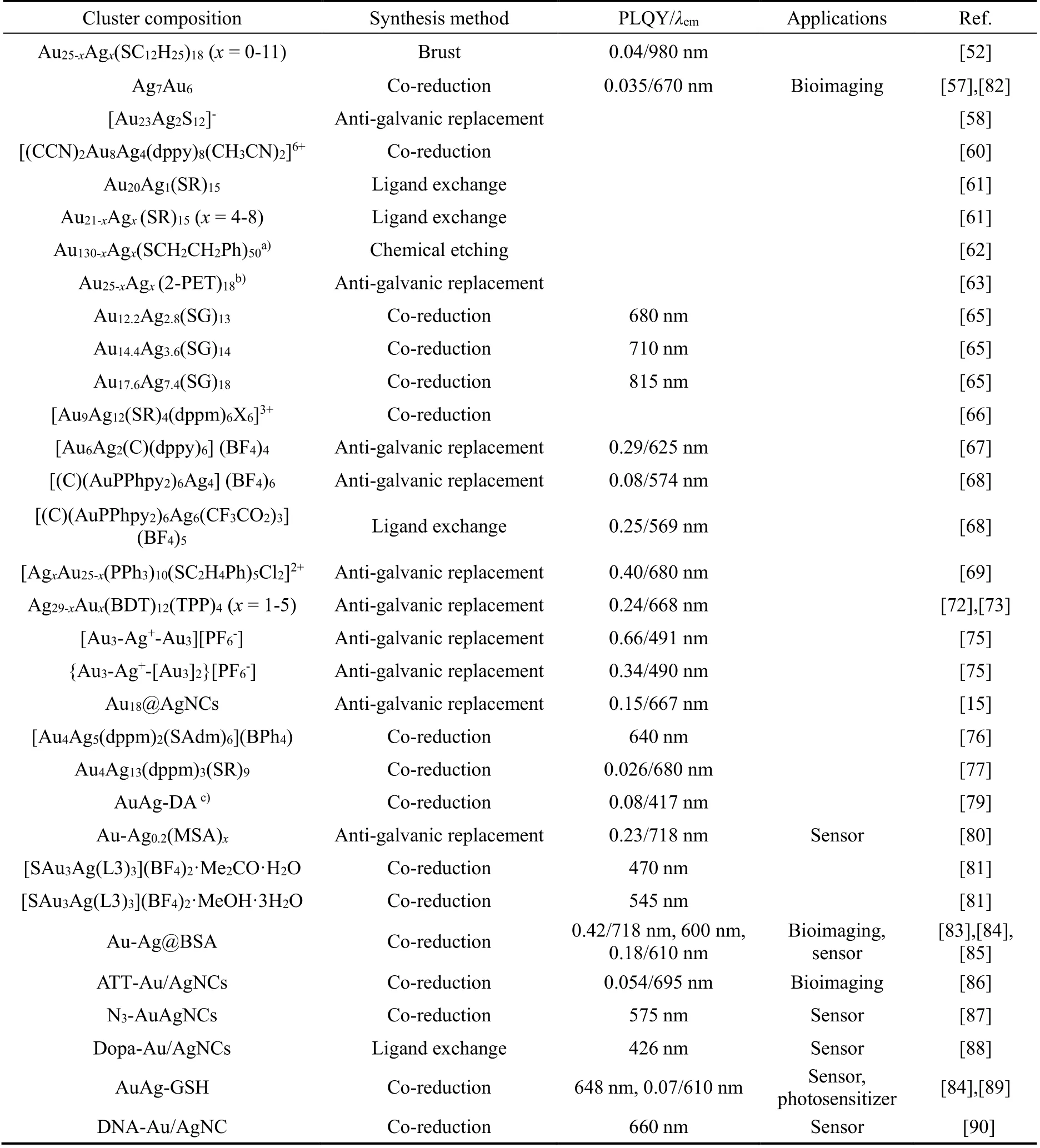
表1 金银合金纳米团簇的结构组成、合成方法、发光性能以及生物应用Table 1 Structural composition, synthesis method, luminescence properties and biological applications of Au-AgNCs
5 金银合金发光纳米团簇的应用
由于金银合金纳米团簇具有超小的尺寸、良好的生物相容性、聚集增强的发光特性以及特有的生物安全性,而且具有结构设计性强、功能和结构精确可调等优异的材料特性,因而可被用于生物成像、分子识别与传感领域,同时作为一种良好的光吸收纳米粒子,可作为光敏剂产生活性氧,从而有望用于肿瘤治疗和抗菌治疗。
5.1 生物成像
基于金银合金纳米团簇上述优良的光学特性、良好的水溶性以及较好的生物安全性,可将其作为一种优秀的纳米发光材料应用于生物医学领域,特别是作为一种潜在的发光成像材料。小于2 nm 的尺寸使金银合金纳米团簇在体内可以很好地通过肾小球的过滤排出体外,避免了在生物体内长期积累造成的生物毒性,因而在细胞生物成像领域具有较广泛的应用研究。已有研究表明,金属纳米团簇的毒性与作为核心的金属以及配体都有关,但更大程度上取决于配体,所以用于生物成像的分子配体通常选用人体自身可合成和代谢的分子。同时,配体应具有抗氧化性、促进血管生成和抑制细胞凋亡的特性,可以使金属纳米团簇保持稳定,例如谷胱甘肽、多巴胺和硫辛酸等,而且需要纳米团簇具有良好的水溶性,并且在生物体环境下具有很强的发光性质便于检测[91]。
Meng 等采用树枝状介孔二氧化硅纳米颗粒作为纳米载体平台,装载金银合金纳米团簇,利用空间限制效应,可显著增强金银合金纳米团簇的发光性质,使发光量子产率达到17%。氨基端粒状二氧化硅球具有超大中心径向孔隙通道,装载金银纳米团簇时可减少团簇繁琐的纯化过程,但是对于生物成像,需要荧光探针完全进入被检测的靶标细胞,由于金银纳米团簇表面功能差,导致细胞摄取纳米团簇困难;同时由于金银纳米团簇尺寸超小,代谢清理迅速,导致肿瘤细胞积累发光纳米团簇不足。而石榴状二氧化硅球具有合适的尺寸,可改善细胞渗透性能。将金银纳米团簇通过自组装的方法封装在二氧化硅球中,可顺利地将其输送进入活的细胞中,由于Cu2+对金银纳米团簇的发光具有淬灭作用,纳米二氧化硅球-金银纳米团簇即可作为细胞内Cu2+的有效探针,可进行生物成像(图9)[92]。Wang等对原本发光很弱(发光量子产率为0.1%)的棒状Au25纳米团簇进行Ag 掺杂,极大提高了其发光量子产率,其中最强的发光量子产率(为40.1%)是普通AgxAu25-x(x=1~12)发光效率的200 倍左右,因而有望用于细胞成像(图10A 和图10B)[69]。
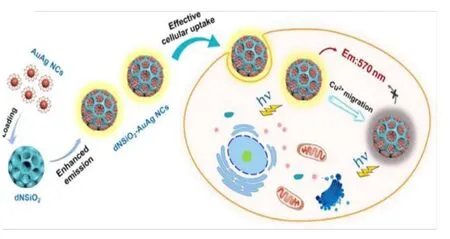
图9 限制在石榴状二氧化硅结构中AuAg NCs用于Cu2+传感和细胞成像[92]Fig.9 Schematic illustration of AuAg NCs in a pomegranate-type silica architecture for improved Cu2+ sensing and imaging [92]
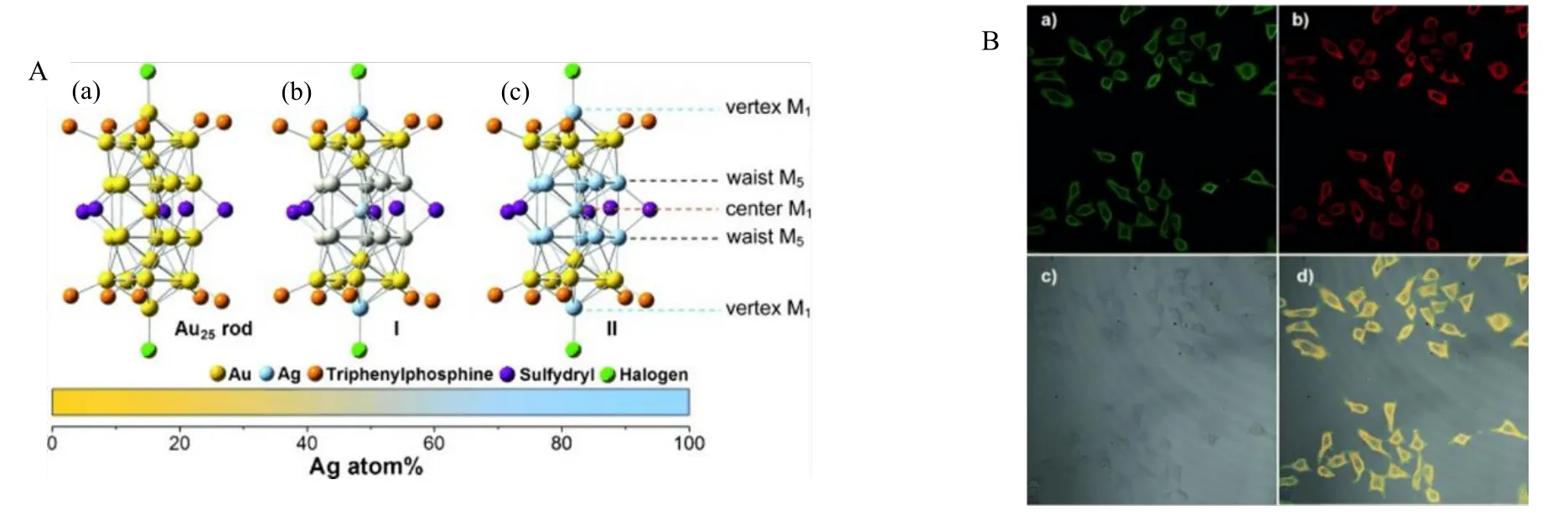
图10 [Au25(PPh3)10(SC2H4Ph) 5Cl2]2+ (a)及其I (b)与II (c)的X 射线结构(A)和双金属纳米团簇用于人源肿瘤细胞成像(B)[69]Fig.10 X-ray structures of [Au25(PPh3)10(SC2H4Ph)5Cl2]2+ (a), the corresponding bimetallic nanoclusters of I (b) and II (c) (A)as well as the AuAg NCs used for labeling human cancer cells (B) [69]
此外,Wang 等通过化学还原法制备AgNCs 后,采用N2H4·2H2O 作为还原剂,加入HAuCl4,并采用谷胱甘肽作为稳定剂,通过电偶还原法制备了Ag/Au 纳米团簇。通过调整Ag:Au 可以得到发射波长范围从可见光到近红外发射的Ag/Au 合金纳米团簇。因谷胱甘肽是一种具有丰富官能团的小分子三肽,可以提供有效的保护层,防止纳米团簇聚集。同时通过谷胱甘肽封端的金属纳米团簇表现出较高的荧光稳定性,可用于CAL-27 细胞成像[82]。Ristig 等利用11-巯基十一烷酸为配体,合成了红色发光的Au/Ag 合金纳米团簇,具有250~300 nm 的大斯托克斯位移(λem为608~645 nm)[93]。Sannigrahi等采用生物大分子牛血清白蛋白(BSA)为配体,构筑了Au/Ag 合金纳米团簇,其展示了680~815 nm可调谐的近红外发光性能,可用于细胞成像以及细胞内Pb2+的检测[83]。Peng 等通过6-Aza-2-硫胸腺嘧啶(ATT)为配体合成了Au/Ag 合金纳米团簇,可用于体内深层组织的双光子成像[86]。
5.2 生物传感与离子识别
谷胱甘肽在维持生物系统的氧化还原活性中起着至关重要的作用,然而谷胱甘肽的过度表达会破坏氧化平衡,是肿瘤、炎症等疾病的重要检测标志物之一。Yang 等构建了一类基于由四面体DNA 块自组装而成具有有序结合位点和空腔结构的3D 的DNA 基质,并用金银纳米团簇作为生物传感器检测谷胱甘肽含量(见图11)[87]。值得一提的是,谷胱甘肽的存在可以通过谷胱甘肽和Cu(II)之间的氧化还原反应诱导形成GSH-Cu(I)复合物,并以此作为引发剂,通过Huisgen 1,3-偶极环加成反应将N3-AuAg NCs 与C≡C-3DM(DM 为富炔烃3D 基质)联系起来。因此,所设计的GSH 生物传感器显示出5~200 μmol/L 的宽线性响应,检测限为0.90 μmol/L。
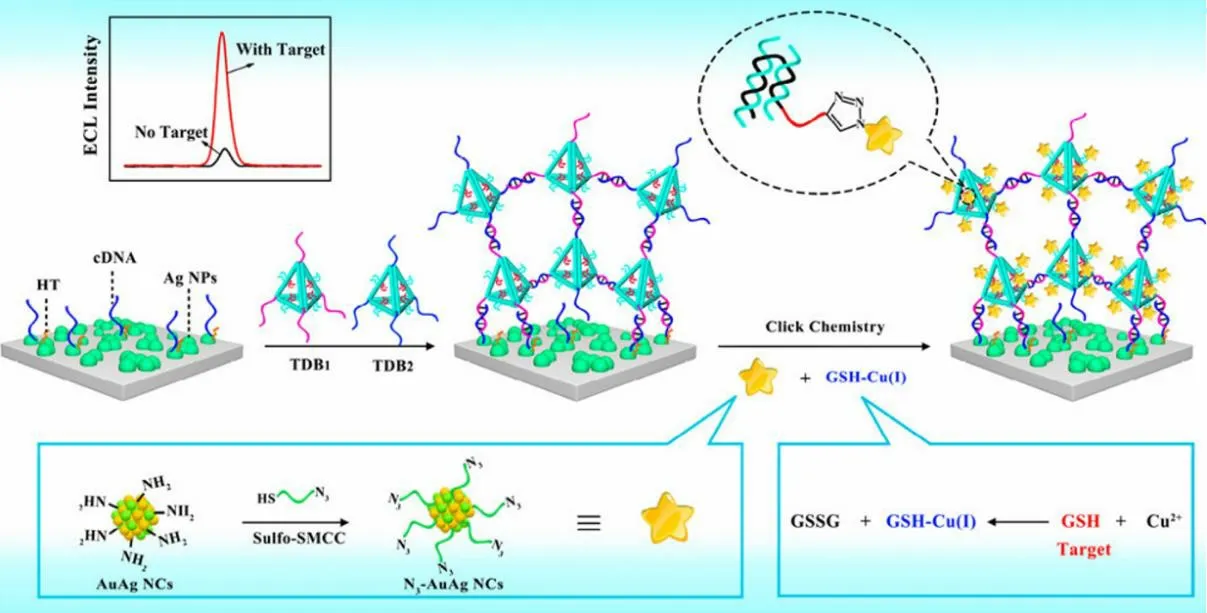
图11 金银双金属发光纳米团簇用于谷胱甘肽灵敏检测示意[87]Fig.11 Schematic illustration of luminescent Au-Ag bimetallic nanoclusters for sensitive detection of GSH [87]
酪氨酸酶在黑色素生物合成中具有重要作用,是黑色素瘤诊断的重要生物标志物之一,开发对其具有高灵敏度的生物相容性材料具有重要意义。Ao 等开发了一种基于多巴胺功能化Au/Ag 纳米团簇(Dopa-Au/Ag NCs),并用于酪氨酸酶活性检测。该研究利用具有生物相容性的多巴胺与Au/Ag NCs表面共价连接,形成了具有强蓝色荧光的Dopa-Au/Ag NCs 生物偶联物。由于多巴胺在酪氨酸酶催化下容易被氧化为邻多巴醌衍生物,邻多巴醌则与Au/Ag NCs 发生颗粒内光诱导电子转移(PET),导致Dopa-Au/Ag NCs 生物偶联物荧光猝灭。因此,该生物传感器可根据光猝灭效率建立酪氨酸酶活性的函数关系,进而实现对酪氨酸酶活性的灵敏度和选择性检测[88]。
多巴胺是人体中重要的神经递质之一,如何实现对其灵敏检测对研究多巴胺成瘾症状、帕金森病、抑郁症等疾病有重要意义。Zhou 等利用牛血清白蛋白(BSA)合成了金银合金纳米团簇(BSA-Au/Ag NCs),加入多巴胺后纳米团簇荧光显著增强,并伴随发射峰的红移。通过光谱和电化学研究揭示了多巴胺与金氧化还原反应导致电化学发光增强的机理。并将其用于多巴胺的定量测量,实现了多巴胺浓度为0.01~1.7 μmol/L 和1.7~10 μmol/L 时对多巴胺的线性响应,检测限为6.9 nmol/L。该研究为多巴胺的测定提供了一种简便有效的方法,该方法在血清样品的相关测定中成功应用(见图12a)[84]。
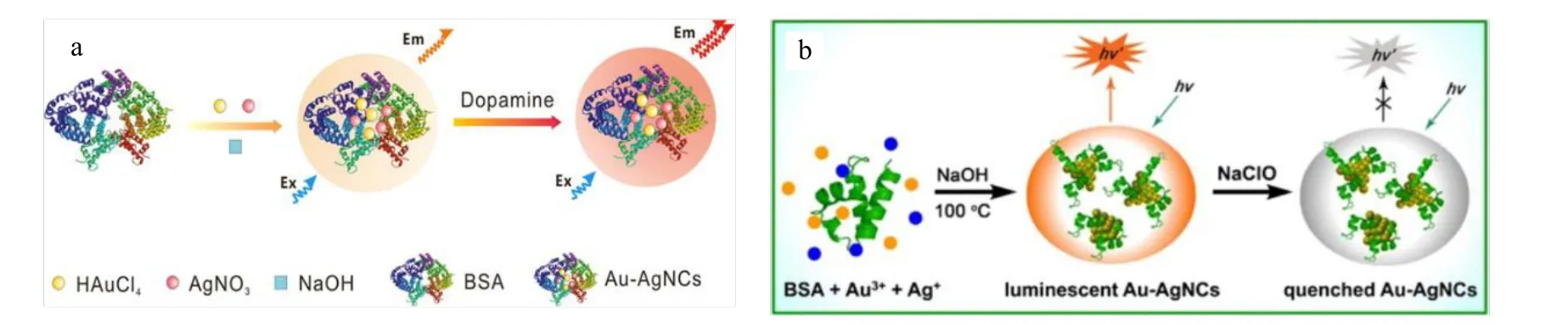
图12 金银双金属发光纳米团簇用于多巴胺(a)[84]和次氯酸盐(b)[85]灵敏检测示意Fig.12 Schematic illustration of luminescent Au-Ag bimetallic nanoclusters for sensitive detection of dopamine (a) [84] and hypochlorite (b) [85]
金银双金属纳米团簇也可用于检测半胱氨酸。Zhang 等采用巯基琥珀酸(MSA)和聚(N-乙烯基咪唑)(PVIm)的协同作用合成的超亮双金属纳米团簇(Au-Ag NCs)实现半胱氨酸的选择性检测,检测限为2.5 μmol/L[80]。Guo 等研究发现精胺(SPM)可以与三乙胺(TEA)作为共反应剂,增强金银双金属纳米团簇(Au-Ag BNCs)的电化学发光强度。并制备了一种检测SPM 的电化学发光传感器,其中含有作为电致化学发光(ECL)发射器的Au-Ag BNCs 和含有聚苯胺-氨基三亚甲基膦酸(PANIATMP)作为固定基质的导电水凝胶。检测发现,SPM 浓度为1 pmol/L~10 μmol/L 时,Au-Ag BNCs的ECL 强度与浓度的对数呈线性关系,而且检测的选择性高、稳定性好,检测限为0.11 pmol/L。该电化学发光传感器实现了尿液样品中SPM 快速且经济的检测,在临床和生物分析中具有潜在应用[90]。
碘元素在神经活动和甲状腺功能等生理过程中起着关键作用。Li 等开发了一种荧光和比色分析检测平台,用基于DNA 模板化金/银纳米团簇(DNA-Au/Ag NCs)实现对碘化物中碘离子的选择性检测。该检测系统基于碘化物离子与DNA-Au/Ag NCs 之间的独特相互作用,加入碘化物离子具有明显的荧光猝灭现象,当浓度为0~10 μmol/L 时显示出良好的线性关系。而且加入碘化物离子的检测系统呈现出从无色透明到紫红色的颜色变化,可实现简单的比色定性检测,已成功应用于测定水样中的碘离子[94]。Zhang 等则以牛血清白蛋白为模板和还原剂,通过一锅法同时化学还原Au(III)和Ag(I)离子,合成了金银纳米团簇(Au-AgNCs)。Au-AgNCs 的平均尺寸为2.4 nm,其显示出强烈的红色荧光(在360 nm 处激发时,发射峰为610 nm),荧光量子产率可达18.6%。该研究发现,次氯酸盐可导致Au-AgNCs 荧光的显著淬灭,而其他常见阴离子对其荧光则无影响或影响甚微(见图12b)。为此,开发了一类双金属簇用于次氯酸盐的荧光检测方法,在0.7~15 μmol/L 的浓度范围内具有线性响应,检测限低至80 nmol/L,并成功用于自来水中次氯酸盐的测定[85]。
5.3 抗菌活性
银可以杀死细菌、病毒和真菌等微生物,并且对人体正常细胞无害,因此银纳米团簇也可以作为抗菌剂。受Ag 纳米粒子作为抗菌剂的成功启发,Yuan 等通过循环还原-分解过程开发了发光的谷胱甘肽保护的AgNCs,并研究了AgNCs 的抗菌活性,发现其对铜绿假单胞菌具有优异的杀菌性能[95]。Guo 等则采用AgNCs 作为杀菌剂,通过化学键结合将AgNCs 修饰在正向渗透(FO)膜中,从而形成高性能的抗菌复合膜。该膜可以有效抑制大肠杆菌的生长,在1 个月的测试期内没有明显的活性衰减。此外,由于Ag 金属芯由一层谷胱甘肽保护形成了稳定活性化合物,可以适应溶液中的各种应用。同时利用外层硫醇基团与内层金属之间的强化学键可以持续可控地调节溶液中银离子的释放,而银离子对细菌、真菌和病毒都具有广谱活性,将银纳米团簇附着在FO 膜上可改善膜被细菌污染的问题[96]。2016 年,Zheng 等将脂肽类抗生素达托霉素和AgNCs 结合合成了D-AgNCs 复合物。复合物中的达托霉素可有效损伤细菌膜,AgNCs 则可产生活性氧(ROS)氧化细菌脂质双层,进一步加重膜损伤,这反过来又允许更多的D-AgNC 进入细菌并在细胞内产生局部高ROS 浓度,随后诱导其DNA 严重损伤,实现对细菌的高效杀灭[97]。与此杀菌机理相同,Li 等采用核黄素(RF)保护合成了银纳米团簇。这种银纳米团簇也诱导ROS 产生,AgNCs 释放的Ag 会损害细胞膜的完整性,导致细菌死亡。RF@AgNCs 对金黄色葡萄球菌、大肠杆菌和白色念珠菌表现出非常好的抗菌性能[98]。
与之前采用肽和硫醇作为配体不同,Xu 等采用聚乙烯亚胺(PEI)作为封端配体,合成了具有杀菌效果的PEI-AgNCs。采用不同分子量的PEI 配体,合成了一系列的PEI-AgNCs,研究发现其粒径受PEIs 分子量的影响很小,说明带正电荷的PEI 配体可很大程度上阻止纳米材料聚集,而且PEI 分子量的降低可以为PEI-AgNCs 提供更高的抗菌性能。其抗菌机制结合了PEI 和银的优点,由于PEI 带正电荷,PEI-AgNCs 可以很容易地在带负电荷的细菌表面上吸收和富集,PEI 可以通过透化作用进而破坏细菌,AgNCs 释放的银离子可以在细菌周围富集并迅速杀死细菌[99]。此外,AgNCs 还可以通过破坏外膜的通透性、抑制细菌的呼吸和生长、破坏膜结构来发挥作用。基于同样的杀菌机理,Haidari等设计并合成了高度单分散、超小(<3 nm)的聚阳离子银纳米团簇(pAgNCs),用于消除一系列常见的革兰氏阴性和革兰氏阳性病原体。同时,pAgNCs 对厌氧菌如具核梭杆菌和血链球菌也显示出显著增强的抗菌功效[100]。这些超小发光AgNCs 可以进一步发展为一类新兴的高效抗菌剂,然而需要进一步研究AgNCs 的毒性以开发出更具生物相容性的抗菌AgNCs。此外,溶菌酶是糖苷水解酶,可以通过攻击肽聚糖(尤其是革兰氏阳性菌中含量丰富)来破坏细菌细胞壁。Chen 等合成了溶菌酶保护的AuNCs,并证明溶菌酶在NCs 上的生物活性得以保留[101]。溶菌酶保护的AuNCs 用于抑制抗生素耐药细菌的生长,如广泛耐药鲍曼不动杆菌和万古霉素耐药肠球菌。
与上述AgNCs 抗菌活性作用机制不同的是利用金银纳米团簇发射磷光的特性。其发光过程经历三重激发态,因此可以将基态的三线态氧敏化成激发态的单线态氧(1O2),1O2的产生不利于变形链球菌的生长,因此起到了抗菌的作用,并用于疾病的光动力治疗。Hikosou 等结合三种策略来提高谷胱甘肽保护的金纳米团簇的1O2生成效率:掺杂银(即使用双金属纳米簇),使用Au(I)-硫代酸盐复合物实现AIE,以及使用聚合物纳米凝胶实现自组装诱导发射(SAIE)。通过这三种效应的结合,抑制了非辐射性衰变途径,显著提高了1O2的产生效率,并增强了受谷胱甘肽保护的金银纳米团簇的发光性能,基于金银纳米团簇与纳米凝胶复合材料的光敏剂成功用于针对口腔细菌的光动力疗法(见图13)[89]。
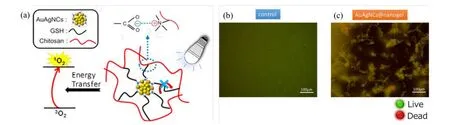
图13 基于AuAg NC@纳米凝胶复合材料的光敏剂(a)及其用于口腔细菌的抗菌活性评价(b,c)[89]Fig.13 Schematic illustration of the photosensitizers based on AuAg NC@ nanogel composites (a), and use for antimicrobial photodynamic therapy against oral bacteria (b, c) [89]
6 总结与展望
本文重点介绍了金纳米团簇、银纳米团簇以及金银合金纳米团簇的设计与合成方法,并针对当前金银合金纳米团簇的研究进展进行了简要概述,介绍了金银合金纳米团簇的制备方法、发光性质、手性性质,以及在生物成像、分子识别和光敏抗菌活性等方面的应用研究。作为一类新型高效的发光纳米粒子,合金纳米团簇在提升发光效率和丰富团簇结构(包括手性结构)等方面还存在非常大的发展空间。鉴于其具有原子级精确可控的结构,表面配体丰富的功能基团以及潜在的超分子作用位点,为实现纳米团簇的组装聚集体结构的设计提供了结构和作用基础,同时也有助于实现其发光效率的提升,并在功能应用方面将具有重要的前景。
近年来,尽管纳米尺度的手性研究越来越多,特别是基于手性配体构筑手性金属纳米团簇,但目前只有有限的案例实现了双金属合金纳米团簇的构建,特别是具有圆偏振发光性能的合金团簇还鲜有报道。如何在原子和分子层次实现合金纳米团簇结构和有机配体的理性设计,结合超分子组装策略实现手性的高效传递、转移和放大,构筑高效率的圆偏振发光纳米团簇材料,以及其功能应用拓展方面如何整合其高效发光属性、超小且精确的结构,实现其在肿瘤诊疗一体化以及活体生物传感方面的应用也是值得发展的方向。此外,其手性可控的结构还可在不对称催化、手性识别与传感、3D 显示方面进行探索和拓展。最后,其作为一种良好的光敏剂,在环境保护、抗菌、肿瘤联合治疗等领域也将大有前景。

