纳米硫化锂/碳复合正极材料的制备及其电化学性能
房彬 徐富良 江永明 叶方敏


摘 要: 为了提高硫化锂正极的倍率性能、抑制多硫化锂穿梭并降低成本,以三硫化二锂作为硫化锂的前驱体,聚乙烯吡咯烷酮和碳纳米管作为碳源,经高温处理制备纳米硫化锂/碳复合材料,以此作为锂硫电池的正极材料。采用扫描电子显微镜、X射线衍射仪、热重分析仪对该复合材料的形貌、結构以及组成进行表征,并进行电化学性能测试。结果表明:制备的纳米硫化锂/碳复合正极材料中,纳米硫化锂分散均匀并被热分解的碳包覆,合成的三硫化二锂前驱体在空气中具有一定的稳定性,能够降低纳米硫化锂的生产成本;将纳米硫化锂/碳复合正极材料用于锂硫电池时,在0.07 C(1 C=1166 mA/g)倍率下初始放电比容量达910 mAh/g,在1.00 C高倍率下循环150次后,可逆容量保持在484 mAh/g,这表明纳米硫化锂/碳的活性物质利用率较高、多硫化锂穿梭较弱。采用三硫化二锂前驱体制备高性能硫化锂复合材料,工艺成本低,有助于硫化锂正极材料的实际应用。
关键词: 硫化锂正极;三硫化二锂前驱体;碳纳米管;聚乙烯吡咯烷酮;锂硫电池;空气稳定性
中图分类号: TM912
文献标志码: A
文章编号: 1673-3851 (2023) 01-0043-07
引文格式:房彬,徐富良,江永明,等. 纳米硫化锂/碳复合正极材料的制备及其电化学性能[J]. 浙江理工大学学报(自然科学),2023,49(1):43-49.
Reference Format: FANG Bin, XU Fuliang, JIANG Yongming,et al. Fabrication of nanoscale Li2S/cabon composite cathode and its electrochemical performance[J]. Journal of Zhejiang Sci-Tech University,2023,49(1):43-49.
Fabrication of nanoscale Li2S/cabon composite cathode and its electrochemical performance
FANG Bin, XU Fuliang, JIANG Yongming, YE Fangmin
(School of Science, Zhejiang Sci-Tech University, Hangzhou 310018, China)
Abstract: In order to improve the rate capability of lithium sulfide cathode, inhibit the shuttle of lithium polysulfides and reduce the cost, a nanoscale lithium sulfide/carbon composite material was prepared by using dilithium trisulfide as the precursor of lithium sulfide, polyvinylpyrrolidone and carbon nanotubes as carbon sources under high temperature treatment, which was used as a cathode material for lithium-sulfur batteries. Scanning electron microscope, X-ray diffractometer and thermogravimetric analyzer were used to detect and analyze the morphology, structure and composition of the composites, and its electrochemical performances were tested. The results have shown that in the prepared nano-lithium sulfide/carbon composite cathode material, nano-lithium sulfide was uniformly dispersed and coated by thermally decomposed carbon, and the synthesized lithium trisulfide precursor had certain stability in air, which could reduce the production cost of nano-lithium sulfide; when the nano-sized lithium sulfide/carbon composite were used in lithium-sulfur batteries cathode, an initial discharge specific capacity of 910 mAh/g (1 C=1166 mA/g) at a rate of 0.07 C could be reached, and the reversible discharge specific capacity remained 484 mAh/g after 150 cycles at a high rate of 1.00 C, indicating the improvement of the utilization of active materials and the weak shuttle effect of lithium polysulfides. Using dilithium trisulfide as precursor to prepare high-performance lithium sulfide composite materials has a low process cost and is conducive to the practical application of lithium sulfide cathode materials.
Key words: Li2S cathode; Li2S3 precursor; carbon nanotubes; polyvinylpyrrolidone; lithium-sulfur batteries; stability in air
0 引 言
锂硫电池因具有很高的理论比能量(2600 Wh/kg)和比容量(1675 mAh/g),受到研究人员的广泛关注[1-3]。但锂硫电池在实际应用中受到诸多问题的限制[4-5],如:a)硫的电子/离子电导率低;b)充放电过程中生成的可溶性多硫化锂会穿梭到负极,引起“穿梭效应”;c)硫在充放电过程中的体积变化巨大;d)匹配的锂金属负极存在安全问题。作为硫的完全锂化态,硫化锂(Li2S)具有高理论比容量(1166 mAh/g),并且可以避免硫正极面临的体积膨胀问题和锂负极的安全问题[6-8]。然而,Li2S正极初始充电过程需要使用高截止电压来进行活化[9],以提高活性物质利用率,但高截止电压可能会导致醚类电解液的分解[10];Li2S极易水解,Li2S正极的制备、存储需要在极干燥环境下进行,大大增加了应用成本。
为降低初始活化势垒,科研人员提出了高能球磨[11]、重结晶[12]和化学反应[13]等多种制备纳米级Li2S的方法,得到的纳米Li2S颗粒具有高比表面积,提高了界面处的锂离子交换速率,进而降低了初始活化势垒。在所有制备纳米级Li2S的方法中,重结晶法效率更高、成本更低[14]。Wu等[12]在Li2S的乙醇溶液中加入聚乙烯吡咯烷酮(Polyvinylpyrrolidone,PVP),利用Li2S和PVP在乙醇蒸发过程中发生共沉淀获得Li2S纳米粒子,再利用热处理将PVP转化为导电碳,得到了纳米结构的Li2S/C复合材料;用作锂硫电池正极时,在0.05 C(1 C=1166 mA/g)的倍率下首次充电截止电压约为3.40 V,放电比容量保持92%。由于Li2S的重结晶过程需要在无水的环境(通常在真空手套箱内)中进行,增加了生产和储存成本,降低了可操控性,因此需要开发能在常规空气环境中实施的重结晶方法。
本文分析了三硫化二锂(Li2S3)在常规空气环境中的稳定性,利用Li2S3作为Li2S的前驱体以实现常规空气环境中的重结晶,将PVP、碳纳米管(Carbon nanotubes,CNTs)作为碳源,通过重结晶、高温碳化,制备纳米硫化锂/碳(n-Li2S/C)复合材料,并将n-Li2S/C复合材料用作锂硫电池正极,进行电化学性能的检测分析。
1 实验部分
1.1 试剂与仪器
1.1.1 试 剂
商业硫化锂粉末(Li2S,99.9%)购于阿法埃莎(中国)化学有限公司;硫、聚乙烯吡咯烷酮(PVP,型号k90,Mw=1300000)购于西格玛奥德里奇(上海)贸易有限公司;无水乙醇(99.5%)购于北京百灵威科技有限公司;聚偏二氟乙烯(PVDF,型号HSV900)黏结剂购于法国阿科玛公司;乙炔黑购于苏州晟尔诺科技有限公司;碳纳米管(CNTs)购于苏州碳丰石墨烯科技有限公司和N-甲基吡咯烷酮(NMP)购于苏州多多化学科技有限公司。所有试剂使用前无需进一步纯化。
1.1.2 仪 器
SKGL-1200型真空管式炉(上海大恒光学精密机械有限公司)、真空手套箱(苏州威格气体纯化科技股份有限公司)、T07型纽扣电池切片机(深圳科晶智达科技公司)、MSK-110型纽扣电池封口机(深圳科晶智达科技公司)、CT2001A型电池测试系统(武汉蓝电电子股份有限公司)、D8 Discover型X射线衍射仪(德国布鲁克公司)、S-4800型场发射扫描电镜(日本日立公司)、PYRIS 1型综合热分析仪(美国柏金-埃尔默公司)和CHI760E型电化学工作站(上海辰华仪器有限公司)。
1.2 n-Li2S/C复合材料的制备
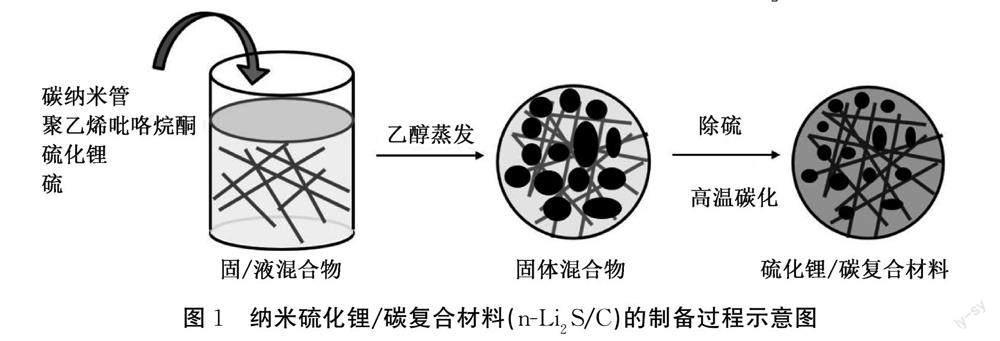
n-Li2S/C复合材料是以Li2S3作为Li2S的前驱体,PVP和CNTs作为碳源制备的,制备过程如图1所示。将Li2S和硫在乙醇中混合,生成Li2S3乙醇溶液,添加PVP和CNTs,得到固/液混合物,該固/液混合物对空气环境稳定,可以在手套箱外蒸发去除乙醇,得到含有Li2S3的固体混合物。将固体混合物在350 ℃分解除去硫,重新生成Li2S,随后升温到600 ℃将PVP碳化,得到n-Li2S/C复合材料。
具体操作步骤如下:在真空手套箱中将345 mg Li2S和510 mg硫加入到10 mL无水乙醇中,搅拌30 min形成棕色的Li2S3前驱体溶液,并加入300 mg PVP和100 mg CNTs,搅拌2 h形成固/液混合物,随后转移至手套箱外,在60 ℃下蒸发去除乙醇得到固体混合物。将固体混合物放入氩气气氛下的管式炉中,以3 ℃/min升温到350 ℃,保温3 h,以3 ℃/min继续升温到600 ℃煅烧1 h,随后降至室温,获得n-Li2S/C复合材料。
1.3 微米硫化锂/碳(m-Li2S/C)复合材料的制备
在手套箱中将345 mg Li2S、130 mg乙炔黑和100 mg CNTs混合研磨1 h,得到m-Li2S/C复合材料。
1.4 材料表征
a)采用S-4800型场发射扫描电镜(日本日立公司)观察样品的表面形貌,加速电压为3 kV。
b)采用D8 Discover型X射线衍射仪(德国布鲁克公司)对样品进行物相分析,工作电压为40 kV,工作电流40 mA,扫描范围为2θ=10°~80°。由于Li2S对湿度敏感,在手套箱中制备测试样品,将n-Li2S/C复合材料使用聚酰亚胺(kapton)胶带密封后,转移至手套箱外进行测试。通过在手套箱中将Li2S3乙醇溶液蒸发得到新鲜的Li2S3样品,使用kapton胶带密封后进行测试。通过将Li2S3乙醇溶液在空气环境中静置6 d后蒸发得到空气暴露6 d的Li2S3测试样品,使用kapton胶带密封后测试。
c)采用PYRIS 1型综合热分析仪(美国柏金-埃尔默公司)对样品进行热重分析(TGA)测试。氧气气氛,温度区间为30~600 ℃,升温速率10 ℃/min。
1.5 电化学测试
电极制备及电池组装均在充满氩气的手套箱中进行,手套箱的水、氧体积含量均低于0.0005‰。实验组和对照组的电极制备、电池组装步骤保持一致,具体方法如下:将n-Li2S/C(或m-Li2S/C)和PVDF按质量比9∶1混合,添加NMP溶剂后搅拌12 h形成均匀浆料,涂覆在铝箔上,在60 ℃下真空干燥12 h,切成圆片电极;将圆片电极组装成2025型纽扣电池,使用锂片作负极,电解液为1 mol/L LiTFSI(VDOL∶VDEM = 1∶1作溶剂,添加质量分数1%的LiNO3)。
使用CT2001A型电池测试系统(武汉蓝电电子股份有限公司)进行恒流充放电测试,测试温度为室温。电池首圈循环以0.07 C充电至3.50 V,放电至1.70 V,之后循环在1.00 C的倍率下进行,电压范围为1.70~2.60 V。循环伏安测试和电化学阻抗谱分析均使用CHI760E型电化学工作站(上海辰华仪器有限公司),循环伏安测试的扫描范围:以0.05 mV/s的速率从开路电压扫描到3.50 V,在1.70~2.60 V循环。电化学阻抗谱测试在0.1 Hz~100 kHz的频率范围内进行,偏压5 mV。
2 结果与讨论
2.1 形貌表征
使用扫描电子显微镜(SEM)对n-Li2S/C的表面形貌结构进行了表征,结果如图2所示。从图2(a)中可以看到,n-Li2S/C复合材料中没有大块的晶体颗粒或团聚,各组分分布均匀,其中有细小的颗粒、线状物和较致密的不定形物质,分别对应于Li2S、CNTs和PVP热分解碳。由于PVP极性官能团具有强亲和力[12],限制了Li2S3在乙醇蒸发过程中的生长,进而减小了最终得到的Li2S的粒径。图2(b)是对图2(a)中虚线区域放大的SEM图,可以清晰地看到直径30~50 nm的Li2S颗粒和CNTs镶嵌在PVP热分解生成的不定形碳中,说明n-Li2S/C复合材料中导电碳与Li2S颗粒具有良好的接触,并能在一定程度上抑制多硫化锂的穿梭。
2.2 X射线衍射分析
图3为n-Li2S/C复合材料和Li2S3的X射线衍射图谱。从图3(a)可见,n-Li2S/C在约20°有一个非晶峰,归于kapton胶带,其他的衍射峰从左向右依次对应硫化锂的(111)、(200)、(220)、(311)、(222)、(400)、(331)、(420)晶面衍射峰,实验结果与Li2S的XRD标准卡片(PDF#77-2145)一致,表明从Li2S3到Li2S的转变是完全的,没有其他杂质生成。
为了探究Li2S3的空气稳定性,对新鲜Li2S3和在空气环境中放置6 d的Li2S3进行X射线衍射分析,结果如图3(b)所示。从图3(b)可见,除了20°附近属于kapton胶带的背景峰外,新鲜Li2S3和空气环境中放置6 d的Li2S3均没有发现其他衍射峰,表明Li2S3为非晶态,且在空气中暴露6 d后没有反应生成其他物质;相比之下,Li2S对湿度高度敏感,Li2S正极的制备通常需要在惰性气体或干燥空气环境中进行,将增加生产、储存和运输成本。其他使用低成本前驱体制备Li2S正极的方法,如高温碳热还原硫酸锂(Li2SO4),通常会得到微米或亚微米级的Li2S颗粒[14]。因此使用Li2S3前驱体生产Li2S将具有综合性优势,既能降低生产、储存和运输成本,又能得到高纯度的纳米级Li2S颗粒。
2.3 热重分析
为确定n-Li2S/C复合材料中Li2S的质量分数,在氧气气氛下进行热重分析测试,结果如图4所示。从图4可见,在300 ℃附近,n-Li2S/C中的Li2S被氧化为Li2SO4,质量增加,在450 ℃附近,n-Li2S/C中的碳被氧化为二氧化碳气体,质量减小,在600 ℃时质量趋于稳定,得到唯一产物Li2SO4。
根据n-Li2S/C在高温处理前后的质量变化可以计算出Li2S的含量[15],计算公式为:
X/%=45.95×m2109.94×m1×100
其中:X為n-Li2S/C中Li2S的含量;m1为n-Li2S/C高温处理前的质量;m2为n-Li2S/C高温处理后的质量。从图4可知,m2为m1的143%,即m2∶m1=143∶100,代入上式计算得到n-Li2S/C复合材料中Li2S的含量为60%。
2.4 电化学性能测试
图5(a)和图5(b)分别为n-Li2S/C和m-Li2S/C电极的循环伏安曲线,第一次循环首先从开路电压扫描至3.50 V,然后反向扫描至1.70 V,第二次循环扫描区间为1.70 ~ 2.60 V,扫描速度均为0.05 mV/s。从图5(a)可见,n-Li2S/C电极的第一次循环在2.70 V显示出宽的氧化峰,对应于Li2S转变为多硫化锂,在3.40 V也出现一个氧化峰,可能对应于多硫化锂转变为硫,在2.27 V和2.05 V观察到两个还原峰,分别对应于硫转变为长链多硫化锂(Li2Sn ,3≤n≤8)和多硫化锂转变为Li2S;第二次循环的氧化峰约为2.38 V,还原峰与第一次循环基本相同。因此,n-Li2S/C电极具有良好的电化学稳定性。从图5(b)可见,m-Li2S/C电极的第一次循环显示出3.15 V和3.45 V的氧化峰,明显高于n-Li2S/C电极,其原因是m-Li2S/C电极中的商业Li2S为微米颗粒,充电势垒较高,需要更高的活化电压才能完成充电,而n-Li2S/C电极中的Li2S为纳米颗粒,使充电势垒大大降低;m-Li2S/C电极第二次循环的氧化峰约为2.35 V,峰形相比n-Li2S/C电极更窄,这是因为m-Li2S/C电极中的Li2S暴露于碳和电解液中,而n-Li2S/C电极中的Li2S被PVP热分解碳包覆,充电过程存在稍强的极化现象。因此,n-Li2S/C电极可以在更低的截止电压活化,并且具有很好的电化学稳定性。
圖5(c)和图5(d)分别为n-Li2S/C和m-Li2S/C电极前三个循环的充放电平台曲线。第一次循环为0.07 C倍率,以充分活化Li2S;第二、三次循环为1.00 C倍率,以测试电池的倍率性能。从图5(c)可见,n-Li2S/C电极第一次循环的充电电压缓慢上升到截止电压3.50 V,与CV曲线中表现出的以2.70 V为中心的活化宽峰一致;第一次循环的放电过程存在2.30 V和2.10 V两个放电平台,其中2.30 V的高放电平台对应于硫转化为长链多硫化锂的过程,2.10 V的低放电平台对应于长链多硫化锂转变为短链多硫化锂并最终转化为Li2S或Li2S2的过程[16];第二、三次循环的充电平台表现出减小趋势,表明Li2S在第二次循环过程中发生了进一步活化;第二、三次循环同样具有两个放电平台,且放电平台电压与第一次循环相比变化较小,说明当倍率从0.07 C增加到1.00 C时,产生的极化对平台电压影响较小。从图5(d)可见,m-Li2S/C电极第一次循环的充电电压迅速上升到3.30 V,随后迅速下降到2.40 V,短暂充电后迅速上升到3.40 V,表现出商业Li2S典型的初始活化行为。由于m-Li2S/C电极的初始活化势垒较高,其初始充放电比容量明显低于n-Li2S/C电极。m-Li2S/C电极的第二、三次循环的放电平台的电压极化现象同样较弱,这可能得益于两种电极中CNT导电骨架对倍率性能的提升。
n-Li2S/C和m-Li2S/C电极在1.00 C倍率下的循环性能和库伦效率如图5(e)所示。从图5(e)可见,n-Li2S/C电极在0.07 C倍率下的首次放电比容量达910 mAh/g(基于活性物质硫化锂),活性物质利用率为78%,而m-Li2S/C电极仅为650 mAh/g和56%。初始活化循环之后,在1.00 C倍率下进行循环,由于电化学反应动力学迟滞,n-Li2S/C电极的放电比容量降至605 mAh/g,而m-Li2S/C电极则降至456 mAh/g;n-Li2S/C电极在前几个循环中出现了容量回升,可能是充放电过程中,活性物质发生了重新分布,增强了与碳的导电接触,电极反应动力学得到了改善,提升了活性物质利用率;n-Li2S/C电极在1.00 C倍率下循环150次后放电比容量为484 mAh/g,表现出优良的倍率性能。除前两次循环外,库伦效率一直平稳地保持在97%以上;而m-Li2S/C电极在150次循环后放电比容量仅为322 mAh/g,库伦效率波动性地保持在96%以上。因此,n-Li2S/C电极具有良好的倍率性能和循环稳定性,这主要由于PVP热分解碳能够抑制多硫化锂穿梭,减缓容量衰减,而CNTs导电骨架能够提供良好的导电性,提升倍率性能。
对n-Li2S/C和m-Li2S/C电极进行循环前的电化学阻抗测试,结果如图6所示。从图6可见,曲线由高频区的半圆和低频区的倾斜线组成,分别对应于电荷转移电阻(Rct)和Warburg阻抗[17],使用等效电路模型进行拟合,得到n-Li2S/C电极的电荷转移电阻为33.3 Ω,远低于m-Li2S/C电极(61.2 Ω)。因此,n-Li2S/C电极具有更快速的离子、电子输运,证明了n-Li2S/C电极所表现出的更优异电化学性能。
3 结 论
本文将硫化锂和硫、碳纳米管、聚乙烯吡咯烷酮在乙醇中进行简单混合及重结晶、高温处理,得到具有增强电子和离子导电性的纳米硫化锂/碳(n-Li2S/C)复合材料,对其形貌、结构和组成进行了表征,并将其用作锂硫电池正极,进行了一系列电化学性能测试,主要结论如下:
a)通过聚乙烯吡咯烷酮对Li2S3的强亲和力限制了最终Li2S的粒径大小,得到被热分解碳和碳纳米管包覆的纳米Li2S颗粒,使n-Li2S/C电极的活性物质利用率达78%,在1.00 C的高倍率下,循环150圈后放电比容量为484 mAh/g,库伦效率平稳保持在97%以上,表现出优异的倍率性能。
b)利用Li2S3前驱体在空气环境中的稳定性来制备Li2S正极,可以降低纳米Li2S基正极材料的生产成本,具有实际应用价值。
参考文献:
[1]Seh Z W, Sun Y M, Zhang Q F, et al. Designing high-energy lithium-sulfur batteries[J]. Chemical Society Reviews, 2016, 45(20): 5605-5634.
[2]Liu M N, Ye F M, Li W F, et al. Chemical routes toward long-lasting lithium/sulfur cells[J]. Nano Research, 2016, 9(1): 94-116.
[3]Zhu J D, Zhu P, Yan C Y, et al. Recent progress in polymer materials for advanced lithium-sulfur batteries[J]. Progress in Polymer Science, 2019, 90: 118-163.
[4]Bruce P G, Freunberger S A, Hardwick L J, et al. Li-O2 and Li-S batteries with high energy storage[J]. Nature Materials, 2012, 11(1): 19-29.
[5]Yao Y, Wang H, Yang H, et al. A dual-functional conductive framework embedded with TiN-VN heterostructures for highly efficient polysulfide and lithium regulation toward stable Li-S full batteries[J]. Advanced Materials, 2020, 32(6): 1905658.
[6]Zheng S Y, Chen Y, Xu Y H, et al. In situ formed lithium sulfide/microporous carbon cathodes for lithium-ion batteries[J]. ACS Nano, 2013, 7(12): 10995-11003.
[7]Hassoun J, Scrosati B. A high-performance polymer tin sulfur lithium ion battery[J]. Angewandte Chemie (International Ed in English), 2010, 49(13): 2371-2374.
[8]Yang Y, McDowell M T, Jackson A, et al. New nanostructured Li2S/silicon rechargeable battery with high specific energy[J]. Nano Letters, 2010, 10(4): 1486-1491.
[9]Yang Y, Zheng G Y, Misra S, et al. High-capacity micrometer-sized Li2S particles as cathode materials for advanced rechargeable lithium-ion batteries[J]. Journal of the American Chemical Society, 2012, 134(37): 15387-15394.
[10]Tsao Y, Lee M, Miller E C, et al. Designing a quinone-based redox mediator to facilitate Li2S oxidation in Li-S batteries[J]. Joule, 2019, 3(3): 872-884.
[11]Li X, Gao M X, Du W B, et al. A mechanochemical synthesis of submicron-sized Li2S and a mesoporous Li2S/C hybrid for high performance lithium/sulfur battery cathodes[J]. Journal of Materials Chemistry A, 2017, 5(14): 6471-6482.
[12]Wu F X, Kim H, Magasinski A, et al. Harnessing steric separation of freshly nucleated Li2S nanoparticles for bottom-up assembly of high-performance cathodes for lithium-sulfur and lithium-ion batteries[J]. Advanced Energy Materials, 2014, 4(11): 1400196.
[13]Chen C G, Li D J, Gao L, et al. Carbon-coated core-shell Li2S@C nanocomposites as high performance cathode materials for lithium-sulfur batteries[J]. Journal of Materials Chemistry A, 2017, 5(4): 1428-1433.
[14]Yuan K, Yuan L X, Chen J, et al. Methods and cost estimation for the synthesis of nanosized lithium sulfide[J]. Small Structures, 2021, 2(3): 2000059.
[15]Ye F M, Hou Y, Liu M N, et al. Fabrication of mesoporous Li2S-C nanofibers for high performance Li/Li2S cell cathodes[J]. Nanoscale, 2015, 7(21): 9472-9476.
[16]Zhang K, Wang L, Hu Z, et al. Ultrasmall Li2S nanoparticles anchored in graphene nanosheets for high-energy lithium-ion batteries[J]. Scientific Reports, 2014, 4: 6467.
[17]Wang D H, Xia X H, Wang Y D, et al. Vertical-aligned Li2S-graphene encapsulated within a carbon shell as a free-standing cathode for lithium-sulfur batteries[J]. Chemistry-A European Journal, 2017, 23(46): 11169-11174.
(責任编辑:张会巍)
收稿日期: 2022-03-17 网络出版日期:2022-06-02网络出版日期
基金项目: 国家自然科学基金项目(22075313);浙江理工大学科研启动基金(18062299-Y)
作者简介: 房 彬(1996— ),男,山东济宁人,硕士研究生,主要从事锂硫电池方面的研究。
通信作者: 叶方敏,E-mail:fmye2018@zstu.edu.cn

