血清尿酸、同型半胱氨酸及超敏C 反应蛋白与非瓣膜性心房颤动患者发生血栓形成的关系
朱琳,杨文静,尤立蕊
非瓣膜性心房颤动(nonvalvular atrial fibrillation,NVAF)是一种心律失常类型,极易引起血栓(发生率为5%~14%)[1-2]。研究表明,尿酸(uric acid,UA)形成过程中常伴有活性氧生成,且活性氧与氧化应激、炎症反应和血栓形成密切相关[3-4]。同型半胱氨酸(homocysteine,Hcy)是一种含硫氨基酸,其可损伤血管内皮细胞,促进动脉粥样硬化形成、血栓调节因子表达及血小板聚集,进而增加动脉血栓形成风险[5-6]。hs-CRP是临床常见的炎性因子[7]。国内研究表明,NVAF与炎症反应密切相关[8],但NVAF患者发生血栓形成是否与炎症反应有关尚未完全明确。基于此,本研究旨在分析血清UA、Hcy、hs-CRP与NVAF患者发生血栓形成的关系,以期进一步明确炎症反应与NVAF的关系。
1 对象与方法
1.1 研究对象 采用整群抽样法选取2020年1月至2022年1月北京市普仁医院和中国医科大学航空总医院收治的186例NVAF患者作为房颤组。纳入标准:符合《2020 ESC/EACTS心房颤动诊断与管理指南》中NVAF的诊断标准[9]。排除标准:(1)近2周内发生感染性疾病者;(2)入组前合并动脉血栓栓塞性疾病者;(3)近3个月内行手术治疗者;(4)合并肿瘤、自身免疫性疾病者;(5)入组前3个月内服用过影响血清UA、Hcy、hs-CRP水平的药物者;(6)合并慢性炎症性疾病者。另选取同期在北京市普仁医院和中国医科大学航空总医院进行体检的53例健康者作为对照组。本研究经北京市普仁医院医学伦理委员会批准(批号:202304120087),患者均对本研究知情并签署知情同意书。
1.2 血栓形成评估方法 收集患者空腹静脉血3 ml,采用酶联免疫吸附试验检测D-二聚体和凝血酶原时间。本研究以D-二聚体>0.5 mg/L和/或凝血酶原时间<10 s判定为存在血栓形成。根据房颤组患者是否发生血栓形成将其分为血栓亚组(n=51)和无血栓亚组(n=135)。
1.3 观察指标
1.3.1 临床特征 收集NVAF患者的临床特征,包括年龄、性别、饮酒年限、合并症(高血压、糖尿病、高脂血症、肌酐异常)情况、心房颤动病程、心房颤动类型(分为持续性心房颤动和阵发性心房颤动)及左心房内径。
1.3.2 实验室检查指标 收集两组受试者空腹静脉血3 ml,采用比色法检测血清UA,所用仪器为GNST-CL201自动比色仪;采用循环酶法检测血清Hcy,所用仪器为Varioskan LUX酶标仪;采用免疫比浊法检测血清hs-CRP,所用仪器为YZ-2000A/3000A型免疫动态比浊仪。
1.4 统计学方法 采用SPSS 23.0统计学软件进行数据处理。符合正态分布的计量资料以(±s)表示,两组间比较采用成组t检验;计数资料比较采用χ2检验;NVAF患者发生血栓形成的影响因素分析采用多因素Logistic回归分析;绘制ROC曲线以评估血清UA、Hcy、hs-CRP对NVAF患者发生血栓形成的预测价值。以P<0.05为差异有统计学意义。
2 结果
2.1 对照组与房颤组实验室检查指标比较 房颤组血清UA、Hcy、hs-CRP高于对照组,差异有统计学意义(P<0.05),见表1。
表1 对照组和房颤组实验室检查指标比较(±s)Table 1 Comparison of laboratory examination indexes between the control group and the observation group
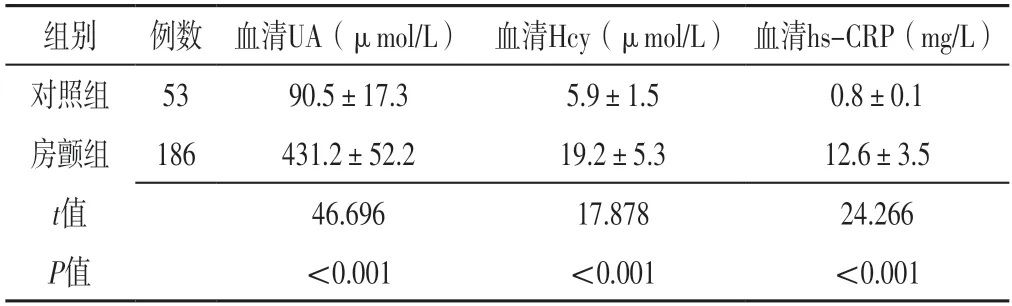
表1 对照组和房颤组实验室检查指标比较(±s)Table 1 Comparison of laboratory examination indexes between the control group and the observation group
注:UA=尿酸,Hcy=同型半胱氨酸
组别例数 血清UA(μmol/L) 血清Hcy(μmol/L) 血清hs-CRP(mg/L)对照组5390.5±17.35.9±1.50.8±0.1房颤组186431.2±52.219.2±5.312.6±3.5 t值46.69617.87824.266 P值<0.001<0.001<0.001
2.2 血栓亚组与无血栓亚组临床特征比较 血栓亚组与无血栓亚组性别、饮酒年限及有肌酐异常者占比比较,差异无统计学意义(P>0.05);血栓亚组年龄和左心房内径大于无血栓亚组,有高血压、糖尿病、高脂血症者占比及持续性心房颤动者占比高于无血栓亚组,心房颤动病程长于无血栓亚组,差异有统计学意义(P<0.05),见表2。
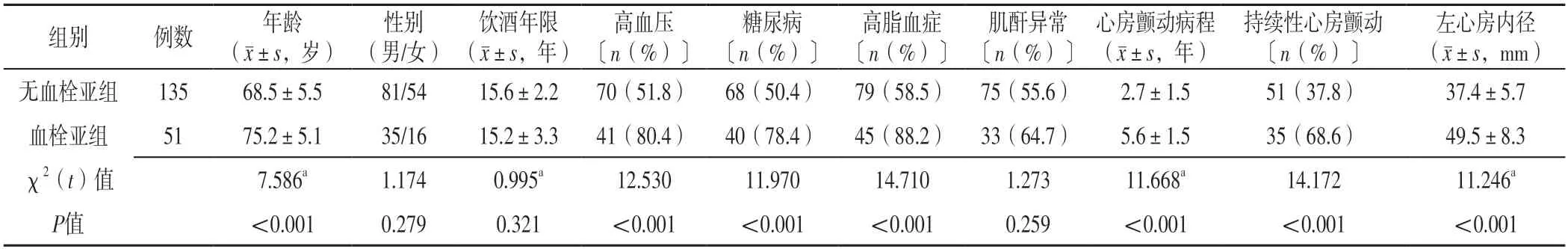
表2 血栓亚组与无血栓亚组临床特征比较Table 2 Comparison of clinical characteristics between thrombus subgroup and non-thrombus subgroup
2.3 血栓亚组与无血栓亚组实验室检查指标比较 血栓亚组血清UA、Hcy、hs-CRP高于无血栓亚组,差异有统计学意义(P<0.05),见表3。
表3 血栓亚组与无血栓亚组实验室检查指标比较(±s)Table 3 Comparison of laboratory examination indexes between thrombus subgroup and non-thrombus subgroup

表3 血栓亚组与无血栓亚组实验室检查指标比较(±s)Table 3 Comparison of laboratory examination indexes between thrombus subgroup and non-thrombus subgroup
组别例数 血清UA(μmol/L) 血清Hcy(μmol/L) 血清hs-CRP(mg/L)无血栓亚组 135364.2±45.210.1±9.88.8±2.5血栓亚组51463.2±55.523.5±8.414.4±2.2 t值12.4848.61313.937 P值<0.001<0.001<0.001
2.4 NVAF患者发生血栓形成的影响因素 以NVAF患者是否发生血栓形成为因变量(赋值:未发生=0,发生=1),以表2~3中有统计学差异的指标为自变量,进行多因素Logistic回归分析,结果显示,年龄、糖尿病、高脂血症、心房颤动病程、左心房内径及血清UA、Hcy、hs-CRP是NVAF患者发生血栓形成的独立影响因素(P<0.05),见表4。

表4 NVAF患者发生血栓形成影响因素的多因素Logistic回归分析Table 4 Multivariate Logistic regression analysis of influencing factors of thrombosis in NVAF patients
2.5 血清UA、Hcy、hs-CRP对NVAF患者发生血栓形成的预测价值 ROC曲线分析结果显示,血清UA、Hcy、hs-CRP预测NVAF患者发生血栓形成的AUC分别为0.964〔95%CI(0.926,0.986)〕、0.934〔95%CI(0.888,0.965)〕、0.976〔95%CI(0.943,0.993)〕,见表5、图1。

图1 血清UA、Hcy、hs-CRP预测NVAF患者发生血栓形成的ROC曲线Figure 1 ROC curve of serum UA,Hcy and hs-CRP in predicting thrombosis in patients with NVAF

表5 血清UA、Hcy、hs-CRP对NVAF患者发生血栓形成的预测价值Table 5 Predictive value of serum UA,Hcy and hs-CRP for thrombosis in patients with NVAF
3 讨论
NAVF为非继发于心瓣膜病(如二尖瓣重度狭窄)的心房颤动[10],其是临床常见的心律失常类型,好发于中老年人群,且可引起严重的并发症如脑栓塞、肾动脉栓塞、肠系膜动脉栓塞、外周动脉栓塞、心肌梗死、心力衰竭等,其中血栓栓塞事件是较为严重的并发症之一,可严重危害患者的生命健康、降低患者的生活质量[11-12]。研究表明,有基础心脏病或肺部疾病的患者发生急性缺氧、代谢紊乱或血流紊乱、高碳酸血症时,可能出现NAVF[13-14];此外,罹患心血管疾病如冠心病、缩窄性心包炎、心肌病、感染性心内膜炎及慢性肺源性心脏病的患者也可能发生NAVF[15]。本研究旨在探讨血清UA、Hcy、hs-CRP与NVAF患者发生血栓形成的关系。
本研究结果显示,房颤组血清UA、Hcy、hs-CRP高于对照组,提示NAVF患者血清UA、Hcy、hs-CRP异常升高,分析其原因可能为:UA产生于嘌呤代谢过程中[16-17],且随着UA增多,超氧阴离子与一氧化氮反应生成亚硝酸阴离子,进而导致一氧化氮生物利用度降低[18],引起脱氧核糖核酸损伤、细胞死亡和脂质过氧化反应加剧[19],从而介导炎症反应,导致NAVF。Hcy是机体某物质代谢的中间产物,其水平升高可能会促进动脉粥样硬化及炎症反应,从而增加NAVF发生概率[20]。而hs-CRP作为系统炎症因子,可参与NAVF的发生[21-22]。
本研究结果显示,血栓亚组血清UA、Hcy、hs-CRP高于非血栓亚组;多因素Logistic回归分析结果显示,血清UA、Hcy、hs-CRP是NAVF患者发生血栓形成的独立影响因素,分析原因可能为:UA可诱发氧化应激和炎症反应,导致心房结构改变、心肌内各种传导束异常及心肌收缩功能异常,进而容易诱发血栓[23];此外,UA可以促进血管平滑肌细胞增殖和血栓素A2合成,使血液处于高凝状态[3],进而增加血栓形成发生风险;再者,UA升高后会通过激活氧化应激和肾素-血管紧张素系统而诱导血管内皮细胞衰老、死亡,进而导致内皮功能损伤,增加血栓形成发生风险[6]。研究表明,Hcy可以引起血管损伤,如血管内膜增厚、弹性膜破坏、平滑肌肥大,进而引起血小板聚集及血栓形成[7]。本研究ROC曲线分析结果显示,血清UA、Hcy、hs-CRP预测NVAF患者发生血栓形成的AUC分别为0.964、0.934、0.976,提示血清UA、Hcy、hs-CRP对NVAF患者发生血栓形成具有较高的预测价值。
综上所述,血清UA、Hcy、hs-CRP升高是NVAF患者发生血栓形成的危险因素,且三者均对NVAF患者发生血栓形成有较高的预测价值。但本研究为单中心研究,观察指标有限,可能存在混杂因素,故所得结论仍有待高质量研究进一步证实。
作者贡献:朱琳进行文章的构思与设计,研究的实施与可行性分析,结果分析与解释,负责撰写、修订论文;杨文静进行数据收集、整理、分析;尤立蕊负责文章的质量控制及审校,对文章整体负责、监督管理。
本文无利益冲突。

