基于网络药理学联合加权基因共表达网络分析黄精治疗代谢性相关脂肪性肝病的作用机制
邬东东,杨启帆,方柔柔,徐守竹*,赵晶
1.陕西中医药大学 公共卫生学院,陕西 咸阳 712046
2.陕西省针药结合重点实验室,陕西 咸阳 712046
随着生活水平的提高、饮食结构和习惯的改变,脂肪肝发病率显著上升且向低龄人群发展趋势,已成为威胁人类健康的常见慢性疾病[1]。代谢性相关脂肪性肝病是一种与胰岛素抵抗和遗传易感性密切相关的代谢应激性肝损伤,分为非酒精性单纯性肝脂肪病变、非酒精性脂肪性肝炎和与之相关的肝硬化,病理表现为弥漫性肝细胞脂肪病变[2]。目前代谢性相关脂肪性肝病的发病原因尚不明确,存在多种假说,如“二次打击”学说[3]、脂毒性学说[4]等。但是,任何一种假说都不能完全阐明代谢性相关脂肪性肝病的病因,以致临床治疗方法多样。中医药在治疗代谢性相关脂肪性肝病方面具有独特的优势[5],但中医药治疗代谢性相关脂肪性肝病的作用机制尚不明确,亟待阐明。
黄精是一种百合科植物,药用部位为根状茎,在我国盛产于内蒙古、河北、陕西、云南等地[6]。《名医别录》中记载黄精具有“补中益气,除风湿,安五脏,久服轻身、延年、不饥”等功效[7]。此外,医书古籍也有记载其可用于治疗脾胃虚弱、体倦乏力、肺虚燥咳、精血不足、内热消渴等症状。近年来研究发现,黄精在抗衰老、调节血糖血脂、抗菌抗肿瘤等方面具有潜在药用价值[8-9],可以通过调控氧化应激损伤发挥对非酒精性脂肪肝大鼠肝保护作用[10],而且能够促进代谢性相关脂肪性肝病的良性转归[11-14]。此外,黄精也是治疗代谢性相关脂肪性肝病常用中成药的主要中药材之一,然而其治疗代谢性相关脂肪性肝病的作用及机制报道较少。
网络药理学是以系统生物学理论为基础,药理学为方向建立“药物–疾病–靶点–通路”系列网络关系的研究方法,其可以建立中药成分与疾病相互作用网络,为中药的复杂性研究提供了清晰的思路和视角[15]。本研究基于网络药理学、加权基因共表达网络分析开展黄精治疗代谢性相关脂肪性肝病的“成分–疾病–靶点–通路”分析,并采用分子对接技术进行验证。
1 材料和方法
1.1 黄精活性成分的筛选
通过中药系统药理学数据库与分析平台(TCMSP,http://tcmsw.com/tcmsp.php)获取黄精有效成分,以口服生物利用度(OB)≥30%,化合物类药性(DL)≥0.18 为标准筛选活性成分。
1.2 基于药效团模型预测黄精活性成分潜在作用靶点
在 Pharm Mapper 网 站(http://www.lilabecust.cn/pharmmapper/)上传MDL Molfile(*mol)文件,在“select a species”中设定“homo sapiens”,获取并筛选Z-score≥0.5 的潜在靶点。
1.3 代谢性相关脂肪性肝病基因差异分析及加权基因共表达网络分析
在GEO 数据库中下载GSE89632 代谢性相关脂肪性肝病基因表达数据集,利用R 软件的limma包进行数据集差异分析;利用“WGCNA”包构建加权基因共表达网络,通过Soft Threshold 函数计算出相关系数和软阈值,依据软阈值进一步计算出拓扑重叠矩阵(TOM),最后利用TOM 进行分层聚类,分割模块,分值较高的模块筛选作为疾病基因模块。
1.4 基于GeneCards 平台构建代谢性相关脂肪性肝病相关基因库
利用GeneCards(https://www.genecards.org/)数据库,输入“non-alcoholic fatty liver disease”检索其相关基因并导出结果,构建GeneCards 的代谢性相关脂肪性肝病数据库。
1.5 疾病数据库验证与靶点筛选
将加权基因共表达网络分析获得疾病基因模块、黄精潜在靶点基因以及GeneCards 数据库获得的代谢性相关脂肪性肝病相关基因利用 Venn Diagram 求取交集,获取黄精治疗代谢性相关脂肪性肝病的靶点基因。
1.6 蛋白相互作用(PPI)网络构建
将1.5 项下获取的潜在靶点基因导入String 数据库(https://string-db.org/),获取黄精活性成分靶点PPI 网络。将潜在靶点基因网络导入Cytoscape 3.8.2软件借助cytoHubba 插件的NCC 算法筛选活性成分治疗代谢性相关脂肪性肝病的核心靶点基因。
1.7 基因本体论(GO)分析和京都基因与基因组百科全书(KEGG)信号通路分析
黄精活性成分治疗代谢性相关脂肪性肝病的共同靶点通过R 语言的enrichplot 包和ggplot2 包进行分子功能(MF)、生物过程(BP)、细胞成分(CC)分析以及KEGG 富集分析。
1.8 分子对接
以筛选的核心靶点为受体,相关黄精活性成分为配体,在PDB 蛋白质结构数据库中下载高分辨率蛋白晶体结构,对受体结构优化后,利用MOE 软件中Dock 功能模块进行分子对接。
2 结果
2.1 黄精活性成分与靶点预测
以OB≥30%,DL≥0.18 为筛查标准,在黄精38 种化合物中获得β-谷甾醇、谷甾醇、薯蓣皂苷元、甘草素等12 种活性成分,见表1。将12 种活性成分导入在Pharm Mapper 数据库中,去除重复靶点筛选出黄精预测靶点327 个。

表1 黄精活性成分信息Table 1 Information of active ingredients in Polygonati Rhizoma
2.2 代谢性相关脂肪性肝病差异基因
利用R 软件的limma 包进行数据集GSE89632的差异分析,以P<0.05 和|log2FC|>1 为筛选标准,获得差异基因452 个,其中下调基因249 个,上调基因203 个,火山图见图1。在GeneCards 数据库获得代谢性相关脂肪性肝病相关基因1 227 个。
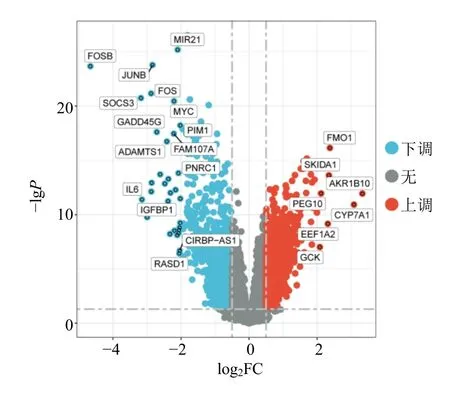
图1 GSE89632 数据集差异基因火山图Fig.1 Volcano plot of GSE89632 differential analysis
2.3 加权基因共表达网络分析
WGCNA 通过R 语言“WGCNA”包对数据集GSE89632 分析,利用Soft Threshold 函数筛选出相关系数为0.92 所对应的软阈值为13,最小模块值为30,见图2A。通过基因聚类结果得到的不同模块分析,发现2 个与代谢性相关脂肪性肝病密切相关的基因模块(MEdarkgreen 和MEdarkorange),共2 639 个基因(图2B、C)。

图2 靶点基因差异分析及WGCNA 分析Fig.2 Difference analysis and WGCNA analysis of key target
2.4 黄精治疗代谢性相关脂肪性肝病潜在靶点基因的获取
通过R 语言的Venn Diagram 包将WGCNA 的疾病模块基因、GeneCards 代谢性相关脂肪性肝病相关基因及黄精潜在靶点取交集,得到黄精治疗代谢性相关脂肪性肝病潜在靶点基因18 个,分别为乙醇脱氢酶5(ADH5)、葡萄糖激酶(GCK)、核受体亚家族1 组I 成员3(NR1I3)、血红素氧合酶1(HMOX1)、趋化因子配体5(CCL5)、磷酸肌醇3-激酶调节亚基1(PIK3R1)、维甲酸X 受体α(RXRA)、胆固醇稳态基因(NR1H3)、人丝氨酸蛋白酶抑制因子1(SERPINA1)、热休克蛋白90α 家族A 类成员1(HSP90AA1)、维生素D3 受体(VDR)、蛋白酪氨酸性磷酸非受体型11(PTPN1)、过氧化物酶体增殖物激活受体α(PPARA)、β 位淀粉样前体蛋白裂解酶1(BACE1)、一氧化氮合酶3(NOS3)、F3、核受体亚家族1 组I 成员2(NR1I2)、S100 钙结合蛋白A9(S100A9)。
2.5 黄精活性成分治疗代谢性相关脂肪性肝病的潜在靶点基因富集分析
富集分析发现,黄精活性成分治疗代谢性相关脂肪性肝病潜在靶点基因参与胆道疾病、脂质蓄积相关疾病、脂肪肝病及动脉粥样硬化等296 种疾病,见图3。靶点基因主要分布在小窝、分泌颗粒腔、胞质囊泡管腔、囊泡腔、溶酶体腔等25 个CC,发挥核受体活性、配体活化、转录因子活性、羧酸结合、类固醇结合、一元羧酸结合、RNA 聚合酶II 特异性DNA 结合转录、核类固醇受体活性等93 个MF,参与对细胞内受体信号通路–胆固醇储存负调控、小分子代谢过程的正调节、肌细胞增殖、胆固醇储存的负调节等767 个BP,见图4。KEGG 富集分析显示,黄精活性成分治疗代谢性相关脂肪性肝病潜在靶点基因参与调控代谢性相关脂肪性肝病、胰岛素抵抗、血脂和动脉粥样硬化、PPAR 信号通路等43 个通路,见图5。其中胰岛素抵抗信号通路在KEGG 通路网络富集中显著性最强,通过R 包绘制相关通路图相互关系图,见图6。
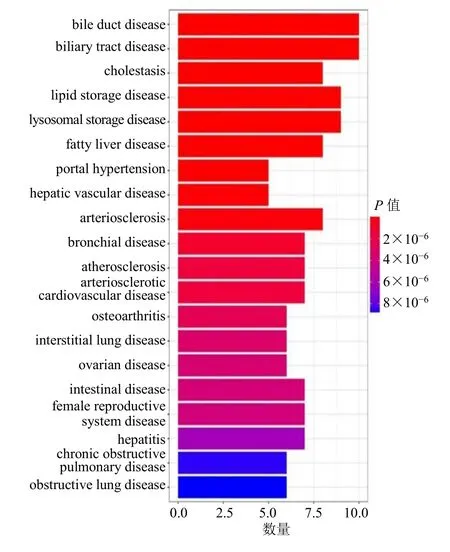
图3 黄精活性成分治疗代谢性相关脂肪性肝病潜在靶点基因参与的相关疾病Fig.3 Active ingredient of Polygonati Rhizoma in treatment of metabolically associated fatty liver disease involving potential target genes related diseases
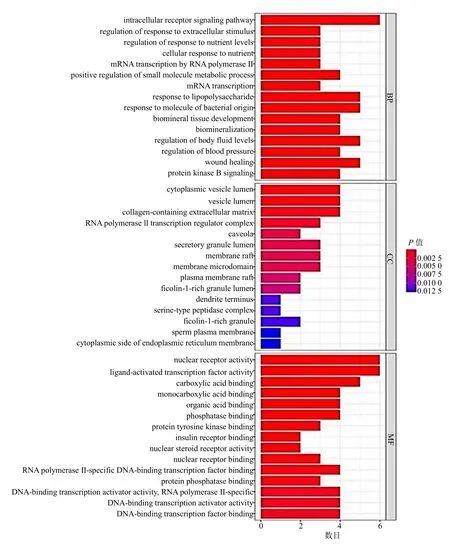
图4 GO 富集分析Fig.4 GO enrichment analysis
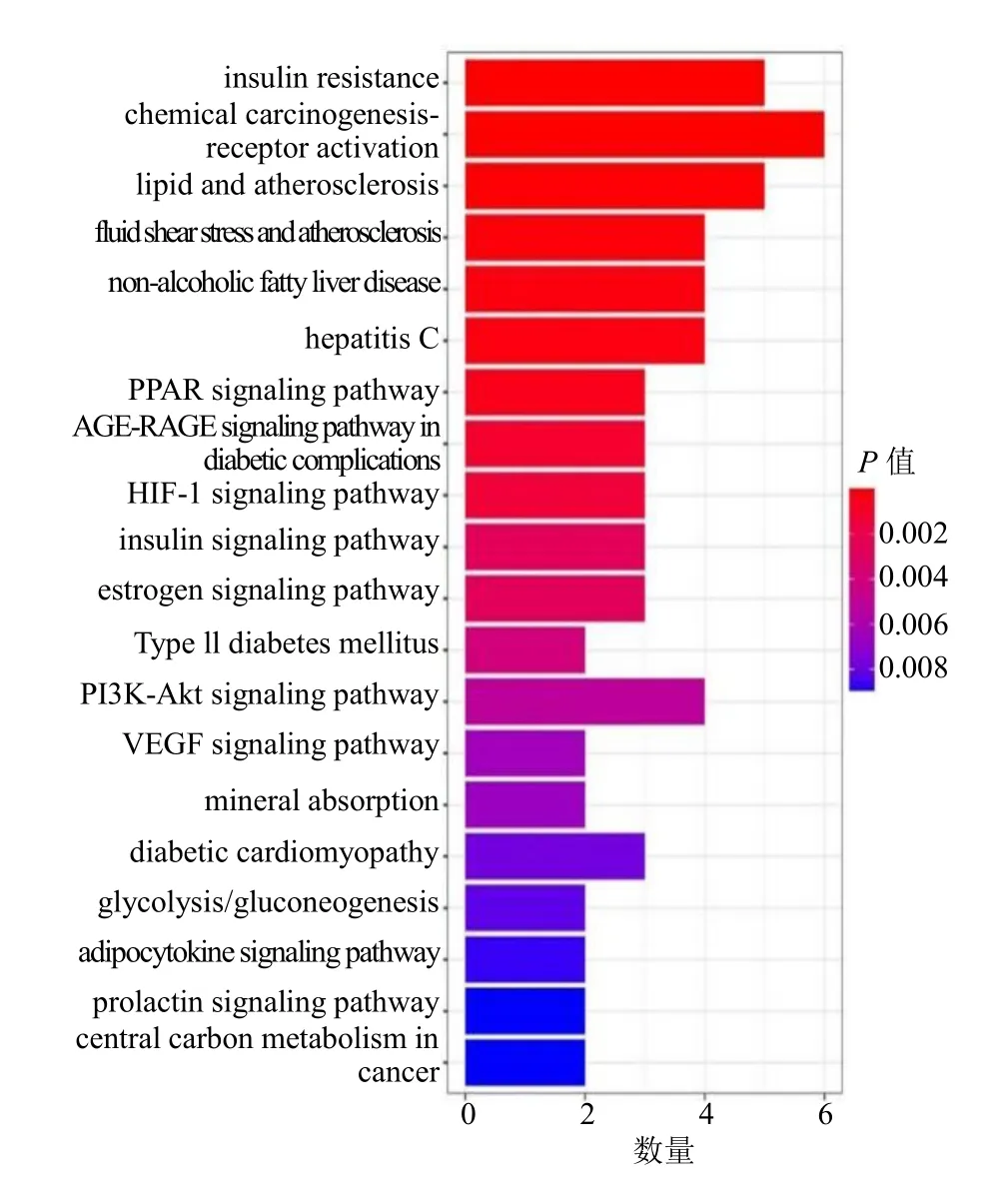
图5 KEGG 通路富集分析Fig.5 KEGG pathway enrichment analysis
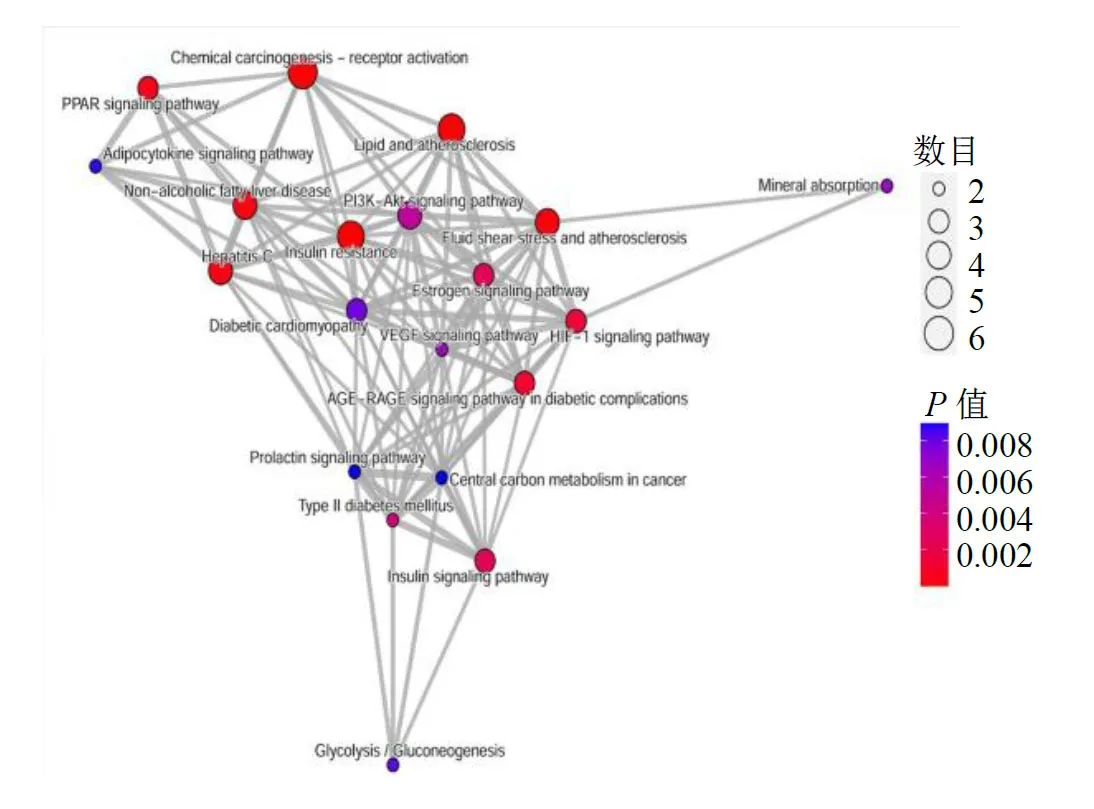
图6 相关通路图相互关系图Fig.6 Correlation path diagram Interrelationship diagram
2.6 黄精活性成分治疗代谢性相关脂肪性肝病的潜在靶点基因PPI 网络及核心基因分析
将黄精活性成分治疗代谢性相关脂肪性肝病的18 个潜在靶点基因导入String 数据库,获取黄精活性成分–代谢性相关脂肪性肝病的潜在靶点基因PPI 网络,包括18 个节点,30 条边,利用Cytoscape 3.8.2 软件的cytoHubba 插件中NCC 算法筛选前5 位的核心靶点HSP90AA1、PPARA、NOS3、PTPN1、HMOX1 进行分子对接验证,见图7。
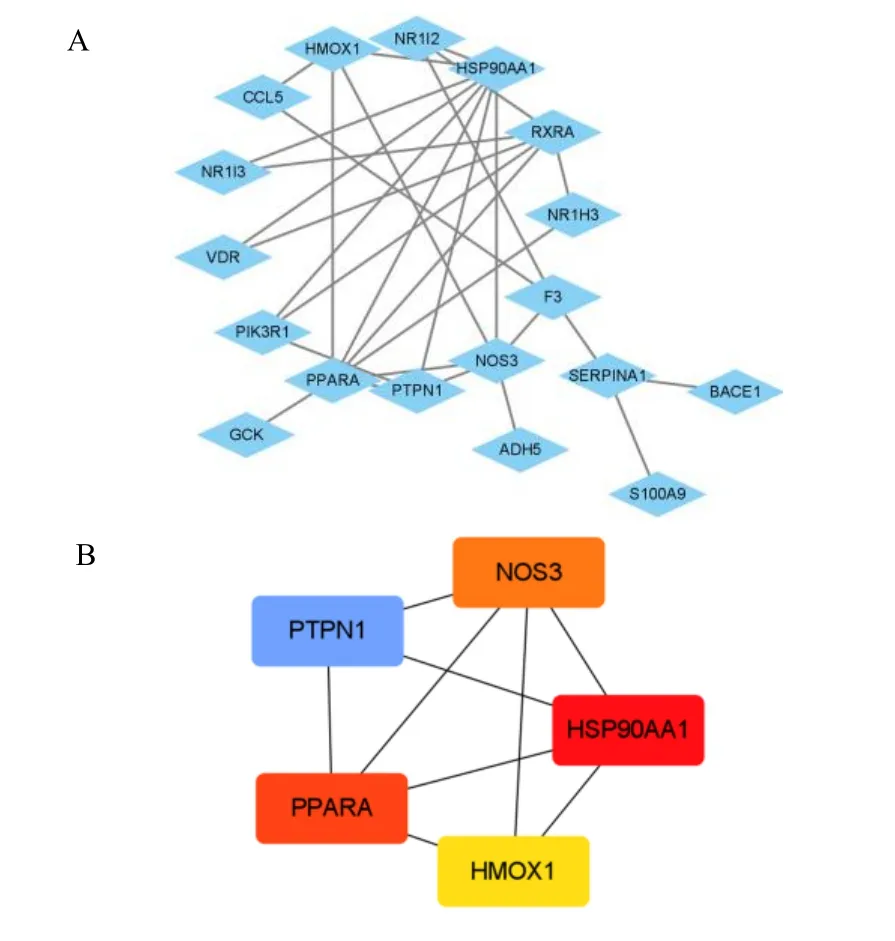
图7 黄精治疗代谢性相关脂肪性肝病靶点PPI 网络(A)及核心靶点网络(B)Fig.7 Protein interaction network (A) and the core target genes of Polygonati Rhizoma in treatment of metabolically associated fatty liver disease (B)
2.7 黄精活性成分与核心靶点分子对接结果
通过MOE 中的Dock 模块功能进行分子对接,选择基于蛋白和配体相互作用能的打分函数ASE,分别得到黄精活性成分与核心靶点的对接,结合能越低,受体与配体的结合越稳定,见表2。结果显示黄精活性成分与核心靶点结合相对稳定,其中结合能<−7.00 kJ/mol 的相互作用可视化见图8。
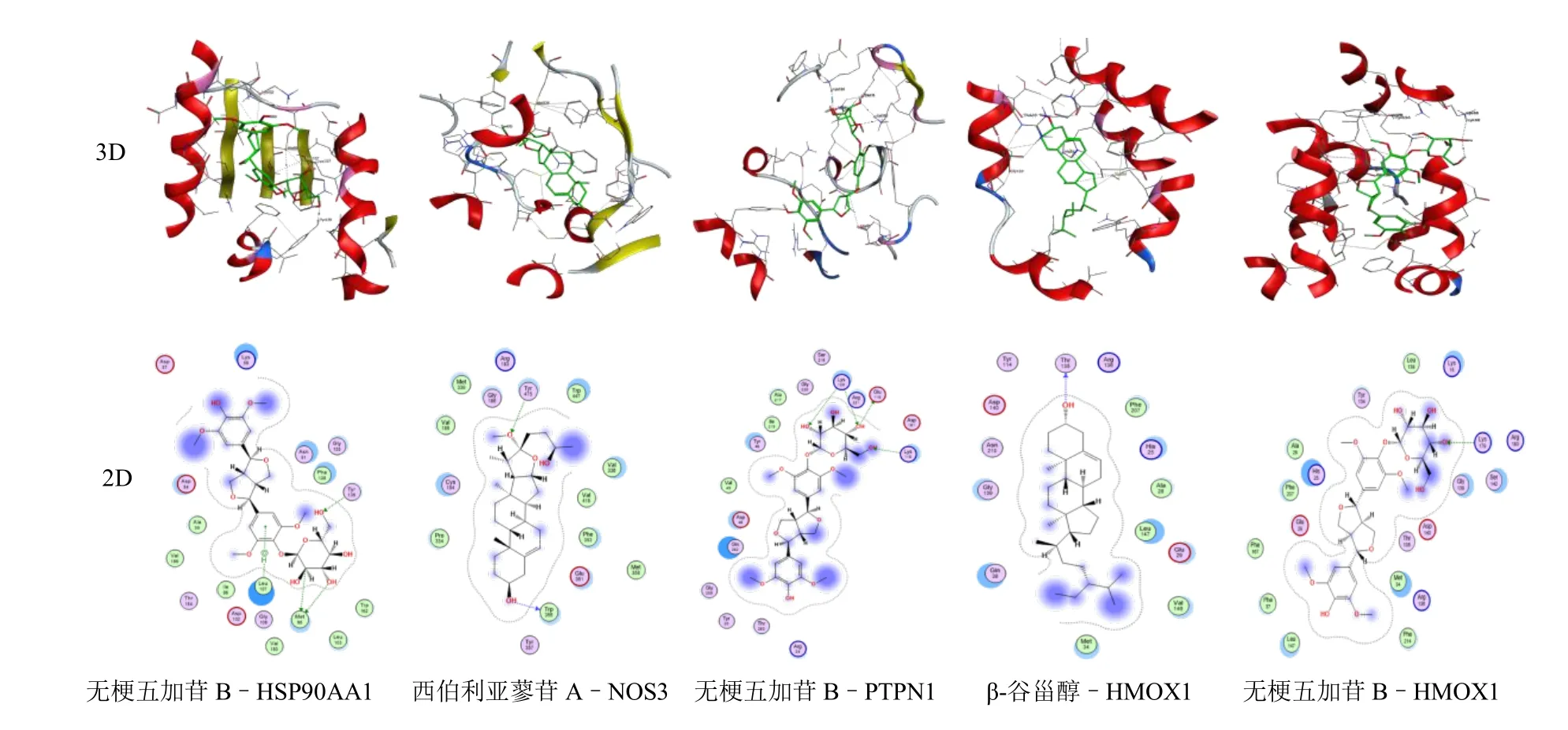
图8 分子对接可视化Fig.8 Molecular docking
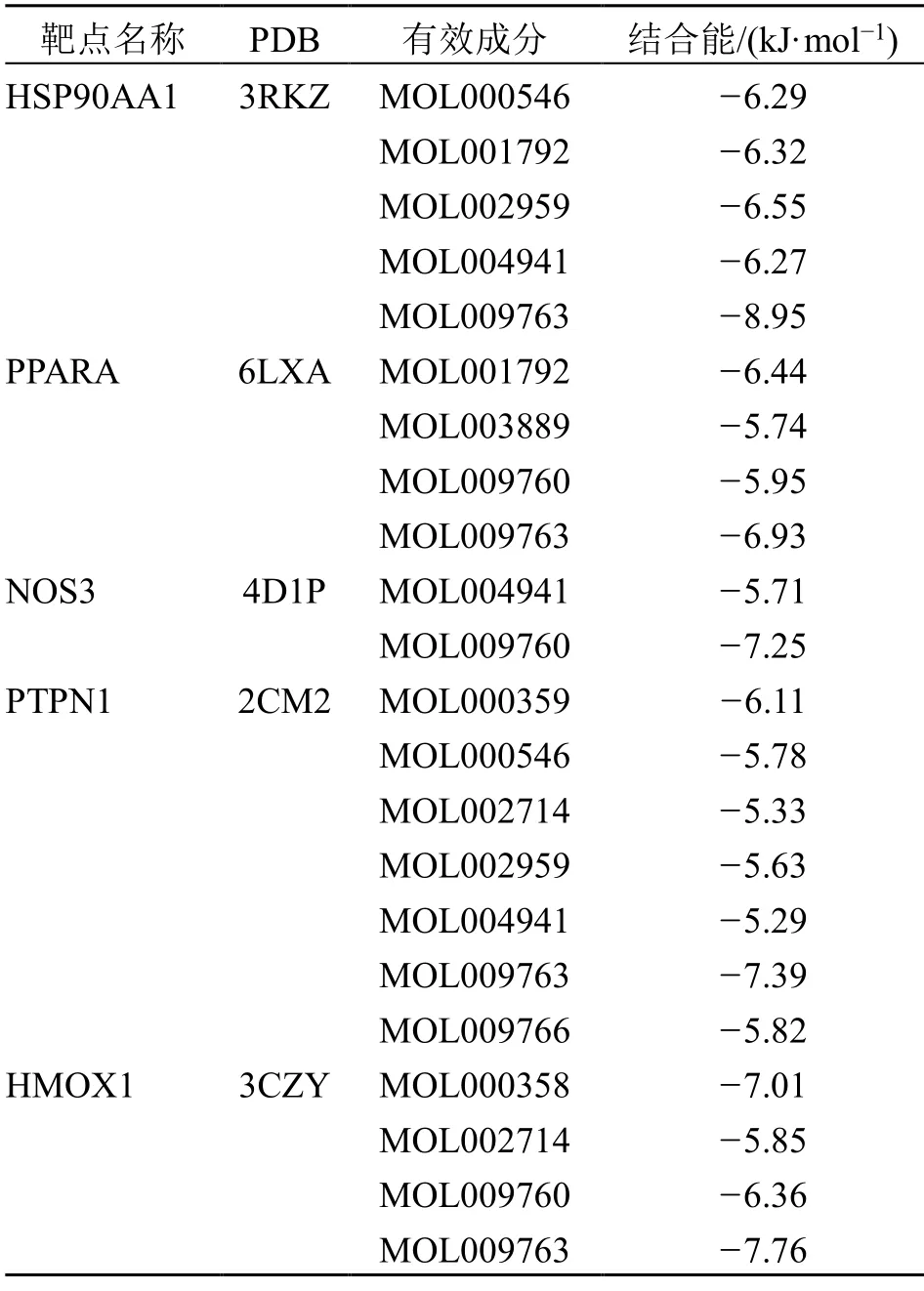
表2 核心靶点与活性成分结合对接信息Table 2 Docking information of the active components and targets
3 讨论
黄精是一味药食同源中药材,具有抗炎、调节脂质代谢、改善动脉粥样硬化等作用[16-17]。虽然现代药理学研究证实黄精的药理学作用广泛,但是其功效成分不清,作用机制不明的现状制约其应用。因此,本研究结合生物信息学与药物网络分析的方法,探讨黄精治疗代谢性相关脂肪性肝病的潜在作用机制。基于TCMSP 数据平台参照OB≥30%,且DL≥0.18 标准筛选并获得β-谷甾醇、黄芩素、薯蓣皂苷元等12 种活性成分。进一步分析文献发现活性成分中,β-谷甾醇可在多种肝脏疾病中发挥重要作用,可改善多种因素引起的肝脏损伤[18];黄芩素在抗脂质沉积造成的肝损伤、抗氧化应激等方面具有良好的效果[19];薯蓣皂苷元在抑制胰岛素抵抗、抗氧化、改善糖脂代谢方面具有重要作用[20],提示黄精在防治代谢性相关脂肪性肝病方面的潜在应用价值。为了进一步挖掘黄精在治疗代谢性相关脂肪性肝病的潜质,借助PharmMapper 平台获取黄精12 个活性成分的潜在作用靶点327 个。在GEO 数据库中获得代谢性相关脂肪性肝病测序数据集,通过 WGCNA 分析筛选疾病基因模块并联合GeneCard 疾病数据库确定代谢性相关脂肪性肝病疾病靶点基因。最终,确定黄精活性成分防治代谢性相关脂肪性肝病的靶点基因16 个,并对其进行了GO 及KEGG 通路分析。通过疾病富集分析发现这16 个靶基因涉及脂质蓄积相关疾病、脂肪肝、肝血管病变、肝炎、胆汁淤积等疾病。脂质沉积在肝细胞是代谢性相关脂肪性肝病的主要病理表现,也是代谢性相关脂肪性肝病的标志特征,改善脂质蓄积可以有效治疗代谢性相关脂肪性肝病[21-22]。此外,诸多研究证实胆汁代谢可以调节肝脏内糖代谢、三酰甘油及胆固醇的等与代谢性相关脂肪性肝病相关危险因素水平,其还可以通过促进脂肪组织和肌肉组织的能量消耗,调节机体免疫来发挥改善代谢性相关脂肪性肝病的作用[23]。这充分说明黄精在治疗代谢性相关脂肪性肝病的潜质。
通过GO 富集分析发现,黄精活性成分治疗代谢性相关脂肪性肝病潜在靶点基因参与调控代谢性相关脂肪性肝病、胰岛素抵抗、血脂和动脉粥样硬化、PPAR 信号通路等通路,参与对细胞内受体信号通路–胆固醇储存负调控、小分子代谢过程的正调节、肌细胞增殖、胆固醇储存的负调节等BP,发挥核受体活性、配体活化、转录因子活性、羧酸结合、类固醇结合、一元羧酸结合、RNA 聚合酶II特异性DNA 结合转录、核类固醇受体活性等MF。相关靶点主要分布在小窝、分泌颗粒腔、胞质囊泡管腔、囊泡腔、溶酶体腔等CC。
通过Cytoscape 3.8.2 软件中cytoHubba 插件的NCC 算法筛选黄精活性成分治疗代谢性相关脂肪性肝病的核心靶点HSP90AA1、PPARA、NOS3、PTPN1、HMOX1。HSP90 是热休克蛋白家族中经典的诱导性应激蛋白,具有广泛的细胞保护作用,HSP90 可以通过激活PPARγ 发挥防治代谢性相关脂肪性肝病的作用[24]。研究表明,PPARα 高表达于肝脏,与过氧化物酶体增殖物反应元件结合后可改善胰岛素抵抗及高脂血症等代谢性相关脂肪性肝病相关疾病,发挥控制代谢性相关脂肪性肝病的发生[25]。研究发现,当细胞内NOS3 表达及一氧化氮(NO)合成受抑制时,给予低剂量NO 供体可促进肝细胞增殖,减少肝细胞内脂肪堆积,并调节肝脏中的脂质和葡萄糖的稳态,提示提高细胞NO 生物利用度对防治代谢性相关脂肪性肝病具有一定的意义[26]。HMOX1 基因可通过多环节、多途径调控核因子-κB(NF-κB)信号通路的活化,抑制细胞间黏附分子-1(ICAM-1)及血小板衍生生长因子(PDGF)等促炎、促纤维化细胞因子表达,阻止或延缓非酒精性脂肪性肝纤维化的发生与进展[27-28]。
综上所述,黄精通过β-谷甾醇、黄芩素、薯蓣皂苷元等12 种活性成分调节HSP90AA1、PPARA、NOS3、PTPN1、HMOX1 等18 个核心靶点,调控代谢性相关脂肪性肝病、胰岛素抵抗、血脂和动脉粥样硬化、PPAR 等通路发挥治疗代谢性相关脂肪性肝病的作用,且在治疗代谢性相关脂肪性肝病中具有多靶点、多成分、协同作用的特点。
利益冲突所有作者均声明不存在利益冲突

