基于多准则决策模型的鸡骨草胶囊临床综合评价
刘 峘,黎元元,谢雁鸣,崔 鑫
基于多准则决策模型的鸡骨草胶囊临床综合评价
刘 峘,黎元元,谢雁鸣*,崔 鑫
中国中医科学院 中医临床基础医学研究所,北京 100700
对鸡骨草胶囊治疗乙型肝炎、胆囊炎(肝胆湿热证)的临床价值进行综合评价,明确临床精准定位。全面系统检索和收集鸡骨草胶囊研究文献和信息,定性研究与定量研究方法相结合,对药品安全性、有效性、经济性、创新性、适宜性、可及性、中医药特色的证据及质量进行评价,利用多准则层决策分析模型及中成药临床证据和价值评估软件,综合评价其临床价值。多源安全性证据表明,鸡骨草胶囊不良反应(adverse drug reaction,ADR)主要累及胃肠道,ADR发生率约为0.001 4%,安全性评为A级。随机对照试验及其Meta分析表明,鸡骨草胶囊联合恩替卡韦片治疗慢性乙型肝炎能够提高患者血清乙型肝炎e抗原(hepatitis B e antigen,HBeAg)转阴率,降低乙肝病毒DNA、谷丙转氨酶、谷草转氨酶、总胆红素水平;治疗胆囊炎可改善临床症状和体征、胆囊壁及收缩功能;有效性评为B级。预算影响分析表明,鸡骨草胶囊纳入医保报销范围,能够减轻医保基金的支出压力,减少患者经济负担,有利于患者的规范治疗以及基金的可持续发展,经济性评为B级。对肝胆湿热证肝胆同治,具有保肝降酶、抗炎镇痛、退黄疸、抗肝纤维化等功效,适用于急性、慢性肝炎的早期和中期,胆囊炎的轻、中症,尤其适用于肝炎合并胆囊炎者,具有临床创新性,有良好的服务创新性和产业创新性,获得8项国家发明专利;创新性评为B级。鸡骨草胶囊便于供应、储运、配制及给药,药品特性与用法适宜个体化治疗,适宜性评为B级。日治疗费用占城镇/农村居民人均可支配日收入的1.21%/3.22%,可负担性良好;全国28个省市在售,涵盖16 292家终端,可获得性良好;可及性评为A级。采用广西特色药材毛鸡骨草等10种中药组方,临床应用近50年,肝胆同治,异病同治,体现了中医药特色。基于现有研究,鸡骨草胶囊临床综合评价为B级,中医药特色+。鸡骨草胶囊临床价值较好,建议按程序有条件转化为基本临床用药管理的相关政策结果。
鸡骨草胶囊;临床综合评价;多准则层决策模型;上市后评价;循证医学;卫生技术评估
乙型肝炎病毒(hepatitis B virus,HBV)感染是全球性重大感染性疾病,患病率从低于2%至8%以上,慢性乙型肝炎(chronic hepatitis B,CHB)的治疗是一个世界性的医学难题。全世界约有3亿人感染HBV,中国约占40%,防治乙型病毒性肝炎是中国健康与传染病防治中的首要问题之一[1-2]。近年来,随着饮食结构的改变,急、慢性胆囊炎的患者也逐渐增多。研究表明,乙型肝炎病毒感染并发胆囊炎的发病率为47%,有肝病基础的患者胆囊炎发病率明显增高[3]。肝胆湿热证是慢性乙型肝炎、慢性胆囊炎的主要证候之一[4-5]。
鸡骨草胶囊(国药准字Z45021655)功能为舒肝利胆、清热解毒,临床用于急、慢性肝炎和胆囊炎属肝胆湿热证者取得良好的疗效[6-8]。该药由毛鸡骨草、三七、人工牛黄、猪胆汁、牛至、白芍、大枣、栀子、茵陈、枸杞子制成,含有相思子碱、栀子苷、绿原酸、芍药苷、胆酸、猪去氧胆酸、人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1等成分[8],主要具有保肝、抗炎、利胆、镇痛和抗肝纤维化等药理作用[8-11]。鸡骨草胶囊执行标准为国家药品标准WS3-3420-98-2011和国药典中发[2012]99号,收载于卫生部颁《药品标准中药成方制剂(第十八册)》[12]。企业内控标准中水分、重量差异项均严于国家标准。工艺规程执行标准为《中国药典》2020年版,并已建立了从原料(药材)、辅料、中间体一系列的全过程质量控制体系。自取得批准文号以来,未出现过产品质量不合格的情况,每年至少开展一批产品的留样考察,均符合质量标准的各项要求。近5年无国家质量抽检不合格,市场抽检及药监日常监督抽检合格率100%。制药企业2019年通过新版GMP再认证,以及澳大利亚TAG的再认证。鸡骨草胶囊曾荣获国家医药管理总局优质产品奖、“国家优质产品”银奖等荣誉,是广西名牌产品。该药自1981年以来,对毛鸡骨草[13]规范化种植、药品品质提升及质量控制技术研究、药效物质基础及创新药物研究等进行了系列上市后研究,但随着同类药物增多,该药的临床价值和优势日趋模糊。为明确鸡骨草胶囊治疗乙型肝炎、胆囊炎(肝胆湿热证)的临床价值以及优势特色,本研究对该药进行临床综合评价研究。
1 资料与方法
1.1 资料来源
计算机检索鸡骨草胶囊相关文献、信息,通过全面、系统地收集证据、信息构建证据体。资料来源包括中外医学文献、药品说明书、政府网站、专业网站、企业网站及公共网络资源以及灰色文献。检索的医学文献数据库包括:中国知网数据库(CNKI)、万方数据库(Wanfang)、中国生物医学文献服务系统(SinoMed)、维普中文科技期刊数据库(VIP)、PubMed、Embase、Cochrane Library。采用主题检索,中文检索词为“鸡骨草胶囊”,英文检索词为“JiGuCaoJiaoNang(YuLin)”和“JiGuCao capsule”,检索时限自建库至2021年4月。对检索文献、信息进行阅读、分类、系统梳理。同时,采用问卷调查、专家访谈、专家会议等研究方法,进一步对研究资料进行补充、研判、共识。
1.2 评价方法
遵照国家卫健委发布的《药品临床综合评价管理指南(2021版试行)》[14]和《中成药临床综合评价技术规范》及报告规范[15-16],主要评价内容包括:安全性、有效性、经济性、创新性、适宜性、可及性以及中医药特色,再运用多准则决策模型(multi criteria decision analysis,MCDA)进行临床价值综合评价。通过对全国范围内135名权威专家开展专家问卷、赋权而建立临床综合评价指标体系,专家学科领域包括卫生政策及方法学、循证医学、药物经济学、中医临床各科、临床药学、数理统计以及中医基础理论等,在此基础上采用层次分析法确定各级指标权重,并经过5轮专家论证达成共识。依据该模型研制了中成药临床证据和价值评估软件(CSC 2.0),输入综合评价各指标评分即可计算各维度评分和综合评分,并按照从优到差分为A、B、C、D 4个等级。
文献检索、文献筛选以及证据质量评价采用双人评价、意见不同时由具有高级技术职称的第3名专业人员决策。分别采用Cochrane ROB工具1.0、AMSTAR对随机对照试验(randomized ccontrolled trial,RCT)、系统评价和Meta分析报告的质量进行评价,采用文献严格评价技能方案(critical appraisal skills programme,CASP)对经济性研究质量进行评价,采用证据推荐分级的评估、制订与评价(grading of recommendations assessment,development and evaluation,GRADE)系统对证据质量进行分级[17-19]。最后评价结果和报告内容由内部专家会议进行全面审定,所有评价相关原始记录存档备查,以保障评价过程严谨性和质量可靠性。
2 结果
2.1 安全性
2.1.1 证据概述
(1)安全性信息:鸡骨草胶囊安全性证据来自文献报告、RCT及其Meta分析、国家药品不良反应监测中心自发呈报系统(spontaneous reporting system,SRS)数据以及非临床安全性实验等。1)药品说明书“不良反应”“禁忌”及“注意事项”均为尚不明确,于2020年主动更新,增加了“药品上市许可持有人”信息。按照年销售金额约2700万元、70%药品使用率计,预估每年接受治疗的人数约13万。上市40余年,接受治疗人数约500万。自上市以来,未发现用药差错及事故。从未被国家药品监督管理局不良反应中心通报。2)国家药品不良反应监测中心自发呈报系统数据显示,2018—2020年共收到41例不良反应报告,其中2018年7例,2019年12例,2020年22例;均为非预期一般个案报告,主要累及胃肠道,主要表现为恶心、腹泻、呕吐、头晕、皮疹。3)定期安全性更新报告表。①药物不良反应(adverse drug reaction,ADR)/ 不良事件(adverse drug events,ADE)特点:2015—2020年共收到SRS个案报告66例,均为一般个案报告,主要累及胃肠道,临床表现为恶心、腹泻、呕吐、头晕、皮疹,转归情况为好转或痊愈,无严重不良反应。按照SRS报告例数和近5年销售量估算的ADR发生率为0.001 4%;②影响因素:66例ADR/ADE报告中,男女比例为0.7∶1,年龄均在30~59岁,中年居多,均为怀疑用药,无合并用药,有极个别不合理用药情况,如未按说明书用法、用量服用;③文献检索:未检索到与鸡骨草胶囊潜在风险有关的文献。4)鸡骨草胶囊治疗肝炎系统评价纳入3篇文献,1篇报道未发现明显不良反应,另2个研究均未报告不良反应发生情况。按照AMSTAR的条目对系统评价质量进行评价,该文献研究方法较规范,可信度为“中级”,但由于纳入的RCT数量非常少,只有1篇RCT报告了安全性信息,无法进一步进行Meta分析,安全性需要更多的临床研究以及其他形式的证据支持。
(2)药物警戒与风险管理:根据该药安全性数据、组方药性,主要风险来自胃肠道反应,可能由于药性偏寒凉,容易引起虚寒体质等患者出现不良反应,应予警戒。药品生产企业成立了药物警戒部和药品安全委员会,设置了专人专岗,建立了完善的质量管理体系,以及涵盖原材料采购相关内容的风险管理文件,建立了不良反应报告和监测管理制度及药物警戒年度报告制度,每年撰写并提交年度报告,每5年上报《定期安全性更新报告》,定期进行安全性文献检索,以及按要求开展说明书更新工作。药品生产企业近3年无因产品不合格而被召回的情况,未有被药品监管机构通报的情况,未有被药品监管机构约谈的情况,无其他品种召回、通报、约谈的相关情况发生。按照相关要求开展风险识别与评估,对已识别药品风险(恶心、呕吐、腹泻、皮疹等)及时撰写风险最小化计划,并及时向公众传达药品安全性新信息。
(3)非临床安全性信息:急性毒性实验显示,小鼠ig给予鸡骨草胶囊的最大耐受量为220.9 g/kg(折合生药计),相当于临床剂量的381倍。长期毒性实验显示,以相当于临床剂量的10、50倍剂量的鸡骨草胶囊ig给予大鼠连续24周,结果表明按临床剂量使用鸡骨草胶囊是安全的。
2.1.2 证据评价 从证据的充分性和已知风险2个方面评价。根据分级原则和标准,鸡骨草胶囊安全性证据充分性评为B级,表明鸡骨草胶囊安全性证据比较充分,安全性结论较明确。基于销售数据估算的ADR发生率为0.001 4%,无严重ADR。已知风险评为A级。经CSC软件计算,鸡骨草胶囊安全性标准化效用分数为0.75,评为A级,即基于现有研究,认为风险可控、安全性好。
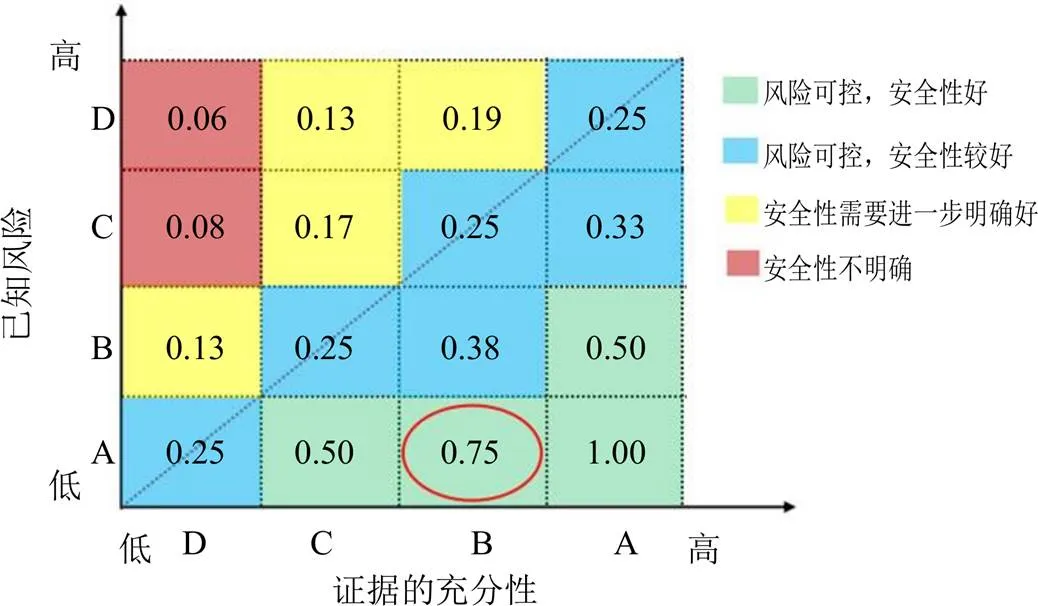
斜向红色虚线为安全性证据与风险的平衡线,平衡线穿过的虚线格表示证据与风险平衡;平衡线下方的虚线格表示在目前已知的风险下研究较为充分
2.2 有效性
2.2.1 证据概述
(1)上市前临床研究:鸡骨草胶囊Ⅲ期临床试验按照《中药新药治疗病毒性肝炎的临床研究指导原则》和《中药新药治疗胆囊炎的临床研究指导原则》共完成360例治疗观察,其中急、慢性肝炎共240例,急性肝炎疗效标准“有效”为主要证候群消失;肝脾肿大消失或回缩,肝区无明显压痛和叩痛;肝功能检查正常;见症积分减少70%以上。慢性肝炎疗效标准“有效”为主要证候群消失或基本消失;肝脾肿大稳定不变,且无明显压痛及叩痛;肝功能检查正常或原值下降50%以上;见症积分减少70%以上。未达有效标准为“无效”。结果急性甲型肝炎60例,有效率为100%;急性乙型肝炎60例,有效率为100%;慢性迁延性肝炎60例,有效率85%;慢性活动性肝炎60例,有效率为70%。急性肝炎总有效率为100%,慢性肝炎总有效率为77.5%。鸡骨草胶囊治疗急慢性胆囊炎120例,疗效判定标准“痊愈”为症状、体征完全消失或基本消失,体温、血象恢复正常,B超影像正常,见证积分减少91%以上;“显效”为症状、体征完全消失或基本消失,体温、血象恢复正常,B超影像明显改善,见证积分减少61%~90%;“有效”为症状、体征明显改善,体温、血象基本正常,B超影像有改善,见证积分减少31%~60%;“无效”为达不到上述标准者。急性胆囊炎疗效标准无体温、血象要求。结果急性胆囊炎60例,显效率、有效率分别为11.7%、63.3%,总有效率为75%;慢性胆囊炎60例,显效率、有效率分别为13.3%、56.7%,总有效率为70%。360例患者均进行了血尿便常规检查和心肝肾功能检查,均未发现明显不良反应和毒副作用。
(2)上市后临床研究:鸡骨草胶囊治疗乙型肝炎的系统评价纳入3篇文献,包括273例患者(试验组137例,对照组136例),Meta分析纳入2篇[6,20],2组研究间的同质性较好(=0.95,2=0),采用固定效应模型合并分析。试验组采用鸡骨草胶囊联合恩替卡韦片,对照组单用恩替卡韦片。治疗48周后,试验组血清乙型肝炎e抗原(hepatitis B e antigen,HBeAg)转阴率优于对照组(RR=1.97,95% CI [1.31,2.95],=0.001),试验组的乙肝病毒(hepatitis B virus,HBV)DNA水平低于对照组(MD=−0.98,95% CI [−1.12,−0.83],<0.000 01),试验组丙氨酸氨基转移酶(alanine aminotransferase,ALT)水平(MD=−16.25,95% CI [−18.31,−14.20],<0.000 01)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)水平(MD=−9.56,95% CI [−10.99,−8.13],<0.000 01)、总胆红素(total bilirubin,TBiL)水平(MD=−10.50,95% CI [−11.89,−9.11],<0.000 01)均低于对照组,鸡骨草胶囊治疗慢性乙型肝炎具有良好的效果。1篇治疗急性肝炎的文献报道了治疗显效率[21],干预措施为鸡骨草胶囊+对症治疗对症治疗,分析结果显示二者疗效没有统计学差异(MD=1.62,95% CI [0.80,3.27],=0.18)。鸡骨草胶囊治疗慢性胆囊炎,可以改善胆囊炎患者临床症状体征、改善B超检查胆囊壁及收缩功能[22-23]。
2.2.2 证据评价 从证据质量和证据价值2个方面进行评价,证据质量评价按照GRADE证据体系,鸡骨草胶囊治疗慢性乙型肝炎有效性证据评为C级;鸡骨草胶囊治疗慢性胆囊炎有效性证据评为D级。证据价值按照PICOS原则衡量,即participants(研究对象)、intervention(干预)、control(对照)、outcome(结局)、study design(研究设计),先计算证据价值的效用分数,再按照等频离散化原则分级。有效性证据综合以证据价值为横坐标,证据质量为纵坐标,构建象限系,如图2所示。经CSC软件计算,有效性标准化效用分数为0.57,评为B级。
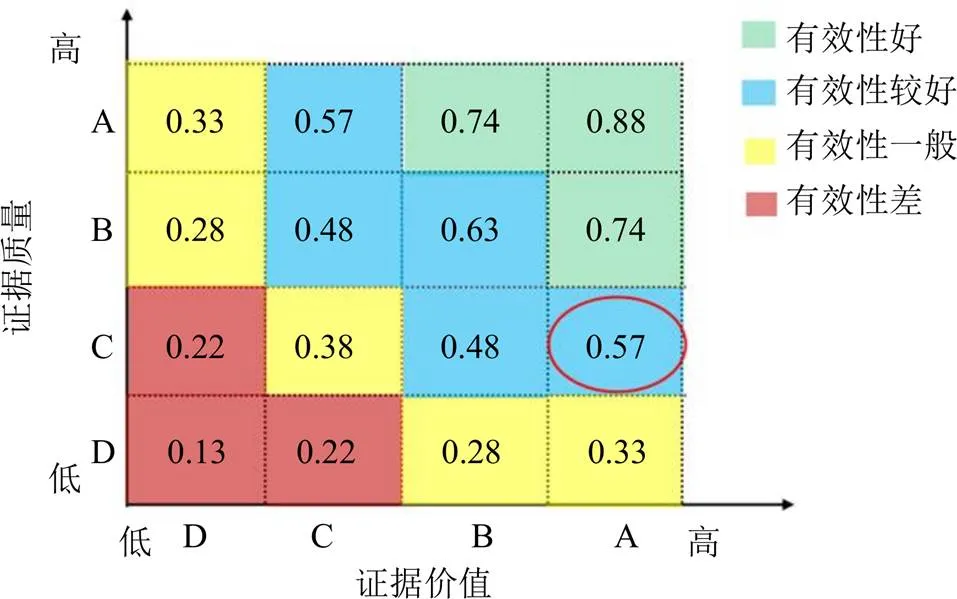
图2 有效性证据价值-质量矩阵
2.3 经济性
2.3.1 证据概述
(1)治疗慢性乙型肝炎预算影响分析:由中山大学公共卫生学院所做鸡骨草胶囊预算影响分析报告显示,以全国为例,对于城镇职工医疗保险和城乡居民医保的总参保人,假设鸡骨草胶囊进入医保目录后,医保基金关于慢性乙型肝炎治疗中成药费用的总支出在2021—2023年可分别减少56.42万元、304.73万元和639.12万元。对于城镇职工医保参保人而言,2021—2023年医保基金支出可减少13.72万元、74.08万元和155.38万元;对于城乡居民医保的参保人而言,3年基金支出可分别减少42.70万元、230.65万元和483.74万元。而我国乙型肝炎患者每年需支付药物费用约2.25万元/人,按照当年我国城市平均收入2.88万元/人计算,则乙型肝炎患者需要支付的药费已超过个人收入的40%,属于灾难性医疗支出。《慢性乙型肝炎防治指南(2019年版)》指出,我国慢性乙型肝炎患者约2000万~3000万例,绝大多数乙型肝炎患者需要进行长期、规范的药物治疗缓解和控制病情。因此,将具有临床疗效的鸡骨草胶囊纳入医保报销范围,可以减轻医保基金的支出压力,同时减轻患者的经济负担,对加强慢性乙型肝炎患者的规范治疗以及医保基金的可持续发展具有重大意义。研究结论认为,考虑到我国慢性乙型肝炎患者人数的增加、慢性乙型肝炎临床治疗中对中医药的需求和医疗费用的上涨,若将鸡骨草胶囊纳入医保药品目录不仅可以增加医生和患者对治疗慢性乙型肝炎中成药的选择,也减少了医保基金的支出。
(2)治疗胆囊炎的预算影响分析:中山大学药学院医药经济研究所通过建立预算影响模型(研究时限2021—2023年),评价鸡骨草胶囊用于治疗慢性胆囊炎对医保基金可能带来的预算影响。如果鸡骨草胶囊纳入医保乙类药品目录,2021—2023年使用中成药治疗慢性胆囊炎的药品总费用分别为19 139.51万元、19 251.31万元和19 501.67万元,其中医保支付金额分别为6 603.13万元、6 641.70万元和6 728.08万元;鸡骨草胶囊的药费分别为1 776.49万元、2 231.72万元和2 804.83万元。综合考虑,2021—2023年对医保基金的净增长分别为452.14万元、504.19万元和584.43万元。预算影响分摊到每个参保人分别为增加0.05、0.05和0.05元。研究结论认为,基于研究结果整体来说,报销鸡骨草胶囊用于治疗慢性胆囊炎后对医保总预算的影响有限,且每年支出增加的额度较小;分摊到每个参保人,增加的医保筹资压力和患者负担较小。
2.3.2 证据评价 通过综合证据质量和价值评价来获得。经济性证据的质量通过CASP清单来进行评价。根据评分标准,计算CASP清单12条目得分的均值,结果鸡骨草胶囊治疗慢性乙型肝炎经济性证据质量评分为0.67。经济性价值评价主要看研究结果中是否能够提供成本节约证据,节约社会总成本,减少医疗卫生资源消耗,根据研究报告的经济学结果打分,分数判定区间为0~1分。鸡骨草胶囊经济性价值评分为0.75。
综合经济学证据质量评价和经济性价值评价,通过对二者得分加权求和,获得经济性标准化效用分数。经CSC软件计算,经济性标准化效用分数为0.73,评为B级,表示经济性结果较好,能够根据现有证据说明相对经济性;证据报告比较充分、结果较明确。
2.4 创新性
2.4.1 创新性概述
(1)临床创新性:鸡骨草胶囊功能为疏肝利胆、清热解毒。针对急、慢性肝炎、胆囊炎的核心病机和主要证候——肝胆湿热进行治疗[24-25],肝胆同治,活血抗纤维化,具有保肝降酶、抗炎镇痛、退黄疸、抗肝纤维化等功效,适用于急、慢性肝炎的早期和中期阶段和胆囊炎的轻、中症,特别适用于肝炎合并胆囊炎的患者。对改善症状、体征和生化检测方面均有疗效,作用全面。方中君药毛鸡骨草是广西特色药材,也是主要创汇产品,其药效成分为皂苷、黄酮、生物碱类物质。其中,鸡骨草皂苷有一定的保肝、护肝作用,黄酮类化合物则具有扩血管、调血脂、抗氧化、抗凝血、清除自由基、治疗白血病、抗炎、镇痛、抗肿瘤、抗辐射等作用且不良反应较少。药理学研究证明其具有保肝作用、抗病毒和抗菌、抗炎、免疫调节、调血脂、清除自由基、肠道平滑肌调节作用。鸡骨草中的相思子碱、相思子皂醇、大豆甾醇等关键成分可通过干预雌激素受体α基因、基质金属蛋白酶9、信号传导与转录激活因子3、JUN等靶标,调节乙型肝炎信号通路、缺氧诱导因子1信号通路及内分泌抗性等通路发挥治疗乙型肝炎作用[26]。
与同类药品比较,鸡骨草胶囊的优势体现在:①消炎、利胆、退黄、降酶、抗纤维化,作用全面,因此适用于肝炎、胆囊炎,且急性期和慢性都可以应用;②肝胆同治,既可治肝又可治胆,利胆有利于肝病好转,尤其适用于合并胆囊炎的患者;③日服用费用相对较低,具有较好的经济性。从病机及主要证候来说,鸡骨草胶囊针对急、慢性肝炎和胆囊炎主要病机肝胆湿热证,作为中成药与个体化辨证论治方剂在精准治疗方面还存在一定差距,但普适性方面有优势,临床可以根据病情需要选择应用或联合用药。
(2)企业服务体系创新性:制药企业广西玉林制药集团有限责任公司始建于1956年,是国家商务部首批认定的“中华老字号”企业,专注中成药的研发与生产和销售,通过不断优化企业管理体系,保证企业的创新性。①创建名优产品中药鸡骨草胶囊主要原料药材毛鸡骨草基地,带动2300多农户种植毛鸡骨草,采取公司+农户的方式,从播种、管理、收购“一条龙”服务,保证药材供应。②创建覆盖全国的销售网络,与国内头部物流企业订立运输协议,统一配送,保证药品质量。公司还具有自营进出口权,远销30多个国家和地区。③药品均贴有电子监管码,一盒(最小包装)一码,可以跟踪每盒药品的生产、销售、流通情况。④保障药品有效:对所有原辅料、中间产品及成品均制定了质量标准及检验程序,严控原辅料的准入及产品放行。⑤实施药品生产质量管理规范。⑥建立中药材经营子公司,保障原材料供应,同时降低采购成本。
(3)产业创新性:始终坚持以市场为导向,项目为载体,加强产学研的联合。从药材资源管理、通过自动化的生产设备实现生产管理智能化和信息化,积极采用新工艺、新技术、新材料、新设备促进绿色生产,采用指纹图谱检测严格控制产品质量[27],创建广西现代中药工程技术研究中心以及院士工作站,获得国家发明专利8项,通过精干高效的生产管理模式,提供多元化购买渠道,提高药品可及性。
2.4.2 创新性评价 将临床创新性、企业服务体系创新性、产业创新性评分的3个一级指标以及保障供应的措施创新、产能及其可扩展性、基层销售渠道覆盖措施、ADR反馈渠道创新、生产销售流通成本控制措施创新、制药工业创新、生产工艺创新、科技研发创新等18个二级指标得分带入CSC软件计算,创新性等级评为B级。
2.5 适宜性
2.5.1 证据概述 鸡骨草胶囊适宜性的证据通过问卷调查获得,采用问卷星APP实施,调查具有鸡骨草胶囊使用经验的医护人员和患者真实的用药体验。调查范围涉及全国21个省市自治区,在地域、医院等级等方面具有代表性。医护版共调查具有药品使用经验的医护人员123人,患者版共调查197名鸡骨草胶囊的使用者。统计分析结果显示,鸡骨草胶囊在配制及给药方便度、不良反应救治难易、个体化治疗、药品特性与用法、供应和储运方便度方面评价为适宜性较好;在医护版政策与宣传促销,患者版的安全性和经济性影响、药品信息影响方面适宜性一般。总体评价适宜性比较好。
2.5.2 证据评价 根据问卷调查结果,对等级资料赋分后,计算各领域的平均分作为各领域得分。医护版5个项目(配制及给药难易、不良反应救治难易、个体化方案、技术与管理要求、政策与宣传要求)及患者版4个项目(药品特性与用法是否方便使用、安全性和经济性是否影响用药、药品信息的影响、供应与贮运是否方便用药)的加权平均分作为适宜性得分。经CSC软件计算,适宜性评分为0.72分,评为B级,表示适宜性较好,基本满足临床用药需求。
2.6 可及性
2.6.1 证据概述
(1)适应证疗程费用:治疗急性肝炎/慢性胆囊炎(28 d疗程)188.2元,治疗慢性肝炎(90 d疗程)604.8元,治疗急性胆囊炎(10 d疗程)67.2元。不需要特殊条件储存或运输;使用时不需要对患者采取特别的药物监测或相关生理指标检测,不会增加医疗成本。
(2)可负担性:鸡骨草胶囊限定日费用(defined daily dose consumption,DDDc)为2.48元/d。根据国家统计局数据,2020年全国城镇和农村居民人均可支配收入中位数分别为40 378元和15 204元[28]。鸡骨草胶囊的疗程费用为治疗急性肝炎/慢性胆囊炎188.2元,国家乙类医保产品城镇报销80%、农村报销70%。应用鸡骨草胶囊治疗,城镇/农村居民治疗费用占比为0.09%/0.37%,每天治疗费用占城镇/农村居民人均可支配日收入的1.21%/3.22%,具有良好的可负担性。
(3)可获得性:鸡骨草胶囊销往全国28个省/自治区/直辖市,16 292家医疗机构。主要在药店销售,并在等级医院配备:三级医院配备比例0.32%,二级医院0.80%,一级医院1.68%。剂型和运输、贮藏要求适合基层临床应用。
鸡骨草胶囊产能约为3.6亿粒/年。方中人工牛黄为人工合成,猪胆汁为养殖业生产,其他均为种植品种,分布广泛,药材资源极其丰富。企业建立了毛鸡骨草、莪术、郁金、栀子、土茯苓等药材规范化种植基地666.67公顷,为持续生产供应临床使用提供了保障。不存在短缺或季节性供应,不会因产地限制而影响及时获得,具有良好的可获得性。
2.6.2 证据评价 综合药品价格水平B级、可负担性A级和可获得性B级,代入CSC计算,鸡骨草胶囊可及性分数为0.69,评为A级,可及性好。
2.7 中医药特色
2.7.1 理论特色 中医学认为病毒性肝炎由湿热疫毒之邪内侵,当人体正气不足无力抗邪时发病,其病机特点是热疫毒隐伏血分,引发湿热蕴结,肝胆湿热证为本病常见证候。在慢性肝炎的治疗中运用利胆法具有重要的理论和实践意义。肝脏与胆腑生理密切相关,病理交互影响,故慢性肝炎多为肝胆同病。胆腑不清,肝无宁日,只有重视疏利胆腑,肝胆同治,方可达到稳定肝功能、缩短慢性肝炎病程的目的。利胆可调整胆腑功能,改善和消除肝病及胆所致胆腑瘀滞,缓解肝脏因胆汁排泄不畅所致的负担和压力,使胆气通畅,胆汁得以注精于小肠“行津液”“化水谷”。因此,在慢性肝炎治疗上,有黄疸时应利胆,无黄疸时亦应利胆,利胆可以保肝,利胆可以改善消化道症状。
2.7.2 人用经验 鸡骨草胶囊是以中医药理论为指导,在治疗肝炎临床验方的基础上研制开发的。采用广西地道药材毛鸡骨草,疏肝利胆、清热解毒、肝胆同治,适合急性、慢性肝炎和胆囊炎肝胆湿热证的病机,疗效显著,具有鲜明的中医药特色。列为《国家基本医疗保险、工伤保险和生育保险药品目录》(2020版)的清肝胆湿热剂乙类品种,《慢性乙型肝炎中医诊疗指南(2018年版)》推荐其治疗肝胆湿热型慢性乙型肝炎,被中华中医药学会《胆囊炎中医诊疗共识意见(2017年)》列入胆囊炎的常用中成药[4,29-30]。
2.7.3 中医药特色维度评价 中医药特色主要考察中医药理论内涵(证候、配伍、民族药等)和人用经验(经典名方、大样本临床研究),评价结果分为0~+++4个等级,鸡骨草胶囊评为中医药特色+,有中医药特色。
2.8 临床价值综合评价
将以上“6+1”维度评价结果通过CSC V2.0软件代入MCDA模型分析,临床综合价值为0.71分,为B级。鸡骨草胶囊治疗乙型肝炎、慢性胆囊炎(肝胆湿热证)临床价值较好,有中医药特色。临床价值综合评价雷达图见图3。
3 讨论
药品临床综合评价是药品供应保障决策的重要技术工具,其标准化、规范化、科学化、同质化可助力药事服务质量的提升,保障临床基本用药的供应与规范使用,控制不合理药品的费用支出,更好地满足人民群众用药的需求和国家药物政策决策的需要[31]。评价过程包括证据收集和综合分析决策2个阶段,证据来源于文献分析、问卷调研、真实世界数据分析等,综合分析决策可采用德尔菲法、层次分析法、多准则决策分析法等方法。药品综合评价的维度方面,《中国药品综合评价指南参考大纲》中主要评价安全性、有效性、药品质量、药品原料、药品工艺、药品包材、药品顺应性、药物经济性、药物临床价值9项内容;第2版则修订为安全性、有效性、体内药学特性、药品质量、药品顺应性、临床药物经济性、药物临床价值、药品信息服务8项;《药品临床综合评价管理指南(2021年版试行)》进一步精简为安全性、有效性、经济性、创新性、适宜性、可及性。在此框架下,《中成药临床综合评价技术规范》采用“6+1”模式,增加了“中医药特色”维度的评价。不同机构也提出了更多的规范和建议[32]。综合评价以价值为基础的卫生决策不仅取决于经济学评价,还取决于政治、伦理、效率、公平、质量、安全等多种其他因素,这就需要采用多准则决策分析。MCDA的理论与方法学已被国内的高校和科研机构应用于药品招标采购、基本药物目录和医疗保险药品报销目录的药品遴选,以及临床治疗方法的评价和医疗保险方案的选择[33]。因此,基于不同的决策需求,综合评价的维度、权重和结果会有所不同。目前,药品安全性和有效性的研究较多,经济性评价研究逐渐增加,而综合6个维度进行药品综合评价的相关研究仍不多。研究方法以系统综述、Meta分析、临床观察性研究和回顾性研究较为多见[34]。
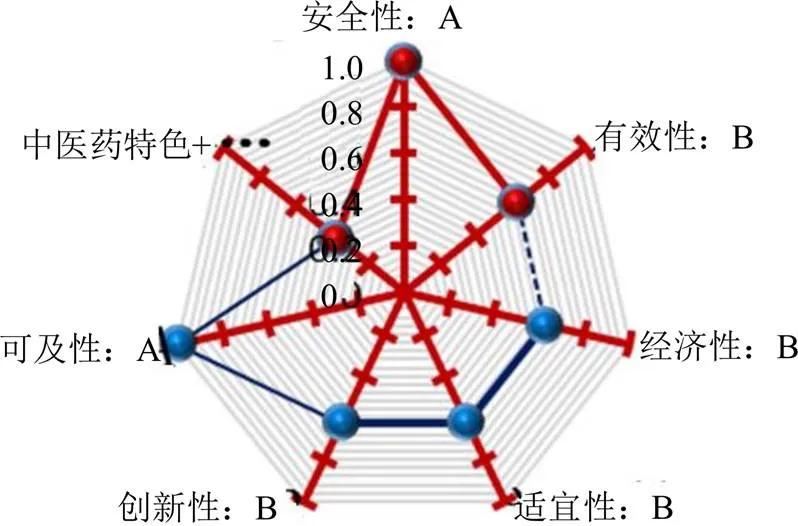
安全性、有效性、中医药特色是中成药内部属性,以红色表示;经济性、创新性、可及性、适宜性是外部属性,以蓝色表示
本研究采用《中成药临床综合评价技术规范》评价框架对鸡骨草胶囊治疗慢性乙型肝炎及胆囊炎的临床价值进行综合评价,该评价体系经全国百余位多学科专家赋权、论证,融合中医药特色,通过“6+1”维度进行综合评价[35]。评价结果显示,鸡骨草胶囊具有良好的临床有效性、经济性、适宜性和创新性,安全性和可及性优异,有中医药特色。本研究结果基于循证证据,随着药品开发研究的深入以及证据的不断更新,对药品的评价将产生新的认识。通过本次评价,梳理了鸡骨草胶囊的研究成果,对该药的临床价值和精准定位有了更清晰的认知,同时提示研究者和药品生产企业今后应进一步提升有效性证据级别,开展大样本、多中心的真实世界研究,加强中医药特色的挖掘和整理,通过疗效机制研究提升临床创新性、增强药品科学内涵。
4 结论
鸡骨草胶囊临床价值较好,建议按程序有条件转化为基本临床用药管理的相关政策结果。
利益冲突 所有作者均声明不存在利益冲突
[1] 张星鑫, 郭津生. 慢性乙型肝炎的现有认识及治疗进展 [J]. 肝脏, 2021, 26(3): 327-330.
[2] 金奇. 2008—2018年中国大陆乙肝发病率与患病率研究的荟萃分析 [D]. 天津: 天津医科大学, 2020.
[3] 张声生, 赵文霞. 胆囊炎中医诊疗专家共识意见(2017) [J]. 中国中西医结合消化杂志, 2017, 25(4): 241-246.
[4] 中华中医药学会肝胆病专业委员会, 中国民族医药学会肝病专业委员会. 慢性乙型肝炎中医诊疗指南(2018年版) [J]. 中西医结合肝病杂志, 2019, 29(1): 97-102.
[5] 韩璐, 赵国强, 张楠, 等. 胆囊炎的中医证型和方药规律分析 [J]. 中国中医药现代远程教育, 2017, 15(8): 45-47.
[6] 雷清瑶. 探讨鸡骨草胶囊联合抗病毒治疗慢性乙型肝炎的疗效及对肝功能、血清TGF-β1、ECM水平的影响 [J]. 现代诊断与治疗, 2018, 29(13): 2036-2038.
[7] 睢凤英, 蒋小红, 江肖明, 等. 鸡骨草胶囊治疗急性肝炎的临床疗效观察 [J]. 右江医学, 2002, 30(3): 247-248.
[8] 张孟丽, 吴芳芳, 谭栀恩, 等. 鸡骨草胶囊及其临床应用的研究进展 [J]. 广西医学, 2021, 43(24): 2981-2984.
[9] 李庭树, 黄锁义. 鸡骨草的化学成分、药理作用及临床应用研究进展 [J]. 中国实验方剂学杂志, 2019, 25(10): 226-234.
[10] 赵平, 叶志文, 何丹璇, 等. 鸡骨草胶囊对大鼠肝纤维化的保护作用研究 [J]. 中国实验方剂学杂志, 2009, 15(10): 99-101.
[11] 吴茜玉. 鸡骨草胶囊对大鼠免疫性肝纤维化的治疗作用 [J]. 中国医药指南, 2010, 8(26): 46-48.
[12] 中华人民共和国卫生部药品标准中药成方制剂(第十八册) [S]. 1998: 150-151.
[13] 广西壮族自治区壮药质量标准(第一卷) [S]. 2008: 68.
[14] 国家卫生健康委药政司. 药品临床综合评价管理指南(2021年版试行) [EB/OL]. (2021-07-28) [2021-08-30]. http://www.nhc.gov.cn/cms-search/xxgk/getManuscriptXxgk.htm? id=532e20800a47415d84adf3797b0f4869.
[15] 张强, 王志飞, 谢雁鸣, 等. 中成药临床综合评价技术规范 [J]. 世界中医药, 2021, 16(22): 3394-3397.
[16] 张强, 王志飞, 谢雁鸣, 等. 中成药临床综合评价报告规范 [J]. 中国中药杂志, 2021, 46(23): 6062-6067.
[17] 葛龙, 潘蓓, 潘佳雪, 等. 解读AMSTAR-2: 基于随机和(或) 非随机对照试验系统评价的质量评价工具 [J]. 中国药物评价, 2017, 34(5): 334-338.
[18] 马思思. 中医辨证论治复杂干预的理论模型构建及疗效要素的探索分析 [D]. 北京: 北京中医药大学, 2020.
[19] 黄笛, 黄瑞秀, 郭晨煜, 等. 临床实践指南制定方法—证据分级与推荐强度 [J]. 中国循证心血管医学杂志, 2018, 10(7): 769-776.
[20] 覃婕, 黄万金, 李东发. 鸡骨草胶囊联合恩替卡韦治疗慢性乙型肝炎24例 [J]. 中医药导报, 2013, 19(8): 116-117.
[21] 睢凤英, 蒋小红, 江肖明, 等. 鸡骨草胶囊治疗急性肝炎的临床疗效观察 [J]. 右江医学, 2002, 30(3): 247-248.
[22] 林新, 张琦, 郝改琳. 鸡骨草胶囊治疗慢性胆囊炎30例 [J]. 陕西中医, 2007, 28(1): 24-25.
[23] 董小平, 张弛, 张鸽. 中西医结合治疗慢性胆囊炎45例 [J]. 山西中医, 2010, 26(4): 23.
[24] 车念聪, 钱英. 从1056例乙肝治疗看中医辨证论治 [J]. 北京中医, 1995, 14(5): 50-52.
[25] 刘志勇. 肝病须重利胆 [J]. 山东中医杂志, 1998, 17(2): 53-54.
[26] 李太平, 吴芳芳, 孙晖, 等. 基于网络药理学和分子对接探究壮药鸡骨草治疗乙型肝炎的作用机制 [J]. 现代药物与临床, 2022, 37(1): 33-41.
[27] 何艳梅, 吴芳芳, 张孟丽, 等. 基于HPLC指纹图谱及多成分含量测定的鸡骨草胶囊质量控制 [J]. 中药材, 2023(3): 687-692.
[28] 国家统计局. 2020年国民经济和社会发展统计公报. [EB/OL]. [2021-02-28]. https://www.gov.cn/xinwen/ 2021-02/28/content_5589283.htm.
[29] 中华医学会外科学分会胆道外科学组. 急性胆道系统感染的诊断和治疗指南(2021版) [J]. 中华外科杂志, 2021, 59(6): 422-429.
[30] 张声生, 赵文霞. 胆囊炎中医诊疗专家共识意见(2017) [J]. 中国中西医结合消化杂志, 2017, 25(4): 241-246.
[31] 董名扬, 王舒, 菅凌燕. 药品临床综合评价方法的应用现状 [J]. 中国药房, 2021, 32(22): 2813-2816.
[32] 张海力, 梁宁, 陈雅馨, 等. 多维度多准则中成药综合评价技术指导原则解读 [J]. 中国循证医学杂志, 2022, 22(7): 762-767.
[33] 胡善联. 多准则决策分析在卫生决策领域中的应用价值 [J]. 中国卫生资源, 2020, 23(4): 325.
[34] 肖秘苏, 张剑萍, 杨全军, 等. 基于CiteSpace的我国药品综合评价研究现状分析 [J]. 中国药房, 2022, 33(8): 911-916.
[35] 雷超, 张强, 王志飞, 等. 复方夏天无片治疗类风湿性关节炎的临床综合评价[J]. 中草药, 2022, 53(21): 6810-6819.
Clinical comprehensive evaluation of Jigucao Capsules based on multi criteria decision analysis
LIU Huan, LI Yuan-yuan, XIE Yan-ming, CUI Xin
Institute of Basic Research in Clinical Medicine, China Academy of Chinese Medical Sciences, Beijing 100700, China
To comprehensively evaluate the clinical value of Jigucao Capsule (鸡骨草胶囊) in the treatment of hepatitis B and cholecystitis (liver and gallbladder dampness and heat syndrome) and clarify the precise clinical positioning.Comprehensively and systematically search and collect the research literature and information of Jigucao Capsule, combine qualitative research with quantitative research methods, evaluate the evidence and quality of the safety, effectiveness, economy, innovation, suitability, accessibility and characteristics of traditional Chinese medicine, and evaluate the clinical value of the medicine by using the multi criteria layer decision analysis model (MCDA) and the Chinese patent medicine clinical evidence and value evaluation software.Multi source safety evidence showed that adverse drug reaction (ADR) of this drug mainly involveed the gastrointestinal tract. The incidence of ADR was about 0.0014%, and the safety rating was A. RCT and Meta-analysis showed that Jigucao Capsule combined with entecavir tablets could improve the negative rate of serum hepatitis B e antigen (HBeAg) and reduce the levels of HBV DNA, alanine aminotransferase (ALT), aspartate aminotransferase (AST), and total bilirubin (TBIL) in patients with chronic hepatitis B; Treatment of cholecystitis can improve clinical symptoms and signs, gallbladder wall and contractile function; The effectiveness was rated as B. The budget impact analysis showed that the drug was included in the scope of medical insurance reimbursement, which can reduce the expenditure pressure of medical insurance fund, reduce the economic burden of patients, and was conducive to the standardized treatment of patients and the sustainable development of the fund. The economic evaluation was B. Aiming at the liver and gallbladder damp heat syndrome, it had the effects of protecting liver and reducing enzymes, anti inflammation and analgesia, reducing jaundice, and anti liver fibrosis. It was suitable for the early and middle stage of acute and chronic hepatitis, and for the mild and moderate symptoms of cholecystitis, especially for the patients with hepatitis and cholecystitis, with clinical innovation; It had service innovation in terms of supply guarantee and capacity expansion; The industrial innovation was better reflected in the enterprise concept, information feedback and communication; It had obtained eight national invention patents; Innovation was rated as B. The suitability of the drug was evaluated as good in terms of convenience of preparation and administration, difficulty in treatment of adverse reactions, individualized treatment, drug characteristics and usage, convenience of supply, storage and transportation, and the suitability was evaluated as B. The daily treatment cost accounts for 1.21%/3.22% of the per capita disposable daily income of urban/rural residents, which was well affordable; It was sold in 28 provinces and cities nationwide, covering 16292 terminals, with good availability; Accessibility was rated as A. It was composed of 10 kinds of traditional Chinese medicines, such as Maojigucao (), which had been used in clinical practice for nearly 50 years. The liver and gallbladder were treated together and different diseases were treated together, reflecting the characteristics of traditional Chinese medicine. Based on the existing research, the comprehensive clinical evaluation was grade B, with characteristic of traditional Chinese medicine +.Jigucao Capsule has good clinical value. It is suggested that it can be converted into relevant policy results of basic clinical medication management according to the procedure.
Jigucao Capsules; clinical comprehensive evaluation; multi-criteria decision analysis (MCDA); post marketing evaluation; evidence based medicine; health technology assessment
R285.64
A
0253 - 2670(2023)16 - 5312 - 09
10.7501/j.issn.0253-2670.2023.16.020
2023-02-20
中国中医科学院科技创新工程重大攻关项目(CI2021A00702);国家重点研发计划“中医药现代化研究”项目(2018YFC1707400)
刘 峘,副研究员,研究方向为中医药循证评价。E-mail: huananne@sina.com
谢雁鸣,研究员,博士生导师,主要从事中药上市后评价研究。E-mail: ktzu2018@163.com
[责任编辑 潘明佳]

