硝酸生产尾气中NOx和N2O联合脱除技术研究进展
李佳,樊星,陈莉,李坚
(北京工业大学区域大气复合污染防治北京市重点实验室,北京 100124)
硝酸作为一种重要的化工原料被广泛用于生产化肥和炸药以及作为氧化剂用于脂肪酸的生产,但其生产过程会导致大量有害气体的排放,最主要的是NOx(NO和NO2)和N2O[1-2]。NOx是主要的大气污染物之一,会导致酸雨和光化学烟雾的形成以及臭氧层的消耗,同时NOx是大气细颗粒物中硝酸盐的主要前体物[1]。我国《硝酸工业污染物排放标准》(GB 26131—2010)规定现有和新建企业分别自2013 年4 月1 日和2011 年3 月1 日起执行300mg/m3的NOx排放限值,同时规定NOx的特别排放限值为200mg/m3[3]。另一方面,N2O 被认为是一种仅次于CO2和CH4的温室气体,其全球增温潜势(global warming potential,GWP)为CO2的310 倍,可在大气中稳定存在长达114年之久[4]。另外N2O是平流层中NOx的主要来源,被认为是人为排放的最重要的臭氧层消耗物质[4-5]。化工行业排放的N2O占人为排放总量的29%,而硝酸生产是最主要的工业N2O排放源,每生产1t硝酸排放约6kg N2O[6]。目前许多工业发达国家对硝酸生产行业实施了严格的N2O排放限制,如2010年11月24日欧洲立法规定硝酸厂出口尾气中N2O浓度限值为20~100μL/L(2006年前建设的工厂限值为20~300μL/L)[1,7]。我国科技部于2022 年8 月18 日发布的《科技支撑碳达峰碳中和实施方案(2022—2030 年)》中明确提出要加强包括N2O在内的非CO2温室气体的监测和减量替代技术研发及标准研究,预计不久的将来我国会对重点行业N2O的排放进行限制。
选择性催化还原(SCR)法是去除硝酸厂尾气中NOx的主流技术之一,但利用传统的SCR催化剂不能有效降低N2O的含量。为了同时去除硝酸生产尾气中的NOx和N2O,需要在原有SCR 脱硝基础上增加N2O 去除单元或通过改进SCR 催化剂以实现NOx和N2O 的同步去除。本文在分析硝酸生产过程中NOx和N2O产生途径及减排措施的基础上重点围绕尾气中NOx和N2O联合脱除技术的研究进展进行了综述,分析了不同技术路线的原理、特点及面临的挑战,以期为硝酸生产尾气NOx和N2O协同净化技术的研发和应用提供参考。
1 稀硝酸生产过程及NOx和N2O的排放
氨氧化法是世界范围内生产稀硝酸(55%~60%,质量分数)的主要方法:以铂-铑贵金属为催化剂,在高温(750~900℃)下催化氨氧化为NO[式(1)],然后通过换热和冷却降低气体温度,促使NO 氧化为NO2[式(2)],在吸收塔内用水吸收NO2,即制得稀硝酸产品[式(3)],硝酸生产典型工艺流程如图1所示[8-9]。

图1 硝酸生产典型工艺流程简图
除氧化为NO[式(1)]外,氨氧化过程中还会发生式(4)~式(7)所示的副反应,导致副产物N2O 的生成以及NH3和NO的消耗[8]。
硝酸生产过程中形成的N2O量取决于氨氧化反应条件(如温度和压力)、氨氧化催化剂的组成和状态以及氨氧化炉的设计等[8]。氨氧化过程中高温、低压有利于提高NO的产率,而低温、高压则会增加N2O的生成量。在典型的氨氧化条件(750~900℃,0.1~1.3MPa)下,NO、N2O 和N2产率分别为95%~97%、1.5%~2.5%、4%~4.5%[8]。离开氨氧化炉的N2O不再参与硝酸生产过程,若不采取末端控制措施,则形成的N2O 都将随尾气排入大气中。另一方面,如式(3)所示,在水吸收NO2生成HNO3的过程中,只有2/3的NO2转化为HNO3,1/3的NO2会转化为NO,虽然NO 会被再次氧化和吸收,最终仍会有部分NO和NO2进入尾气中[10]。表1列出了硝酸生产尾气的典型组成[4]。
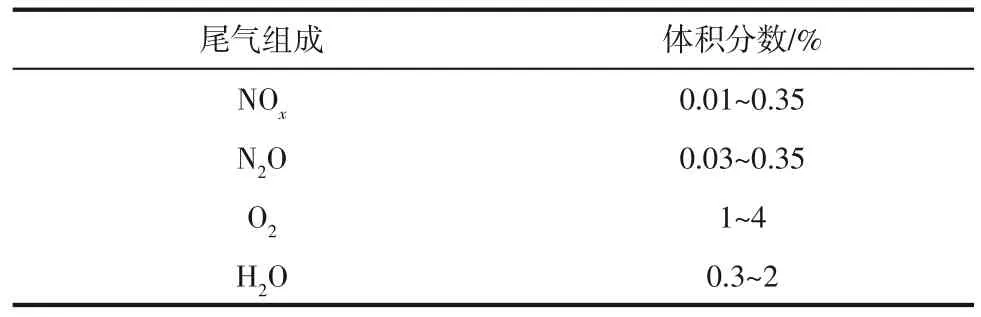
表1 硝酸生产尾气典型组成[4]
2 NOx和N2O控制措施概述
2.1 NOx控制措施
硝酸生产尾气中NOx的脱除广泛采用催化法,包括非选择性催化还原(NSCR)和选择性催化还原(SCR)[11]。根据催化反应所需温度的不同,NSCR 和SCR反应器可安装在尾气膨胀机的入口或出口侧(图1),其中入口侧尾气典型温度为250~500℃,出口侧为200~300℃[8,12]。
NSCR 法是在一定的温度和催化剂(氧化铝或蜂窝陶瓷负载Pt、V2O5、FeOx等)作用下,NOx被还原剂[甲烷、丙烷、丁烷、氨驰放气(含NH3、H2等)]还原为N2和H2O[7-8,13]。NSCR 法的优点是除NOx外,N2O也会被还原,NOx和N2O脱除率分别可达90%和70%左右,缺点是还原剂会优先与尾气中的O2反应,导致还原剂需求量增加,且使用碳氢化合物(HCs)作为还原剂会导致大量CO和CO2排放[7-8,13]。另外NSCR 反应器通常布设在尾气膨胀机上游,由于NSCR反应放热,尾气温度可能升至800℃以上,因此需要额外增加冷却单元以满足尾气膨胀机的工作条件[7-8]。虽然欧美国家广泛采用NSCR 技术脱除硝酸生产尾气中的NOx和N2O,但从长远来看,NSCR 同时脱除NOx和N2O 不具有技术和经济方面的优势,进一步开发的潜力不大[8]。
SCR 法主要是以NH3为还原剂,在催化剂的作用下,选择性地将NOx还原为N2和H2O[14]。NH3-SCR 是应用最广泛的工业尾气NOx处理技术,其核心是具有较高活性、N2选择性和水热稳定性以及较强抗中毒能力的催化剂[15-16]。目前已广泛研究/应用的SCR 脱硝催化剂包括锰基、钒基氧化物催化剂以及铜、铁分子筛催化剂等,表2总结了这几类SCR催化剂的特点[15,17-21]。

表2 典型NH3-SCR脱硝催化剂的特点[15]
目前硝酸厂尾气脱硝主要采用传统的钒钛催化剂,所需反应温度较高(300~400℃),脱硝装置需要布置在尾气膨胀机上游[22-23]。近年来,为了适应工业锅炉烟气低温脱硝的要求,我国着力研发了包括改性钒钛系催化剂在内的多种低温(<250℃)SCR脱硝催化剂,这为在硝酸生产工艺末端(尾气膨胀机下游)脱除NOx奠定了基础[24]。
2.2 N2O控制措施
根据在硝酸生产工艺流程中的布设位置,N2O控制措施可分为一级、二级和三级控制措施三类[13]。其中一级控制措施包括改进氨氧化催化剂以减少N2O的形成、增大氨氧化炉尺寸(延长氨氧化后的气体在高温区的停留时间)以促使形成的N2O发生分解等,可减少30%~85%的N2O,缺点是仅适于新建厂采用[7,13]。
二级控制措施是指在氨氧化催化剂之后布设N2O 高温分解催化剂以使氨氧化形成的N2O 在炉内发生分解,优点是可在不消耗还原剂、不进行大的工艺改动的前提下减排N2O,缺点是会增加压损以及会有少量NO发生分解而造成NO的损失[25]。该技术的核心在于开发能够耐受高温以及高浓度NO、O2和H2O影响的N2O分解催化剂,目前工业化应用的催化剂主要由Yara(挪威)、BASF(德国)、Johnson Matthey(英国)和Heraeus(德国)等公司研发,催化活性组分为贵金属或金属氧化物[25-26]。国内方面,据报道,四川蜀泰化工科技有限公司自主研发的铈锆固溶体负载金属氧化物型N2O炉内分解催化剂也在硝酸生产装置上实现了工业应用[27-28]。国内外实践表明,约80%采用了炉内N2O催化分解技术的项目减排N2O超过70%[13]。
三级控制措施是指借助催化分解或催化还原等技术脱除硝酸生产尾气中的N2O,根据反应所需温度的不同可布设在尾气膨胀机的上游或下游,不会对硝酸生产过程造成显著影响,且可通过放大反应器、优化工艺条件等实现N2O的高效脱除[29]。与催化N2O 还原相比,催化N2O 分解不需要使用还原剂,具有较为明显的经济优势。目前研究较多的硝酸生产尾气N2O分解催化剂主要包括分子筛和金属氧化物[30]。研究表明,Fe-分子筛(如Fe-beta、Fe-ZSM-5)同时具备催化N2O分解和还原的能力,与催化N2O分解相比,催化N2O还原所需温度降低约100℃[31-32]。另一方面,尖晶石结构的金属氧化物,尤其是在过渡金属氧化物中具有最弱金属—O键的Co3O4被广泛研究用于N2O 的催化分解[33-39]。Inger 等[37]采用K-ZnxCo3-xO4催化剂净化实际的硝酸生产尾气,发现空速为20000h-1、尾气温度为350℃时可去除95%以上的N2O 且催化剂具备较强的抗水抗氧能力,但NOx的存在会从一定程度上抑制N2O的分解。总的来说,随着温室气体减排要求的不断提升,无论是否已采取炉内(一级和二级)N2O控制措施,采用尾气净化技术高效脱除硝酸生产尾气中的N2O都势在必行。
3 NOx和N2O联合脱除技术
从国内外研发和应用情况来看,联合脱除硝酸生产尾气中NOx和N2O的技术路线主要包括在一段催化床内同步脱除NOx和N2O以及在两段催化床内分别脱除NOx和N2O 两类,其中同步脱除NOx和N2O 的技术主要包括采用NSCR 或SCR 催化剂同时催化NOx和N2O还原以及采用复合式催化剂同时催化NOx还原和N2O 分解两类。与NSCR 相比,SCR工艺选择性高,还原剂消耗量少,因此更具发展潜力。两段催化床内分别脱除NOx和N2O的工艺包括先催化N2O 分解后催化NOx还原、先催化NOx还原后催化N2O 还原以及先催化NOx还原后催化N2O 分解等。采取两段式工艺时,前后两类催化反应的活性温度窗口应较为接近以避免段间换热的需要。图2 为主要的联合脱除硝酸生产尾气中NOx和N2O 工艺的示意图。
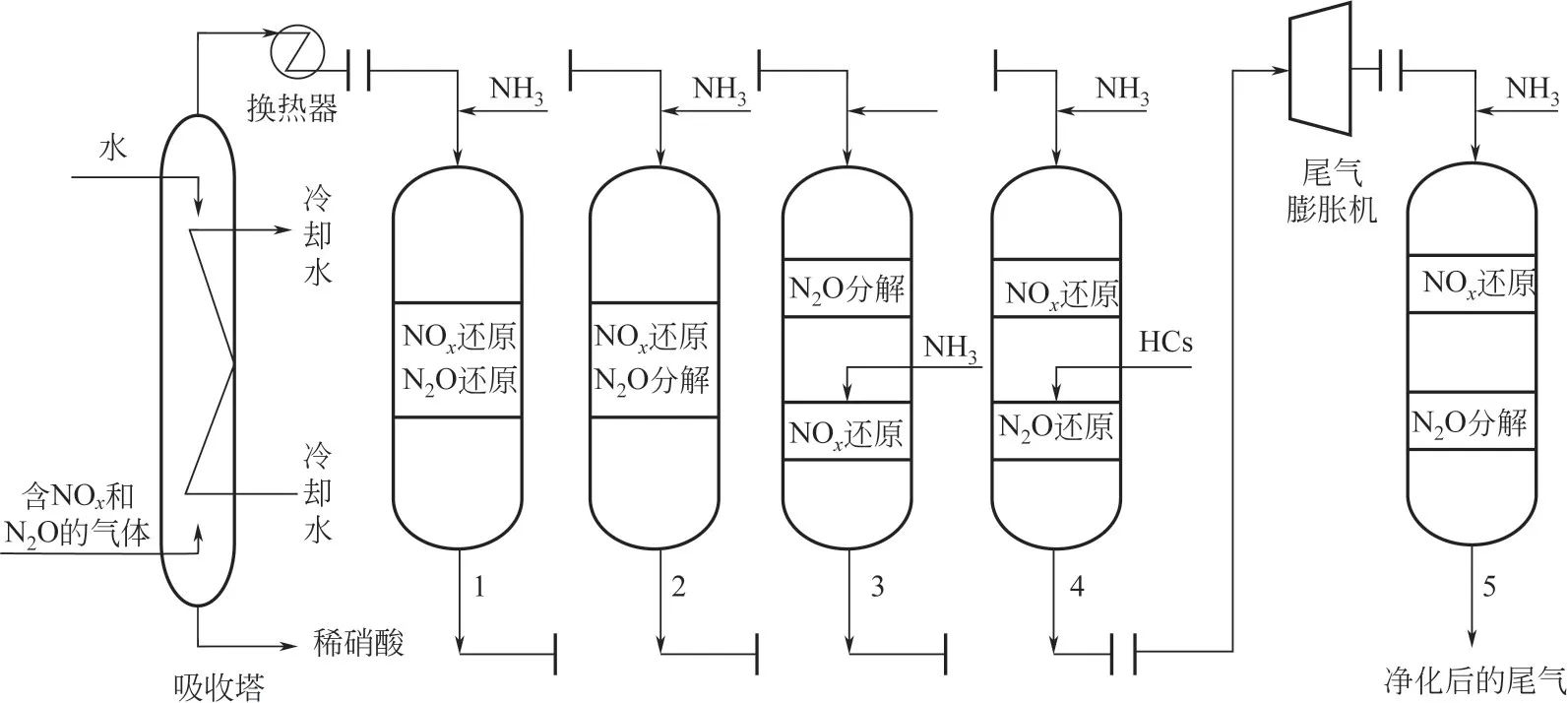
图2 硝酸生产尾气中NOx和N2O联合脱除工艺示意图
3.1 SCR催化剂同时催化NOx和N2O还原
近年来利用NH3-SCR 同时脱除NOx和N2O 受到了研究人员的广泛关注,目前已有研究主要以Fe-分子筛为催化剂。Zeng 等[40]研究发现,与Fe-SAPO-34 和Fe-ZSM-5 相比,Fe-beta 催化剂具有更好的催化NH3同时还原NO和N2O性能,NO和N2O同时还原时相互之间的抑制作用较小,当空速为40000mL/(g·h)、温度为400℃时NO 和N2O 转化率都高于90%。Baek 等[41]考察了反应气含H2O 对Fe-beta 催化剂催化NH3同时 还 原NO 和N2O 的影响,发现相同温度下N2O 转化率低于NO,N2O 转化率随H2O 含量升高而显著降低,而H2O 含量对NO转化影响不大。Colombo等[42]基于动力学分析发现,Fe-分子筛表面NH3还原N2O需要的活化能(100~150kJ/mol)显著高于NH3还原NO(40~50kJ/mol),强化N2O 的还原是实现NO 和N2O 同时高效去除的关键所在。
为了考察催化剂在实际尾气条件下的使用性能,Lee 等[43]对Fe/beta 催化剂催化NH3同时还原硝酸厂尾气中NOx和N2O 的性能进行了现场实验研究,发现采用颗粒状的催化剂且控制空速为约20000h-1、催化床入口气体温度为约360℃时,NOx和N2O平均转化率分别达95%和90%左右;采用蜂窝状的催化剂且控制空速为8200h-1、催化床入口气体温度为354~373℃时,NOx和N2O 转化率高于96%,同时NH3逃逸低于25μL/L。
上述研究表明,含铁分子筛尤其是Fe-beta 催化剂是具有实际应用潜力的NO 和N2O 同时还原催化剂,未来可围绕降低反应所需温度(拓宽催化剂活性温度窗口)以及提高催化剂对共存气体(H2O)的耐受性等方面开展进一步研究。
3.2 复合式催化剂同时催化NOx还原和N2O分解
研究人员也探索了利用复合式催化剂同时催化NOx还原和N2O 分解的可行性,如Zhao 等[44]在V2O5-MoO3/TiO2催化剂表面引入能够催化N2O 分解的Bi-Ni混合金属氧化物,虽然从一定程度上抑制了催化剂催化脱硝的性能,但大大提高了其催化N2O 分解的性能,在Bi-Ni 混合金属氧化物添加量为40%(质量分数),反应气组成为250μL/L NO+125μL/L N2O+250μL/L NH3+3% O2+N2(平衡),空速为45000h-1、温度为390℃的条件下获得的NO和N2O去除率分别为90%和72%左右;催化剂具有较好的抗水性,但NH3、O2和SO2的存在会从不同程度上抑制N2O 的分解。Kim 等[45]研究发现,V2O5-WO3/TiO2催化剂催化NH3-SCR 脱硝过程中,温度高于400℃时会形成可观的N2O,在V2O5-WO3/TiO2表面涂覆Fe-ZSM-5 可有效抑制N2O 的形成,与高温(>350℃)下Fe-ZSM-5促进了N2O的分解和还原有关,但负载Fe-ZSM-5 后催化剂催化NOx还原性能有所降低。
由此可见,在传统的SCR 脱硝催化剂表面引入能够催化N2O分解的活性成分是同步实现NOx还原和N2O分解的途径之一,未来需从改善催化剂的低温活性(尤其是催化N2O分解的活性)以及提高催化剂抗共存气体干扰性等方面开展进一步研究。
3.3 先催化N2O分解后催化NOx还原
先催化N2O 分解后催化NOx还原是指在第一段催化床内使N2O 分解为N2和O2,然后引入还原剂(NH3),在第二段催化床内使NOx还原为N2和H2O(图2中工艺3)。Uhde和Süd-Chemie公司开发的同时脱除硝酸厂尾气中NOx和N2O 的EnviNOх®技术包含两种技术路线,其中之一便是先催化N2O分解后催化NOx还原[12]。EnviNOх®技术中N2O 分解和NOx还原均采用Fe-分子筛催化剂,需要的反应温度较高(>425℃)[12]。有研究表明,与NOx对金属氧化物催化N2O分解产生抑制作用不同,NO对Fe-分子筛(如Fe-ZSM-5)催化N2O 分解具有促进作用,与Fe-分子筛表面NO 氧化消耗氧物种、从而促进N2O 分解(N2O+NON2+NO2)有关[42,46-47]。也就是说,将N2O分解设置在NOx还原之前可充分利用NOx对N2O 分解的促进作用,但在NOx还原阶段需精确控制还原剂的投加量(NH3/NOx比)以避免再次形成N2O(脱硝副产物)[7]。
实践表明,对于尾气温度可达425℃以上的大型双压和现代高(单)压硝酸工厂,借助先催化N2O 分解后催化NOx还原的工艺可脱除尾气中98%以上的N2O,同时通过精确控制脱硝时NH3的投加量可使出口NOx含量控制在5~40μL/L[12]。
3.4 先催化NOx还原后催化N2O还原
先催化NOx还原后催化N2O 还原是指先引入NOx还原剂(NH3),在第一段催化床中脱除NOx,后引入N2O 还原剂(如甲烷、丙烷等),在第二段催化床中脱除N2O(图2中工艺4)。与使用一种催化剂催化NH3同时还原NOx和N2O 不同,采用先催化NOx还原后催化N2O还原的工艺可针对两段催化床分别选择有利于NOx和N2O还原的催化剂和还原剂,减少NOx对N2O 还原的抑制作用。研究表明,以Fe-分子筛为催化剂时,碳氢化合物还原N2O 的性能好于NH3,但共存的NO 会抑制N2O 的还原,因此应确保NOx在第一段催化床内被高效脱除[48]。
EnviNOх®的另一种技术路线即为先催化NOx还原后催化N2O 还原,由于催化剂(Fe-分子筛)催化N2O还原较催化N2O分解所需温度低,因此该工艺可适用于尾气温度更低(330~520℃)的情形[12]。埃及的Abu Qir Fertilizer 和韩国的HU CHEMS 等硝酸厂将该工艺用于NOx和N2O的联合脱除,均实现了出口NOx浓度在0~7μL/L、N2O 去除率超过98%的净化效果[12]。
3.5 先催化NOx还原后催化N2O分解
与先催化N2O 分解后催化NOx还原相比,采取先催化NOx还原后催化N2O 分解的工艺(图2 中工艺5)不需要精确控制NOx还原剂的投加量(NH3/NOx比),脱硝阶段生成的N2O副产物可通过后续的催化分解去除,因此在促进NOx去除和减少N2O排放方面更具优势。Chumachenko 等[7]也认为,先催化NOx还原后催化N2O分解是高效脱除硝酸厂尾气中NOx和N2O的可行路线。考虑到目前已成功开发和应用多种低温(<250℃)SCR 脱硝催化剂[24,49-51],为了在尾气膨胀机下游温度较低(200~300℃)的条件下高效脱除NOx和N2O,需要开发具有较高低温活性的N2O分解催化剂。
为了进一步提高Co3O4催化剂低温下催化N2O分解的性能,研究人员围绕Co3O4的改性开展了大量研究,包括在催化剂表面引入碱金属(如K、Cs)以降低催化剂的逸出功、用过渡金属离子(如Ni2+、Ni3+、Zn2+)取代Co3O4晶格中的部分Co2+或Co3+以加速电子转移/氧化还原循环以及引入其他金属氧化物(如PbO2、CeO2)并使其与Co3O4通过界面发挥协同作用等[52-65]。联合使用不同改性方法也被认为是同时改善催化剂活性和抗共存气体干扰性的重要途径,如Xiong等[66-67]发现用Gd改性Co3O4后再引入K 可在空速为20000h-1时将N2O 完全转化温度从350℃降至300℃,联合改性后催化剂对共存气体(O2、H2O、NO)的耐受性也有所提高。虽然已有低温SCR脱硝以及N2O低温催化分解的研究都较多,但将两者联合起来用于脱除硝酸生产尾气中NOx和N2O的报道较少。Chumachenko 等[7]提出了先采用V2O5/Al2O3催化剂催化NOx还原、后采用Cs/NixCo3-xO4催化剂催化N2O分解的硝酸生产尾气净化工艺,模拟结果显示NOx还原段空速为9664h-1、温度为220~240℃,N2O 分解段空速为7667h-1、温度为230~260℃时,NOx和N2O 脱除率均可达98%以上,但该工艺的实际净化效果尚待验证。
虽然Co3O4基催化剂被认为是目前最具实际应用前景的N2O低温分解催化剂,其应用于实际硝酸生产尾气净化时仍存在着活性温度高、对共存气体耐受性差等问题,未来尚需将催化剂的活性温度窗口进一步向低温区拓展,同时考虑NOx还原与N2O分解对于温度需求的匹配,提高先催化NOx还原后催化N2O分解工艺在实际硝酸生产尾气条件下联合脱除NOx和N2O的性能。
3.6 不同联合脱除工艺性能比较
综上所述可以看出,不同联合脱除工艺的布设位置、工艺特点、开发阶段以及未来重点研发的方向都有所不同。表3对比了五种主要联合脱除工艺的综合性能,也列出了代表性的研究和应用结果。通常而言,联合脱除工艺布设在尾气膨胀机上游时,尾气温度较高,有利于N2O的去除,但净化后尾气压力降低,可能会对尾气膨胀机的运行产生不利影响[8]。联合脱除工艺布设在尾气膨胀机下游时对原有硝酸生产工艺无影响,同时净化装置受安装场地的限制较小,但由于尾气温度较低,难以实现N2O的高效去除。

表3 NOx和N2O联合脱除工艺性能比较
先催化N2O 分解后催化NOx还原和先催化NOx还原后催化N2O 还原两种工艺虽已投入实际应用,但先催化N2O分解后催化NOx还原工艺需要的温度达425℃以上,仅适用于膨胀机之前尾气温度足够高的硝酸厂;先催化NOx还原后催化N2O还原工艺需要的温度略低,但需同时消耗NOx和N2O 还原剂,增加成本的同时可能由于还原剂的排放导致二次污染。其余三种联合脱除工艺均处于研发阶段,其中两种一段式工艺(SCR催化剂同时催化NOx和N2O 还原和复合式催化剂同时催化NOx还原和N2O分解)净化NOx性能较好,但净化N2O的性能有待进一步提升;先催化NOx还原后催化N2O分解是目前唯一可望布设在尾气膨胀机下游的工艺,其在减少还原剂消耗、促进N2O去除等方面具有优势,未来应重点围绕降低N2O分解所需温度、提高联合脱除工艺对共存气体(O2、H2O等)的耐受性等方面开展研究。
4 结语
氨氧化法是世界范围内生产稀硝酸的主要方法,未完全吸收的NOx以及氨氧化形成的N2O副产物是硝酸厂排放的主要有害气体。目前NOx普遍采用SCR 或NSCR 法从末端去除,而N2O 有三级控制措施,包括改进氨氧化催化剂、增大氨氧化炉尺寸以减少N2O形成的一级控制措施、在氨氧化催化剂之后布设N2O高温分解催化剂以使N2O在炉内发生分解的二级控制措施以及在尾气末端借助催化还原/分解技术脱除N2O 的三级控制措施。随着大气污染控制和温室气体减排要求的不断提升,采取措施高效脱除硝酸生产尾气中的NOx和N2O 势在必行。
目前研究和应用的联合脱除硝酸生产尾气中NOx和N2O 的工艺包括采用SCR 催化剂同时催化NOx和N2O 还原、采用复合式催化剂同时催化NOx还原和N2O分解等一段式工艺以及先催化N2O分解后催化NOx还原、先催化NOx还原后催化N2O 还原和先催化NOx还原后催化N2O 分解等两段式工艺。其中SCR催化剂同时催化NOx和N2O还原工艺通常以NH3为还原剂,借助Fe-beta 分子筛等催化剂同时催化NOx和N2O 还原;复合式催化剂同时催化NOx还原和N2O 分解工艺是在传统的SCR 脱硝催化剂表面引入能够催化N2O 分解的活性组分以使NOx还原和N2O分解同时进行;先催化N2O分解后催化NOx还原工艺是以Fe-分子筛等为催化剂,先催化N2O分解,后引入NH3以促使NOx还原;先催化NOx还原后催化N2O 还原工艺也以Fe-分子筛等为催化剂,先引入NH3以还原NOx,后引入HCs 以还原N2O;先催化NOx还原后催化N2O 分解工艺则是分别选用NOx还原(如V2O5/TiO2)和N2O 分解(如改性Co3O4)催化剂,在两段内分别实现NOx和N2O的脱除。
联合脱除NOx和N2O 的工艺中,一段式工艺布置紧凑,可同步脱除NOx和N2O,但N2O 的还原/分解性能有待进一步提升;两段式工艺中先催化N2O分解后催化NOx还原和先催化NOx还原后催化N2O还原工艺已投入实际应用且取得了较好的联合脱除效果,但存在工艺运行温度高、N2O还原需要额外消耗还原剂等问题;先催化NOx还原后催化N2O分解是目前唯一可望布设在尾气膨胀机下游的工艺,具有对硝酸生产过程无影响、还原剂消耗少、有利于N2O去除等优势,未来尚需将催化剂的活性温度窗口进一步向低温区拓展,同时考虑NOx还原与N2O分解对于温度需求的匹配,提高工艺在实际硝酸生产尾气条件下联合脱除NOx和N2O的性能。此外,采用不同联合脱除工艺时,NOx和N2O 脱除时的相互影响、尾气中其余共存气体(O2、H2O 等)对NOx和N2O 脱除的影响以及NOx和N2O 联合脱除的机理等也需进一步探究。

