KBF4含量对FA75Mn添加剂熔化实收率的影响
刘志远,尹冬松,毛 勇,翟凤龙,张忠凯,李 洲,王春阳,张春宇
(1.黑龙江科技大学 材料科学与工程学院,黑龙江 哈尔滨 150022; 2.广东海洋大学 机械工程学院,广东 湛江 524088; 3.哈尔滨东盛金材科技(集团)股份有限公司,黑龙江 哈尔滨 150090)
铝合金的应用十分广泛,合金化是铝合金生产流程中重要的一环。大部分合金元素如Mn、Ti、Ni、Fe等的熔点显著高于Al的熔点,如果直接加入到铝合金熔体中,需要提高铝液温度,并且显著增长熔化时间,会造成氧化和吸气,因此,有必要改变这种单质添加方式。目前常用的添加方式有铝中间合金和铝添加剂两种形式[1]。
铝添加剂最早是英国用于铝合金的熔炼生产,含有助熔剂的铝添加剂加入熔体后,利用铝热反应在局部产生高温,使铝添加剂中的高熔点合金元素迅速熔化。Mn作为铝合金主要的合金元素之一,在铸造铝合金、变形铝合金中广泛使用,可以大大提高铝合金的综合性能。然而,锰添加剂的熔化过程对原料、助熔剂、混合工艺、压制工艺都极为敏感。影响锰添加剂性能的关键因素有多种,比如原料、助熔剂的种类及成分配比等[3]。目前,锰添加剂熔化速度较慢,实收率较低,而且容易带入其他杂质,从而影响铝制品的质量。
本试验采用少量的KBF4作为助熔剂,通过改变助熔剂的含量,制备三种KBF4含量的添加剂,研究其实收率,并对其机理进行分析,希望对FA75Mn添加剂的生产实践和理论研究提供参考。
1 试验材料和方法
本试验采用锰粉(机械破碎纯锰粉,纯度不小于99.7%,粒度20目~100目),铝粉(A00空气雾化纯铝粉,纯度不小于97%,粒度80目~200目),KBF4(纯度不小于98.0%),氧化铒(纯度不小于99.9%),铝锭(纯度不小于99.9%),固体石蜡(纯度不小于99.9%)。将原料精确称重计量,严格按照生产配方投料制成混合粉体,使用陶瓷研钵研磨30 min,直至粉体混合均匀,粉体总质量为500 g,在哈尔滨东盛金属材料有限公司将配置好的粉体在液压机上压制成型。表1为FA75Mn成分配比(w(KBF4)=1%、3%、5%依次记为1#添加剂、2#添加剂、3#添加剂)。试样宏观形貌如图1所示。

图1 液压试样宏观形貌Fig.1 Macroscopic morphology of a hydraulic sample
称取(5±0.2)kg铝锭使用井式电阻炉进行熔炼,在井式电阻炉中将铝锭升温730 ℃,待铝锭熔化后,加入添加剂,分别在FA75Mn添加剂投入的1 min、2 min、4 min、6 min、10 min、20 min、22 min取样(70±2)g,测量各时间点铝液中的锰含量,进而计算各时间点的实收率。实收率计算公式:
(1)

(2)
2 试验结果及讨论
各时间点测得的实收率数据变化趋势如图2所示。由图2可以看出,随着FA75Mn添加剂投入时间的增加,三种添加剂实收率都呈增加趋势。其中,2#添加剂的试样在开始时间实收率增速最为显著,当投入时间达到6 min时,实收率就达到86.58%;投入时间增加到10 min时,3#添加剂的试样实收率迅速增加,并且超过另外两种添加剂的实收率,达到93.075%;继续增加三种添加剂投入时间,实收率都有增加,但增速变缓;当投入时间达到20 min以后,三种添加的实收率相差不大。
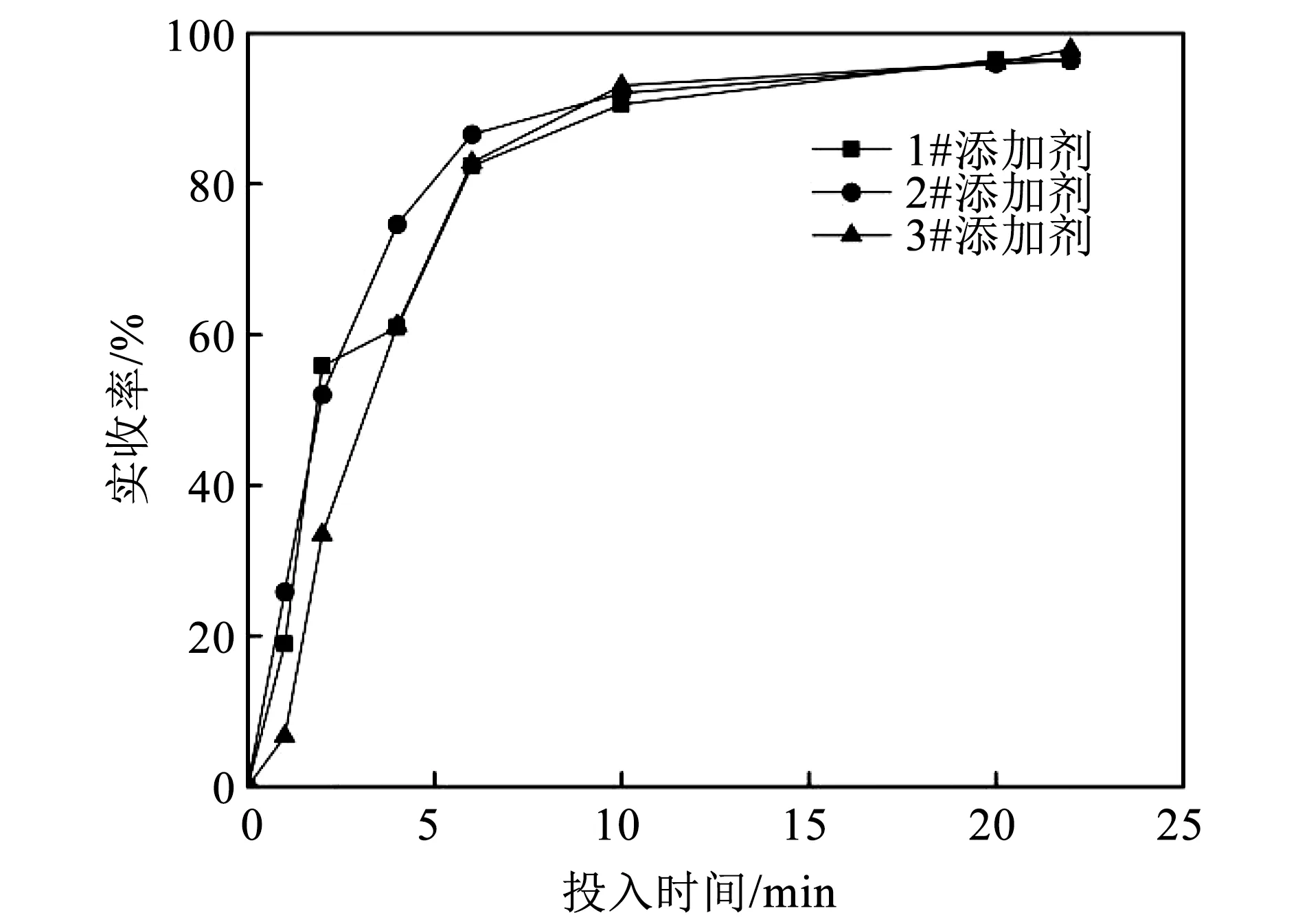
图2 FA75Mn添加剂实收率随时间变化Fig.2 Yield of FA75Mn additives varies with time
KBF4与熔融态的铝液接触后迅速发生反应[4]:
KBF4(l)=KF(l)+BF3(g)
ΔH=168.154 kJ/mol
(3)
BF3(g)+Al(l)=B(l)+AlF3(l)
ΔH=-287.019 kJ/mol
(4)
AlF3(l)+KF(l)=KAlF4(g)
ΔH=31.339 kJ/mol
(5)
KBF4(l)+Al(l)=B(l)+KAlF4(g)
ΔH=-87.526 kJ/mol
(6)
KBF4在投入熔体中会迅速地分解,产生的BF3气体在铝液中发生反应产生AlF3,AlF3与KF发生反应生成KAlF4,在反应式(4)与反应式(6)中产生的B原子会逐渐地扩散到铝液中,随着反应的进行,熔体中B的浓度逐渐增加,最终在界面处与铝液发生反应,析出硼化物颗粒:
Al(l)+2B(l)=AlB2(s)
ΔH=-165.126 kJ/mol
(7)
Al(l)+12B(l)=AlB12(s)
ΔH=-288.293 kJ/mol
(8)
AlB12(S)+5Al=6AlB2
ΔH=-702.464 kJ/mol
(9)
通过上述反应可知,KBF4与铝液反应放出大量的热。在试验过程中发现,当w(KBF4)=5%的FA75Mn添加剂投入到铝液时,铝液的温度从730 ℃初始温度升高到745 ℃,发生了明显的升高。
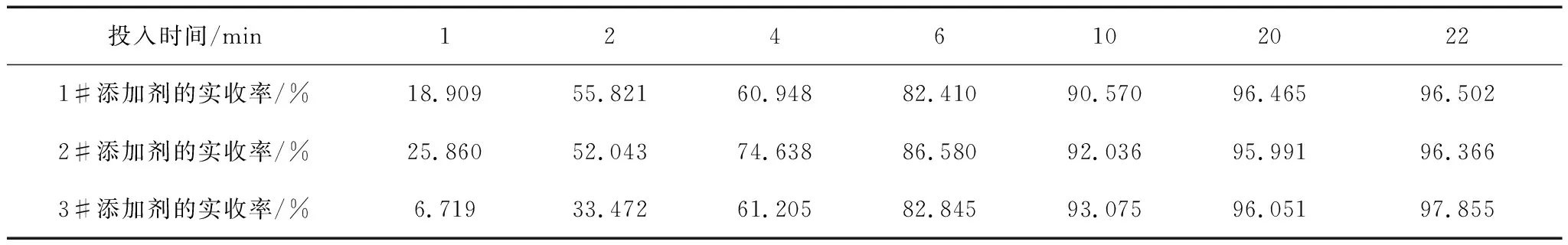
表2 各时间点FA75Mn添加剂实收率Table 2 Yield of FA75Mn additives at each time point
反应式(7)~式(9)的标准反应吉布斯自由能变化,计算结果如图3所示。3个反应的吉布斯自由能均小于0,所以3个反应均能自发进行。反应式(9)的吉布斯自由能变化最小,反应最容易发生,因此在铝液中最终生成稳定的AlB2。
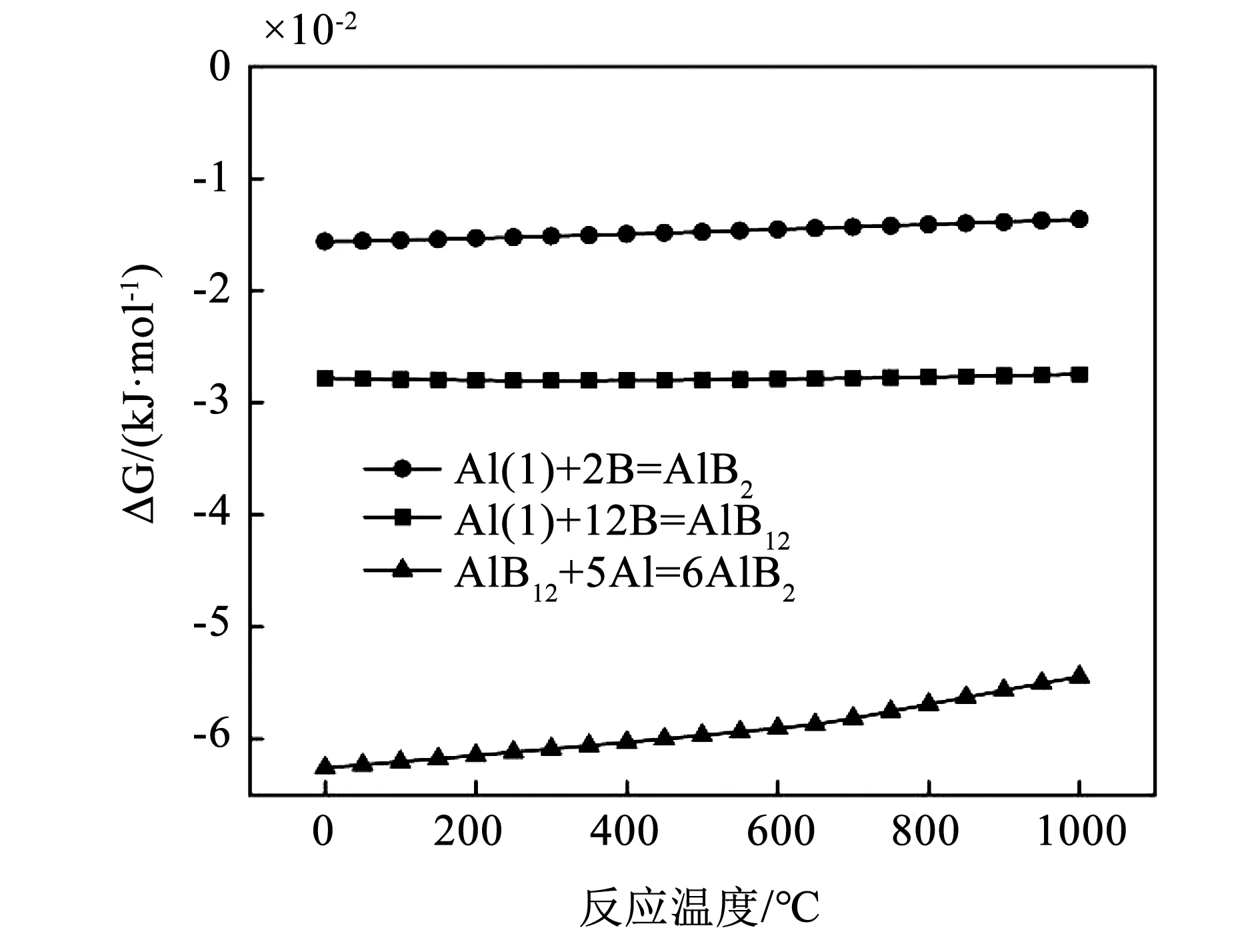
图3 铝硼反应吉布斯自由能Fig.3 Gibbs free energy of aluminum-boron reaction
AlB2颗粒与基体材料之间的润湿性好,且界面结合性好[5]。研究发现[6],AlB2可以作为某些铝合金异质形核的质点。特别是对于铝硅合金,AlB2表面可以形成稳定的Al-Si二元原子结构层,这种稳定的二维Al-Si原子层在随后的异质形核过程中起着重要的过渡作用,在此条件下AlB2成为α-Al有效异质核心。此外,AlB2也有提高铝合金材料强度和刚度的作用。
Mn对铝合金的综合性能提高尤为关键,根据Al-Mn合金系平衡相图,在共晶温度658 ℃时,Mn在固溶体中的最大溶解度为1.82%。Mn是铝合金的重要合金元素,Mn元素的原子半径与Fe原子接近,能够替换富铁相中的部分晶格节点的Fe原子,将粗大的针状Fe相转变为鱼骨状、花型和粗枝晶型的α-Al(Fe,Mn)Si相,可改善合金的力学性能。在腐蚀性能方面,Al的标准电位为-1.663 V,而Mn的标准电位为-1.179 V,两者的标准电位差为-0.484 V,形成的自腐蚀电流较小,因此,Mn的加入能保证合金保持较高的耐蚀性能。同时,由于Mn元素在Al合金中的固溶度较大,在实际凝固下极易固溶到Al基体中,造成严重的晶格畸变,增大合金中自由电子的衍射作用,从而较大地改变合金的导热导电性能。在铝合金中,Mn可以和基体生成Al6Mn相, 提高合金的再结晶温度,提高合金强度和抗腐蚀性能,且可使含Fe相的边角圆钝化并降低其脆性,从而降低Fe元素对材料性能的不利影响。
3 结 论
将KBF4质量分数分别为1%、3%和5%的三种FA75Mn添加剂投入铝液中,并测试其实收率变化规律,得到如下结论:
1)随着投入时间增加,三种添加剂的实收率都呈上升状态,投入10 min后三种添加剂的实收率都能够达到90%以上,显示了良好的速熔和高实收率的优势。
2)当投入铝液时间超过6 min后,随着KBF4添加量增加,添加剂的实收率也呈增加趋势;投入铝液时间达到22 min时,添加w(KBF4)=5%的FA75Mn添加剂实收率达到97.855%。

