吡虫啉毒性作用机制及治疗进展
尼亚孜艾力·萨伊提,张敏,李倩
(皖南医学院弋矶山医院急诊内科,安徽 芜湖 241001)
吡虫啉是新烟碱类杀虫剂,以烟碱性乙酰胆碱受体(nAChRs)为靶标。吡虫啉选择性结合nAChRs,可导致乙酰胆碱在机体内蓄积,导致昆虫麻痹而死亡[1]。nAChRs作为吡虫啉的靶受体广泛表达在中枢和周围神经系统中,当患者吡虫啉暴露时,吡虫啉作为nAChRs的激动剂使患者表现为烟碱样症状,严重时出现神经系统损伤的表现[2]。此外,肝、肾作为毒素的代谢器官,也会被吡虫啉不同程度的损伤,其典型表现为肝细胞变性、肝毛细血管充血和水肿、肾小管上皮细胞的损伤和坏死等[3,4]。
1 吡虫啉对机体的毒性作用
1.1 神经系统的毒性作用 吡虫啉中毒会导致中枢神经系统的损伤。吡虫啉能通过血脑屏障,在神经细胞内被脱硝基后的代谢产物吡虫啉烯烃(IMI-ole)竞争性抑制 nAChRs和下调nAChRs基因的表达[5]。此外,吡虫啉脱硝基后的产物结合于蓝斑去甲肾上腺素能神经元、多巴胺能神经元以及与认知功能相关的海马体等神经元表达的nAChRs,促进神经元钙离子内流,使细胞内依赖钙离子的磷脂酶、蛋白酶和一氧化氮合酶(NOS)均被激活,进而启动氧化应激反应损伤神经细胞[6]。在外周神经,吡虫啉持久性的激活nAChRs下游的PKA/CREB和Rho信号通路,促进与儿茶酚胺合成相关基因的表达,包括酪氨酸羟化酶(TH)和苯乙醇胺N-甲基转移酶(PNMT),使吡虫啉中毒患者表现为交感神经兴奋的心动过速、恶心、高血压等症状[7]。
1.2 脏器的毒性 肝脏为体内吡虫啉的主要代谢器官。吡虫啉被胃肠道吸收进入体内后,在肝脏微粒体内分别发生加羟基、脱硝基、还原、烯烃化和氧化等代谢反应[8]。当体内吡虫啉的量超过肝脏的代谢能力时,肝细胞不可避免的被损害。给成年大鼠经口服用吡虫啉时,肝细胞内谷胱甘肽还原酶活性下降,导致依赖巯基(-SH)的抗氧化酶(SOD、GST、GPx及CAT)活性被抑制,细胞内活性氧、活性氮含量升高,从而导致肝细胞的抗氧化能力降低[9]。肝细胞内氧化应激和内质网应激反应进一步诱导细胞膜蛋白和脂质的过氧化反应,使膜的通透性增加,为肝细胞内的酶(包括转氨酶、碱性磷酸酶和SOD)和炎症因子(TNF-α 、IFN-γ等)的渗出开通了绿色通道[10]。激活的炎症因子TNF-α 和 IFN-γ参与细胞免疫系统的维持、炎症反应和宿主防御。肝细胞损害的病理变化是肝细胞变性,中央静脉和肝血窦的扩张和充血[3]。
吡虫啉对肾脏也有毒性。吡虫啉以剂量依赖的方式导致肾小管上皮细胞空泡变性,局灶凝固性坏死等病理学变化[4]。也有研究发现,给幼年和成年大鼠经口服用吡虫啉时,肾组织内脂肪酸、胆固醇以及维生素的含量均升高[11]。其中,脂肪酸和胆固醇对维持细胞内稳态和代谢至关重要,其含量过高具有细胞毒性,可导致细胞凋亡[12]。
1.3 免疫功能的毒性 研究发现,与对照组相比,吡虫啉抑制脾和胸腺细胞的增殖活性,同时促进腹腔巨噬细胞(Pmø)分泌IL-1β、TNF-α,进而直接损伤免疫器官和细胞免疫功能[13]。肥大细胞位于机体免疫系统的第一屏障,防御病原微生物的入侵,在超敏性反应的病变中起着重要作用。石林波等[14]研究发现,吡虫啉以nAChRs为靶点抑制IgE介导的体内外肥大细胞脱颗粒及Toll样受体2介导的肥大细胞活化,为吡虫啉对过敏性疾病及宿主防御免疫能力的影响提供了依据。
1.4 其他毒性 细胞实验显示,吡虫啉可干扰内分泌功能,产生胰岛素抵抗,使体内脂肪储量增加[15]。吡虫啉可导致食管胃黏膜细胞组织学改变,使细胞质空泡化,黏膜上皮与基地膜的间隙增宽,以及促进黏膜上皮细胞凋亡等[16]。此外,吡虫啉在遗传水平上损伤DNA和RNA,影响蛋白质合成,干扰细胞代谢平衡,影响机体生长发育[17]。
2 吡虫啉中毒的治疗
虽然吡虫啉是低毒类农药,但随着其大量应用,急、慢性中毒事件不可避免,临床上也会遇到不按常规出牌的案例。吡虫啉中毒患者临床表现多样,轻者仅出现乏力、恶心、呕吐、困倦、头晕及头疼,重者可出血心脏骤停、消化道的灼伤性出血、呼吸衰竭、肝肾衰竭、昏迷甚至死亡[16,18-19]。回顾国内外吡虫啉中毒患者的临床研究,吸入性肺炎、呼吸衰竭、肝肾功能衰竭、神经毒性以及心脏功能受损是影响患者住院时间、送到ICU概率以及死亡率密切相关的因素(表1)。吡虫啉虽然毒性较低,摄入量较大时可能引起严重的中毒,且目前尚无特效拮抗剂,治疗主要以促进排毒,保护脏器,对症治疗为主,重度中毒患者早期可考虑给予血液灌流等治疗。
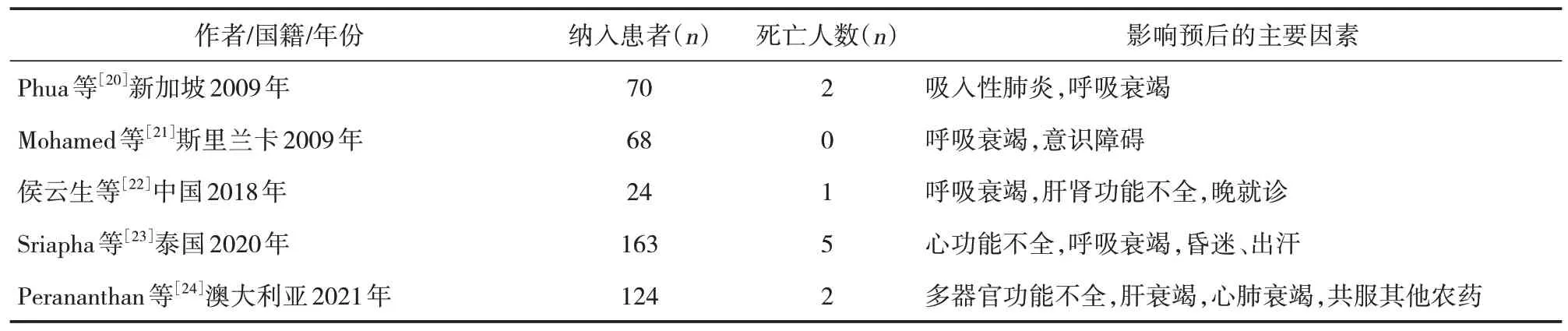
表1 吡虫啉中毒患者的回顾性研究
2.1 常规治疗 急性吡虫啉中毒的常规治疗包括洗胃,纠正酸碱失衡,控制感染,以及彻底清洁皮肤以去除未吸收的毒物[25]。洗胃时用常规温清水洗胃,每次洗胃液量300~500 ml,直至胃管洗出澄清,无味无色液体,接着由胃管注入甘露醇250 ml来导泻[26]。吡虫啉中毒可导致胆碱酯酶活性降低,这可能与患者入院后未行常规的洗胃,导泻,导致吡虫啉在体内残留时间过长有关[27]。Sriapha等[23]通过对163例吡虫啉中毒病例进行回顾性研究,探讨吡虫啉中毒患者的危险因素,研究发现,呼吸衰竭是影响患者预后的重要因素。中毒患者要密切监测呼吸氧合变化,出现呼吸衰竭,肺部湿啰音或分泌物增多时,尽快行气管插管或气管切开进行机械通气,必要时肌内注射阿托品,能极大程度改善患者预后生存率[19-22]。此外,应纠正代谢性酸中毒,进行补液治疗,心动过缓时予以阿托品,保护肝功能,出现神经功能受损症状在常规治疗的基础上联合应用维生素B1、B12类营养神经药物并预防应激性溃疡[27-28]。初步诊断时肝功能正常的患者,随后的住院期间密切关注肝功能,并嘱患者出院后在门诊复查肝功能,以避免迟发性肝功能减退。
2.2 血液净化治疗 血液净化的目的是清除血液循环中的毒物、炎症因子、细胞因子,以及纠正酸碱平衡紊乱,从而减轻肝肾功能损害。祝玉慧等[29]报道,通过序贯消化道净化联合血液灌注,可显著减少重度吡虫啉中毒患者住院时间,降低死亡率。侯云生等[23]研究发现,对肝肾功能损害伴肾功能不全,代谢性酸中毒患者,行床旁血液灌流后治疗效果显著,肝肾功能恢复较快,增加吡虫啉中毒患者治愈率。
2.3 控制炎症反应 咖啡酸苯乙基酯(caffeic acid phenethyl ester,CAPE)是来源于蜜蜂蜂巢的一种酯类化合物,具有清除自由基,抗炎症反应,抗氧化应激和免疫调节等多种药理活性[30]。Shao等[31]在急性吡虫啉中毒小鼠模型中发现,CAPE能抑制肝细胞TNF-α、INF-γ炎症因子,抑制肝细胞内质网氧化应激反应,下调NO产生和脂质过氧化,从而对小鼠肝细胞起保护作用。李亚萍等[32]在人肝细胞中发现,CAPE通过过氧化物酶体增值激活受体共激活因子1α(peroxisome activated receptor coactivator1α,PGC1α)通路促进SOD2的表达,并抑制TNF-α、IF-6的产生,使细胞线粒体ROS水平降低,改善线粒体氧化应激,从而改善细胞脂毒性。
3 小结与展望
吡虫啉对人类的毒性较小,症状较轻,因此逐渐取代毒性强的有机磷农药。呼吸衰竭,心血管功能受损以及神经毒性是吡虫啉中毒引起的危及患者生命但稀有并发症,治疗时务必采取必要的防御措施。目前吡虫啉中毒患者没有特效解毒药,以排泄毒物和支持治疗为主,患者出现误吸或呼吸衰竭时应用预防性抗生素并辅助呼吸治疗。肝肾功能衰竭的患者血液灌注,血液透析治疗能及时纠正电解质、酸碱平衡紊乱,清除体内外源性毒物,有肯定的疗效。此外,随着大规模多中心临床研究的开展,急性吡虫啉中毒的诊断和治疗将会逐步完善,进一步降低患者的病死率和改善生存。

