ε-MnO2纳米片的可控制备及其电容去离子特性的研究
王 伟,李海波
(宁夏大学 材料与新能源学院,宁夏回族自治区 银川 750021)
1 引言
人口的快速增长和工业的高速发展使得水资源紧缺问题越发严重[1],同时全球水资源分布不均导致一些国家对淡水的需求巨大,促使了海水淡化产业的兴起[2,3]。与已经得到良好商业化应用的海水淡化技术,如反渗透[4]、多效闪蒸[5]和电渗析[6]等相比,电容去离子(Capacitive deionization, CDI)是一项新兴的海水淡化技术。其具有工作电压低、脱盐率高、化学品需求低和无二次污染等优点,符合低碳可持续发展的理念[7,8]。CDI脱盐技术基于电化学双电层理论,即通过对CDI电极两端施加不高于2 V的直流电压,所建立的静电场促使溶液中的阴阳离子在电场力的作用下,向与之电荷相反的电极移动并被之吸附,从而实现脱盐[7-9]。因此,电极材料的特性与CDI整体的脱盐性能紧密相关。
近年来,多种多样的碳材料是CDI电极的主要候选电极材料[10]。与碳电极相比,法拉第电极具有更加优异的脱盐容量和电荷效率[10-13]。过渡金属氧化物作为典型的法拉第电极材料,具有制备成本低、电化学活性高且在水溶液中具有良好的适应性等优点[14-16]。氧化锰(MnO2)因其资源丰富、成本低、环境友好、电化学窗口宽、氧化还原位点丰富以及理论比电容高(1 100~1 300 F·g-1),被广泛应用于储能领域[17-19]。此外,MnO2在中性电解质环境中具有极高的化学稳定性[20],因此十分适合作为CDI电极。对MnO2而言,MnO6八面体通过端点或边缘连接,形成隧道或层状结构,使其具有多种晶型,如α-MnO2、β-MnO2、γ-MnO2和δ-MnO2等[19,21,22]。结构、形态和电导率的不同都会影响MnO2的离子储存能力[21]。Yang等人[23]系统研究了1D锰钡矿型α-MnO2,2D水钠锰矿型δ-MnO2和3D尖晶石型λ-MnO2在杂化CDI中的脱盐特性,其中δ-MnO2具有最高9.35 mg·g-1的比脱盐量。此外,该研究还证明低结晶态的α-MnO2和δ-MnO2在进行脱盐时以表面吸附为主。相较于其他MnO2晶型,ε-MnO2中存在更多的结构缺陷,导致其具有高氧化还原反应活性[21],意味着ε-MnO2在脱盐时可能会同时拥有双电层吸附和赝电容反应,从而具有出更优异的脱盐特性。
通过溶剂热反应结合后退火处理制备了具有纳米片状结构的ε-MnO2,系统研究了其电化学性能及CDI脱盐特性。结果表明,当工作电压为1.20 V,流速为40 mL·min-1时,ε-MnO2电极在1 000 μS·cm-1的NaCl溶液中的脱盐比容量高达119.94 mg·g-1。MnO2‖AC CDI系统在循环20圈后,容量保持率为56.82%。
2 材料与实验方法
2.1 材料制备
采用溶剂热反应制备锰氧化物前驱体,随后通过退火及硫酸氧化处理得到ε-MnO2纳米片。首先,将1 mmol Mn(CH3COO)2·4H2O和0.80 g聚乙烯吡咯烷酮(Polyvinyl pyrrolidone,PVP,K30)溶解在80 mL甲醇中,随后将溶液移至100 mL聚四氟乙烯内衬的不锈钢反应釜中,在120 ℃下静置12 h。通过离心分离得到前驱体,将前驱体在650 ℃的空气中退火10 h,随后用40 ℃的稀硫酸处理12 h,得到ε-MnO2纳米片。
2.2 材料表征仪器及参数
采用粉末X射线衍射(XRD,Smart Lab, Japan)分析材料物相,测试管电压和管电流分别为45 kV和200 mA,扫描角度为10°~80°,步长为0.02°。采用扫描电子显微镜(SEM,Hitachi SU500, Japan)和透射电子显微镜(TEM,FEI Talos200s, USA)观察样品的微观形貌特征。采用全自动氮气吸/脱附仪(JW-BK200C,China)测试材料的比表面积和孔径分布。
2.3 电极制备
将活性物质、导电炭黑和聚偏氟乙烯〔(Poly(vinylidenefluoride),PVDF〕(质量比为8∶1∶1)研磨混合后加入N-甲基吡咯烷酮(N-Methylpyrrolidone,NMP)充分搅拌。将所得浆料均匀地涂覆在石墨纸表面,浆料厚度约为100 μm。
2.4 电化学与CDI测试
采用三电极系统测试ε-MnO2的循环伏安(Cyclic voltammetry, CV)、电化学阻抗谱(Electrochemical impedance spectrum, EIS)和恒流充放电(Galvanostatic charge discharge, GCD)。ε-MnO2、Ag/AgCl和Pt分别为工作电极、参比电极和对电极。电解液为1 mol·L-1NaCl溶液。CV测试电压窗口为-1~0 V,GCD测试电压窗口为-1~0 V,EIS测试频率为0.01~106Hz。通过CV曲线,计算电极比电容公式为
(1)
式中C为比电容(F·g-1),i为电流(A),v为扫描速率(mV·s-1),m为工作电极的活性物质质量(g)。
采用批处理模式对ε-MnO2电极进行脱盐测试,其中ε-MnO2电极作为阴极,活性炭(Activated carbon,AC)电极为阳极,测试流程及CDI单元模块构成如图1所示。测试过程中,通过恒压源为CDI单元提供直流电压,蠕动泵控制整个系统中水的流速,电导率仪实时测定溶液的电导率。电极表面均覆盖离子交换膜抑制共离子效应。脱盐容量计算公式为
(2)
式中Γ为脱盐比容量(mg·g-1);C0和Ct分别为测试溶液的初始浓度和最终浓度(mg·L-1);V为NaCl溶液体积(L),实验中V=0.04 L;m为电极活性材料质量(g)。
电荷效率通常用来评价CDI的电能使用效率,计算公式如
(3)
(4)
式中F为法拉第常数(96 485 C·mol-1);M为NaCl的摩尔质量;Q为电荷量(C·g-1),i为电流(A),m为活性物质质量(g)。
在对ε-MnO2‖AC CDI系统进行流速和初始电导率影响的脱盐实验时,采用1 V进行充电,采用0.80 V反向电压进行电极再生。
3 实验结果与讨论
3.1 物相与结构表征
图2(a)是所制备的MnO2的XRD图谱,其全部特征峰与XRD标准卡片中PDF#30-0820(Akhtenskite相MnO2)匹配。特别注意的是,与标准卡片不同,代表(1 0 0)晶面的衍射峰的相对强度更强,表明ε-MnO2的(1 0 0)晶面暴露较多。图2(b)是ε-MnO2的结构示意图,Mn原子与6个O原子形成八面体结构,同时相邻两个八面体连接共同形成层状结构。图2(c)为ε-MnO2等温氮气吸脱附曲线。其呈现出标准的IV型吸附曲线,并具有明显的H3型滞回环,表明材料具有平板狭缝结构。图2(d)是相应的孔径分布图,显示出ε-MnO2存在大量平均孔径为2.68 nm的介孔。根据多点BET法计算,ε-MnO2比表面积为27.53 m2/g。
图3(a)是ε-MnO2的SEM图像,可以看出ε-MnO2整体是由片状结构相互穿插而成,构成了多孔纳米结构,这有利于电解液渗透。图3(b)的TEM图像显示片状结构长度为200~300 nm。图3(c)是ε-MnO2的高分辨TEM图像,图中0.24 nm的晶格间距与ε-MnO2的(1 0 0)晶面吻合。此外,从图3(d)局部放大得到的快速傅里叶变换图像(Fast Fourier Transform,FFT)可以观察到ε-MnO2的(1 0 0)和(1 0 3)晶面的衍射斑点,如图3(e)所示。图3(f)是ε-MnO2的高角环形暗场图像(High-Angle Annular Dark Field,HAADF)及Mn、O的元素映射图,表明Mn和O元素在纳米片上分布非常均匀。
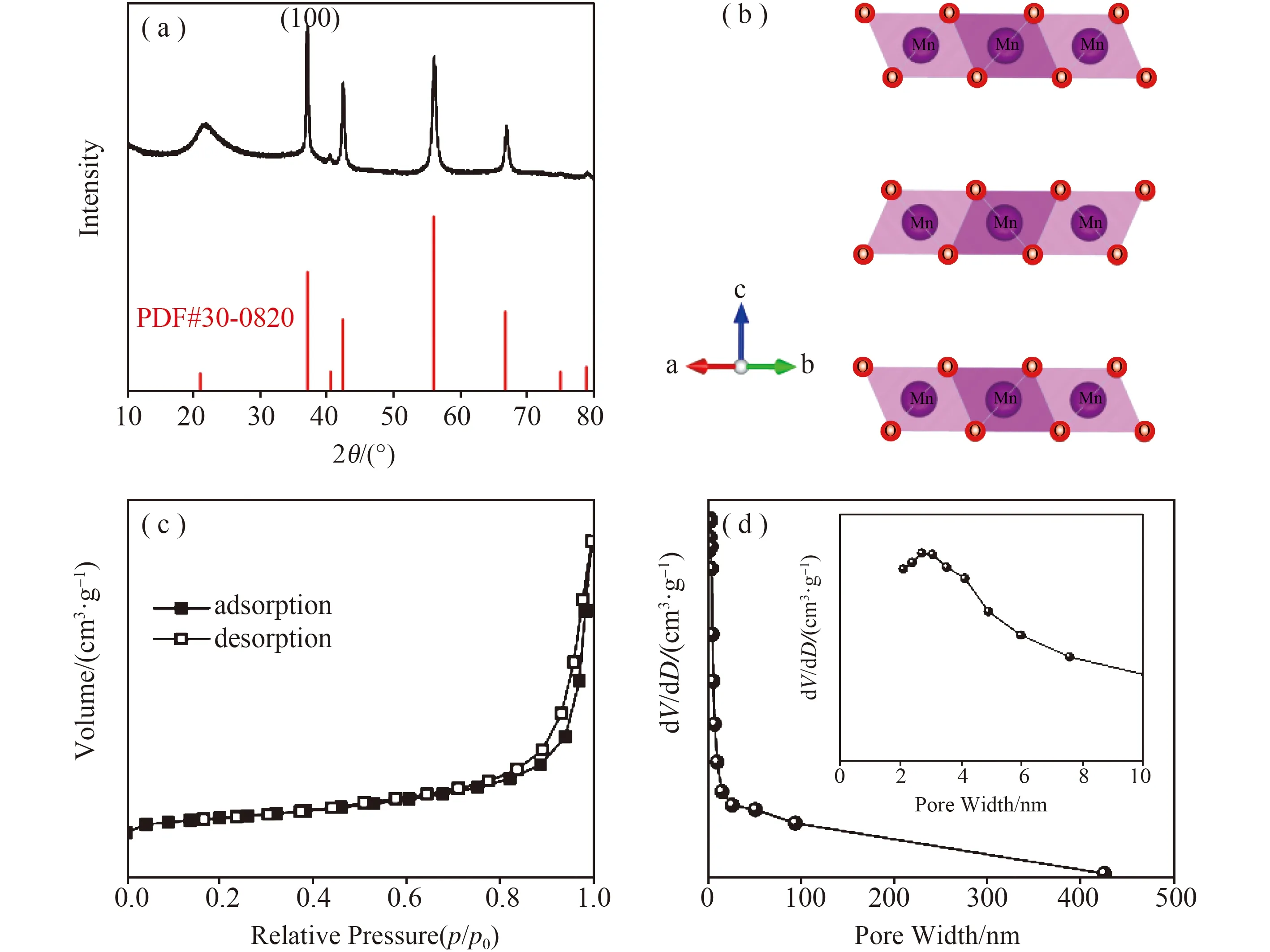
图2 MnO2的(a)XRD图谱;(b)结构示意图;(c)等温N2吸脱附曲线;(d)孔径分布图

图3 ε-MnO2的(a)SEM图;(b)TEM图;(c,d)高分辨TEM图;(e)FFT图;(f)HAADF及Mn、O的元素映射图
3.2 电化学与CDI测试结果
通过循环伏安法测试电极材料在-1~0 V电压窗口下的电化学行为,结果如图4(a, b)所示。在-1~0 V电压窗口中,CV曲线呈现对称的菱形,表明ε-MnO2在该电压窗口下发生了赝电容行为,且具有良好的可逆性。经计算,比电容为119.51 F·g-1。在水系电解质中,基于MnO2的充放电机制分为表面离子吸附和体插层过程[17],由式(5)和(6)表示:
(MnO2)surface+ C++ e-=(MnO2-C+)surface,
(5)
(MnO2) + C++ e-= MnOOC,
(6)
式中C+为H+和碱金属离子(K+、Na+和Li+)。
为了探究ε-MnO2电化学行为中扩散过程和电容行为的比率,通过公式(7)计算
i=k1v+k2v1/2,
(7)
式中k1v和k2v1/2分别为表面电容贡献和扩散行为贡献。如图4(c, d)所示,在10 mV·s-1扫速下,电容贡献占比为16.59%。此外,当扫速为1、5、10、50和100 mV·s-1时,电容贡献占比分别为11.41%、16.77%、16.59%、34.05%和52.63%,说明基于氧化还原反应的电化学行为占据主导地位,这为ε-MnO2实现高容量脱盐奠定了基础。

图4 ε-MnO2在(a)1 mV·s-1扫速下和(b)不同扫速下的CV曲线;ε-MnO2在(c)10 mV·s-1下的电容贡献率和(d)不同扫速下的电容贡献率;ε-MnO2的(e)EIS图谱和(f)不同电流密度下的GCD曲线
图4(e)为EIS图谱。拟合结果显示,ε-MnO2电极在1 mol·L-1NaCl中的电荷转移电阻为134.40 Ω,电极电解质界面阻抗为6.01 Ω。低频区直线与x轴夹角约为45°,证明其具有良好的离子扩散速率[24]。如图4(f)所示,GCD曲线没有明显的充放电平台。随着电流密度的减小,充放电时间逐渐增加。当电流密度为0.50 A·g-1时,充电和放电比容量分别为11.46和7.57 mA·h·g-1,库伦效率为66.06%,较低的库伦效率和放电过程中较明显的IR降与ε-MnO2较大的电阻有关。
对ε-MnO2‖AC系统在不同电压、不同流速和不同初始电导率下进行脱盐测试,结果如图5所示。图5(a)为不同工作电压下溶液电导率随时间的变化。当施加工作电压后,溶液中的Na+和Cl-被迅速吸附在电极表面,使溶液电导率呈对数式下降。而随着充电持续,电极逐渐达到饱和。相应的即时电流和电荷效率如图5(b, c)所示。充电电流随时间逐渐降低,与电导率变化趋势相同。伴随着工作电压的增加,系统的电荷效率逐渐增加。当电压为1.20 V时,电荷效率为66.61%。电荷的损失主要是由材料的高电荷转移电阻引起的。不同条件下脱盐持续60 min时,ε-MnO2‖AC系统的脱盐量见图5(d~f)。随着工作电压从0.80 V增加至1.20 V,脱盐量从86.94 mg·g-1增加至119.94 mg·g-1。流速对系统脱盐容量也有一定影响。当流速为40 mL·min-1时,系统脱盐容量最大。当流速过大时,离子吸附的不充分导致脱盐容量下降。进一步地,伴随着溶液初始电导率从500 μS·cm-1上升至1 000 μS·cm-1时,系统脱盐容量增加较为明显。但是,当溶液初始电导率为2 000 μS·cm-1时,脱盐容量没有进一步增加,意味着ε-MnO2的脱盐容量基本达到了吸附极限。随后对ε-MnO2‖AC系统在1.20 V电压下,初始电导率为1 000 μS·cm-1的NaCl溶液中进行循环性能测试,结果如图5(g)所示。随着循环次数的增加,ε-MnO2的脱盐容量逐渐减小,首圈脱盐容量为119.94 mg·g-1,20次循环后,脱盐容量降至68.15 mg·g-1,容量保持率为56.82%。
基于以上实验结果,ε-MnO2电极超高的脱盐容量可以归因于以下两个方面。特殊的片状结构和均匀的孔径分布为离子传输提供了快速通道,并且较高的比表面积提供了丰富的吸附位点。基于氧化还原反应的电化学行为占据主导地位,使ε-MnO2电极在1 mV·s-1扫速下具有119.51 F·g-1的高比电容。活跃的赝电容行为是ε-MnO2电极具有高脱盐容量的主要原因。为进一步说明ε-MnO2电极优异的脱盐特性,表1总结对比了不同MnO2电极的脱盐容量。

表1 不同MnO2电极的脱盐性能对比
尽管ε-MnO2电极具有超高的脱盐容量,但在随后的循环测试中发现,经过20次循环后,ε-MnO2电极的脱盐容量仅能保持初始值的56.82%。进一步地,对循环测试后的电极进行XRD表征发现,对应于(1 0 0)、(1 0 1)、(1 0 2)和(1 1 0)晶面的衍射峰消失〔图6(a)〕,表明循环过程中频繁的赝电容反应使得ε-MnO2向非晶化转变。图6(c)和6(d)分别是ε-MnO2电极的初始和20次循环后的形貌。循环后的ε-MnO2电极发生结构坍塌现象,片状结构转变为针状结构,与XRD表征结果一致。非晶态的转化以及结构的破坏使ε-MnO2电极的脱盐容量急剧下降。图6(b)所示为20次循环后ε-MnO2电极的EIS图谱,拟合结果显示电荷转移电阻降低至17.77 Ω。

图6 ε-MnO2电极(a)初始和20次循环后的XRD图谱;(b)20次循环后的EIS;(c)初始形貌和(d)20次循环后的形貌
3 结论
通过溶剂热反应后的热处理,制备了大小为200~300 nm的ε-MnO2纳米片,研究了其电化学性能及CDI脱盐特性。电化学测试结果显示,ε-MnO2为典型的赝电容材料,具有良好的循环可逆性,在1 mV·s-1扫速下具有119.51 F·g-1的比电容,其中88.59%的比电容由基于氧化还原反应的赝电容过程提供;GCD测试结果显示,ε-MnO2在0.50 A·g-1电流密度下,充放电比容量分别为11.46和7.57 mA·h·g-1,库伦效率为66.06%;EIS测试结果显示,ε-MnO2的电荷转移电阻为134.40 Ω,电极电解质界面阻抗为6.01 Ω。系统的CDI测试结果表明,ε-MnO2‖AC在1.20 V电压下,初始电导率为1 000 μS·cm-1的NaCl溶液中运行60 min具有119.94 mg·g-1的脱盐容量,经20次循环后容量保持率为56.82%。以上结果说明,ε-MnO2特殊的片状结构有利于盐离子的传输和扩散,提高了脱盐动力学特性;优异的赝电容反应使ε-MnO2电极可以存储更多的盐离子,从而表现出超高的脱盐容量。进一步,循环过程中的结构坍塌是脱盐容量衰减的主要原因。

