早产儿视网膜病变风险预测模型研究进展
张少伟,曹淑卿
1.天津中医药大学,天津 301600;2.天津市眼科医院
早产儿视网膜病变(retinopathy of prematurity,ROP)是一种因视网膜未成熟引起异常增殖性血管形成的疾病[1]。有研究报道,接受早产儿视网膜病变筛查的早产儿中视网膜病变的发病率为15.9%~43.0%[2-3]。早产儿视网膜病变是全球范围内导致儿童失明和视力障碍的主要原因,高收入国家儿童失明可归因于早产儿视网膜病变的比例不足10%,而我国属于发展中国家,这一比例高达40%[4]。早期筛查和及时治疗可以预防早产儿视网膜病变所致的视力损失,因此,有必要对具有视网膜病变高危因素的早产儿实施筛查和治疗来控制早产儿视网膜病变[5]。由于现行筛查标准存在资源浪费和加重家庭经济负担等方面的不足,学者们致力于风险预测模型的开发及验证。风险预测模型是用多变量风险因子来预测不良事件发生的概率,评估疾病发生可能性的工具[6],具有较好的预测能力,在早产儿视网膜病变预防方面起着重要作用。因此,现从早产儿视网膜病变危险因素和风险预测模型开发及预测能力方面对早产儿视网膜病变风险预测模型相关研究进行综述,为构建适合我国早产儿视网膜病变风险的预测模型提供参考。
1 早产儿视网膜病变危险因素
早产儿出生时胎龄和出生体重是公认的早产儿视网膜病变的主要危险因素。有研究表明,胎龄小及出生体重低的患儿,其视网膜神经和血管发育不成熟,易致视网膜损伤[7-8]。此外,早期胰岛素样生长因子1(insulin-like growth factor 1,IGF-1)长时间缺乏往往会引起严重早产儿视网膜病变。IGF-1 是一种具有较强促生长作用的多肽类物质,是儿童期的重要生长因子。血清IGF-1 水平低下会抑制其对视网膜血管内皮生长因子的激活,使新生儿出生后早期视网膜血管生长不良,外在表现为体重增加缓慢。其他危险因素还包括输血、机械通气、贫血、呼吸窘迫、呼吸困难和健康状况不佳[9-10]。
2 构建早产儿视网膜病变风险预测模型的必要性
目前,早产儿视网膜病变指南的筛查标准包括出生体重和出生时胎龄,比如美国标准为出生体重<1 501 g或出生时胎龄≤30 周的早产儿需要接受筛查,使用筛查标准虽具有较高的敏感性,但特异性低[11]。敏感性反映模型识别真阳性病人的能力,特异性指模型识别不需要接受筛查的早产儿的能力,两者均为评价风险预测模型性能的常用指标。另外,加拿大[12]、美国[13]和英国[14]等国家的大型研究结果显示,接受筛查的早产儿中需进行激光手术治疗的不到5%。上述研究结果提示现行筛查标准会产生许多不必要的筛查,造成资源浪费。高收入国家平均每次早产儿视网膜病变筛查成本为106~250 美元[15],会加重家庭经济负担。研究表明,视网膜筛查相对耗时,导致早产儿在新生儿重症监护病房的住院时间延长和早产儿的父母焦虑[16-17]。因此,开发预测性能良好的风险预测模型具有重要的临床意义,可以提高早产儿视网膜病变筛查的敏感性,改善筛查特异性以减少接受筛查的早产儿数量,使医疗资源得到合理分配。
3 早产儿视网膜病变风险预测模型
目前常用的早产儿视网膜病变风险预测模型分别为体重胰岛素样生长因子新生儿早产儿视网膜病变(WINROP)模型、费城儿童医院早产儿视网膜病变(Children's Hospital of Philadelphia ROP,CHOPROP)模型、出生后生长早产儿视网膜病变(Postnatal Growth ROP,G- ROP)模型、科罗拉多早产儿视网膜病变(Colorado ROP,CO-ROP)模型和数字早产儿视网膜病变(Digital ROP-Birth,DIGI ROP-Birth)模型,各模型均具有各自的特点。从模型预测性能和研究设计中筛查标准操作的难易程度、样本量大小等多方面分析其优势和局限性。一般认为,良好的预测模型预测严重早产儿视网膜病变的敏感性较强并可大幅减少早产儿筛查次数。
3.1 WINROP
Löfqvist 等[18]基于对IGF-1 和早产儿视网膜病变的研究开发了一种名为WINROP 的累计偏差模型,可根据早产儿出生体重、出生时胎龄和出生后体重增加率来预测严重早产儿视网膜病变,并能极大地减少需要筛查的早产儿数量。WINROP 模型最初在开发研究中识别严重早产儿视网膜病变患儿的敏感性为100%,但在美国一项多中心验证研究中敏感性降低[19],在中国一项纳入432 例早产儿的研究中敏感性只有56%[20]。临床使用WINROP 模型需要每周测量体重和血清IGF-1 水平,模型计算复杂导致信息不透明,为改善这一不足,研究人员开发了线上程序,允许用户在线访问,使临床实用性得到了提高。目前,WINROP 模型已在多个国家进行了外部验证,敏感性不一,预测性能不稳定,因此没有取代传统筛查,该模型是第一个将出生后体重增加纳入早产儿视网膜病变的预测模型,为减少早产儿筛查数量提供了一种新可能。
3.2 CHOPROP
2011 年,Gil 等[21]开发了需要输血的早产儿视网膜病变(Premature Infants in Need of Transfusion ROP,PINTROP)模型,这是一种基于Logistic 回归的预测模型,筛查标准包括出生体重、出生时胎龄和体重增加率。该模型是使用369 例体重<1 kg 的早产儿随机输血试验数据建立的,每周评估,以预测早产儿视网膜病变的风险,在风险大于预定的警报水平时提示筛查。PINTROP 模型正确预测了所有需要激光治疗的早产儿,同时将需要筛查的早产儿数量减少了30%。但由于PINTROP 模型筛查对象为需要输血的早产儿,不具有普适性,因此,Gil 等[22]在2012 年用与PINTROP模型相同的建模方法在PINTROP 模型基础上开发了CHOPROP 模型。该模型用于预测1 型或2 型早产儿视网膜病变,使用出生体重、出生时胎龄和每日体重增加率这3 个指标预测,修正了模型系数和警报风险级别,CHOPROP 模型预测1 型早产儿视网膜病变的敏感性为100%,同时将需要筛查的早产儿数量减少了49%。之后,CHOPROP 模型正确地预测了445 例意大利队列中所有患有1 型早产儿视网膜病变的早产儿[23],研究不足在于样本量小。还有学者分别于2019年和2021 年进行了外部验证,使用不同的截断值均得到了100%的敏感性,使接受筛查的早产儿分别减少了1/2 和1/3[10,18]。CHOPROP 模型可用于筛查极低体重早产儿,因为此因素在模型中权重很大,局限性在于样本量太小,使研究结果可信度降低。外部验证结果显示了模型在发展中国家有良好的预测潜能,但由于验证队列样本量较小,在临床推广应用之前仍需开展多中心研究去检验模型的可行性。
3.3 G-ROP 模型
Gil 等[19]采用回顾性研究方法对在美国和加拿大的30 家医院接受早产儿视网膜病变筛查的7 483 例早产儿进行队列研究,以期在这个多样化的多中心队列中验证CHOPROP 模型,结果显示模型预测1 型早产儿视网膜病变早产儿的敏感性为98.5%,将需要筛查的早产儿数量减少了34.3%。如果为了涵盖所有1 型早产儿视网膜病变病例而降低临界点,那么只有6.8%的早产儿不需要筛查。由于模型敏感性没达到预期且高达2.5%的1 型或2 型早产儿视网膜病变早产儿可能被遗漏,Gil 等[2]于2018 年将CHOPROP 模型更新为G-ROP,新模型包括6 个筛查标准:体重<1 051 g;出生时胎龄<28 周;出生后第2 个10 d(10~19 d)体重增加<120 g;第3 个10 d(20~29 d)体重增加<180 g;第4个10 d(30~39 d)体重增加<170 g;或脑影像筛查(B超、计算机断层扫描或磁共振成像)诊断为脑积水。更新标准后模型预测1 型早产儿视网膜病变早产儿的敏感性为100%,同时将需要筛查的早产儿数量减少了30.3%。此模型开发样本量较大,有助于解决数据过度拟合所致的预测能力偏高问题,可提供较准确的敏感性估计。因G-ROP 模型的开发采用多中心研究且模型显示出了良好的预测能力,之后多个国家学者对其进行了外部验证,见表1。使用原筛查标准或调整后标准均可达到100%的敏感性并使接受筛查的早产儿数量显著减少,模型在外部验证队列中表现良好,未来可考虑对模型进行本土化验证后在临床推广。
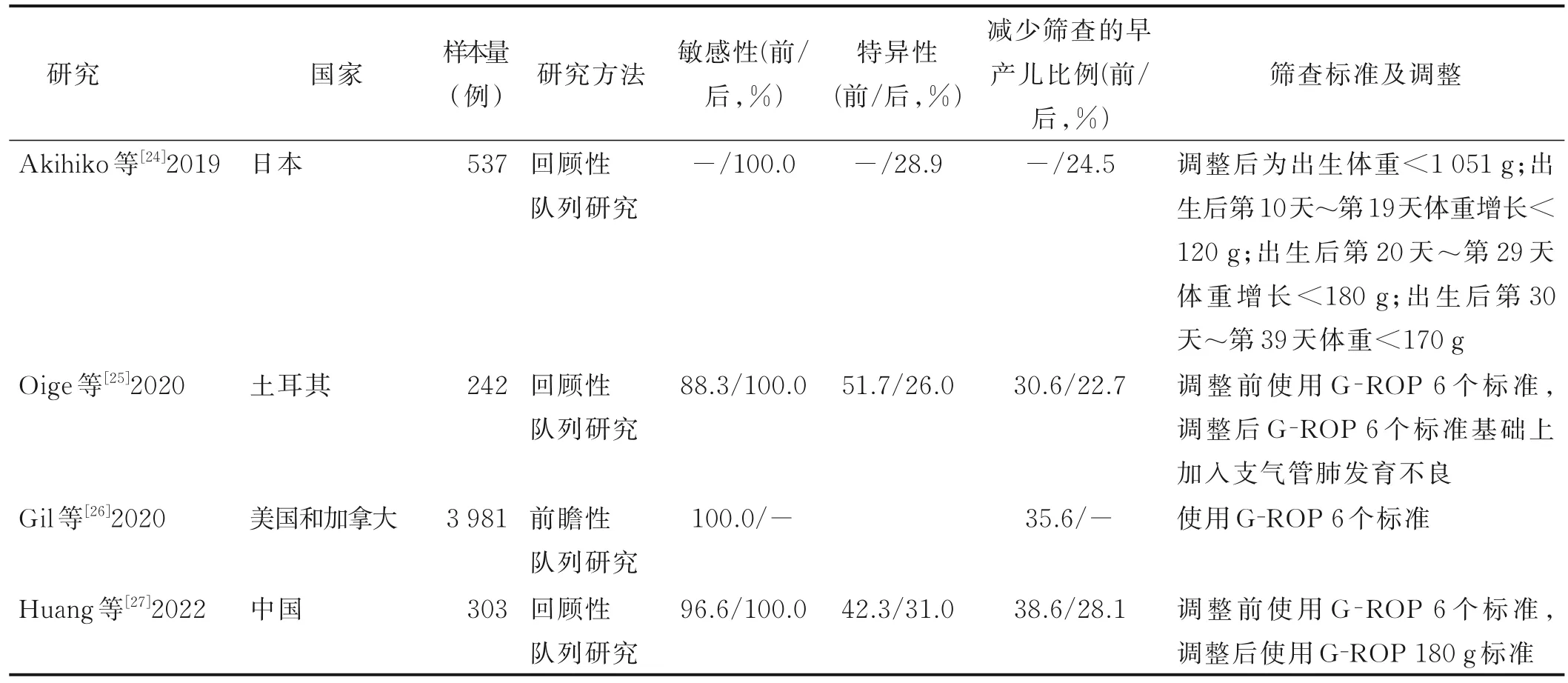
表1 G-ROP 模型外部验证
3.4 CO-ROP 模型
Cao 等[28]于科罗拉多州对499 名新生儿进行了一项回顾性队列研究,构建了CO-ROP 模型。学者将新生儿细分为3类:高级别(1型或2型早产儿视网膜病变)、低级别(早产儿视网膜病变不符合1 型或2 型标准)和无早产儿视网膜病变,使用标准Logistic 回归分析每周体重,确定最能预测早产儿视网膜病变发展的年龄,最终研究建议对出生时胎龄≤30 周、出生体重≤1 500 g、出生至1 月龄净增重≤650 g 的早产儿进行早产儿视网膜病变筛查。与2013 年的筛查指南相比,CO-ROP模型将筛查的早产儿总数减少了23.7%,对高级别早产儿视网膜病变的敏感性为100%。2016 年,Cao 等[29]对该模型进行了外部验证,纳入了858 例早产儿,结果显示,模型对所有分级的早产儿视网膜病变的敏感性为95.0%,使接受筛查的早产儿总数减少了23.9%。在验证队列中,敏感性降低。Emily 等[30]于2018 年在一项更大的队列中对CO-ROP 模型做了外部验证,队列含6 351 例早产儿,验证结果为模型检测重度早产儿视网膜病变的敏感性为96.9%,特异性为40.9%,可以减少26.1%需要进行早产儿视网膜病变筛查的早产儿。如前所述的任一模型均需计算体重增加率,意味着医护人员需要对新生儿连续监测,时间跨度为10周甚至更长,每周计算也会加重医护人员工作负担。CO-ROP模型将早产儿在特定时间点的体重增加量作为筛查标准纳入风险预测模型,操作省时,但使用该预测模型会漏掉3.1%重度早产儿视网膜病变的早产儿。从以上两项外部验证结果来看,模型敏感性有待提高,在临床使用之前有必要进行额外的验证,进一步探索其对临床结局的预测能力。
3.5 DIGIROP-Birth 模型
前4 种模型预测需使用出生以后的指标,不能及时预测。2019 年,Aldina 等[31]在瑞典进行了一项大型回顾性队列研究开发了DIGIROP-Birth 模型,学者对6 947 例出生时胎龄在24~30 周早产儿的时变数据(产后年龄、胎龄、性别、出生体重和重要交互作用)进行了泊松回归分析,纳入了出生时胎龄、性别和出生体重这3 个度量标准。该模型增加了受试者工作特征(ROC)曲线下面积这一评价模型预测性能的综合性指标。ROC 曲线下面积为0.50~1.00,模型所得数值越大,表示预测性能越好[32]。模型已做了内部和外部(美国和欧洲队列)验证,内部验证的ROC 曲线下面积为0.90,美国和欧洲外部验证ROC 曲线下面积分别为0.87 和0.90。DIGIROP-Birth 模型显示出了100%的敏感性和19.0%的特异性,调整截断值后敏感性为99.0%,特异性为53.8%,与更新的G-ROP 模型的预测能力相似。由于该模型可以作为风险计算器在线访问并在大型多中心的队列中显示出良好的预测性能。广州南方医科大学珠江医院Chen 等[33]采用回顾性研究方法在接受早产儿视网膜病变筛查的732 例早产儿中获取了442 例符合条件的早产儿数据对DIGIROP-Birth 进行外部验证,结果显示ROC 曲线下面积为0.63,敏感性51.6%,特异性85.4%,将呼吸暂停和脑室出血作为危险因素修正模型后,敏感性和特异性分别提高到95.7%、98.5%。之后Aldina 等[15]在瑞典又对模型做了外部验证,模型的敏感性、特异性、ROC 曲线下面积分别为96.5%、49.9%和0.93。DIGIROP-Birth 模型仅使用出生特征预测早产儿视网膜病变风险并可在线访问,方便实用,但受缺乏出生体重参考算法的限制,不能预测胎龄小于24 周的早产儿。该模型预测性能及临床实用性均较好,但我国进行的外部验证结果显示纳入出生后风险因素会提高其适用性。
4 早产儿视网膜病变风险预测模型比较分析
从预测对象分析,尽管G-ROP 模型被开发出来时,多个国家修正其模型系数后敏感性均能达到100%并能大幅减少接受筛查的早产儿数量,但WINROP 模型、CHOP-ROP 模型和G-ROP 模型都被设计为仅识别高等级早产儿视网膜病变,而对低等级早产儿视网膜病变的敏感性分析有限,CO-ROP 模型则纳入了低级别视网膜病变的早产儿。研究表明,患有低度视网膜病变的早产儿虽然不需要激光光凝治疗,但屈光不正(特别是近视)、斜视和弱视的风险增加,CO-ROP 模型通过划分早产儿等级解决了这一问题[28]。DIGIROP-Birth模型预测对象为出生时胎龄在24~30 周的早产儿,使用具有一定的局限性。
从研究设计分析,在当前大数据时代背景下,WINROP 模型和DIGIROP-Birth 模型可在线访问,使用便捷,线上程序在未来有更广阔的开发空间。仅有一项外部验证研究[30]为前瞻性研究,其余均为回顾性队列研究。回顾性研究虽资料易获取、耗时少,但会出现相关资料缺失情况,若处理不当,会影响模型预测性能;前瞻性研究可以明确因在前果在后,使用统一的诊断和评判标准,获得较为全面的临床资料,但研究耗时且样本失访率高。
从纳入标准分析,WINROP 模型和CHOP-ROP模型筛查标准为出生时胎龄、出生体重和出生后体重增加率,G-ROP 模型在这3 个指标基础上加了脑影像筛查(B 超、计算机断层扫描或磁共振成像)诊断为脑积水,这3 个模型需连续监测,每周测量,相对耗时;而CO-ROP 模型使用出生时胎龄、出生体重和出生至1 个月龄体重增加量,DIGIROP-Birth 模型使用出生时胎龄、出生体重和性别预测早产儿视网膜病变,因此,仅使用出生特征的DIGIROP-Birth 模型和不需动态监测的CO-ROP 模型在易操作性方面较好,使用简便,节省人力资源。
5 小结
综上所述,风险预测模型已成为早产儿视网膜病变预防测重要筛查工具,早产儿视网膜病变风险预测模型指标一般包含出生体重、出生时胎龄和增重率等,建模方法大多数采用传统数学模型,当前机器算法在风险预测模型领域已成为研究热点,但早产儿视网膜病变风险预测模型在此方面仍处于起步阶段,因此本研究没有做过多阐述。学者们致力于模型开发和外部验证,修正模型系数或增加新变量以提高模型预测性能和减少需要接受筛查的早产儿。使用预测模型可提高传统筛查的特异性,尽可能保护早产儿身心健康,同时也可一定程度上减轻家庭经济负担。由于不同模型的样本人群、样本量和研究设计差异较大,在模型可以安全地应用于临床实践之前,需要本土、大规模的样本去验证其预测能力,若模型敏感性未能达到100%,或未进行大规模、多中心外部验证,建议模型仅可作为当前筛查指南的辅助方法。

