拷贝数变异测序在先天性心脏病胎儿基因组拷贝数变异筛查中的应用
杨水艳,肖艳华,曾蓓,张明洁
(焦作市妇幼保健院 孕产保健科,河南 焦作 454000)
先天性心脏病(congenital heart disease,CHD)是指胎儿时期心血管发育异常或障碍导致的心血管畸形,是临床常见的出生缺陷性疾病[1]。CHD在出生缺陷中占比高达26.7%,在活产新生儿中的发病率高达0.8%~1.0%,是新生儿非感染性死亡的首要原因[2],严重威胁新生儿健康。基因组拷贝数变异(copy number variation,CNV)是指由基因组重排所致的长度1 000 bp以上基因片段的拷贝数增减,是遗传变异的重要因素,也是造成CHD的重要原因之一[3]。拷贝数变异测序(copy number variation sequencing,CNV-seq)技术是指基于高通量测序技术对样本DNA进行全基因组范围的低深度CNV测序[4],具有检测范围广、阳性检出率高、通量高、检测速度快、成本低、操作简便等优点,故而近年来被广泛应用于胎儿的产前诊断[5]。鉴于此,本研究特采用CNV-seq技术对中孕超声筛查出的胎儿CHD孕妇行遗传学病因诊断,以期为胎儿CHD孕妇的干预提供指导,提升生育质量。
1 资料与方法
1.1 研究对象选取2019年12月至2022年1月在焦作市妇幼保健院超声筛查出的77例胎儿CHD的中孕期孕妇作为研究对象,孕妇年龄21~39岁,平均(29.53±4.28)岁;初产妇59例,经产妇18例;孕周17~26周,平均(21.52±3.48)周。本研究经医院医学伦理委员会批准同意。(1)纳入标准:①为自然受孕、单胎孕妇;②孕周在14~27周;③经中孕期超声筛查诊断为胎儿CHD;④孕妇签署本研究知情同意书。(2)排除标准:①合并有严重的妊娠高血压、糖尿病、甲状腺功能障碍等疾病者;②胎儿宫内窘迫、阴道大出血者;③异位妊娠者;④有精神障碍疾病者;⑤具有宫内感染史、致畸物质接触史的孕妇。
1.2 超声诊断胎儿CHD的方法孕妇在孕中期(14~27周)时,采用彩色多普勒超声诊断仪(Voluson E10)进行CHD筛查。孕妇取仰卧位,二维超声探头频率调节至3~5 MHz,四维超声探头频率调节至2.0~6.0 MHz。先参考常规心脏诊断模式对胎儿腹部行横切,调整并获取胎儿标准四腔心切面,观察胎儿心脏位置、形态、大小是否正常,心房、心室间隔的完整性,二尖瓣与三尖瓣的形态、大小、位置是否正常,记录胎儿肺动脉、动脉管等发育情况与胎儿心律、心率。对孕妇行四维超声检查,以四腔心切面为初始平面,按照灰阶二位方式收集胎儿心脏房、室、腔、血管、血流等的声像信息。若发现异常,则通过超声心电图复查,由2名及以上主治医生共同确认。
1.3 胎儿CNV-seq检测在超声筛出的胎儿CHD孕妇知情并自愿行CNV-seq检测的前提下开展以下检查。(1)DNA提取:妊娠未终止者,超声引导下经腹羊膜腔穿刺抽取羊水5 mL,采用纯化柱法(QIAamp DNA Blood Mini Kit,德国QIAGEN公司)提取羊水细胞基因组DNA;流产胎儿取大腿内侧直径3 cm左右的皮肤肌肉组织,采用磁珠法提取试剂盒(Blood DNA Midi Kit D3494,美国OmegaBio-tek公司)与自动DNA提取设备(艾本德中国有限公司)提取DNA,操作流程严格按照说明书进行。(2)CNV-seq检测:使用商品化CNV检测文库构建试剂盒(北京贝瑞和康生物技术有限公司),通过本科室illumina测序平台NextSeq 500进行CNV检测,测序类型SE45(单端测序,读长45 bp),平均测序深度0.1X。人类基因组参考序列选择GRCh37[加州大学克鲁兹分校主办基因组检索数据库(UCSC),http://genome.ucsc.edu/cgibin/hgGateway],检测分析出分辨率为100 kb以上的CNVs。(3)CNV致病性分析:主要参考人群多态性数据库(DGV,http://dgv.tcag.ca/dgv/app/home)、病例数据库(DECIPHER,http://decipher.sanger.ac.uk)和在线人类孟德尔遗传数据库(OMIM,http://omim.org),同时参考基因剂量效应数据库(ClinGen,https://www.ncbi.nim.nih.gov/projects/dbvar/clingen)分析拷贝数缺失、重复。CNV可根据性质分为良性、可能良性、不确定意义(variant of uncertain significance,VOUS)、可能致病性和致病性CNV[6]。
1.4 染色体核型分析在孕妇知情同意前提下,对行羊水穿刺检查的孕妇同时抽取羊水10 mL,离心收集胎儿羊水细胞并接种于5 mL羊水培养基上,置于含体积分数为5%二氧化碳的37 ℃恒温箱内培育5~7 d,获取细胞之前2 h加入秋水仙碱10 μL,随后依次经过低渗、固定、制片、G显带染色,常规分析30个分裂相,嵌合体分析50~100个分裂相。
1.5 妊娠结局随访对孕妇随访至妊娠终止或胎儿娩出,在孕妇知情同意的前提下,流产胎儿均通过尸体解剖诊断心脏状态,活产新生儿通过超声心动图检查心脏状态,上述诊断结果作为CHD诊断“金标准”。
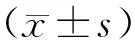
2 结果
2.1 中孕期筛查胎儿CHD发生情况及妊娠结局中孕超声筛查的77例胎儿CHD的超声诊断结果见表1,其中室间隔缺损占比最高,孕妇均完成随访。其中13例选择直接流产,64例选择羊水穿刺,经随访此64例中最终有12例选择引产,52例选择继续妊娠。经尸检或活产后超声心动图检查发现有74例被证实为胎儿CHD,中孕超声诊断CHD的准确率为96.10%(74/77)。
2.2 染色体核型分析74例胎儿CHD孕妇中共有61例行羊水穿刺后染色体核型分析检查(37例在焦作市妇幼保健院检查,24例在外院检查)。共检出8例异常,检出率为13.11%(8/61)。其中有5例染色体数目异常:核型为47,XN,+18者2例;47,XN,+13者1例;45,X,del(18)者1例,47,XXY者1例;2例染色体异位:46,XN,t(4;7)(q31.1;q11.2)1例;46,XN,t(11;20)(q13;p11.2)1例;1例染色体倒位:46,XN,inv(4)(p15.2q31.1) 。典型染色体核型图见图1。
2.3 CNV-seq分析CHD胎儿CNV的结果74例胎儿CHD孕妇均行胎儿基因组CNV-seq检查,其中45例在焦作市妇幼保健院检查(37例行羊水穿刺后胎儿基因组CNV-seq检查,8例行流产后胎儿基因组CNV-seq检查),29例在外院检查(24例行羊水穿刺后胎儿基因组CNV-seq检查,5例行流产后胎儿基因组CNV-seq检查),共检出异常CNV 13例,检出率为17.57%(13/74),包括致病性CNV 11例,可能致病性CNV1例,VOUS 1例。其中61例行羊水穿刺染色体核型分析的孕妇胎儿基因组CNV-seq检查共检出11例CNV异常,包括10例致病性CNV(5例染色体数目异常、2例基因微重复、3例基因微缺失)、1例VOUS(基因微缺失),其中5例染色体数目异常与染色体核型分析结果一致;余13例仅在流产后行胎儿基因组CNV-seq检查的孕妇中共检出2例CNV异常,包括1例致病性CNV(基因微缺失)、1例可能致病性CNV(基因微重复)。见表2、3。典型的CNN-seq检测结果见图2。
表1 中孕超声诊断结果

a为47,XN,+18;b为47,XN,+13;c为45,X,del(18);d为47,XXY

表2 11例被羊水穿刺后CNV-seq检出基因CNV的CHD胎儿CNV-seq结果

表3 2例流产后CNV-seq检出基因CNV的CHD胎儿CNV-seq结果
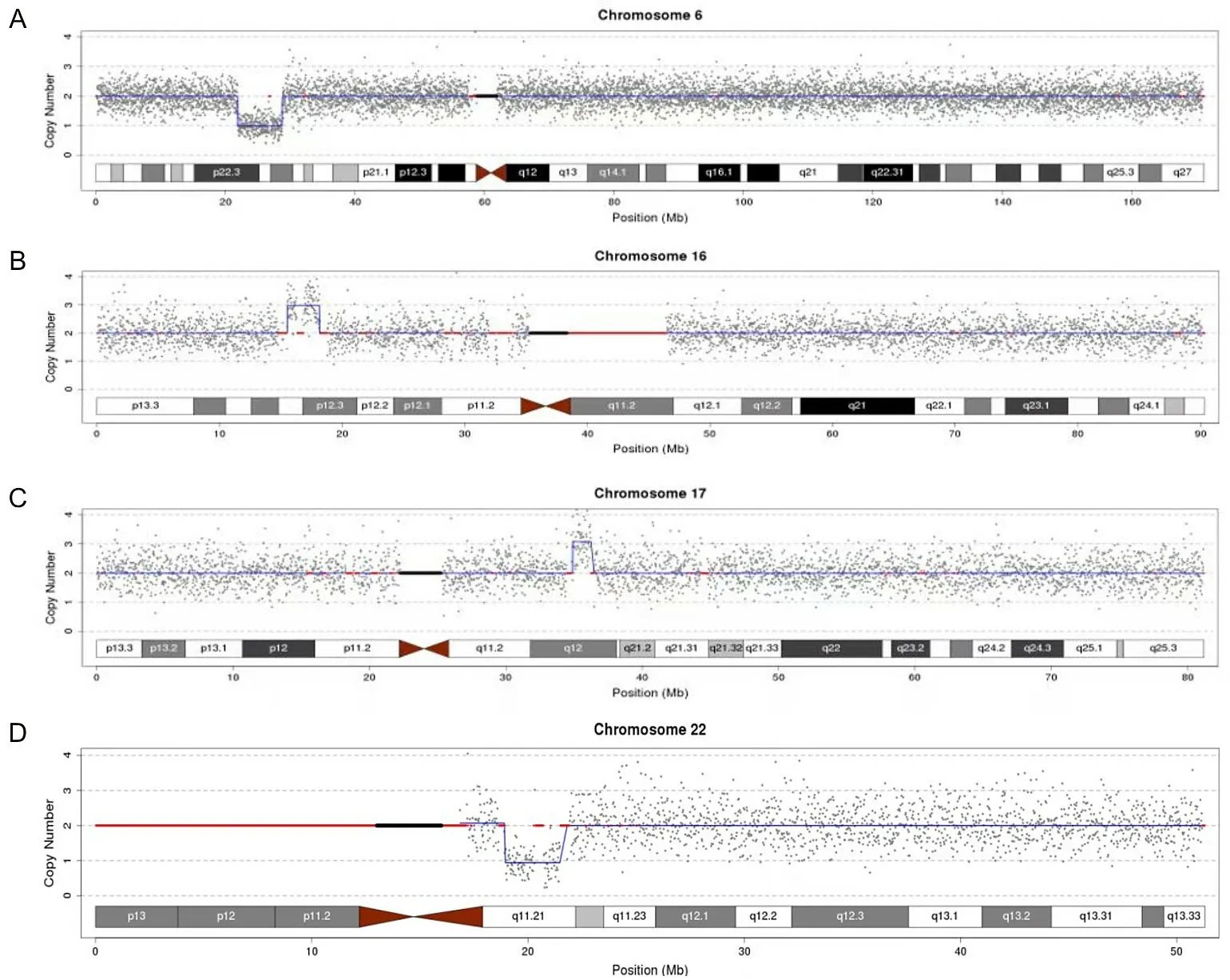
A为6号染色体微缺失;B为16号染色体微重复;C为17号染色体微重复;D为22号染色体微缺失。
3 讨论
CHD是一类在胎儿中表现出高度异质性的先天性疾病,病因复杂,诊断困难,其中基因组CNV是其重要的致病因素之一[7]。CNV主要包括基因组缺失、插入、重复和复杂的多位点变异等表现形式,可通过扰乱基因活性、剂量、表达等方式导致CHD[8],尤其致病性CNV会造成胎儿不良预后,故在孕期对胎儿CHD孕妇做CNV筛查对预防出生缺陷具有重要的临床意义。目前,染色体核型分析仍然是CHD胎儿产前诊断的“金标准”,可检测出染色体的数目异常与大的结构变化,但由于其具有检测周期较长、漏诊率高、对10 Mb以下的微缺失/重复无法检出等不足,检测的局限性也比较明显[9-10],故探讨更准确高效的CNV筛查技术仍然是临床研究的重点方向。
超声检查是通过观察胎儿心脏的位置、形态、大小、结构、不同的切面构造、血流等方面的特征对胎儿心脏是否异常做出较为准确的判断,其为无创、安全、高效的孕期CHD筛查方法,在临床上应用广泛[11]。本研究对中孕超声诊断为胎儿CHD的77例孕妇随访到妊娠结局,其中有74例被证实为胎儿CHD,以ASD为主,超声诊断准确率为96.10%(74/77),略高于谢彩丽等[12]报道的92.17%的结果,分析原因,可能是由于不同孕周胎儿的心脏发育状态差别大,CHD特征在不同胎儿中的异质性较大,噪声信号造成伪像、母体的腹壁瘢痕、羊水量异常等因素干扰诊断,故超声诊断存在误诊现象[13]。
本研究显示,74例被证实为胎儿CHD孕妇中有61例行羊水穿刺后胎儿染色体核型检查,染色体核型检出8例异常,检出率为13.11%;74例被证实为胎儿CHD孕妇均进行了胎儿基因组CNV-seq检查者,共检测出13例CNV,检出率为17.57%(13/74),此与邓新娥等[2]报道的17.2%的结果相近。其中染色体数目异常5例,分别为13-三体综合征1例、18-三体综合征2例、克氏综合征1例、特纳综合征1例,均与染色体核型分析结果一致;基因组致病性CNV 6例,分别为22q11.2微缺失综合征2例,22q11.2微重复综合征、Williams综合征、16p13.11微重复综合征、6号染色体部分缺失各1例;可能致病性CNV 1例,17号染色体部分重复;VOUS者1例,3号染色体微缺失。此8例染色体微缺失/微重复者染色体核型分析技术均未检出。本研究发现上述常见的致病性综合征胎儿常伴有CHD,而其多由22q11.21的变异、染色体三拷贝等因素引发。陈晓等[14]报道22q11.21微缺失或重复常伴有室间隔缺损、永存左上腔静脉右位主动脉弓等,18-三倍体综合征常伴有室间隔缺损、单心房等;汪敏等[15]表明18-三体综合征常伴有法洛四联症、心室发育不良等。上述报道与本研究均证实了CNV在CHD发病中的致病作用,故产前对胎儿的CNV进行筛选具有重要的临床意义。CNV-seq技术是基于下一代测序技术的基因测序手段,其相较于传统的核型分析技术而言,其诊断的分辨率更高,可以检测到核型分析无法检测到的微小基因重复或缺失,也可以规避核型分析时由于细胞培养失败所致的CNV无法检测的情况,提升检出率,临床上常将其与核型分析结合,不仅使得国内目前产前诊断供给严重不足的状况得以缓解,也为核型分析结果提供了有效的补充,提升CNV的整体检出率[16-17]。CNV-seq技术相较于传统的荧光原位杂交技术而言,在流产物中检测CNV的检出效率更高[18];相较于效率、精度、成功率等与自身相当的染色体微阵列分析技术而言,更加节约成本,经济效益更好,更便于推广应用[19]。但CNV-seq技术也存在明显的缺点,其无法检测出染色体中发生的易位、倒位等染色体平衡性结构重排的现象,无法检测单基因与极小基因片段异常引发的单基因病等,无法区分易位型与游离型三体,故必要时需与其他检测手段结合提升诊断准确率[20]。
综上,本研究通过对比中孕超声筛查出的胎儿CHD孕妇染色体核型分析与CNV-seq分析结果,明确了两项技术的优势与不足,建议临床上对疑似胎儿CHD做羊水穿刺,行染色体核型分析,同时行CNV-seq检测提高微小基因重复或缺失检出率,以期明确胎儿CHD遗传学病因,指导伴有致病CNV胎儿的孕妇做出正确妊娠选择,为产前咨询与胎儿预后提供可靠参考,进而减少出生缺陷,提升生育质量。

