美托洛尔与氯沙坦对中青年高血压患者的影响
吴新榕
(福建省莆田市城厢区医院药剂科 莆田 351100)
高血压是临床多发慢性疾病,也是心脑血管相关疾病常见的危险因素。中老年是高血压多发群体,但随着近年来人们生活水平的不断提高,且受饮食结构、生活习惯改变等因素影响,高血压发病人群已呈年轻化趋势发展[1]。高血压患者可在感觉不到任何不适情况下出现头痛、心律失常、心悸等非特异症状,且随着病情的不断发展(血压≥180/120 mm Hg),患者可出现高血压危象,伴有意识丧失、视野模糊、心肌梗死、肾功能损伤等,对生活质量产生不利影响[2]。目前,临床针对高血压的治疗以短期内降低血压水平为主要目标,并进一步降低心脑血管并发症发生风险。临床有研究表明,中青年高血压患者以舒张压(DBP)升高为主要特征,易增加心脏后负荷,并发展为高血压心脏病,故治疗方案多以β 受体阻滞剂为首选[3]。美托洛尔为选择性β1受体阻滞剂,在高血压、心绞痛、心肌梗死等疾病中应用较为广泛[4]。氯沙坦为血管紧张素Ⅱ受体阻滞剂(Angiotensin ⅡReceptor Blocker, ARB)类抗高血压药物,其所含的科素亚能够阻断血管紧张素Ⅱ,从而调节血压水平[5]。鉴于此,本研究探讨美托洛尔与氯沙坦治疗中青年高血压患者的效果及对患者糖脂代谢的影响。现报道如下:
1 资料与方法
1.1 一般资料 选取莆田市城厢区医院2018 年5月至2021 年5 月收治的中青年高血压患者300 例,按随机对照原则分为两组。A 组150 例,男、女分别为79 例、71 例;年龄30~39 岁,平均(34.68±2.36)岁;病程2 个月至5 年,平均(1.68±0.72)年;腹围92~115 cm,平均(102.18±6.73)cm;体质量指数(BMI)23.8~25.6 kg/m2,平均(24.83±2.08)kg/m2;吸烟史74 例。B 组150 例,男、女分别为82 例、68 例;年龄31~39 岁,平均(34.39±2.31)岁;病程2 个月至5 年,平均(1.60±0.74)年;腹围92~118 cm,平均(101.87 ±6.46)cm;BMI 23.6~25.9 kg/m2, 平均(25.07±2.14)kg/m2;吸烟史69 例。两组一般资料比较均衡性良好(P>0.05)。本研究经医院医学伦理委员会审查并批准。
1.2 纳入与排除标准 (1)纳入标准:符合高血压病诊断标准[6];年龄30~39 岁;对本研究使用药物无过敏史;自愿参与并签署知情同意书。(2)排除标准:诊断为继发性高血压者;合并恶性肿瘤者;合并多脏器功能不全者;严重精神功能障碍者;妊娠期或哺乳期女性。
1.3 治疗方法 两组均接受常规膳食方案调整、改善生活方式等一般治疗。在上述基础上,A 组给予美托洛尔治疗。琥珀酸美托洛尔缓释片(国药准字J20150044)47.5 mg 口服,1 次/d。B 组给予氯沙坦治疗,氯沙坦钾片(普美沙)(国药准字H20110040)50 mg 口服,1 次/d,根据具体血压、心率及药物耐受情况对剂量进行调整,最大量为100 mg。两组均治疗6 个月。
1.4 观察指标 (1)临床疗效。显效,疗程后舒张压(Diastolic Blood Pressure,DBP)下降≥10 mm Hg 且恢复至正常范围内;有效,10 mm Hg≤DBP 下降<20 mm Hg,或DBP 下降未达10 mm Hg 但恢复正常正常水平,或收缩压(Systolic Blood Pressure, SBP)下降≥30 mm Hg;无效,未满足上述标准。总有效率=(显效例数+有效例数)/总例数×100%。(2)血压水平。于治疗前、治疗6 个月后上午9:00~10:00,采用标准袖带台式水银柱血压计,测定患者右上臂血压(SBP、DBP)。(3)糖脂代谢水平。于治疗前、治疗6 个月后采集两组空腹静脉血5 ml,用STAT-Site WB 血糖检测仪测定空腹血糖(Fasting Blood Glucose,FBG),采用全自动生化分析仪、甘油磷酸氧化酶法检测血脂水平,包括总胆固醇(Total Cholesterol, TC)、高密度脂蛋白胆固醇(High Density Lipoprotein Cholestero, HDL-C)、甘油三酯(Triglyceride, TG)、低密度脂蛋白胆固醇(Low Density Lipoprotein-C,LDL-C)。(4)血管内皮功能。于治疗前后收集两组空腹静脉血5 ml,以3 000 r/min 离心处理10 min 后分离血浆保存待检。采用放射免疫法检测内皮素-1(Endothelin-1,ET-1),采用Greiss 法检测一氧化氮(Nitric Oxide,NO)水平。所有操作严格按照试剂盒说明书进行。(5)生活质量。采用简明健康生活状况量表(The MOS Item Short From Health Survey,SF-36)从8 个维度、36 个条目评估患者治疗前、治疗6 个月后生活质量,各项分值为0~100 分,得分与生活质量呈正比。(6)不良反应发生情况,包括腹痛、腹泻、恶心呕吐等。
1.5 统计学方法 采用SPSS23.0 软件处理数据。血压、糖脂代谢水平及生活质量评分等计量资料以()表示,行t检验;临床疗效及不良反应发生率等计数资料用%表示,行χ2检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组糖脂代谢水平对比 两组治疗后FBG、TC、TG、LDL-C 水平较治疗前降低,HDL-C 水平较治疗前升高(P<0.05);两组治疗前后FBG、TC、TG、HDL-C、LDL-C 水平对比无显著性差异(P>0.05)。见表1。
表1 两组治疗前后糖脂代谢水平对比(mmol/L,)
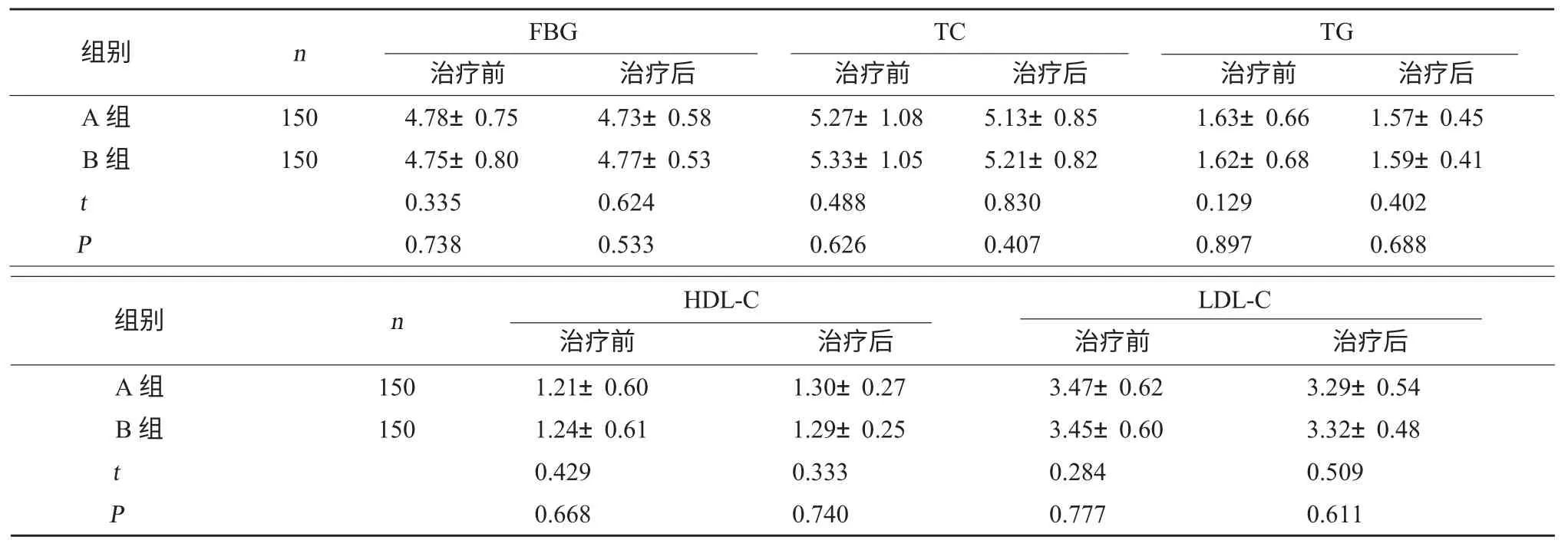
表1 两组治疗前后糖脂代谢水平对比(mmol/L,)
组别nFBG治疗前治疗后TG治疗前治疗后A 组B 组TC治疗前治疗后150 150 t P 4.78±0.75 4.75±0.80 0.335 0.738 4.73±0.58 4.77±0.53 0.624 0.533 5.27±1.08 5.33±1.05 0.488 0.626 5.13±0.85 5.21±0.82 0.830 0.407 1.63±0.66 1.62±0.68 0.129 0.897 1.57±0.45 1.59±0.41 0.402 0.688组别nHDL-C治疗前治疗后LDL-C治疗前治疗后A 组B 组150 150 t P 1.21±0.60 1.24±0.61 0.429 0.668 1.30±0.27 1.29±0.25 0.333 0.740 3.47±0.62 3.45±0.60 0.284 0.777 3.29±0.54 3.32±0.48 0.509 0.611
2.2 两组临床疗效对比 两组治疗总有效率(94.00% vs 96.00%)对比无显著性差异(P>0.05)。见表2。

表2 两组临床疗效对比[例(%)]
2.3 两组血压水平对比 两组治疗后SBP、DBP 水平较治疗前降低(P<0.05),但组间对比无显著性差异(P>0.05)。见表3。
表3 两组治疗前后血压水平对比(mm Hg,)

表3 两组治疗前后血压水平对比(mm Hg,)
注:与本组治疗前相比,*P<0.05。
DBP治疗前治疗后A 组B 组组别nSBP治疗前治疗后150 150 t P 150.27±10.04 151.05±10.21 0.667 0.505 134.62±8.35*135.27±7.68*0.702 0.483 106.11±8.72 105.86±8.53 0.251 0.802 78.64±7.05*79.23±6.88*0.734 0.464
2.4 两组生活质量评分对比 两组治疗后SF-36各项评分较治疗前提高(P<0.05),但组间对比无显著性差异(P>0.05)。见表4。
表4 两组治疗前后生活质量评分对比(分,)

表4 两组治疗前后生活质量评分对比(分,)
注:与本组治疗前相比,*P<0.05。
组别n生理功能治疗前治疗后情感职能治疗前治疗后A 组B 组躯体疼痛治疗前治疗后生理职能治疗前治疗后150 150 t P 38.65±3.76 37.92±4.04 1.620 0.106 55.27±4.31*55.82±4.18*1.122 0.263 64.78±5.26 65.03±5.71 0.394 0.694 70.24±4.62*70.53±4.83*0.531 0.596 44.65±5.33 44.82±5.27 0.278 0.781 55.26±4.33*54.76±4.82*0.945 0.345 45.26±5.78 45.77±5.63 0.774 0.440 65.63±5.26*66.14±5.34*0.833 0.405总体健康治疗前治疗后A 组B 组组别n社会功能治疗前治疗后心理健康治疗前治疗后精力治疗前治疗后150 150 t P 48.25±4.48 47.53±4.36 1.411 0.159 60.72±5.64*61.28±6.33*0.809 0.419 58.75±5.68 59.42±5.37 1.050 0.295 74.26±7.21*72.85±7.61*1.647 0.101 49.50±5.08 48.83±5.64 1.081 0.281 67.26±5.41*68.36±5.28*1.782 0.076 69.45±5.26 68.83±6.42 0.915 0.361 84.36±9.17*85.28±9.60*0.849 0.397
2.5 两组血管内皮功能指标对比 两组治疗后ET-1 水平较治疗前降低,NO 水平较治疗前升高(P<0.05);两组治疗前后ET-1、NO 水平对比无显著性差异(P>0.05)。见表5。
表5 两组治疗前后血管内皮功能指标对比(mg/L,)

表5 两组治疗前后血管内皮功能指标对比(mg/L,)
组别nET-1治疗前治疗后NO治疗前治疗后A 组B 组150 150 t P 120.64±15.32 120.78±15.39 0.079 0.937 67.62±10.87 66.54±10.28 0.884 0.377 35.42±4.83 35.61±4.36 0.358 0.721 75.27±6.84 76.38±6.53 1.438 0.152
2.6 两组不良反应发生情况对比 两组不良反应发生率对比无显著性差异(P>0.05)。见表6。
3 讨论
随着近年来人们生活方式的不断改变,我国高血压患者数量日益上升,且发病群体呈年轻化发展趋势。我国中青年群体高血压患者数量与日俱增。由于大部分患者缺乏对高血压疾病的防治意识,故中青年高血压的控制率与治疗率相对较低[7~8]。目前,临床治疗中青年高血压的首要目的在于控制血压水平,由于个体差异相对较大,且降压药物种类繁多,故选择一种疗效确切且安全性高的药物具有重要意义。
相比老年高血压患者,中青年高血压以DBP 升高为主要表现,SBP 有升高趋势或处于正常水平,这可能与中青年高血压患者伴有外周血管收缩,外周血管阻力随之增加致使DBP 升高相关[9]。本研究结果显示,两组治疗后SBP、DBP 水平较治疗前降低,但两组治疗后SBP、DBP 水平,治疗总有效率与不良反应发生率未见显著性差异,提示美托洛尔、氯沙坦均可有效治疗中青年高血压,可降低血压水平。分析原因为:(1)美托洛尔通过抑制中枢与周围组织,阻滞血管壁、心脏、肾素-血管紧张素-醛固酮系统(Renin-Angiolensin-Aldosterone System, RAAS),可减缓心率与心输出量,从而达到良好的降压效果。(2)作为ARB 之一,氯沙坦可对血管紧张素Ⅱ与其受体相结合起到阻滞效果,从而减弱血管紧张素Ⅱ作用而达到降压效果[10~11]。
目前,临床多采用β 受体阻滞剂、ARB、血管紧张素转化酶抑制剂(ACEI)等药物治疗高血压病[12],虽可达到良好的降压效果,但对于机体糖脂代谢水平影响的报道较少。国内研究指出,高血压患者常伴有血糖、血脂水平紊乱,而糖脂代谢异常可能会诱发其他相关疾病的发生,造成恶性循环,影响患者的生活质量[13]。此外,第二代β 受体阻滞剂通过阻断β2受体,可促进糖原分解,抑制胰岛素分泌,易导致机体糖脂代谢指标异常[14]。血管内皮功能被认为在高血压疾病的发生与发展过程中起到重要作用,其中NO 为经血管内皮细胞释放后的稳定血压舒张因子,参与血管张力的调节;ET-1 为内源性长效血管收缩调节因子,可调节基础血管的张力并对稳定血管系统起到重要作用。本研究结果显示,两组治疗前后FBG、TC、TG、HDL-C、LDL-C、ET-1、NO 水平对比无显著性差异,表明美托洛尔与氯沙坦对青年高血压病患者糖脂代谢及血管内皮功能无明显影响。分析原因可能是由于美托洛尔与氯沙坦均可促进降钙素基因相关肽(Calcitonin Gene Related Peptide,CGRP)的分泌,平衡血浆ET-1 与NO 水平,增强血管收缩能力并改善血管内皮功能。杨春强等[15]通过对比分析美托洛尔与氯沙坦治疗中青年高血压病患者的疗效及对糖脂代谢的影响,结果发现,美托洛尔与氯沙坦均可有效降低患者的血压与心率,且对远期糖脂代谢无明显影响,这与本研究结果一致。此外,本研究结果还显示,两组治疗后SF-36 各项评分均较治疗前提高,提示美托洛尔与氯沙坦可提高中青年高血压病患者的生活质量。
综上所述,美托洛尔与氯沙坦均可安全、有效治疗中青年高血压病,可降低患者血压水平,改善血管内皮功能,提高生活质量,且对患者糖脂代谢无明显影响。

