电离辐射导致男性生育素质低下的机制及其防护措施
张香香 杨勇

通信作者简介:杨勇,主任医师、教授,博士研究生导师,长春中医药大学附属医院副院长、泌尿外科首席专家,国家自然科学基金面上项目负责人,华夏医学一等奖获得者。1985年毕业于白求恩医科大学,1995年毕业于协和医科大学研究生院,从事泌尿外科临床、教学、科研工作30余年。目前研究重点集中于干细胞及淫羊藿次苷防治男性勃起功能障碍、放射性膀胱炎等泌尿生殖系统放射性损伤的作用机制。担任中国医师协会男科医师分会常委、中国医疗保健国际交流促进会泌尿生殖专业委员会常委、亚洲男科学会常委、北京医学会肿瘤微创学组委员、中华外科杂志编委、微创泌尿外科杂志编委。主持完成国家自然科学基金等多个科研课题,发表学术论文40余篇,SCI收录近20篇。
【摘要】 在核科技高速发展的现代世界,电离辐射广泛存在于民众日常生活与工作环境之中,其伤人于无形,对人类各系统器官产生多种不良作用。作为对电离辐射高度敏感的细胞之一,男性睾丸生殖细胞极易受到损害,在置露于不同程度电离辐射后将引起包括精子参数和精子染色体及DNA在内的一系列不利影响,导致男性生育素质下降和后代发育异常。基于此,在倡导合理地、科学地进行电离辐射损害防护同时,重视男性生育素质保障的生命事业显得极为重要,事关人类后代福祉。该文介绍了电离辐射对男性生殖系统器官的生物效应、电离辐射对男性睾丸生殖细胞的损伤效应以及电离辐射致男性生育素质低下的防护,为临床相关研究提供参考。
【关键词】 电离辐射;电离辐射防护;精子;男性;生育素质
Mechanism and protective measures of low fertility quality in men caused by ionizing radiation Zhang Xiangxiang△,Yang Yong. △Changchun University of Chinese Medicine, Changchun 130117, China
Corresponding author, Yang Yong, E-mail: yongyang301@163.com
【Abstract】 In the modern world, ionizing radiation has been prevalent in daily lives and work environment due to rapid development of nuclear technology. It is invisible and exerts multiple adverse effects on various human systems and organs. As one of the cells that are highly-sensitive to ionizing radiation, male testicular germ cells are highly-susceptible to damage and exposure to varying levels of ionizing radiation can cause a range of adverse effects, including sperm parameters and sperm chromosomes and DNA, leading to a decline in male fertility and abnormal offspring development. Consequently, it is of utmost importance to promote rational and scientific protection against ionizing radiation damage while attaching importance to the life-saving cause of safeguarding male fertility, which is of great importance to the well-being of future generations. In this article, the biological effect of ionizing radiation on male reproductive organs, the damage effect of ionizing radiation on male testicular germ cells, and the protection of declined male fertility caused by ionizing radiation were illustrated, aiming to provide reference for relevant clinical trials.
【Key words】 Ionizing radiation; Ionizing radiation protection; Sperm; Male;Fertility quality
電离辐射是包括阿尔法(α)、贝塔(β)、伽马(γ)、伦琴(X)、中子、质子以及重离子束等在内的射线,其特点是波长较短、频率较高、有较大能量,能使物质原子或分子失去能量或获得电子成为离子。在人类社会生产和生活中,电离辐射无处不在,除天然本底辐射外,随现代社会核能核技术飞速发展,放射性核素被广泛应用于各行各业,产生了各种人工辐射源,人类置露在电离辐射环境中的危险性、严重性日益增加[1]。与大众诊疗密切相关且来自医疗源的照射占其中的绝大多数,尤其医疗人员对于医用电离辐射详细知识的知晓程度并不是很理想[2]。多项相关研究报道,电离辐射引起的生物学效应可致机体细胞生命活动障碍,对人类身体健康产生各种不良作用,并可诱发癌症和引致各种遗传疾病。近年,因诸多因素影响,不育症与生殖健康问题逐渐增多,人类自身繁衍及后代素质面临重大挑战。WHO分析了来自五大洲89个国家关于不育症发病率的392篇文献,得出全球不育平均发病率约为16.7%,其中男性因素几乎占50%以上,大量流行病学调查显示,近几十年男性精液质量呈逐年下降走势[3-4]。随辅助生殖医学技术的兴起,影响男性生育素质的各种不利因素成为探索焦点。本文就电离辐射对男性生育素质的影响做一综述,旨在为临床相关研究提供参考。
一、电离辐射对男性生殖系统器官的生物效应
依据辐射剂量/剂量率、方法、效应发生情况,一般将生物体受电离辐射作用时的生物效应分型表述,即按辐射剂量/剂量率分为瞬时、慢性效应;按辐射方法分为高、低传能线密度(LET)辐射、单次与重复辐射、局部与全身辐射;按效应发生时间分为近期效应(受照射后几个星期内发生)和远期效应(受照射后数月后发生);按效应发生细胞分为躯体效应与遗传效应。多项研究表明,电离辐射还存在旁观者效应,Hargitai等[5]观察受照小鼠细胞外囊泡(EV)能否诱导旁观小鼠体内氧化还原状态和辐射应答基因表达改变,结果表明电离辐射引起细胞抗氧化系统的改变可能是通过来自直接辐射动物的EV以旁观者方式在体内传递[5]。在实际研究工作中,通常按辐射剂量/剂量率和效应发生关系分类,将电离辐射对男性生殖系统的生物效应分为随机效应和确定效应。
1. 随机效应
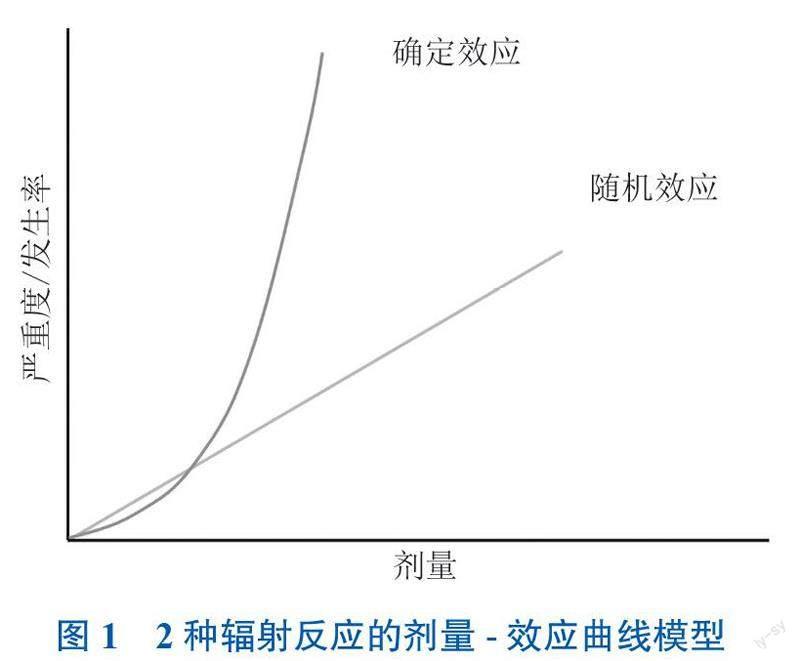
随机效应指效应发生率与辐射剂量呈正相关,多发生在低剂量/剂量率(剂量累计低于或可超过100 mGy,但剂量率低于5 mGy/h)辐射后,其剂量-效应曲线常用线性无阈(LNT)模型(图1)描述。随机效应发生不存在剂量阈值,效应风险源于细胞核DNA损伤后未及时和错误修复。在受辐射一段时间后,机体产生的适应效应、兴奋效应、遗传效应、癌变效应以及血液系统恶性疾病和免疫系统功能紊乱等统归属于随机效应[6]。作为人类遗传物质载体,男性精子受电离辐射后所致的遗传效应需予以重视。
2. 确定效应
确定效应指严重度和辐射剂量呈正相关,一般发生于高剂量/剂量率急性辐射时,剂量效应曲线适用线性二次方模型解释,当达到阈剂量辐射时,即可在小范围内迅速爆发剧烈的生物效应,且剂量愈大,所致生物效应愈发严重[6]。男性睾丸对电离辐射极为敏感,青春期前男性睾丸接受6 Gy辐射可致无精子症,在成年男性中这一剂量阈值为2.5 Gy[7]。联合国原子辐射效应科学委员会于1982年报告中明确指出,1次1.5~4.0 Gy剂量的辐射会致男性短暂性生育能力丧失,辐射剂量为5.0~9.5 Gy则会导致男性永久性丧失生育能力。
二、电离辐射对男性睾丸生殖细胞的损伤效应
一般而言,电离辐射通过直接效应(作用于生物大分子)和间接效应(作用于水分子)两种途径作用于相应生物靶点,诱导发挥主要攻击作用的自由基及其代谢物产生。在分子层面,可致双链DNA分子损伤、DNA加合物形成阻碍其合成修复、DNA 分解代谢增强、引发蛋白交联及酶活性破坏所致代谢事件改变等[8]。细胞水平上,会导致间期染色体畸变、线粒体功能障碍、胞膜裂解、细胞凋亡及周期阻滞等[9-10]。男性精子由睾丸曲细精管生精上皮细胞产生,后由支持细胞散放至管腔中央,经历精原细胞有丝分裂增殖分化、精母细胞2次减数分裂和精子形成这3个过程,随即入附睾进一步发育成熟,整个阶段置露于不同条件、不同程度的电离辐射下可对精子造成不同生物效应的损伤。
1. 对精子数量、活力以及形态的影响
临床上,电离辐射诱导生精细胞凋亡、精子数量减少较为常见。Abuelhija等(2013年)研究发现,一次性接受辐射剂量为0.15 Gy时,精子数量减少持续6个月,辐射剂量为0.5 Gy时,精子减少将持续8个月,而6 Gy剂量的辐射可致精子缺乏达2年之久。值得注意的是,辐射剂量≥1.2 Gy时精子就有降低风险,当分段辐射剂量累计超过2.5 Gy时,可引起精子发生不可逆性损伤[11]。在引起同等程度辐射损伤所接收到的照射剂量上各学者研究结果不一,但普遍有一个共识,即电离辐射致精子数量下降存在剂量阈值,在阈剂量范围内可以恢复,超过这个阈值时精子数量即开始显著减少,并且随着剂量的增大而愈发严重,直至完全无精子发生导致永久性不育症。
精子活力在一定程度上也常受电离辐射作用影响。李仲辉等(2013年)用不同剂量X线(1、2、4、6 Gy)照射活体SD大鼠外生殖系统不同时间(1、4、8、12、24 h)后,发现4 Gy X线在照射12 h后大鼠精子活力明显降低。Li等(2013年)研究团队在给予雄性Wistar大鼠0.5 Gy以上电离辐射后,热应激蛋白70-2、谷胱甘肽过氧化物酶4、磷脂酶C、β-微管蛋白以及3-磷酸甘油醛脱氢酶等与精子活力相关的蛋白均发生差异表达。此外,睾丸生物钟调控着精子活力,电离辐射作用于睾丸,造成生物钟节律紊乱,引起生育素质下降而致生殖障碍[12]。Qin等[13]模拟宇航员在太空中应对每日环境变化(光照/黑暗、进食、休息/活动和温度功能的循环)所形成的生物昼夜时钟和在太阳粒子事件中睾丸暴露辐射剂量,给予已形成生物节律性雄性小鼠3 Gy X线全身照射,观察到小鼠精子活力的日平均值变化从64.41%下降至27.64%。
精子形态通常是衡量精液质量优劣的基本标准,常以精子畸形率评估,是受精潛能最佳预测指标。有关电离辐射对精子形态的影响,系列研究罕少。Wdowiak等[14]在分析2000—2016年波兰东部卢布林地区向不育治疗机构报告的男性本底放射性与精液质量之间关系的研究中,发现暴露于人造来源β同位素和大气γ辐射的人群,其形态正常精子百分比呈现长期下降趋势(r = ?0.970,P < 0.001,2000—2009年;r = ?0.925,P = 0.003,2010—2016年),认为这不仅在于患者年龄,长期辐射暴露更是起决定性作用的因素。低剂量电离辐射诱导的适应性效应在精子形态表现上尤为突出。Woon等(2011年)发现,黑线姬鼠附睾尾端在暴露于1 Gy高剂量率(0.8 Gy/min)照射环境下比暴露于低剂量率(0.7 mGy/h)照射环境下的畸形精子百分比增加,且低剂量率照射畸形精子百分比随吸收剂量上升呈下降趋势,作者认为这是当剂量率从急性照射水平下降到慢性照射水平时,产生了强大减少效应的缘故。
2. 對精子染色体以及DNA的影响
多项研究证明,精子染色体对电离辐射有较高敏感性,它是评估小剂量辐射损伤遗传效应的重要生物学指标,且随吸收剂量的增加,其畸变和微核发生呈上升趋势。Agadzhanian等(2010年)对切尔诺贝利核电站事故后1987—2004年出生儿童进行研究,发现受辐射父亲的子女染色体畸变水平也明显增加,认为低辐射剂量引起的基因组不稳定的个体特征在其后代中存在跨代现象。
精子DNA完整性、正确性关乎遗传信息高质量逐代接递,电离辐射对精子DNA损伤效应现有两大主流观点。一方认为,由辐射暴露后细胞水介质辐射分解产生的自由基介导,它们攻击的靶标为DNA碱基,DNA双链断裂(DSB)是辐射诱导基因组破坏中最严重、最重要的损伤类型,主要由羟基自由基(·OH)介导,被认为是引发生殖细胞程序性凋亡主因[15-16]。另一方认为,电离辐射会影响精子DNA启动子区域CpG二核苷序列起抑制转录作用的甲基化修饰,由此引发相应生育风险,如表观遗传改变和跨代效应等[17]。Nakata等[18]分析新生小鼠在急性高剂量电离辐射(HDR)和慢性低剂量电离辐射(LDR)后睾丸整体DNA甲基化模式,未受辐射小鼠甲基化水平随其生长增加,而LDR组甲基化水平保持不变,HDR组甲基化水平与鼠龄呈负相关,认为电离辐射影响了性成熟前小鼠精子的发生和发育。Wdowiak等[19]研究认为,在精子发生过程中,细胞分化遗传风险仅限一个精子发生周期,而遗传不稳定性可能会延续整个生命周期,电离辐射造成的这种可被检测到的DNA损伤可能会递接给后代,致损的最低剂量为30 Gy,超过这个剂量,单链DNA断裂数量随之增加[19]。
三、电离辐射致男性生育素质低下的防护
1. 过程防护
对于如健康体检、疾病诊断、恶性肿瘤和某些病种治疗以及职业暴露等这些日常会接触到的可预知性电离辐射事件,严格做好过程中辐照防护对预防或减少辐射损害起关键作用。国际辐射防护委员会(ICRP)倡议“可合理达到的尽量低原则”,并提出辐射防护三大基本原则,分别是实践正当性、防护最优化和剂量当量限值。各医务人员在医疗实践中应最大限度地去遵循,严格规范过程操作,提高业务水平,并且要尽可能地避免不必要和过度的放射检查。提倡育龄男性青年人群多关注了解电离辐射相关知识,提高辐射防范意识,要高度重视对自身生殖系统器官的辐射防护。
2. 防护药物应用
尽管现有的放射治疗技术能更具针对性地向病灶输送较高单位的辐射能量,以达到改善或者治愈这些疾病的目的,但不排除某些对电离辐射极为敏感的邻近器官,不可避免地会在这个过程中受到不同程度的辐射损害。男性睾丸是对辐射性最敏感的器官,在疾病放射治疗阶段中,极易受到影响而致男性生育素质下降。再有,出乎意料的辐射暴露对于男性生殖系统也是严重打击。
当前还缺乏官方批准的用于防治放射性损伤的制剂,故迫切需要一种高效、不良反应少、价格合理的抗辐射制品,用以辐射损害防护和补救。近年有多位学者关注于药物预防电离辐射损伤的研究,对其进行了探索性工作。Huang等[20]在5 Gy X线辐照前用单剂量二甲基亚砜腹腔注射处理雄性小鼠以观察其辐射防护作用,发现辐照前预处理能明显减轻睾丸质量的下降,增强辐照后精原干细胞和精原细胞的存活、再生,且有利于DNA双链断裂同源重组修复,有效降低DNA损伤累积,据此认为二甲基亚砜对生殖系统的电离辐射保护作用显著,值得进一步研究[20]。Dobrzy Ska等[21]观察雄性小鼠在接受辐照后给予番茄红素治疗对生殖细胞的影响,持续2周后检测精子参数和DNA损伤,发现与单独辐照相比,从24 h开始补充番茄红素后精子数量增加,且在几乎所有番茄红素治疗组中,异常精子的百分率及DNA损伤均明显下降,认为番茄红素可改善辐射对精子的有害影响。Ma等[22]研究发现,虎杖根天然提取物白藜芦醇苷能够有效地减轻4 Gy同位素钴[60Co] γ射线电离辐照后小鼠睾丸的损伤,保留精子活力及显著抑制细胞凋亡。Shaban等[23]研究认为,橙皮苷所具有的抗氧化和抗凋亡活性,对同位素铯[137Cs] γ射线辐射所致的睾丸氧化应激损伤及凋亡具有保护作用,并且发现辐照暴露前就注射橙皮苷比暴露后注射更有效。Rossi等[24]探讨青少年癌症放射治疗中如何给予保护以避免性腺辐照毒性事件的发生,通过研究小鼠青春期睾丸模型发现西红花素可显著降低2 Gy X线辐照后小鼠睾丸细胞广泛损伤,并可调节DNA损伤和氧化应激反应。
其他如N-乙酰半胱氨酸、硫辛酸、维生素E、阿托伐他汀、单磷酰脂A、绿茶多酚、中药方剂益气解毒汤等防护电离辐射损害的制剂也有研究文献报道。然而上述研究多数仅基于动物模型的研究结果,对人体的保护作用及其作用机制仍需进一步探索。
四、结 语
无论是辐射过程防护还是抗辐射制剂应用,均有不可规避的电离辐射损伤存在,因此在接触电离辐射前给生育素质一份保障,对后代福祉具有重要意义。精子冷冻保存是临床上发展比较成熟的一种辅助生殖手段,被认为是比较可靠的生育素质保障技术。然而对国内芸芸民众而言,自精冷冻保存仍然不太熟悉,这可能与传统认知抵抗和相关信息科普不到位有关,人类精子库大多保存的供精者精液,存在有电离辐射生育素质损害风险的人群事先积极主动要求精子冷冻保存的极少。作为当前男性生育素质保障的最佳选择,精子冷冻保存的概念及实践意义应该要向大众普及,精子库应该发挥其更大、更有意义的作用[25]。
参 考 文 献
[1] 王承, 黄月英, 唐大海. 中药抗电离辐射损伤作用的研究概况. 海军医学杂志, 2019, 40(5): 495-498.
[2] 林青青, 康福新. 医务人员对医用电离辐射相关知识的知晓情况调查. 中国辐射卫生, 2018, 27(5): 462-464.
[3] 孫文希, 胡凌娟. 国内外不孕不育症现状及我国的干预策略探讨. 人口与健康, 2019(12): 19-23.
[4] 张永利, 郭亭飞. 男性不育症的流行病学调查动态.第十二次全国中西医结合男科学术大会暨全国中西医结合男科诊疗技术研修班暨2017上海市中西医结合学会上海市中医药学会泌尿男科专业委员会学术年会讲义论文资料汇编. 上海, 2017: 245-246.
[5] Hargitai R, Kis D, Persa E, et al. Oxidative stress and gene expression modifications mediated by extracellular vesicles: an in vivo study of the radiation-induced bystander effect. Antioxidants (Basel), 2021, 10(2): 156.
[6] Richard W, Janet T E. The meaning of low dose and low dose-rate. J Radiol Prot, 2010, 30(1): 1-3.
[7] Burns K C, Hoefgen H, Strine A, et al. Fertility preservation options in pediatric and adolescent patients with cancer. Cancer, 2018, 124(9): 1867-1876.
[8] Albi E, Cataldi S, Lazzarini A, et al. Radiation and thyroid cancer. Int J Mol Sci, 2017, 18(5): 911.
[9] Islam M T. Radiation interactions with biological systems. Int J Radiat Biol, 2017, 93: 487-493.
[10] Nakano T, Xu X, Salem A M H, et al. Radiation-induced DNA-protein cross-links: mechanisms and biological significance. Free Radic Biol Med, 2017, 107: 136-145.
[11] Howell S J, Shalet S M. Spermatogenesis after cancer treatment: damage and recovery. J Natl Cancer Inst Monogr, 2005(34): 12-17.
[12] 邱宇, 张芯, 胡霖霖. 个体日周期节律的生物学机制及影响因素概况. 新医学, 2020, 51(7): 497-500.
[13] Qin F, Liu N, Nie J, et al. Circadian effects of ionizing radiation on reproductive function and clock genes expression in male mouse. Environ Health Prev Med, 2021, 26(1): 103.
[14] Wdowiak A, Stec M, Raczkiewicz D, et al. Background ionizing radiation and semen parameters of men with reproductive problems. Ann Agric Environ Med, 2020, 27(1): 43-48.
[15] Singh V K, Seed T M. A review of radiation countermeasures focusing on injury-specific medicinals and regulatory approval status: part I. Radiation sub-syndromes, animal models and FDA-approved countermeasures. Int J Radiat Biol, 2017, 93(9): 851-869.
[16] Ciccia A, Elledge S J. The DNA damage response: making it safe to play with knives. Mol Cell, 2010, 40(2): 179-204.
[17] Leung C T, Yang Y, Yu K N, et al. Low-dose radiation can cause epigenetic alterations associated with impairments in both male and female reproductive cells. Front Genet, 2021, 12: 710143.
[18] Nakata A, Sato K, Fujishima Y, et al. Evaluation of global DNA methylation and gene expression of Izumo1 and Izumo1r in gonads after high- and low-dose radiation in neonatal mice. Biology (Basel), 2021, 10(12): 1270.
[19] Wdowiak A, Skrzypek M, Stec M, et al. Effect of ionizing radiation on the male reproductive system. Ann Agric Environ Med, 2019, 26(2): 210-216.
[20] Huang Z, Peng R, Yu H, et al. Dimethyl sulfoxide attenuates radiation-induced testicular injury through facilitating DNA double-strand break repair. Oxid Med Cell Longev, 2022, 2022: 9137812.
[21] Dobrzy Ska M G M, Gajowik A. Amelioration of sperm count and sperm quality by lycopene supplementation in irradiated mice. Reprod Fertil Dev, 2020, 32(12): 1040-1047.
[22] Ma Y, Jia X. Polydatin alleviates radiation-induced testes injury by scavenging ROS and inhibiting apoptosis pathways. Med Sci Monit, 2018, 24: 8993-9000.
[23] Shaban N Z, Ahmed Zahran A M, El-Rashidy F H, et al. Protective role of hesperidin against γ-radiation-induced oxidative stress and apoptosis in rat testis. J Biol Res (Thessalon), 2017, 24: 5.
[24] Rossi G, Placidi M, Castellini C, et al. Crocetin mitigates irradiation injury in an in vitro model of the pubertal testis: focus on biological effects and molecular mechanisms. Molecules, 2021, 26(6): 1676.
[25] Law C. Biologically infallible? Mens views on male age-related fertility decline and sperm freezing. Sociol Health Illn, 2020, 42(6): 1409-1423.
(收稿日期:2023-02-12)
(本文編辑:林燕薇)

