实体瘤自体造血干细胞动员不佳患儿应用普乐沙福的经验分享
刘红艳 刘琦 张迎丽 房建铭 董泽宇 刘周阳 吴南海 刘玉爽 张莹 唐锁勤 孙媛
自体造血干细胞移植是治疗儿童恶性实体瘤的重要方法之一,其应用越来越广泛,在神经母细胞瘤、髓母细胞瘤、视网膜母细胞瘤(retinoblastoma,RB)、非典型畸胎样/横纹肌样瘤(atypical teratoid/rhabdoid tumor,AT/RT)等多种儿童实体肿瘤中已纳入规范和指南,为提高疗效,在神经母细胞瘤中已推荐串联双移植。而外周血造血干细胞(peripheral blood stem cell,PBSC)成功采集是移植成功的关键之一。患儿由于在治疗早期接受放、化疗的强度较大,造成骨髓造血干细胞受损,动员足够造血干细胞进入外周血供采集通常存在困难。因此,临床急需一种新的方案可以安全有效动员骨髓造血干细胞至外周提高采集成功率。普乐沙福作为趋化因子受体4(CXCR4) 拮抗剂,可动员造血干细胞自骨髓释放至外周血中,为患儿成功采集足够的造血干细胞带来希望,并于2019 年获欧洲药品管理局(EMA)批准在儿童实体瘤和淋巴瘤的动员中应用,已发表的相关研究涵盖了儿童神经母细胞瘤、淋巴瘤、髓母细胞瘤、尤文氏肉瘤(Ewing's sarcoma,ES)、原始神经外胚层肿瘤、肉瘤和生殖细胞肿瘤[1-3]。普乐沙福分别于2018年12 月和 2020 年8 月获中国国家药品监督管理局批准用于非霍奇金淋巴瘤(NHL)和多发性骨髓瘤(MM)患儿的自体造血干细胞动员。截至目前,尽管普乐沙福已在国外上市10 余年,但因其在国内获批上市时间较短,临床实践应用经验尚不足,特别是儿童实体瘤患儿应用的相关经验更少,仍处于探索阶段。本文回顾性总结5 例实体瘤造血干细胞预计动员不佳患儿在CD34+细胞计数指导下抢先应用普乐沙福的经验、疗效及安全性,以期为国内该动员方案的临床研究提供参考。
1 资料与方法
1.1 一般资料 选取2021 年3 月~2022 年9 月本院5 例实体瘤造血干细胞动员不佳患儿作为研究对象,其中男1 例,女4 例;年龄2.2~6.0 岁,中位年龄2.3 岁;体重12.9~29.8 kg,中位体重16.0 kg。病理学明确诊断为非典型畸胎瘤样/横纹肌样瘤1 例,视网膜母细胞瘤2例,尤文氏肉瘤1例,伯基特淋巴瘤(Burkitt's Lymphoma,BL)1 例。5 例患儿动员失败危险因素:4 例患儿既往化疗>6 个疗程,化疗周期4~17 个疗程,中位化疗周期8 个疗程;4 例患儿含铂治疗方案>2 个疗程;3 例患儿进行了全脑全脊髓放疗。5 例患儿一般资料见表1。动员失败高危因素分类标准[4]参考表2。
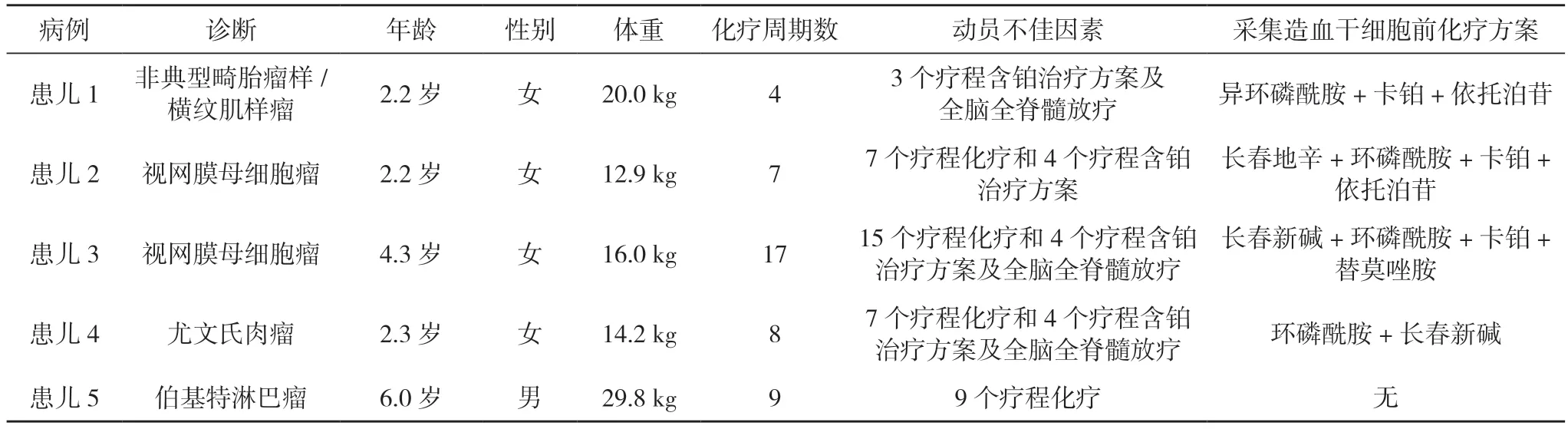
表1 5 例患儿一般资料

表2 动员失败的高危因素分类标准
1.2 方法
1.2.1 化疗动员 患儿1~4 为化疗动员,化疗方案为该疾病的用药方案。见表1。化疗动员的患儿于化疗后在白细胞下降至低谷并回升时开始动员,给予粒细胞集落刺激因子(G-CSF)15 μg/(kg·d)皮下注射,观察并记录生命体征、血常规变化,动员至第4~6 天,白细胞≥10×109/L 时开始采集。若患儿在动员第6 天白细胞仍未达上述标准则终止干细胞采集。采集前1 d 取外周血检测CD34+细胞计数,CD34+细胞计数<10 cells/µl或者第1 天采集物CD34+细胞计数<1.5×106/kg 时晚21:00 加用普乐沙福。外周血CD34+细胞计数见表3。
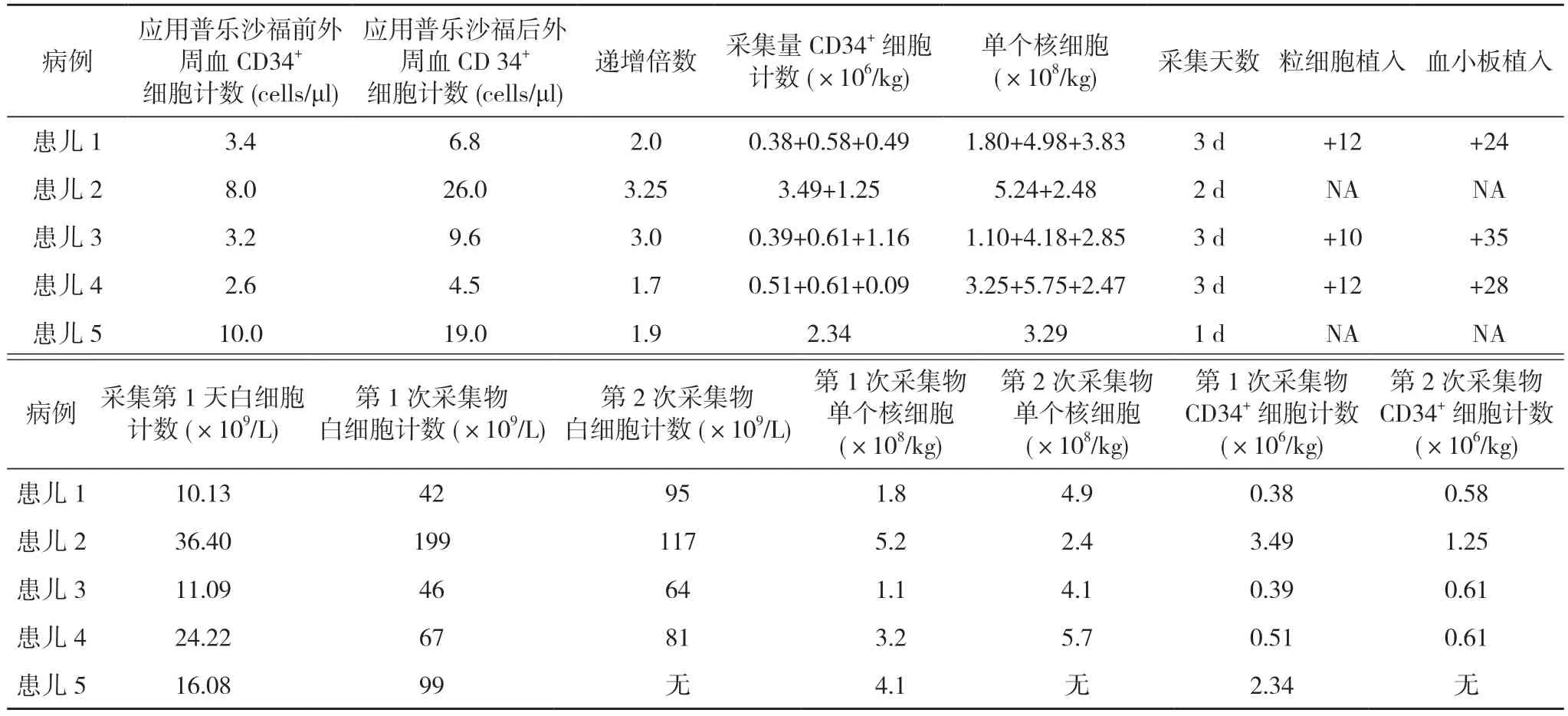
表3 5 例患儿应用普乐沙福的血象变化及采集结果
1.2.2 稳态动员 患儿5 为稳态动员,应用G-CSF 15 μg/(kg·d)皮下注射,连续4 d,第4 天检测外周血CD34+细胞计数,CD34+细胞计数<10 cells/µl 晚21:00加用普乐沙福。外周血 CD34+细胞计数见表3。
1.2.3 普乐沙福使用方法 在干细胞采集前11 h 给予普乐沙福注射液[商品名:释倍灵,Genzyme Corporation,注册证号J20190003,规格:1.2 ml∶24 mg],推荐剂量0.24 mg/(kg·d),皮下注射;中重度肾功能损害的患儿肌酐清除率<50 ml/min,剂量降至0.16 mg/kg,最大剂量≤27 mg/d,最长≤4 d(具体见普乐沙福注射液说明书)。5 例患儿的肾功能均正常,未调整普乐沙福剂量;患儿1、3、4 各采集3 次,第1 次采集物中未达到目标干细胞量,第1 次采集当晚开始使用普乐沙福,连用2 d;患儿2 采集前11 h 使用普乐沙福,使用1 次,干细胞采集2 次;患儿5 采集前11 h 使用普乐沙福,使用1 次,干细胞采集1 次。
1.2.4 PBSC 采集物分析 全部使用美国泰尔茂比斯特公司生产的COBE Spectra 血细胞分离机(version 6.1 PBSC software)的半自动采集程序(MNC 程序)。5 例患儿共采集12 例次。静脉通路中采血通路为7F 股静脉导管(美国ARROW),回血通路为18G 外周静脉留置针(美国BD)。抗凝血使用血液保存液(Ⅰ) ACD-A(山东威高集团医用高分子制品股份有限公司),生理盐水1000 ml(辰欣药业)。输入/抗凝剂比率为(12~15)∶1,总处理血容量为2901~6501 ml。采集过程中5%葡萄糖+葡萄糖酸钙注射液3 g 缓慢静脉滴注,预防抗凝剂枸橼酸钠与钙离子结合引起低钙血症。
1.3 观察指标及判定标准
1.3.1 干细胞动员及采集 血常规采用血细胞分析仪(型号:XS-500i,深圳希森美康生物科技有限公司)检测PBSC;采集物细胞计数采用全自动血细胞分析仪(型号:XS-500i,深圳希森美康生物科技有限公司)检测;血涂片进行采集物白细胞分类,CD34+细胞计数采用流式细胞检测仪[型号BD FACSCantoTM Ⅱ,碧迪医疗器械(上海)有限公司]检测。CD34+细胞计数(×106/kg)=[采集物白细胞计数(×109/L)×采集物体积(L)×CD34+%×1000]/患儿体重(kg)。采集物单个核细胞数(×108/kg)=[采集物白细胞计数(×109/L)× 采集物体积(L)× 采集物中单个核细胞%×10]/患儿体重(kg),其中采集物中单个核细胞%=采集物血涂片淋巴细胞%+单核细胞%[5]。大多数研究认为CD34+细胞计数≥2×106/kg 是移植成功的阈值[6]。故本研究中,干细胞采集物中CD34+细胞计数≥2×106/kg 时视为动员采集成功,而动员6 d 白细胞计数<10×109/L 或者采集物中 CD34+细胞计数<2×106/kg 时视为动员采集失败。采集成功率=动员采集成功的例数/总采集例数。
1.3.2 不良反应 普乐沙福给药安全性评估采用问卷调查法,采集当日由采集护士调查患儿注射普乐沙福后的不良反应,排除注射G-CSF 后已有的不适症状,不良反应评价参照 CTCAE 5.0 版本分级标准[7]。
2 结果
2.1 干细胞动员血象变化及采集结果分析 5 例患儿动员过程中,白细胞计数5 d 内均上升至≥10×109/L,均完成了采集过程。见表3。采集物单个核细胞中位值为 8.1(4.05,11.47)×108/kg,采集物CD34+细胞计数中位值为2.1(1.21,4.74)×106/kg。其中1 例患儿采集1 次,1 例患儿采集2 次,3 例患儿采集3 次,3 例采集干细胞CD34+计数>2×106/kg,2 例采集干细胞CD34+计数<2×106/kg。使用普乐沙福后外周血CD34+细胞计数约为使用前外周血CD34+细胞计数的2 倍(1.7~3.25 倍);详细记录CD34+细胞计数、单个核细胞、采集物白细胞计数。见表3。将所采集的PBSC 计数后交由北京脐血库,去浆后加5%二甲基亚砜 (DMSO)保存液放入液氮罐保存。干细胞回输在预处理结束后24~36 h 进行,将冻存干细胞在水浴 40~42℃快速解冻后立即快速回输。3 d 后开始使用G-CSF 10 μg/(kg·d)促进造血重建。患儿1、3、4 完成自体造血干细胞移植,中性粒细胞和血小板植活中位时间分别为12、10、12 d 和24、35、28 d。
2.2 不良反应发生情况分析 5 例患儿均未出现乏力、失眠、腹痛、腹泻、头晕、关节痛等不良反应。
3 讨论
大剂量化疗联合自体外周血干细胞移植是儿童恶性实体瘤的有效治疗手段。自体外周血干细胞的常规动员方案包括G-CSF 单用及联合化疗。部分患儿使用常规动员方案无法采集到目标剂量的 CD34+细胞计数,严重影响造血干细胞移植治疗。一项在美国梅奥中心进行的回顾性分析:共包括2001~2007 年该中心的1775 例次干细胞动员,结果显示,使用传统动员方案有22%的患儿动员失败(其中10%的患儿CD34+细胞计数采集量<2×106/kg;12%的患儿采集前外周血CD34+细胞计数<10 cells/μl,故放弃第1 次采集)[8]。我国多家移植中心报道,传统动员的失败率仍然较高,约为11.3%~47.5%[9-14]。欧洲血液和骨髓移植协会(EBMT)根据CD34+细胞计数定义动员效果[15]:≥20 cells/µl 为动员良好;11~19 cells/µl 为临界动员不佳;6~10 cells/µl 为相对动员不佳;0~5 cells/µl 为绝对动员不佳。绝对动员不佳患儿使用普乐沙福尽管可改善动员效果,但仍有较高采集失败风险。一项西班牙回顾性研究[16]:入选2008 年1 月~2011 年9 月的多发性骨髓瘤和非霍奇金淋巴瘤患儿(N=105),上述患儿均符合以下条件:在G-CSF 10 µg/kg,2 次/d,动员第4 天时外周血CD34+细胞计数<10 cells/µl,结果显示:第4 天外周血 CD34+细胞计数<3.5 cells/µl,单用G-CSF组采集失败率为97%。因此针对动员不佳及具有危险因素的患儿,为降低动员失败的风险,采取联合使用普乐沙福的动员方案。美国希望之城国家医疗中心的研究结果显示[17]:研究时间为2007~2015 年,普乐沙福的引用采集成功率从95.1%升至99.2%;平均采集时间从4.5 d 缩短至2.8 d。随着采集成功率提升、采集次数减少,推动了自体造血干细胞移植增加,同期该中心自体PBSC 采集人数增加>50%,作者认为,普乐沙福的使用是自体PBSC 采集人数快速增加的重要原因。普乐沙福是首个因理解动员机制而开发的动员剂,其作为 CXCR4 的可逆拮抗剂,通过阻断CXCR4 与基质细胞衍生因子-1(SDF-1α)的结合,驱动CD34+细胞向外周血中释放,使循环中CD34+细胞增多[18]。普乐沙福为成功采集带来希望。
许多可能影响 PBSC 动员采集的因素已被纳入研究,包括年龄、性别、疾病类型、疾病分期、化疗疗程及是否放疗等,但结果不一[19-23]。2021 版中国专家共识强调从既往的治疗及采集前患儿评估筛选出预计动员不佳的患儿,选择合适的动员方案,使患儿的管理实现个体化、精细化[4]。共识中指出预计动员失败的预测因素包括治疗、患者自身、骨髓相关因素。治疗相关因素:①既往多线化疗(2 线化疗);②既往多个疗程化疗(6 个疗程化疗);③既往暴露过马法兰(累积剂量>150 mg)、氟达拉滨(>4 个疗程)、含铂治疗方案(2 个疗程)、来那度胺(4~6 个疗程)或大剂量阿糖胞苷(2 个疗程)等;④既往广泛骨髓放疗(特别是红骨髓部位,如骨盆、纵隔)。患者自身相关因素:①高龄(60~65 岁);②计划做序贯双次移植的患儿。骨髓相关因素:①动员时骨髓广泛侵犯;②动员时骨髓容积<30%;③血小板减少症。本研究中5 例患儿在采集前评估时均存在动员不佳危险因素。本研究在采集前筛选出含动员失败危险因素的患儿,同时监测采集前1 d CD34+细胞计数及采集第1 天采集物CD34+细胞计数调整动员策略,采集前1 d CD34+细胞计数<10 cells/µl 或者第1 天采集后预估采集失败率高的患儿当天在常规方案中联合普乐沙福进行动员。5 例患儿中有2 例是在动员第4 天监测CD34+细胞计数发现不足,及时给予普乐沙福;另3 例患儿第1 天采集后预估采集失败率高,当晚给予普乐沙福,一定程度上也是将预计动员不佳的患儿精细化分为两类,直接进行G-CSF+普乐沙福稳态动员与G-CSF+化疗基础上给予普乐沙福抢先干预。
本研究中5 例患儿,平均采集2.2 次,患儿1、3、4 采集了3 次,采集第1 天预估为动员失败可能性大后加用普乐沙福,患儿2、5 采集前加用了普乐沙福为稳态动员,患儿2 采集2 次,患儿5 采集1 次;使用普乐沙福后外周血CD34+细胞计数约为使用前外周血CD34+细胞计数的2 倍;5 例患儿中3 例采集干细胞CD34+细胞计数>2×106/kg。一项以色列单中心、开放标签、ⅡB 期临床研究显示[24]:G-CSF+普乐沙福稳态动员,1 次采集83%患儿达标;外周血CD34+细胞计数使用普乐沙福后为42.8 cells/µl,使用普乐沙福前为14.4 cells/µl,使用普乐沙福后外周血CD34+细胞计数较基线显著升高,提高了约3 倍。本研究成功率较既往研究偏低,考虑和患儿化疗次数多及使用含铂类化疗次数多及行放疗有关。研究同时发现,患儿3因第一次出现败血症原因,行2 轮化疗后再次行采集,此次采集前调整化疗方案未含有铂类,采集未使用普乐沙福也实现了动员达标,采集量与第一次联合普乐沙福采集量相当。提示采集前的化疗含铂类药物影响采集效果,建议避免,但是因本次研究中选取的患儿量少,因此仍需要更多研究进一步证实。
一项西班牙回顾性研究显示[15]:动员第4 天外周血CD34+细胞计数<3.5 cells/µl,单用G-CSF 组采集失败率为97%,而G-CSF+普乐沙福(G+P)组采集失败率为37%;第4 天外周血CD34+细胞计数3.5~10.0 cells/µl,G+P 组采集失败率为16%。本研究5 例患儿在采集前监测外周血 CD34+细胞计数,3 例患儿外周血CD34+细胞计数<3.5 cells/µl,采集第1 天预估为动员失败可能性大后加用普乐沙福;2 例患儿外周血 CD34+细胞计数3.5~10.0 cells/µl 采集前加用了普乐沙福;5 例患儿中2 例患儿采集干细胞CD34+细胞计数<2×106/kg;绝对动员不佳的患儿采集成功率较文献低,临界动员不佳成功率较文献高,因患儿例数少,需要扩充病例做进一步比较。本研究结果显示,对于预计动员不佳的患儿采集前监测CD34+细胞,及时给予普乐沙福,可有效提高成功率。目前5 例患儿中患儿1、3、4 已行自体干细胞移植,CD34+细胞计数分别为1.45×106/kg、2.16×106/kg、1.21×106/kg,2 例<2×106/kg。移植过程中,3 例患儿均达Ⅳ度骨髓抑制,Ⅰ~Ⅲ度口腔黏膜炎,血尿Ⅱ度,肝、肾、肺、心、脑、神经毒性反应0 度,合并中性粒细胞缺乏伴发热,无败血症,粒细胞及血小板均已植入,无移植相关死亡。提示CD34+干细胞虽未达到2×106/kg 标准,也可实现植入。
本研究5 例患儿未出现不良反应,较说明书及文献报道不良反应轻。陈秀慧等[25]报道,普乐沙福在干细胞动员不佳患儿中的疗效与安全性研究显示3 例患儿未见不良反应。卢桂馀等[26]报道,4 例患儿应用普乐沙福,均未出现不良反应。本研究不良反应与之相似。由此提示儿童耐受性好,因样本量少,需要更多研究进一步验证。
综上所述,PBSC 成功采集是移植的关键之一,普乐沙福为动员失败高风险患儿实现成功动员带来希望,基于采集前外周血CD34+干细胞计数指导下选用普乐沙福的动员模式,从含高危因素的患儿中筛出可以不使用普乐沙福即可采集成功的患儿,节省了费用,同时可以实现按需用药,及时用药。普乐沙福动员效果明显,为动员不佳的患儿带来福音,同时儿童使用不良反应轻微,值得临床推广应用。但本研究病例数少,具有一定局限性,未来需要更多更为深入的探索,为该领域的研究提供更加强有力的证据支持。

