眼科超声乳化手柄清洗方法及效果分析
□ 陈茹 CHEN Ru 马思文 MA Si-wen 陈丹琦 CHEN Dan-qi
白内障超声乳化技术作为白内障显微手术的一项突破性成果[1],其使白内障手术更加迅速高效,近年来白内障手术量日益增大[2]。超声乳化手柄是白内障超声乳化手术的核心手术器械[3],其再处理质量日益受到关注。超声乳化手柄由于其设计结构的特殊性以及受限的清洗方式,其清洗难度远大于一般眼科手术器械。首先,超声乳化手柄结构精密小巧,带有多条细长的管腔,增大了其再处理的难度[4]。其次,由于眼部细胞较人体其他组织细胞更为敏感,高浓度的清洗剂、消毒剂残留于器械表面会造成眼前节毒性反应综合症、角膜水肿、内皮细胞损伤等[5-9]。我国眼科手术管理、感染控制、消毒灭菌指南[10]不推荐使用清洗剂或消毒剂清洗超声乳化手柄,建议仅使用去离子水清洗此类手术器械。然而,在超声乳化手术中,常有晶状体皮质与粘弹剂残留于手柄管腔内,仅使用去离子水清洗可能无法完全清除此类物质。目前,国内外对超声乳化手柄是否需要使用洗涤剂,使用哪种洗涤剂可以既保证合格的清洗质量,又没有清洗剂残留的研究和报道较少,因此对这个问题的研究和探讨既有意义也有必要。
我院是浙江省唯一一家三级甲等眼科医院,目前共有24 个亚专科,5 个病区,手术中心共有20 个手术间。我院消毒供应中心自2018 年8 月搬入全新的医教楼之后,在建筑布局,仪器配置等方面都得到了较大的改善,符合行业标准和医院感控要求。2021 年1 月至2021 年12 月,我院共实施白内障超声乳化手术7518 台,玻璃体切除联合白内障手术2773 台,处理超声乳化手柄共计11213 个,平均每个工作日处理45 个超乳手柄。
对象和方法
1.研究对象。在日常工作中随机抽取使用后的超声乳化手柄共180 件,并随机分成三组,分别是碱性清洗剂组、多酶清洗剂组和纯化水组,每组60 件。超声乳化手柄纳入标准:(1)器械品牌为ALCON;(2)器械各零部件完整,接入配套超声乳化机时功能完好;(3)使用年限为0 ~3 年;(4)超乳手柄的手术使用时间为1 ~5 分钟,并在术后及时使用纯化水进行预处理;(5)超乳手柄表面无锈迹或肉眼可见明显污垢。
2.试验方法
2.1 碱性清洗剂组清洗方法。根据医院消毒供应中心行业标准[11],参照《眼科手术器械清洗消毒及灭菌技术操作指南》[12]和ALCON 超乳手柄说明书要求制定清洗方案:(1)冲洗:在流动水下冲洗器械表面,用水枪分别冲洗灌注和抽吸两条管路。(2)洗涤:选择眼科器械专用碱性清洗剂配置成合理的浓度,用低纤维絮纱布擦拭手柄表面,合适的管腔刷液面下进行灌注管腔和抽吸管腔的刷洗,用20mL 注射器灌满碱性清洗剂,冲洗手柄管腔至少3 次,至水流呈直线。(3)漂洗:流动水下冲洗器械表面,使用水枪冲洗两个管腔至少30 秒。(4)终末漂洗:用纯化水彻底冲洗器械表面,再次用纯水水枪冲洗管腔至少30s,使用PH 测试纸测试管腔内液体的PH 值。(5)消毒:用沾有75%乙醇的纱布进行器械外表面的擦拭消毒,用20mL 注射器抽取乙醇溶液冲洗各管腔。(6)干燥:使用热风气枪吹干超乳手柄器械表面和各管腔内的残余水滴。
2.2 多酶清洗剂组清洗方法。冲洗、漂洗、终末漂洗、消毒、干燥步骤同碱性清洗剂组。洗涤:选择眼科器械专用碱性清洗剂配置成合理的浓度,用低纤维絮纱布擦拭手柄表面,合适的管腔刷液面下进行灌注管腔和抽吸管腔的刷洗,用20mL注射器灌满碱性清洗剂,冲洗手柄管腔至少3 次,至水流呈直线。
2.3 纯化水组清洗方法。(1)冲洗:在流动水下冲洗器械表面,用水枪分别冲洗灌注和抽吸两条管路。(2)洗涤:用纯水再次冲洗超乳手柄表面,合适的管腔刷液面下进行灌注管腔和抽吸管腔的刷洗。(3)漂洗和终末漂洗:不使用任何洗涤剂,直接用纯水水枪冲洗器械外表面和各管腔,每条管腔冲洗时间不得少于1 分钟。(4)消毒:用沾有75%乙醇的纱布进行器械外表面的擦拭消毒,用20mL 注射器抽取乙醇溶液冲洗各管腔。(5)干燥:使用热风气枪吹干超乳手柄器械表面和各管腔内的残余水滴。
2.4 清洗效果的控制和检测。(1)实验的三组超乳手柄由同一清洗人员严格按照行业标准和指南进行清洗,由经过严格培训的同一采样人员进行采样,实验操作人员均经过严格培训考核通过后方可进行实验操作。(2)目测法:在20 倍带光源放大镜下,观察超声乳化手柄金属表面、手柄连接处、电源接头、螺纹缝隙等处的清洁度,各表面光洁,无血渍、污渍,无锈迹、水垢为合格[13]。(3)ATP 生物荧光法:取出路博ATP 水样采样拭子,对超声乳化手柄管腔中流出的洗脱液进行采样,再将拭子放入检测管内,立即振荡后放入路博QM6ATP 检测仪内操作读数,ATP 值≤45RLU 为合格。
3.统计学方法。采用SPSS 26.0 软件进行统计学分析。ATP 生物荧光法检测结果为计量资料,因数据不符合正态分布,故用中位数(第一四分位数,第三四分位数)表示,采用Kruskal Wallis H 检验进行比较;清洗合格率为计数资料,以频数、百分比表示,采用χ2检验进行比较,采用双侧检验,α=0.05,p<0.05 则为差异有统计学意义。
结果
结果表明,三组超声乳化手柄管腔及表面的清洗质量几乎相同,纯化水组、碱性清洗剂组、多酶清洗剂组三组间比较,差异无统计学意义(p=0.944)。三组超乳手柄管腔清洗质量的评价,ATP 生物荧光法检测3 组超乳手柄清洗合格率均为100%,见表1。
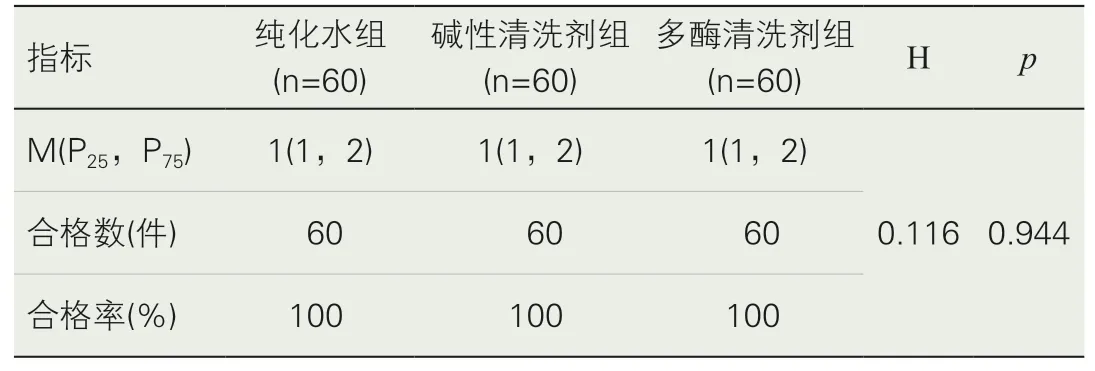
表1 ATP检测三组清洗效果
三组超乳手柄表面清洗质量的评价,使用目测法对三组进行检测,清洗合格率分别为98.3%、98.3%和100%,三组间比较,差异无统计学意义(p>0.999),见表2。
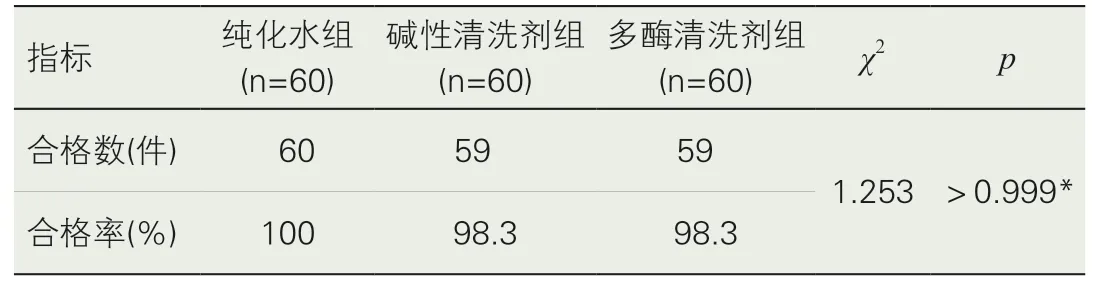
表2 目测法检测三组清洗效果
讨论
眼前节毒性反应综合征(toxic anterior segment syndrome,TASS)是一种眼前节急性非感染性炎症[14],发生的有关原因包括:灌注液、一切可进人眼内的药物、与眼内器械清洗和消毒有关的因素、人工晶状体及推注器、硅油、可进人眼内的医用异物、个体因素等[14]。
眼科手术器械以显微器械为主,由于其结构精密,常带有狭窄内腔与缝隙,致使清洗难度增大[15]。有研究报道,眼科手术器械已成为最常见清洗失败的手术器械之一[16]。超乳手柄是眼科器械中较独特,使用频次高的器械之一,使用后管腔内可能会残留晶状体皮质、粘弹剂、内毒素等物质,如果漂洗不到位亦可能残留清洗剂、消毒剂、水等物质,一旦进入到眼内极易引起TASS,对患者造成不必要的伤害。
眼科手术器械清洗消毒及灭菌技术操作指南中指出超乳手柄洗涤时要遵循眼科器械厂家说明书选择使用医用清洗剂[12],并制定了超乳手柄清洗的操作规程,但在使用哪种类型的清洗剂,如何规避TASS 的发生等方面均未做出明确的提示,在实际工作中,管理者仍然存在一些困惑。2016 版的我国眼科手术管理、感染控制、消毒灭菌指南[10]中指出不推荐使用清洗剂或消毒剂清洗超声乳化手柄,不同权威发表的观点亦存在前后矛盾之处。因此,超乳手柄规范的处理方法一直是眼科医生讨论的热点。
本研究试图寻找清洗超乳手柄的最佳方案,在其他条件不变的情况下,只变化清洗剂的种类,使用碱性清洗剂和多酶清洗剂,以及在不使用任何清洗剂只用纯化水清洗的情况下,来比较三种清洗方案的清洗效果是否合格。从结果可以看出,纯化水组、碱性清洗剂组、多酶清洗剂组的清洗质量均合格,清洗效果几乎相同,在考虑减少临床发生TASS 的情况下,宜直接使用纯化水清洗超乳手柄,而不使用任何其他清洗剂为最佳方案。
综上所述,与在酶洗环节中使用碱性清洗剂和多酶清洗剂相比,直接使用纯化水充分擦拭超乳手柄进行表面和冲洗管腔可以有效去除器械上晶状体皮质等污垢,并避免将清洗剂等物质带入眼内从而引发TASS。直接使用纯化水清洗超声乳化手柄是一种更安全有效的清洗方案。

