临床药师参与重症监护室感染性疾病会诊实践及切入点探讨*
宋龙辉,周 冉
(1. 安徽省濉溪县医院,安徽淮北 235100; 2. 中国科学技术大学附属第一医院·安徽省立医院,安徽合肥 230001)
国家六部委2020 年联合发布的《关于加强医疗机构药事管理促进合理用药的意见》中指出,在疑难复杂疾病多学科诊疗过程中,必须要有临床药师参与,指导精准用药,探索实施临床药师院际会诊制度[1]。参与临床会诊,优化感染性疾病的治疗,对临床药师的药学专业知识和临床思维能力提出了较高的要求,尤其是在重症监护室(ICU),由于危重症患者感染部位复杂、感染程度严重、细菌耐药率高,加之持续肾脏替代治疗(CRRT)、体外膜肺氧合(ECMO)等支持手段的影响,临床药师发挥自身专业特长,积极参与ICU感染性疾病会诊既重要又困难。本研究中评价了临床药师参与医院ICU 感染性疾病会诊的效果,并探讨了会诊中的药学切入点,为临床药师参与药学实践提供参考。现报道如下。
1 资料与方法
收集医院临床药师2021 年5 月至2022 年5 月参与ICU 抗感染治疗会诊的病例103 例,使用Excel 软件统计患者的性别、年龄、推测感染部位、检出病原体,会诊目的、会诊意见等情况。统计临床药师会诊意见采纳情况,临床医师完全或部分接受会诊意见为采纳,其余情况为未采纳。根据会诊24~48 h 后患者的症状、体征及实验室检查指标,结合临床医师的反馈评估疗效。有效,患者症状、体征、实验室检查3项中至少1项好转或恢复正常,无效,上述3项均未改善;其他,会诊后48 h内因患者自动出院、死亡等情况无法随访,无法获知疗效[2]。有效率(%)=有效例数/采纳(或未采纳)例数×100%。
2 结果
2.1 患者基本情况及感染部位
103例会诊患者中,男74例,女29例;年龄15~91岁,以≥75 岁最多,详见表1。41 例患者存在至少2 个部位感染,以肺部感染最多,详见表2。
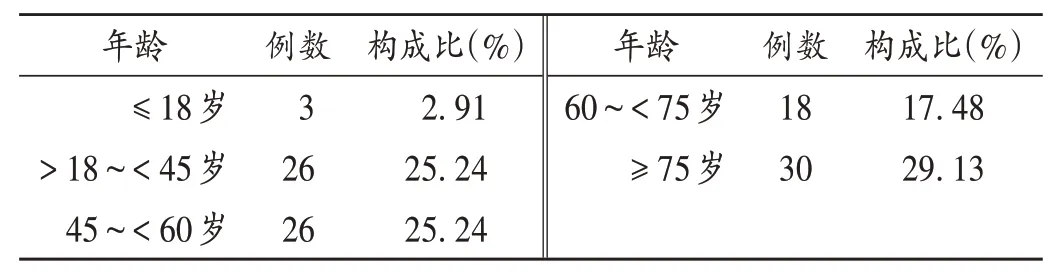
表1 会诊患者年龄分布(n=103)Tab.1 Distribution of ages of patients receiving consultation(n=103)

表2 会诊患者感染部位分布(n=149)Tab.2 Distribution of infection sites of patients receiving consultation(n=149)
2.2 病原体分布
共检出病原体139 份,包括宏基因组二代测序(NGS)结果49份(其中细菌25份,病毒15份,真菌9份),细菌培养结果79 份,真菌培养结果11 份(其中念珠菌7 份,曲霉2 份,冠耳霉、镰刀菌各1 份);合并并剔除重复结果后,总计检出病原体的患者72例。详见表3。

表3 检出病原体分布情况(n=131)Tab.3 Distribution of detected pathogens(n=131)
多重耐药(MDR)菌、广泛耐药(XDR)菌、泛耐药(PDR)菌的判断标准参考《MDR、XDR、PDR 多重耐药菌暂行标准定义——国际专家建议》[3]。耐药革兰阳性菌(G+)以金黄色葡萄球菌的MDR 菌为主;耐药革兰阴性菌(G-)中,MDR 菌主要为鲍曼不动杆菌和肺炎克雷伯菌,XDR菌主要为鲍曼不动杆菌;PDR菌2例,均为肺炎克雷伯菌。详见表4。

表4 细菌培养耐药情况(例次,n=79)Tab.4 Drug resistance of cultured bacteria(case,n=79)
2.3 会诊情况
会诊目的,103例中有55例为制订抗感染方案,32例为调整抗菌药物用法用量,16 例为病情评估及“降阶”治疗。
会诊意见采纳率为80.58%(83 / 103),其中有效54 例(65.06%),无效13 例(15.66%),其他16 例(19.28%);未采纳的20 例中,有效7 例(35.00%),无效8例(40.00%),其他5例(25.00%)。
2.4 典型病例分析
2.4.1 罕见病原微生物感染患者抗感染方案制订
病例1,男,57岁,因“发热伴意识障碍1周”入院,诊断为“病毒性脑炎、腔隙性脑梗死、肺部感染”。患者职业为屠夫,外院头颅磁共振(MRI)示双侧额顶叶、侧脑室旁、基底节区、脑干受累,治疗中出现高热、意识模糊、抽搐。入院第2 天,脑脊液生化结果示,蛋白质0.68 g/ L,葡萄糖2.95 mmol/ L,有核细胞计数48 × 106/ L;脑脊液涂片未检出细菌,脑脊液培养48 h 均为阴性,药师建议送检脑脊液NGS,回报结果提示猪α 疱疹病毒1 型(序列数19),临床遂请药师会诊指导制订抗感染方案。
猪α 疱疹病毒1 型又称伪狂犬病毒(PRV),为以猪为自然宿主的双链DNA 病毒。2017 年,AI 等[4]首次在基因水平上证实了PRV 可跨物种感染人,引起脑炎、视网膜炎及肺炎[5-6]。在中枢神经系统感染(CNSI)中,NGS 技术能显著提高新发、罕见、疑难感染性疾病的病原体检出率,可作为上述疾病的一线检测手段(A 级推荐,Ⅲ级证据)[7]。目前临床对于PRV 感染所致CNSI 缺少实验室检测手段,脑脊液NGS 是确诊的主要依据[8]。既往研究显示,PRV 感染临床症状以高热、癫痫、意识障碍、呼吸衰竭、视力障碍、头痛为主;脑脊液检查常伴白细胞计数(WBC)、蛋白质升高,葡萄糖正常或升高;脑炎患者MRI 可示边缘系统、基底节区、脑干的异常病灶[5]。文献[9]报告了4 例PRV 脑炎患者的脑脊液NGS结果(7~6 198条序列,覆盖率0.244 6%~80.58%)。该患者病前有明确的猪肉加工及接触史,脑脊液涂片、培养均为阴性,NGS 阳性,脑脊液常规与生化结果、临床症状、影像学表现均符合相关文献报道,药师认为PRV脑炎诊断明确。早期足量的抗病毒治疗对部分患者有效[5],可采用阿昔洛韦、更昔洛韦、喷昔洛韦、伐昔洛韦、膦甲酸等,重症患者可联用激素或免疫球蛋白治疗。药师建议给予阿昔洛韦(每次0.75 g,每8 h 1 次,静脉滴注)抗病毒治疗,根据该患者临床体征结合感染指标、影像学改变可联合膦甲酸。医师采纳会诊意见后,给予患者阿昔洛韦联合甲泼尼龙及人免疫球蛋白,治疗21 d后停药,复查脑脊液NGS提示PRV阴性,炎症指标降低,呼吸循环稳定,抗感染治疗有效,遂未再联合膦甲酸。
2.4.2 特殊人群通过治疗药物监测(TDM)制订个体化精准治疗方案
病例2,男,51 岁,因“多发伤10 d 伴发热7 d”入院,诊断为“发热、严重多发伤、重度颅脑损伤、急性呼吸衰竭、2型糖尿病”。患者外院治疗中行腹腔干造影+髂动脉造影+ 髂动脉栓塞术;左侧外伤大骨瓣开颅脑挫裂伤,予脑内血肿清除+去骨瓣减压术,术后予头孢曲松+阿米卡星,血培养见表皮葡萄球菌、痰培养见黏质沙雷菌,调整为头孢他啶+万古霉素抗感染治疗,患者病情无好转。入院后考虑CNSI,予美罗培南(每次2 g、每8 h 1次)+万古霉素(每次1 g、每12 h 1次)静脉滴注抗感染治疗3 d 后,测得万古霉素血药谷浓度为6.19 μg/mL,临床遂请药师会诊,协助调整用药方案。
根据《中国万古霉素治疗药物监测指南(2020 更新版)》推荐意见[10],推荐万古霉素血药谷浓度为10~20 μg/mL。临床药师排除TDM 标本采集时间及操作误差后,认为结果可信,患者血清肌酐(SCr)为54 μmol/ L,使用Cockcroft-Gault(CG)公式计算得患者的肌酐清除率(CCr)为135.59 mL/min[>130 mL/(min·1.73 m2)[11-12]],提示肾功能亢进(ARC)。ARC 多见于危重症患者,目前认为ARC 发生的危险因素有男性、年龄相对较小(≤50 岁)、创伤、颅脑损伤、序贯性器官功能衰竭评分(SOFA)较低等[13],该患者合并多项可能导致ARC 的危险因素,其ARC 发生从入院第4 天持续至出院。因ARC 能显著加快经肾脏代谢药物的清除导致治疗失败[14],而万古霉素是糖肽类抗菌药物,主要通过肾小球滤过而在尿液中排泄,故肾功能是万古霉素药物代谢动力学(PK)和剂量的决定性因素。药师查阅文献发现,现有文献均推荐ARC 患者的万古霉素维持较高剂量。如HE 等[15]研究认为,ARC患者为达到10 μg/mL的万古霉素血药谷浓度,维持剂量应达到46 mg/(kg·d),若目标谷浓度为15 μg/mL,则需25 mg/kg的负荷剂量及69 mg/(kg·d)的维持剂量,给药剂量需根据TDM 结果进行个体化调整。石璐等[16]通过蒙特卡罗模拟优化ARC 患者万古霉素给药方案,建议最低抑菌浓度(MIC)为0.5 mg/L 时,给予万古霉素2 g/ d,可实现达标概率(PTA)> 90%;MIC= 1 mg/ L 时,给予4.5 g/ d 才可实现PTA > 90%;MIC≥2时,常规剂量(2~4 g/d)很难达标。因此药师认为万古霉素给药剂量不足,建议调整为每次1 g、每8 h 1次,临床采纳。给药4剂后,测得万古霉素血药谷浓度为8.48 μg/mL,仍低于目标值,临床再次申请会诊。此时患者SCr 54 μmol/ L,CCr 146.44 mL/ min,仍存在ARC,药师认为继续增加万古霉素的日剂量可能导致肾毒性等不良反应发生率的增加。既往研究发现,对于同一患者,万古霉素延长输注时间可在不提高日总剂量的情况下提高其血药谷浓度[13,17];SILVA 等[14]的综述认为,对于ARC 患者,抗菌药物的常规给药剂量只有延长或连续输注,才能成功在PTA > 90%时达到PK/ 药物效应动力学(PD)目标,延长或连续输液可增加血浆药物暴露时间(%T)大于MIC的覆盖率,建议ARC 患者使用万古霉素及其他药物(如美罗培南)时延长或持续输注;因此药师建议延长万古霉素输注时间4~6 h,同时延长美罗培南输注时间3 h,临床采纳,48 h后患者复测万古霉素血药谷浓度11.42 μg/mL,已达目标值,患者WBC 由10.11×109/L 降至7.79×109/L,中性粒细胞百分比(Neut%)由91.6%降至85.3%,降钙素原(PCT)由0.66 ng/mL 降至0.21 ng/mL,C 反应蛋白(CRP)由114.22 mg/ L 降至36.64 mg/ L,表明调整方案后抗感染有效。
2.4.3 根据抗菌药物PK/PD 调整抗感染方案
病例3,男,47 岁,因“胸闷呼吸困难5 d”入院,诊断为“重症肺炎、呼吸衰竭、急性肾功能不全”。入院后血病原学二代测序提示耶氏肺孢子菌,给予复方磺胺甲噁唑(SMZ)/ 甲氧苄啶(TMP)复合制剂+ 莫西沙星抗感染治疗。入院后第3天,患者呼吸窘迫未改善,氧合指数< 100 mmHg(1 mmHg = 0.133 kPa),遂行静脉- 静脉(VV)-ECMO,患者持续高热,换莫西沙星为万古霉素。入院后第8 天,血钾6.28 mmol/ L,肌酐持续上升,同时行床旁CRRT[连续静脉- 静脉血液滤过(CVVH)模式],由于患者出现寒战高热,WBC 10.11 × 109/ L,Neut%97.3%,CRP 307.18 mg/ L,PCT 1.550 ng/ mL,临床拟加亚胺培南西司他丁加强抗感染,遂请临床药师会诊,调整抗感染药物给药剂量。
重症患者行CRRT 时,药物的总清除率为肾脏清除率、肾外清除率和CRRT清除率之和,若CRRT清除率占药物总清除率的25%及以上,则应调整给药剂量[18]。研究证实,在CVVH 模式下,亚胺培南的CRRT 清除率可达(2.211±0.539)L/h,占总清除率的(30.1±15.7)%[19],药师认为需调整亚胺培南剂量为0.5~1 g,每12 h 1次。同时患者行ECMO支持治疗,表观分布容积由于预充和液体复苏的原因增大,加之管路和膜肺对药物的吸附,均将导致有效药物浓度降低[18]。研究认为,给予亚胺培南每次1 g、每8 h 1 次,MIC= 2 mg/ L 时可实现%T >MIC,当MIC= 4 mg/ L 时只有部分患者实现%T >MIC[20],而重症患者为获得最佳疗效,往往需要%T >4~5 倍MIC[18],因此建议对于实施ECMO 的重症患者,可考虑给予高剂量亚胺培南(每次1 g、每6 h 1 次),以达到有效抗微生物治疗的PK/PD 目标[21]。最终药师考虑患者同时予ECMO和CRRT支持治疗,建议予亚胺培南每次1 g、每8 h 1次、静脉滴注。DHANANI等[22]研究发现,SMZ/TMP在ECMO与非ECMO患者中的PK特征(两药各自的清除率)无显著差异,认为行ECMO治疗患者可能无须调整SMZ/ TMP 剂量。研究证实,在CVVH 及持续静脉- 静脉血液透析(CVVHD)模式下,CRRT 可导致TMP的清除率显著高于SMZ,建议以TMP 10 mg/(kg·d)计算SMZ/TMP 日总剂量,并以12 h 1 次分次给药[23]。综上,临床药师认为仅需考虑CRRT 对SMZ/TMP 的影响,建议予SMZ/TMP每次1.92 g、每12 h 1次、口服。近年来,关于万古霉素在ECMO 中的PK 研究表明,ECMO对该药影响较小[21],但PARK 等[24]的研究发现,ECMO患者在治疗初期万古霉素血药谷浓度达标率显著低于非ECMO 患者(66.7%比95.0%,P< 0.05),可能原因为ECMO使用的初始阶段循环容量增加,血液稀释导致药物浓度不足。LI等[23]的研究认为,万古霉素为大分子药物,受CRRT 影响较大,超滤模式及超滤液流速的选择也造成其清除效率的不同,CVVH 模式的清除率理论上大于CVVHD,因此在不同CRRT 模式下推荐了不同的维持剂量[CVVH,400~650 mg,每12 h 1次;CVVHD,500 mg,每8 h 1 次;连续性静脉- 静脉血液透析滤过(CVVHDF),500 mg,每24 h 1 次],并建议根据患者的TDM 结果进行个体化调整。因患者已使用万古霉素治疗5 d,药师认为万古霉素血药浓度已达稳态,考虑ECMO 对其血药浓度影响较小,应依据CRRT 调整,建议予万古霉素每次0.5 g、每12 h 1次、静脉滴注,调整抗感染药物剂量治疗,2 d 后患者WBC 由10.11 × 109/ L降至5.01 × 109/ L,CRP 由145 mg/ L 降至113 mg/ L,表明抗感染有效。72 h 后万古霉素血药谷浓度为15.97 μg/mL,达目标值。
2.4.4 XDR 感染患者抗感染方案调整
病例4,男,40 岁,因“脑外伤1 月余”入院,诊断为“重症肺炎、呼吸衰竭、粒细胞缺乏、闭合性颅脑损伤重型”。入院后CT 提示两肺弥漫性间质病变,给予美罗培南抗感染治疗,第4天血培养结果提示非耐药铜绿假单胞菌及XDR 肺炎克雷伯菌,药物敏感性试验结果提示仅对多黏菌素、替加环素、头孢他啶/ 阿维巴坦(CAZ/AVI)敏感,对其余药物耐药,痰培养结果亦提示XDR肺炎克雷伯菌。患者粒细胞缺乏伴发热,WBC 2.3×109/L,Neut% 47.7%,PCT 33.16 ng/ mL,CRP 133.35 mg/ L,考虑耐碳青霉烯类的肺炎克雷伯菌(CR-KP)感染,遂请临床药师会诊,调整抗感染方案。
肺炎克雷伯菌是临床常见的医院或社区获得性感染病原菌,可引起血流感染、肺部感染、尿路感染等。CR-KP 为耐碳青霉烯类肠杆菌科细菌(CRE),研究表明,CR - KP 血流感染患者的死亡率明显更高(52.2%~71.4%),其高死亡率与抗菌药物选择不当相关[25]。CR-KP治疗常需联合用药[26],主要方案有以多黏菌素、替加环素或碳青霉烯类为基础(MIC≤8 mg/ L)的两药或三药联合治疗,以及其他联合治疗如CAZ/AVI+氨曲南、磷霉素+氨基苷类等。目前,患者存在血流感染和肺部感染,病原学上存在XDR 肺炎克雷伯菌和非耐药铜绿假单胞菌,由于替加环素抗菌谱无法覆盖铜绿假单胞菌,药师认为应采用以CAZ/AVI 或多黏菌素为基础的治疗方案。VAN DUIN 等[27]的研究比较了CAZ/ AVI 和多黏菌素对CRE 感染(97%为CR - KP感染)的疗效,其中血流(46%)和肺部(22%)感染较多,使用CAZ/ AVI 的30 d 病死率显著低于使用多黏菌素(9%比32%,P< 0.01);HAKEAM 等[28]的研究显示,CRE 血流感染患者中,CAZ/AVI 的14 d 死亡风险较多黏菌素更低,临床治疗成功率更高(46.8%比20.4%,P=0.047)。加之多黏菌素在CRE引起的血流感染中存在异质性耐药问题[26],因此临床药师建议调整抗感染方案为CAZ/AVI 每次2.5 g、每8 h 1 次、静脉滴注2 h。CAZ/AVI 对产金属β 内酰胺酶的CRE 无效,这类感染多需联合氨曲南治疗[25],因药物敏感性试验结果提示对CAZ/ AVI 敏感,药师认为可排除产金属酶的CR -KP,不必再联合氨曲南。治疗2 d 后,患者PCT 降至2.366 ng/ mL,CRP 降至103.07 mg/ L,中性粒细胞绝对值由未测出升至1.1×109/L,表明抗感染有效。
3 讨论
重症感染、感染性休克,一直是临床面临的难题(死亡率为20%~30%)[18]。危重症患者由于低蛋白血症、脏器功能损伤、体内液体容量和高动力循环状态的急剧变化,常导致抗菌药物的代谢和清除显著异于普通患者,因此,如何个体化、精准化地合理使用抗菌药物是临床药师发挥自身专业特长参与临床治疗极为重要的切入点,本研究中列举了临床药师的4个药学会诊切入点,可为相应疾病的临床诊治提供思路。103 例会诊病例中,会诊意见采纳率超80%,表明临床对药师会诊质量的认可度较高,获采纳会诊意见的有效率高于未采纳的会诊意见,表明临床药师参与会诊,协助制订治疗方案,对促进患者病情改善起到了重要作用。通过探寻更多、更适宜的药学会诊切入点,可进一步提升临床合理用药水平。

