基于UPLC特征图谱和一测多评法的穿心莲药材质量研究
李振雨,赵书运,刘晓霞,何民友,冯涌微,位翠杰,张芳平,邓淙友,陈向东,孙冬梅
广东一方制药有限公司,广东省中药配方颗粒企业重点实验室,广东 佛山 528244
穿心莲为爵床科植物穿心莲Andrographis paniculata(Burm.f.)Nees.的干燥地上部位[1],是常用的清热解毒中药。其代表性有效成分为二萜内酯,除可抗病原微生物、治疗感染性疾病外,还具有保肝、利胆、抗肿瘤、调节免疫、治疗心脑血管系统疾病的作用[2-5]。此外,穿心莲含有较多的黄酮和酚酸类成分[6-8],均在其药效中发挥重要作用[9]。目前,对穿心莲指纹图谱的研究报道多集中于对二萜内酯类成分的表征方面[10-12],而对穿心莲中黄酮和酚酸类成分的指认和表征报道较少。指纹/特征图谱结合一测多评模式将定性、定量相结合,能够发挥中药多指标质量控制的优势[13],尤其是超高效液相色谱法(UPLC)的使用,可提高化学成分的分析效能,缩短分析周期[14]。本研究采用UPLC建立穿心莲药材特征图谱,利用高分辨质谱对图谱中的主要色谱峰进行质谱分析,结合一测多评法(QAMS)定量模式,为穿心莲药材的整体质量控制提供参考。
1 仪器与试药
Themo Vanquish 超高效液相色谱仪、Thermo Vanquish Flex超高效液相-Thermo Fisher QE高分辨质谱联用仪,赛默飞世尔科技有限公司;JJ600型百分之一天平,常熟市双杰测试仪器厂;ME204E型万分之一天平、XP26型百万分之一天平,梅特勒-托利多公司;KQ-500DE型数控超声波清洗器,昆山市超声仪器有限公司。
对照品绿原酸(批号110753-201706,含量99.3%)、穿心莲内酯(批号110797-201609,含量99.7%)、脱水穿心莲内酯(批号110854-201710,含量99.4%),中国食品药品检定研究院;对照品14-去氧穿心莲内酯(批号wkq19012203,含量98%)、新穿心莲内酯(批号wkq18120308,含量98%)、木犀草素-7-Oβ-D-葡萄糖醛酸(批号wkq20211875,含量≥98%)、芹菜素-7-O-葡萄糖醛酸苷(批号wkq20021905,含量≥98%),四川省维克奇生物科技有限公司。乙腈(色谱纯),默克股份有限公司;甲醇(分析纯),西陇科学股份有限公司;磷酸(色谱纯),天津市科密欧化学试剂有限公司。12批穿心莲药材由广东一方制药有限公司采购管理部采收,经广东一方制药有限公司魏梅主任中药师鉴定为爵床科植物穿心莲Andrographis paniculata(Burm.f.)Nees.的干燥地上部分,来源信息见表1。
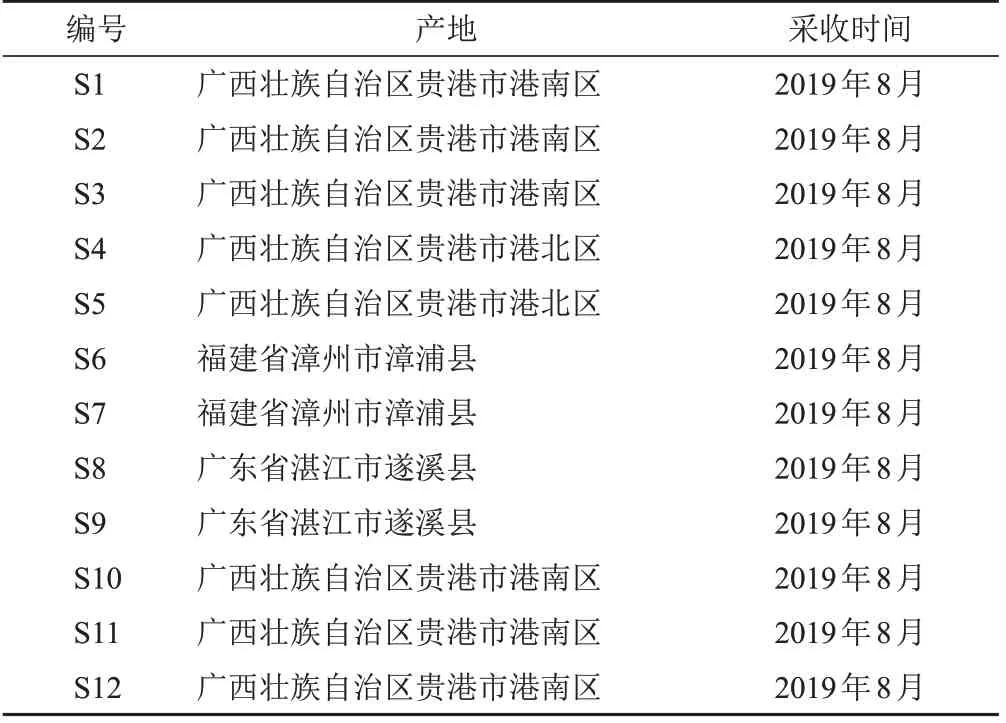
表1 穿心莲药材样品来源信息
2 方法与结果
2.1 特征图谱建立
2.1.1 液相色谱和质谱条件
色谱条件:采用ACQUITY UPLC HSS T3色谱柱(2.1 mm×100 mm,1.8 μm);流动相A为乙腈、B为0.075%磷酸水溶液,高分辨质谱分析时流动相B 为0.1%甲酸水溶液,梯度洗脱(0~7 min,8%→19%A;7~16 min,19%→28%A;16~28 min,28%→50%A);流速0.3 mL/min;柱温25 ℃;检测波长205 nm;进样量1 μL。
质谱条件:电喷雾离子源,喷雾电压3.80 kV,正、负离子扫描模式,扫描范围100~1 500 m/z;鞘气流速35 Arb;辅助气流速10 Arb;毛细管温度350 ℃;辅助器加热温度350 ℃;碰撞能量在负离子模式下为40 EV,正离子模式下为60 EV;S-lens电压50 V。
2.1.2 对照品溶液制备
精密称取对照品穿心莲内酯、脱水穿心莲内酯、新穿心莲内酯和14-去氧穿心莲内酯适量,加甲醇制成每1 mL 含穿心莲内酯169.370 μg、脱水穿心莲内酯120.274 μg、新穿心莲内酯106.428 μg、14-去氧穿心莲内酯88.514 μg的混合溶液,摇匀,即得。
2.1.3 供试品溶液制备
取穿心莲药材粉末(过4号筛)约0.5 g,精密称定,置具塞锥形瓶中,精密加入40%甲醇25 mL,称定质量,超声处理(功率250 W,频率40 kHz)30 min,放冷,再称定质量,用40%甲醇补足减失的质量,摇匀,过滤,取续滤液,即得。
2.1.4 特征图谱方法学考察
2.1.4.1 精密度试验
取穿心莲药材(编号S3)供试品溶液,按“2.1.1”项下色谱条件重复进样6次,记录特征图谱,以穿心莲内酯峰为参照峰S,计算各共有特征峰与S峰的相对保留时间RSD 为0.01%~0.25%,相对峰面积RSD 为0.06%~0.87%,表明该方法精密度良好。
2.1.4.2 重复性试验
取穿心莲药材粉末(编号S3,过4号筛)约0.5 g,平行6份,按“2.1.3”项下方法制备供试品溶液6份,按“2.1.1”项下色谱条件进样分析,记录6份样品特征图谱,以穿心莲内酯峰为参照峰S,计算各共有特征峰与S峰的相对保留时间RSD为0.03%~0.12%,相对峰面积RSD为0.24%~2.72%,表明该方法重复性良好。
2.1.4.3 稳定性试验
取“2.1.4.2”项下供试品溶液,按“2.1.1”项下色谱条件,分别于0、2、4、8、10、12、24 h进样分析,记录不同时间点样品特征图谱,以穿心莲内酯峰为参照峰S,计算各共有特征峰与S峰的相对保留时间RSD 为0.04%~0.17%,相对峰面积RSD 为0.35%~2.65%,表明供试品溶液在24 h内稳定性良好。
2.1.5 特征图谱
按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件,对12批穿心莲药材进行特征图谱测定,记录色谱图,利用Chromeleon7.3软件导出特征图谱CDF格式,并导入国家药典委员会《中药色谱指纹图谱相似度评价系统》(2012.130723版),以S1样品特征图谱为参照图谱,时间窗宽度设定为0.1 min,进行多点校正和色谱峰匹配,选择分离度较好、纯度较高且成分已知的共有峰作为穿心莲药材特征图谱的特征峰。12批穿心莲药材特征图谱共标出12个特征峰,样品叠加图见图1。采用中位数法自动生成穿心莲药材对照特征图谱,见图2。
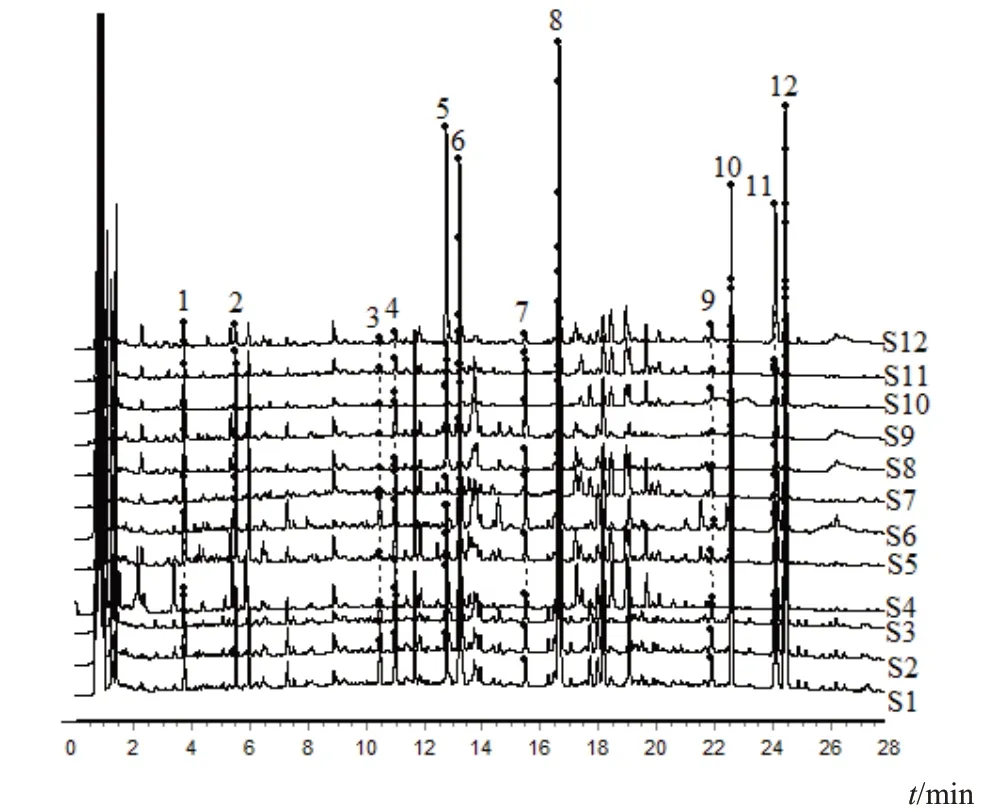
图1 12批穿心莲药材特征图谱叠加图
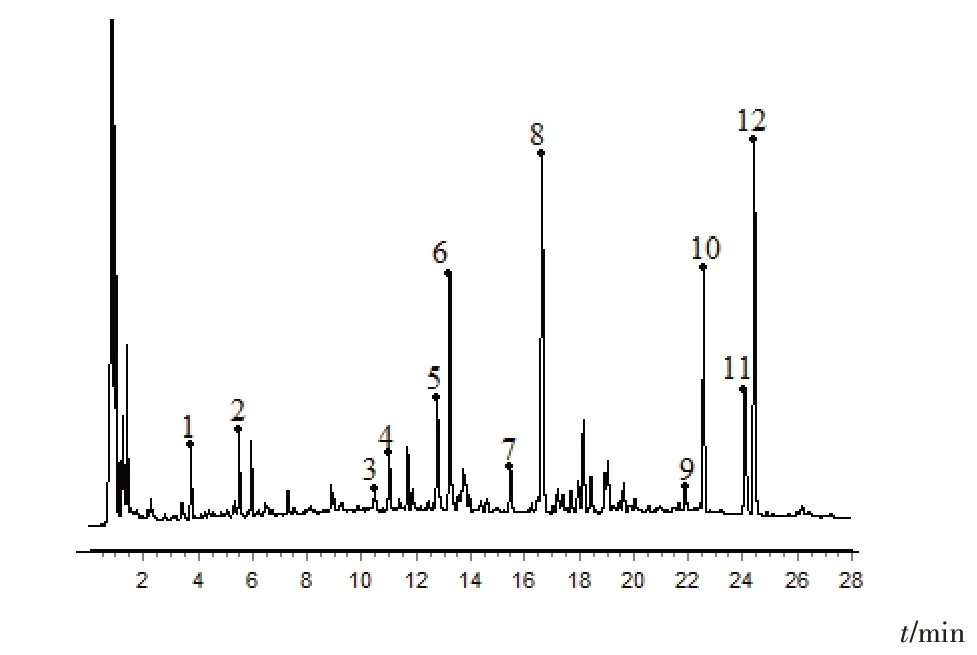
图2 穿心莲药材对照特征图谱
2.1.6 相似度评价
分别计算12批穿心莲药材特征图谱与对照特征图谱的相似度,结果见表2。12批样品相似度为0.905~0.995,均大于0.9,整体相似度较高,表明特征图谱能够用于穿心莲药材的鉴别和质量表征。
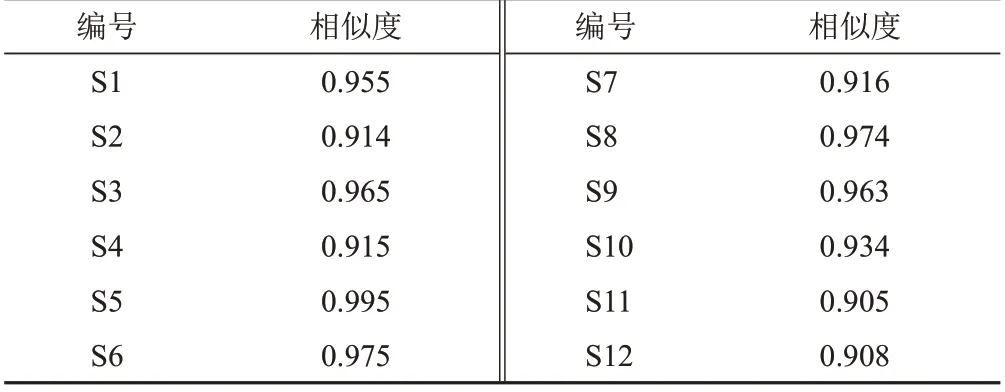
表2 12批穿心莲药材特征图谱相似度评价
2.1.7 共有峰指认与确认
通过质谱精确分子量、碎片离子对比分析,对穿心莲药材特征图谱12个特征峰进行指认。按“2.1.1”项下液相色谱和质谱条件,采集正、负离子扫描模式下总离子流(TIC)图,见图3。结果显示,正离子模式下,穿心莲中的二萜内酯类成分信息更完整,考虑到负离子模式下酚酸、黄酮类成分的裂解模式更明确,因此,选择正、负离子同时扫描分析,保证未知成分得到最大限度的指认。通过目标成分精确分子量、二级碎片信息、裂解模式分析,并结合mzCloud标准数据库的成分比对,指认出其中7个特征性成分(见表3)。经与对照品保留时间及紫外吸收光谱比对,进一步确认峰2为绿原酸,峰4为木犀草素-7-O-β-D-葡萄糖醛酸苷,峰6为芹菜素-7-O-葡萄糖醛酸苷,峰8为穿心莲内酯,峰10为新穿心莲内酯,峰11为14-去氧穿心莲内酯,峰12为脱水穿心莲内酯,结果见图4。
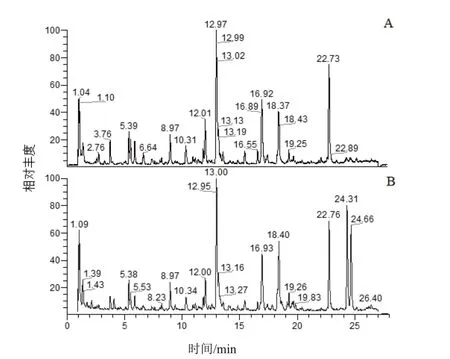
图3 穿心莲药材TIC图
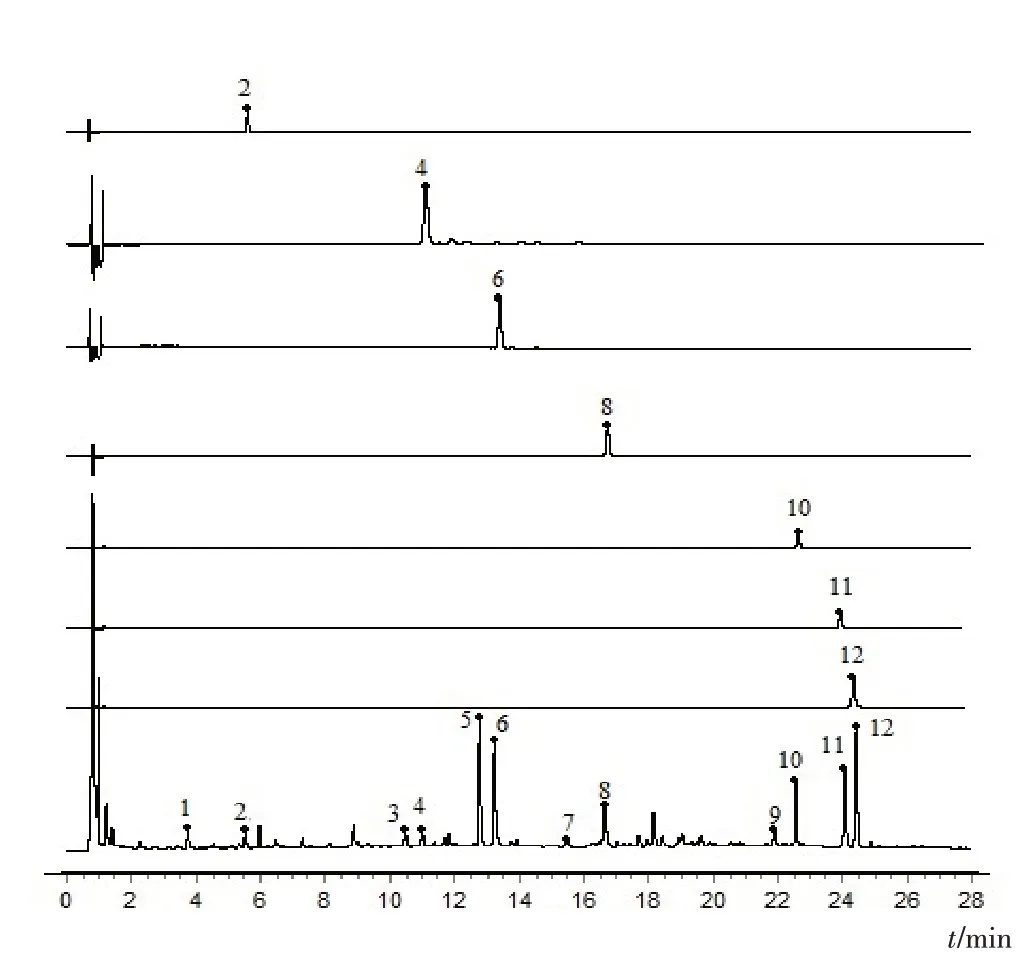
图4 穿心莲药材特征图谱共有峰确认
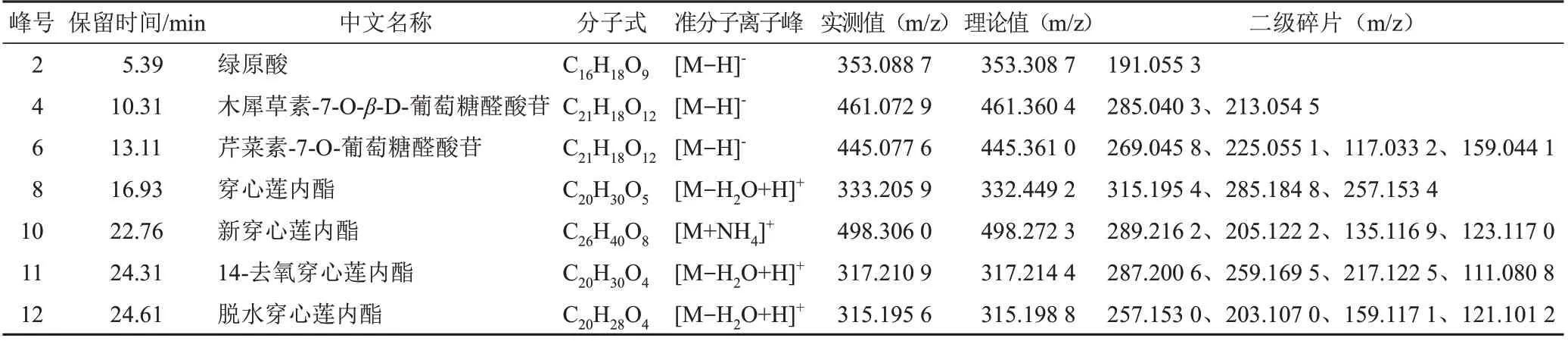
表3 穿心莲药材特征图谱共有峰质谱指认
2.2 一测多评法建立
2.2.1 精密度试验
精密吸取“2.1.2”项下混合对照品溶液,按“2.1.1”项下色谱条件重复进样6次,记录穿心莲内酯、新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯的色谱峰面积,并计算峰面积RSD 分别为0.38%、0.40%、0.37%和0.37%,表明仪器精密度良好。
2.2.2 线性关系考察
精密称定对照品穿心莲内酯20.169 mg、新穿心莲内酯13.884 mg、14-去氧穿心莲内酯5.446 mg、脱水穿心莲内酯22.635 mg,置25 mL 量瓶中,加甲醇至刻度,即得混合对照品贮备液。精密量取上述对照品贮备液1.0 mL,分别置2、5、10、25、50 mL 量瓶中,加甲醇制成系列浓度的混合对照品工作液;分别取上述混合对照品贮备液和混合对照品工作液,按“2.1.1”项下色谱条件依次进样1 μL,记录色谱峰面积,以峰面积为纵坐标,对照品浓度为横坐标,绘制标准曲线,计算回归方程和相关系数(r),结果见表4。各成分在相应范围内峰面积与对照品浓度线性关系良好。
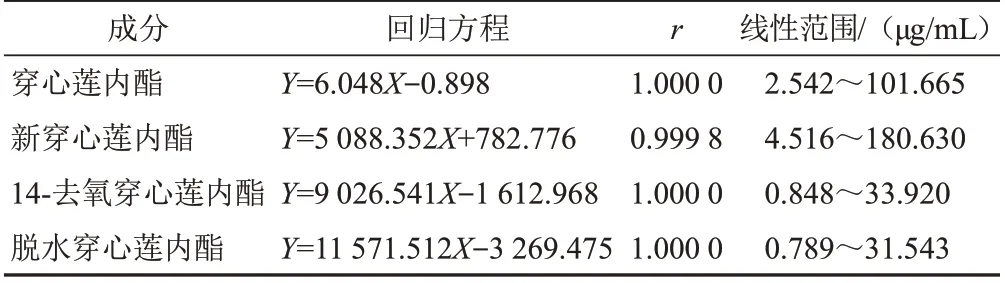
表4 4个成分线性关系考察结果
2.2.3 重复性试验
取穿心莲药材粉末(编号S3,过4号筛)约0.5 g,精密称定,平行称定6份,按“2.1.3”项下方法制备供试品溶液6份,每份精密吸取1 μL,按“2.1.1”项下色谱条件进样分析,外标法计算穿心莲内酯、新穿心莲内酯、14-去氧穿心莲内酯、脱水穿心莲内酯的含量分别为11.248、9.415、2.950、8.648 mg/g,RSD分别为0.21%、0.57%、0.72%、0.63%。
2.2.4 稳定性试验
取穿心莲药材粉末(编号S1,过4号筛)约0.5 g,精密称定,按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件,分别于0、2、4、8、10、12、24 h进样,记录穿心莲内酯、14-去氧穿心莲内酯、新穿心莲内酯和脱水穿心莲内酯的峰面积,并计算峰面积RSD为0.17%~1.02%,表明供试品溶液在24 h内稳定性良好。
2.2.5 加样回收率试验
取对照品穿心莲内酯14.105 mg、新穿心莲内酯12.065 mg、14-去氧穿心莲内酯3.780 mg、脱水穿心莲内酯10.885 mg,置于10 mL 量瓶中,加甲醇制成每1 mL含穿心莲内酯1.406 mg、新穿心莲内酯1.182 mg、14-去氧穿心莲内酯0.370 mg、脱水穿心莲内酯1.082 mg的混合对照品溶液。精密吸取上述混合对照品溶液1.0、2.0、3.0 mL于具塞锥形瓶中,分为3组,每组平行3份,共9份,挥干溶剂,再取已知含量的穿心莲药材粉末(编号S3,过4号筛)约0.25 g,精密称定,置上述9个锥形瓶中,按“2.1.3”项下方法制备供试品溶液9份,按“2.1.1”项下色谱条件测定,计算穿心莲内酯、新穿心莲内酯、14-去氧穿心莲内酯、脱水穿心莲内酯的平均加样回收率分别为99.06%、101.17%、100.20%、101.13%,RSD 分别为2.62%、1.35%、1.22%、1.24%,结果见表5。
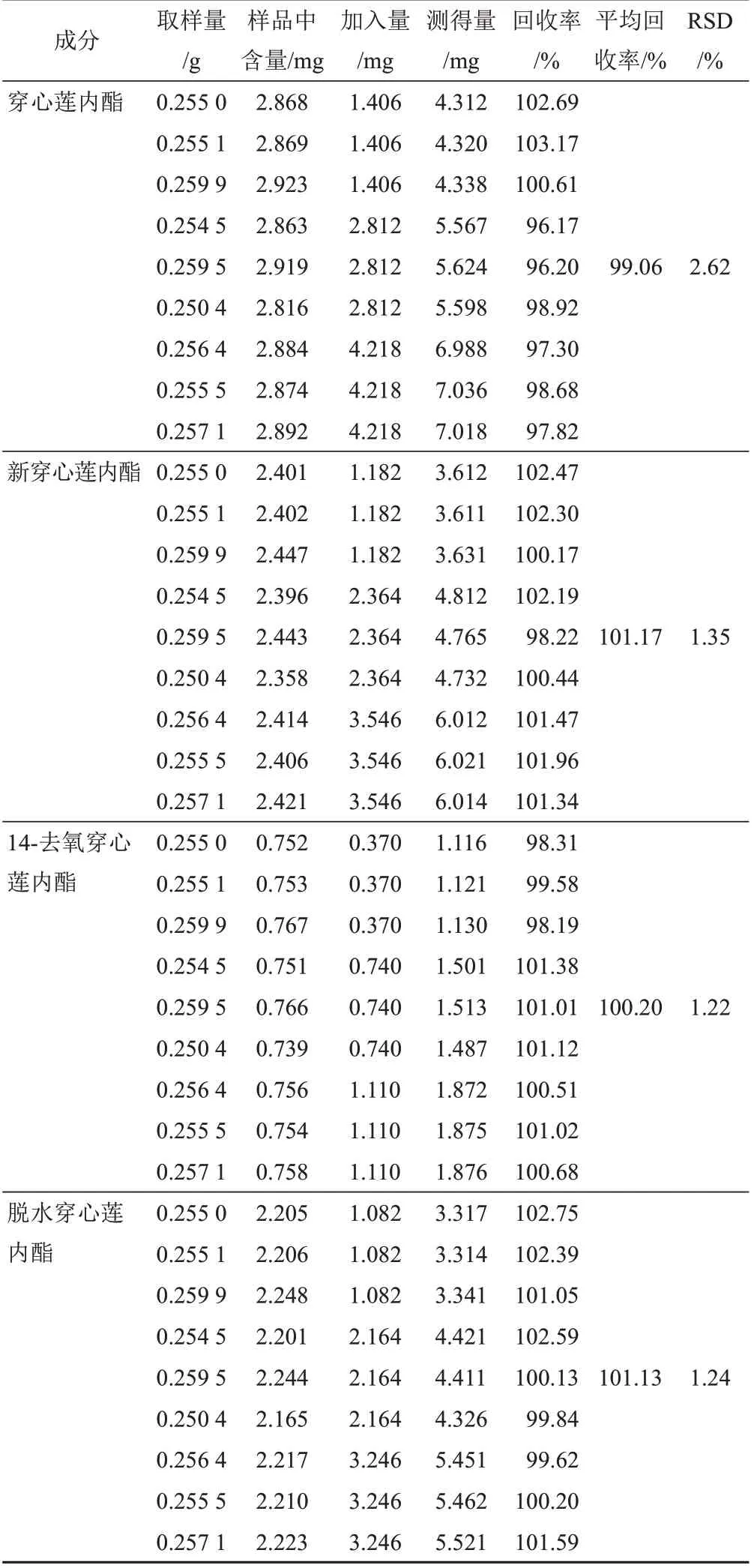
表5 穿心莲中4个成分加样回收率试验结果
2.2.6 相对校正因子计算
以穿心莲内酯为参照,根据“2.2.2”项下线性关系考察结果,以对照品浓度及其对应的色谱峰面积,分别计算新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯的相对校正因子(f)。f参照/待测=(C待测×A参照)÷(C参照×A待测)。式中,C为对照品浓度,A为对照品峰面积。结果新穿心莲内酯、14-去氧穿心莲内酯、脱水穿心莲内酯的平均相对校正因子分别为1.07、0.81、0.61,见表6。
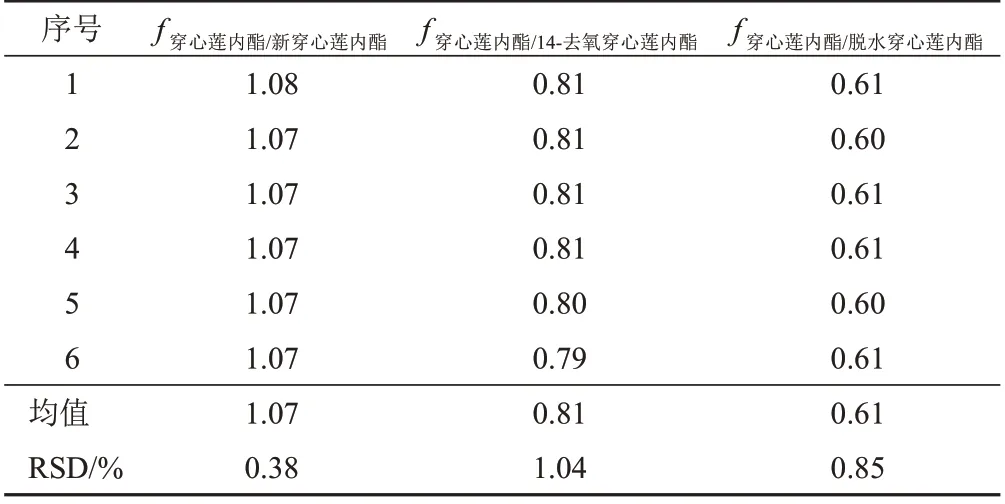
表6 穿心莲中3个成分相对校正因子计算结果
2.2.7 系统适用性试验
2.2.7.1 不同色谱柱考察
以穿心莲内酯为参照,计算新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯在不同品牌色谱柱上的相对保留时间和相对校正因子,结果见表7。上述3个成分的相对保留时间RSD为1.39%~2.72%,相对校正因子RSD为0.93%~2.49%,表明不同品牌色谱柱对新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯的相对保留时间和相对校正因子影响较小。

表7 不同色谱柱的穿心莲中3个成分相对保留时间和相对校正因子测定结果
2.2.7.2 不同流速考察
以穿心莲内酯为参照,计算新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯在不同流速下的相对保留时间和相对校正因子,结果见表8。上述3个成分的相对保留时间为1.04%~1.47%,相对校正因子RSD为0.93%~2.52%,表明不同流速对新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯的相对保留时间和相对校正因子影响较小。
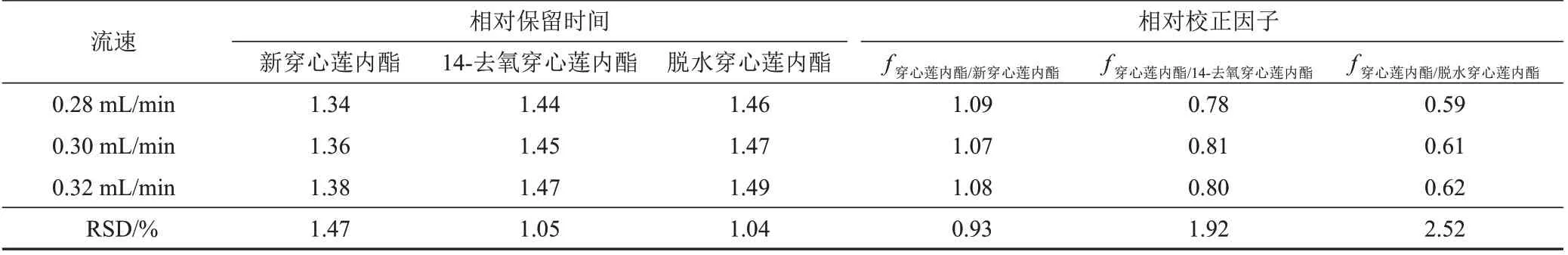
表8 不同流速的穿心莲中3个成分相对保留时间和相对校正因子测定结果
2.2.7.3 不同柱温考察
以穿心莲内酯为参照,计算新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯在不同柱温下的相对保留时间和相对校正因子,结果见表9。上述3个成分的相对保留时间为0.39%~0.74%,相对校正因子RSD为1.41%~1.92%,表明不同柱温对新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯的相对保留时间和相对校正因子影响较小。

表9 不同柱温的穿心莲中3个成分相对保留时间和相对校正因子测定结果
2.2.7.4 不同仪器考察
以穿心莲内酯为参照,计算新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯在不同品牌仪器上的相对保留时间和相对校正因子,结果见表10。上述3个成分的相对保留时间为0.48%~0.97%,相对校正因子RSD 为1.31%~2.67%,表明不同仪器对新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯的相对保留时间和相对校正因子影响较小。
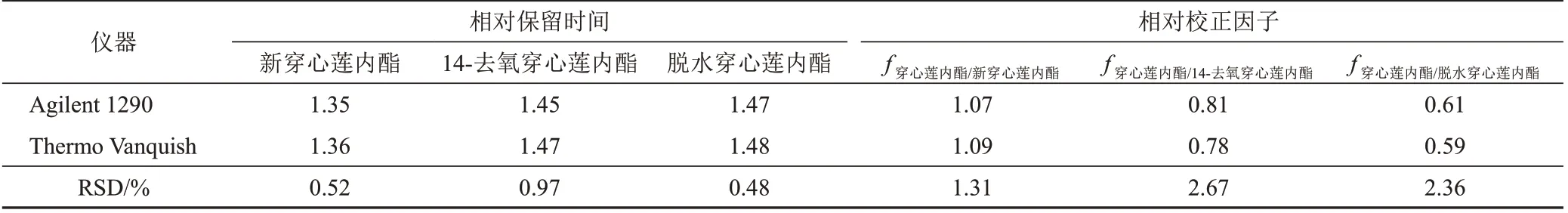
表10 不同仪器的相对保留时间和相对校正因子测定结果
2.2.8 色谱峰定位
取“2.2.7”项下不同色谱柱、不同流速、不同柱温和不同色谱仪的相对保留时间均值,确定新穿心莲内酯、14-去氧穿心莲内酯和脱水穿心莲内酯的相对保留时间为1.37、1.46和1.48。
2.2.9 样品测定
取12批穿心莲药材,按“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件测定,以穿心莲内酯为参照,分别采用外标法(ESM)和QAMS计算其余3个二萜内酯成分含量,并比较2种方法的相对偏差,结果见表11。上述2种方法测得3个二萜内酯成分含量的相对偏差均在5.0%范围内,表明QAMS测定结果与ESM无明显差异,准确性良好。采用QAMS含量数据计算12批穿心莲药材4个二萜内酯成分总量,结果显示,不同产地穿心莲药材4个二萜内酯成分含量无明显差异。
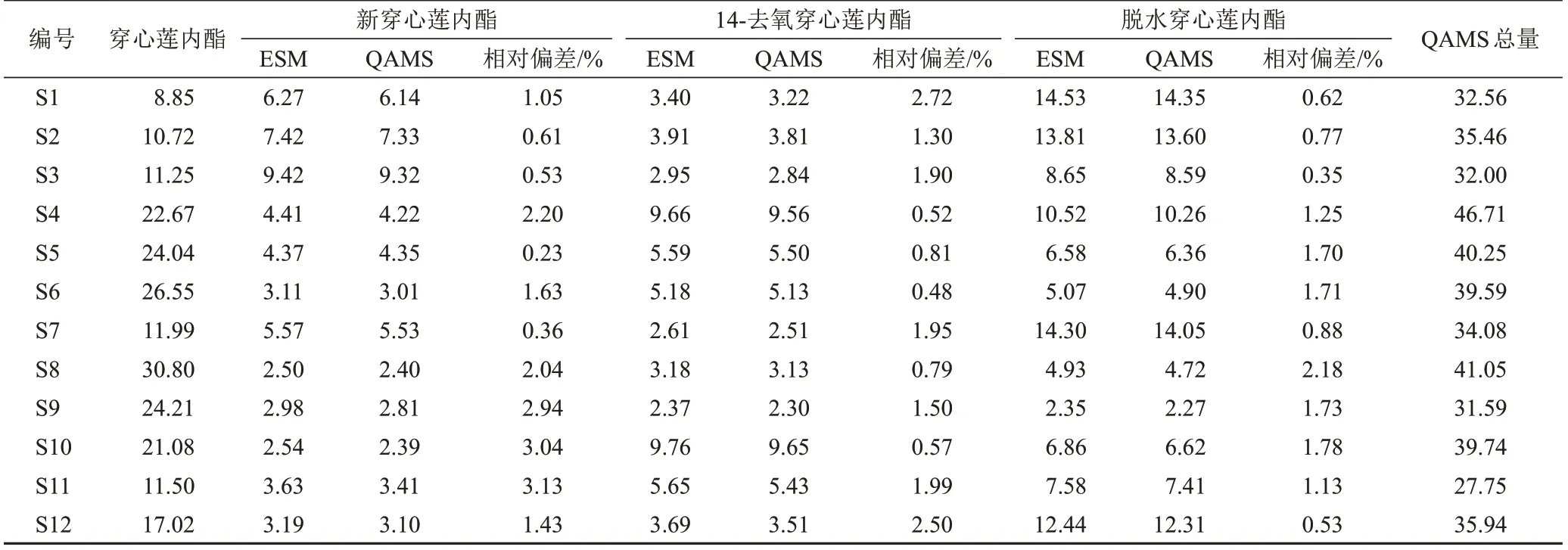
表11 12批穿心莲药材4个成分ESM与QAMS结果(mg/g)
3 讨论
指纹图谱与特征图谱均是常用的中药整体质量控制模式。指纹图谱侧重于将化学成分尽可能多地展现在图谱上,通过对各色谱峰进行积分,利用相似度软件计算,从而对不同批次样品进行一致性评价。指纹图谱将共有峰和非共有峰均纳入计算,主要强调图谱的相似性和一致性,评价方式具有一定的模糊性,对单个色谱峰的关注度不高,图谱的整体性受仪器、色谱柱及图谱积分参数影响较大,因此,在中药的诸多法定标准中使用受限,仅在中药注射剂评价中使用较多[15]。而特征图谱侧重于在前期物质基础研究较明确的情况下,有目的地针对中药的主要有效成分进行表征,强调图谱的整体专属性与药效的相关性,关注共有峰的特征性、特征峰的分离度,以及方法在不同色谱仪、色谱柱中的重现性,利用共有特征峰的相似度评价,采用相对保留时间定位、相对峰面积半定量分析等手段,从而评价中药的质量。
穿心莲药材主要有效成分为二萜内酯、黄酮和酚酸类,因此,特征图谱的建立主要为表征上述成分,并兼顾QAMS对二萜内酯色谱峰分离度的要求,为缩短分析时间,采用UPLC。此外,本研究考察了不同色谱仪及不同品牌和粒径色谱柱对方法重现性的影响,结果显示,该方法在一些粒径为1.6~2.2 μm的不同品牌色谱柱上重现性良好。
根据产地调研,目前穿心莲主要产区在广东、广西和福建,以栽培为主,野生资源较少。本研究对穿心莲药材二萜内酯成分含量测定结果显示,不同产地药材质量差异不大。广西产区药材资源丰富、产量较大,因此,可选择广西为穿心莲药材的固定产地。
2020年版《中华人民共和国药典》规定穿心莲药材于秋初茎叶茂盛时采收。研究显示,不同生长期穿心莲药材中穿心莲内酯和脱水穿心莲内酯的含量在8、9月较高,因此,建议穿心莲药材的最佳采收期为8-9月[16]。陈两绵等[17]研究显示,穿心莲生长过程可分为6期,从枝叶茂盛期到花蕾期4个二萜内酯成分总量最高且比较稳定,为最佳采收期,采收时间也在8月。我们研究穿心莲不同产地加工方式对药材质量的影响时发现,其产地加工分为晒干和阴干,阴干样品中穿心莲内酯含量较低,脱水穿心莲内酯和新穿心莲内酯含量较高,提示阴干过程可能导致穿心莲内酯分解和转化,而晒干样品4个成分总量较高,因此,在天气条件允许的情况下,产地加工宜尽量采用晒干法进行干燥。此外,考察不同烘干方式处理药材对4个二萜内酯成分含量的影响,结果显示,烘干温度对穿心莲二萜内酯含量影响较大,当烘干温度达到80 ℃、时间超过3 h,二萜内酯含量逐渐降低,采用低温干燥的方式有助于保存穿心莲有效成分。以上研究表明不同采收期和产地加工方式对穿心莲药材质量影响较大,建议严格控制药材的采收时间和产地加工方式,从而保证药材质量。

